文档内容
第一章 化学反应的热效应
课题 第一节 反应热
课时2 热化学方程式 燃烧热
1、了解燃烧热的概念,并能进行简单的计算。
知识与技
2、知道化学反应中能量转化的原因,能说出常见的能量转化形式。
能
3、了解资源、能源、环保是当今社会的重要热点问题。
1、通过学习及查阅资料了解研究燃烧热的实际意义。
过程与方 2、通过查阅资料说明能源是人类生存和发展的重要基础,了解化学在
教 学 法 解决能源危机中的重要作用。知道节约能源、提高能量利用效率的实际
目 标 意义。
1、发展学习化学的兴趣,乐于探究物质变化的奥秘,体验科学探究的
艰辛与喜悦,感受化学世界的奇妙与和谐。
情感态度
2、有参与化学科技活动的热情,有将化学能与热能的化学知识应用于
与价值观
生产、生活实践的意识,能够对与化学有关的社会问题和生活问题做出
合理的判断。
教学
燃烧热的概念及相关计算。
重点
教学
燃烧热的概念。
难点
教
学
设
教
材 《化学反应与能量变化》选择于人教版高中化学(选修4)第一章第一节,是必修2第
分 二章的延续,这一章里我们继续学习有关它们知识。
析
学
对高中学生来说,大部分人的抽象思维比较困难,有些学生学得比较呆板,不太
情
会灵活运用所学的知识,学习方法上往往更多的习惯死记硬背,不习惯对知识的理解
分
记忆和独立思考,在动手探究方面的能力则更差。
析
教
法 讲授、学生实验、学生活动、实验条件控制、比较、类比、归纳、抽象等
想 设
计
教学 教 学 内 容 设计意图
环节
教师活动设计 学生活动设计我们知道物质的燃烧可以放出大量的热,
那么不同的物质燃烧放出的热量是否相等呢?
复习热化学方程
下面我们来学习燃烧热。
式的意义,书写
[板书] 第二节 燃烧热 能源
热化学方程式的
一、燃烧热
注意事项,引入
[探究1] 阅读教材指出燃烧热的概念。
新课。
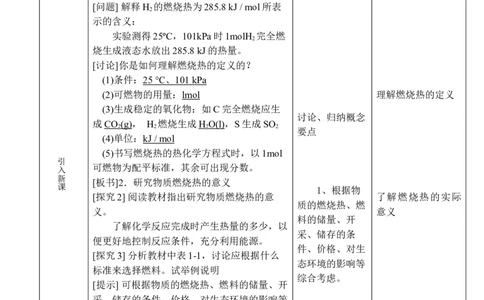
[板书]1.定义:在 25 ℃、101 kPa时,lmol
物质完全燃烧生成稳定的氧化物时所放出的热
量,叫做该物质的燃烧热。
[问题] 解释H 的燃烧热为285.8 kJ / mol所表
2
示的含义:
实验测得25ºC,101kPa时1molH 完全燃
2
烧生成液态水放出285.8 kJ的热量。
[讨论]你是如何理解燃烧热的定义的?
(1)条件: 25 ℃ 、 101 kPa
(2)可燃物的用量:lmol 理解燃烧热的定义
(3)生成稳定的氧化物:如C完全燃烧应生
讨论、归纳概念
成CO (g), H 燃烧生成H O(l),S生成SO
2 2 2 2
要点
(4)单位:kJ / mol
(5)书写燃烧热的热化学方程式时,以1mol
引
可燃物为配平标准,其余可出现分数。
入
新
[板书]2.研究物质燃烧热的意义
课
1、根据物
[探究2] 阅读教材指出研究物质燃烧热的意 了解燃烧热的实际
质的燃烧热、燃
义。 意义
料的储量、开
了解化学反应完成时产生热量的多少,以
采、储存的条
便更好地控制反应条件,充分利用能源。
件、价格、对生
[探究3] 分析教材中表1-1,讨论应根据什么
态环境的影响等
标准来选择燃料。试举例说明
综合考虑。
[提示] 可根据物质的燃烧热、燃料的储量、开
采、储存的条件、价格、对生态环境的影响等
综合考虑。
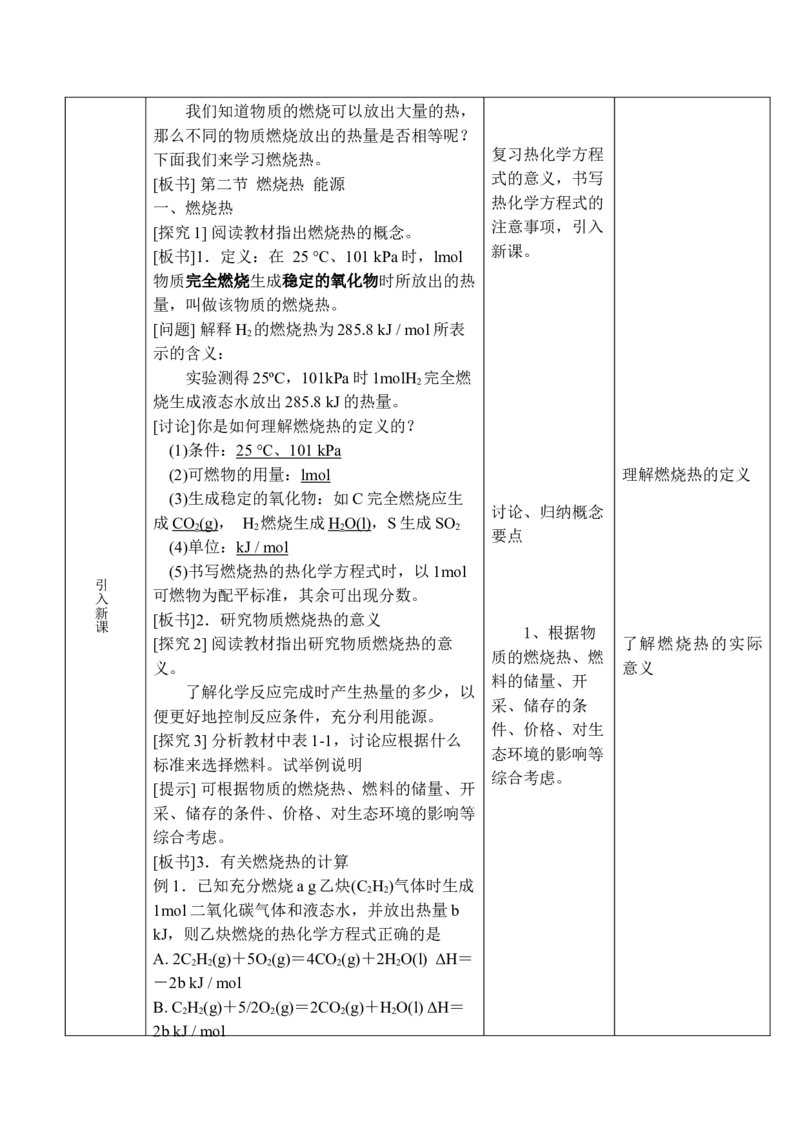
[板书]3.有关燃烧热的计算
例1.已知充分燃烧a g乙炔(C H )气体时生成
2 2
1mol二氧化碳气体和液态水,并放出热量b
kJ,则乙炔燃烧的热化学方程式正确的是
A. 2C H (g)+5O (g)=4CO (g)+2H O(l) ΔH=
2 2 2 2 2
-2b kJ / mol
B. C H (g)+5/2O (g)=2CO (g)+H O(l) ΔH=
2 2 2 2 2
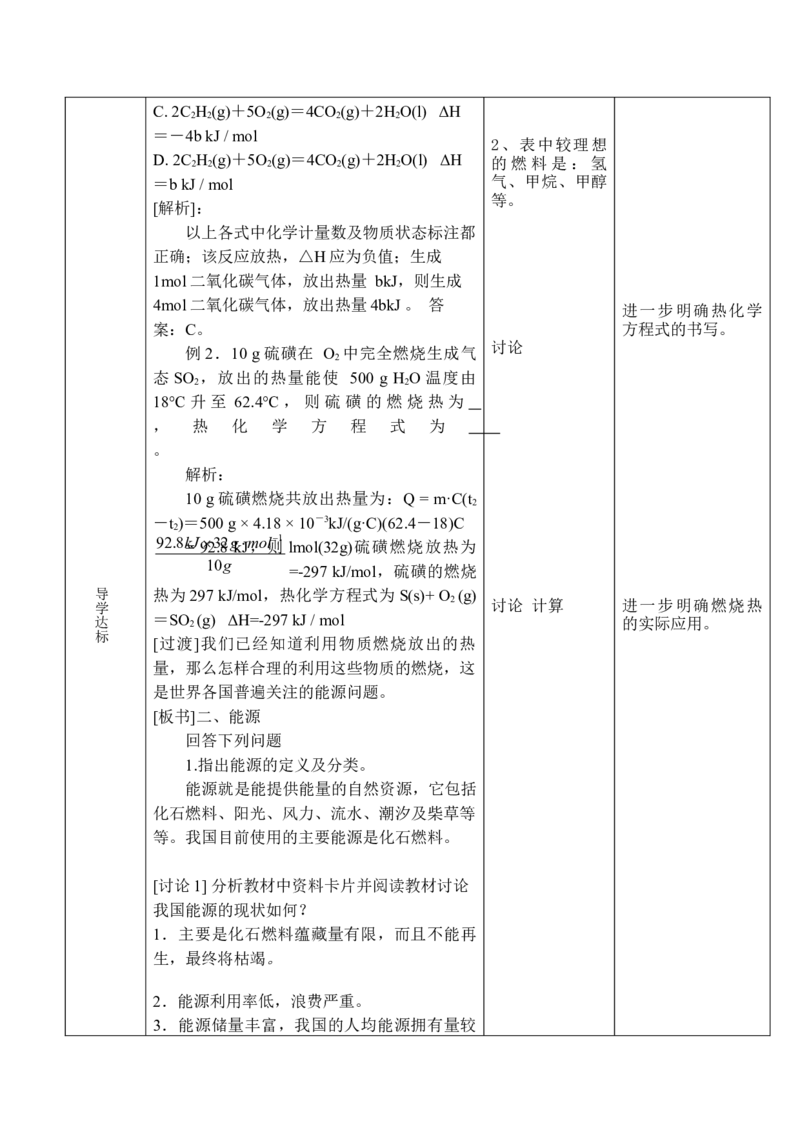
2b kJ / molC. 2C H (g)+5O (g)=4CO (g)+2H O(l) ΔH
2 2 2 2 2
=-4b kJ / mol
2、表中较理想
D. 2C H (g)+5O (g)=4CO (g)+2H O(l) ΔH 的燃料是:氢
2 2 2 2 2
=b kJ / mol 气、甲烷、甲醇
等。
[解析]:
以上各式中化学计量数及物质状态标注都
正确;该反应放热,△H应为负值;生成
1mol二氧化碳气体,放出热量 bkJ,则生成
4mol二氧化碳气体,放出热量4bkJ 。 答
进一步明确热化学
案:C。 方程式的书写。
讨论
例2.10 g硫磺在 O 中完全燃烧生成气
2
态 SO ,放出的热量能使 500 g H O 温度由
2 2
18℃ 升 至 62.4℃ , 则 硫 磺 的 燃 烧 热 为
, 热 化 学 方 程 式 为
。
解析:
10 g硫磺燃烧共放出热量为:Q = m·C(t
2
-t )=500 g × 4.18 × 10-3kJ/(g·C)(62.4-18)C
2
92.8k = J 9 2 3 .8 2 g k J m,ol则 1 lmol(32g)硫磺燃烧放热为
10g
=-297 kJ/mol,硫磺的燃烧
导 热为297 kJ/mol,热化学方程式为 S(s)+ O (g)
学 2 讨论 计算 进一步明确燃烧热
达 =SO 2 (g) ΔH=-297 kJ / mol 的实际应用。
标
[过渡]我们已经知道利用物质燃烧放出的热
量,那么怎样合理的利用这些物质的燃烧,这
是世界各国普遍关注的能源问题。
[板书]二、能源
回答下列问题
1.指出能源的定义及分类。
能源就是能提供能量的自然资源,它包括
化石燃料、阳光、风力、流水、潮汐及柴草等
等。我国目前使用的主要能源是化石燃料。
[讨论1] 分析教材中资料卡片并阅读教材讨论
我国能源的现状如何?
1.主要是化石燃料蕴藏量有限,而且不能再
生,最终将枯竭。
2.能源利用率低,浪费严重。
3.能源储量丰富,我国的人均能源拥有量较[讨论2] 如何解决我国的能源危机问题?
1.调整和优化能源结构。
2.加强科技投入,提高管理水平,科学的控 阅读教材
制燃烧反应,使燃料充分燃烧,提高能源的使 锻炼自主学习的能
力
用效率。
3.节约利用现有能源。
回答问题
4.研究开发新能源。
[讲述]在现有的能源即将出现危机之时,
导
人们很自然地把目光转向那些储量更丰富、更
学
达
清洁、可以再生的新能源,并惊奇地发现,这
标 了解我国能源结果
些新能源大多数与我们日常生活一直息息相
听 和现状
关。人们在不知不觉地使用着它们,只不过今
后我们将采取新的方式利用它们。
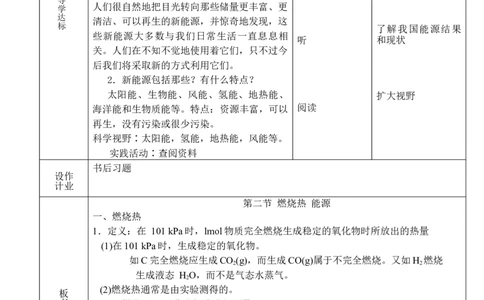
2.新能源包括那些?有什么特点?
太阳能、生物能、风能、氢能、地热能、 扩大视野
海洋能和生物质能等。特点:资源丰富,可以 阅读
再生,没有污染或很少污染。
科学视野∶太阳能,氢能,地热能,风能等。
实践活动∶查阅资料
书后习题
设作
计业
第二节 燃烧热 能源
一、燃烧热
1.定义:在 101 kPa时,lmol物质完全燃烧生成稳定的氧化物时所放出的热量
(1)在101 kPa时,生成稳定的氧化物。
如C完全燃烧应生成CO (g),而生成CO(g)属于不完全燃烧。又如H 燃烧
2 2
生成液态 H O,而不是气态水蒸气。
2
(2)燃烧热通常是由实验测得的。
板
书 (3)可燃物以lmol作为标准进行测量。
设
(4)计算燃烧热时,热化学方程式常以分数表示。
计
2.研究物质燃烧热的意义:了解化学反应完成时产生热量的多少,以便更好地控制
反应条件,充分利用能源。
3.有关燃烧热的计算
二、能源
1、新能源:太阳能、生物能、风能、氢能、地热能、海洋能。
2、新能源介绍: