文档内容
第 1 章 有机化合物的结构特点与研究方法
第2节有机化合物的结构特点
第1课时 有机物的分离提纯
【学习目标】1.了解有机化合物结构测定的一般步骤和程序,能进行确定有机化合物分子式的简单计
算,形成宏观辨识与微观探析的化学学科核心素养。
2.能利用官能团的化学检验方法鉴定官能团,培养证据推理与模型认知的化学学科核心素养。
3.初步了解一些测定有机化合物结构的现代手段,懂得有机化合物结构测定是有机化合物合成的重要
环节,培养科学态度与社会责任的化学学科核心素养。
【学习难点】1.有机物分离方法的原理理解
2.分离方法的实际应用
一、有机物的分离提纯
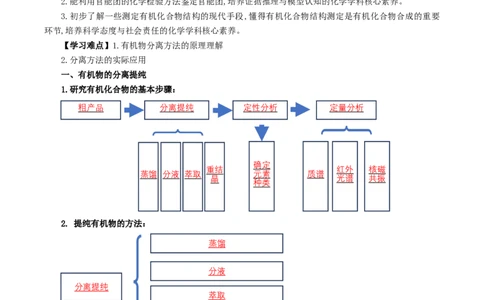
1.研究有机化合物的基本步骤:
粗产品 分离提纯 定性分析 定量分析
确定
重结 红外 核磁
蒸馏 分液 萃取 元素 质谱
晶 光谱 共振
种类
2. 提纯有机物的方法:
蒸馏
分液
分离提纯
萃取
重结晶
一、蒸馏
1. 适用范围:常用于分馏,提纯互溶且 沸点 不同的液态有机物。
2. 适用条件:
有机物与杂质的沸点相差较大,一般差 30℃ 以上。
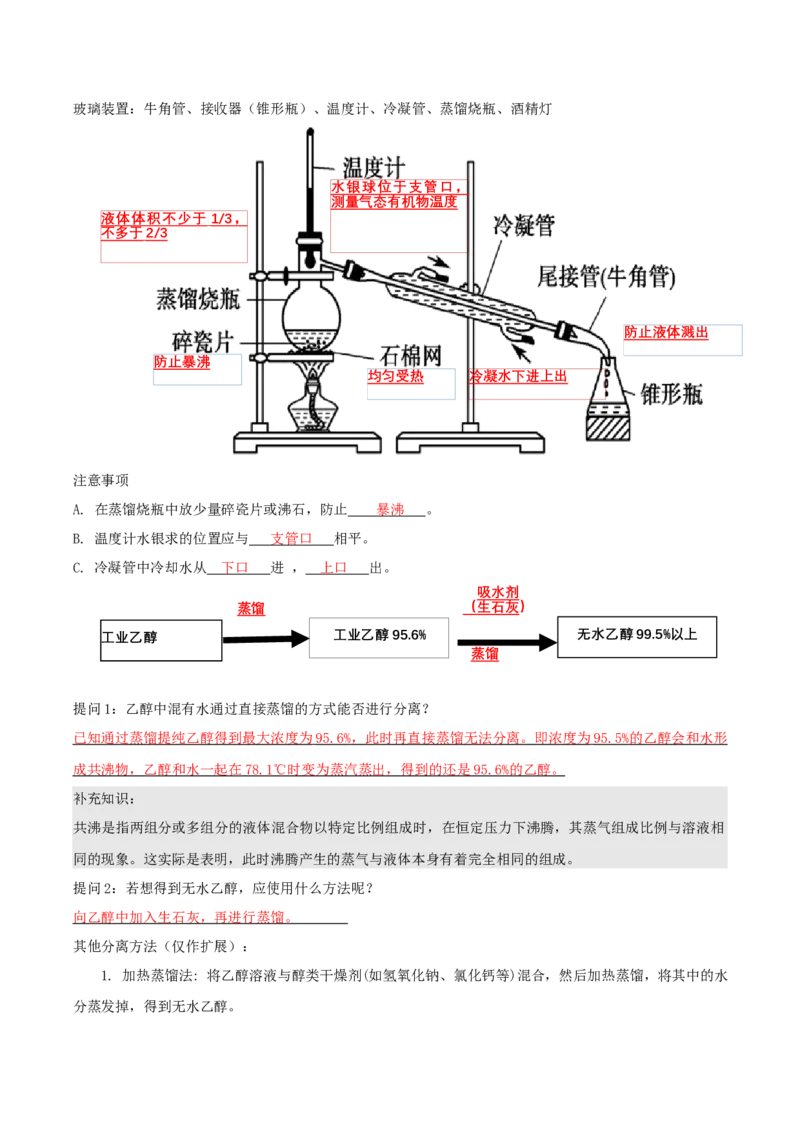
3. 实验装置玻璃装置:牛角管、接收器(锥形瓶)、温度计、冷凝管、蒸馏烧瓶、酒精灯
水银球位于支管口,
测量气态有机物温度
液体体积不少于 1/3 ,
不多于 2/3
防止液体溅出
防止暴沸
均匀受热 冷凝水下进上出
注意事项
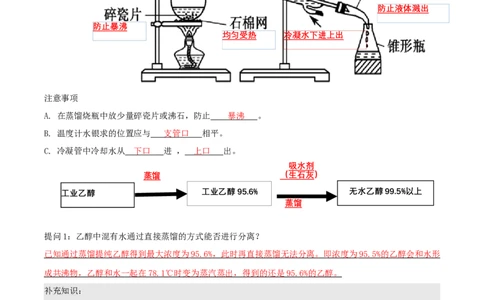
A. 在蒸馏烧瓶中放少量碎瓷片或沸石,防止 暴沸 。
B. 温度计水银求的位置应与 支管口 相平。
C. 冷凝管中冷却水从 下口 进 , 上口 出。
吸水剂
蒸馏 (生石灰)
工业乙醇 工业乙醇95.6% 无水乙醇99.5%以上
蒸馏
提问1:乙醇中混有水通过直接蒸馏的方式能否进行分离?
已知通过蒸馏提纯乙醇得到最大浓度为 95.6 % ,此时再直接蒸馏无法分离。即浓度为 95.5 % 的乙醇会和水形
成共沸物,乙醇和水一起在 78.1℃ 时变为蒸汽蒸出,得到的还是 95.6 % 的乙醇。
补充知识:
共沸是指两组分或多组分的液体混合物以特定比例组成时,在恒定压力下沸腾,其蒸气组成比例与溶液相
同的现象。这实际是表明,此时沸腾产生的蒸气与液体本身有着完全相同的组成。
提问2:若想得到无水乙醇,应使用什么方法呢?
向乙醇中加入生石灰,再进行蒸馏。
其他分离方法(仅作扩展):
1. 加热蒸馏法: 将乙醇溶液与醇类干燥剂(如氢氧化钠、氯化钙等)混合,然后加热蒸馏,将其中的水
分蒸发掉,得到无水乙醇。2. 分子筛法: 将乙醇溶液与分子筛(如三维交联型硅胶分子筛)接触,分子筛能吸附溶液中的水分,从
而使乙醇脱水。随后通过脱附或再生处理,得到无水乙醇。
3. 混合溶剂法: 将乙醇溶液与其他易挥发的有机物(如正丁醇、丁醚等)混合,之后加热蒸馏,将乙醇
与有机物混合物中的水分蒸发掉,得到无水乙醇。
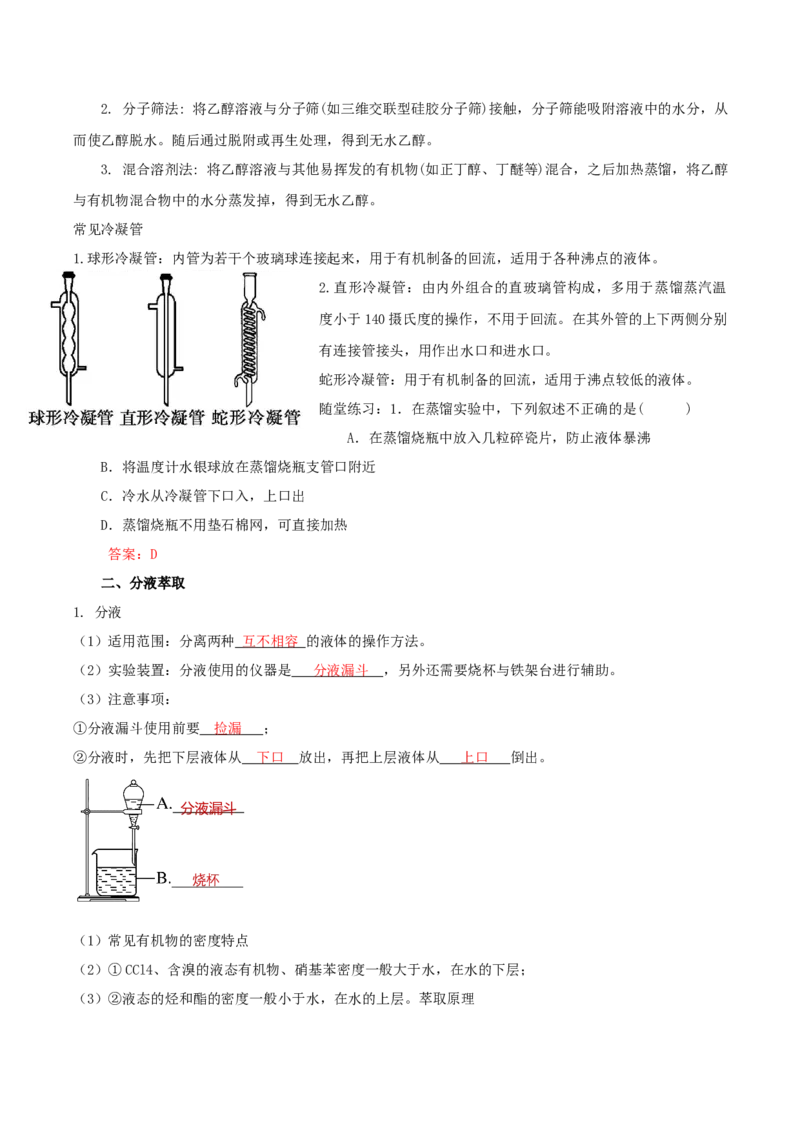
常见冷凝管
1.球形冷凝管:内管为若干个玻璃球连接起来,用于有机制备的回流,适用于各种沸点的液体。
2.直形冷凝管:由内外组合的直玻璃管构成,多用于蒸馏蒸汽温
度小于140摄氏度的操作,不用于回流。在其外管的上下两侧分别
有连接管接头,用作出水口和进水口。
蛇形冷凝管:用于有机制备的回流,适用于沸点较低的液体。
随堂练习:1.在蒸馏实验中,下列叙述不正确的是( )
A.在蒸馏烧瓶中放入几粒碎瓷片,防止液体暴沸
B.将温度计水银球放在蒸馏烧瓶支管口附近
C.冷水从冷凝管下口入,上口出
D.蒸馏烧瓶不用垫石棉网,可直接加热
答案:D
二、分液萃取
1. 分液
(1)适用范围:分离两种 互不相容 的液体的操作方法。
(2)实验装置:分液使用的仪器是 分液漏斗 ,另外还需要烧杯与铁架台进行辅助。
(3)注意事项:
①分液漏斗使用前要 捡漏 ;
②分液时,先把下层液体从 下口 放出,再把上层液体从 上口 倒出。
分液漏斗
烧杯
(1)常见有机物的密度特点
(2)①CCl4、含溴的液态有机物、硝基苯密度一般大于水,在水的下层;
(3)②液态的烃和酯的密度一般小于水,在水的上层。萃取原理液-液萃取是利用溶质在两种互不相容的溶剂里溶解能力的不同,用一种溶剂(萃取剂)将其从原溶剂中
提取出来的方法。萃取剂的要求
①萃取剂与原溶剂 不互溶 ;
②溶质在萃取剂中的溶解度 远大于 在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应。
常用萃取剂: 乙醚 、 乙酸乙酯 、 二氯甲烷 等。
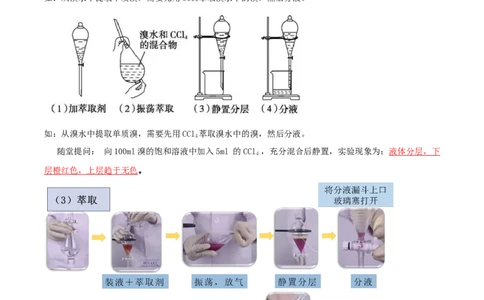
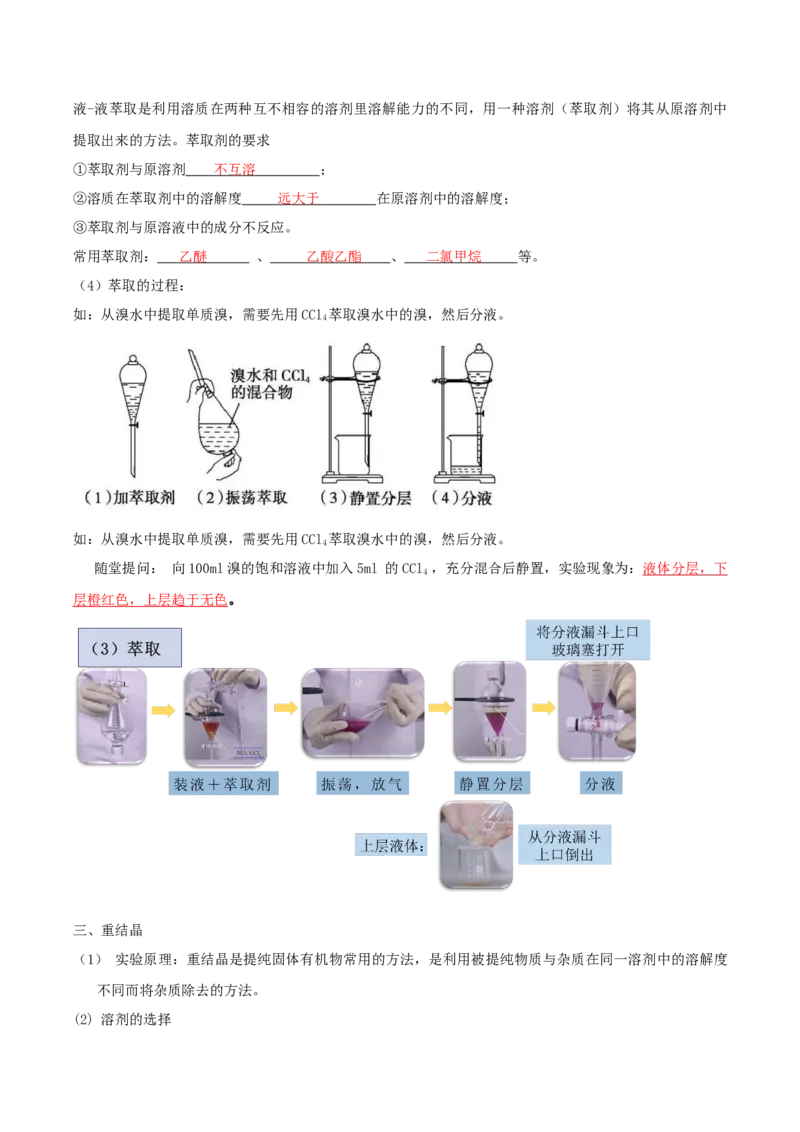
(4)萃取的过程:
如:从溴水中提取单质溴,需要先用CCl 萃取溴水中的溴,然后分液。
4
如:从溴水中提取单质溴,需要先用CCl 萃取溴水中的溴,然后分液。
4
随堂提问: 向100ml溴的饱和溶液中加入5ml 的CCl ,充分混合后静置,实验现象为:液体分层,下
4
层橙红色,上层趋于无色。
三、重结晶
(1) 实验原理:重结晶是提纯固体有机物常用的方法,是利用被提纯物质与杂质在同一溶剂中的溶解度
不同而将杂质除去的方法。
(2) 溶剂的选择1.选用合适的溶剂,使得杂质在所选溶剂中溶解度 很大或很小 ,易于除去;
2.被提纯的有机化合物在所选溶剂中的溶解度受温度的影响 较大 ,能够进行 冷却结晶 。
3.杂质在此溶剂中溶解度很小(杂质在热过滤时被滤去)或者很大(杂质留在母液中,不析出),易于除
去。
4.被提纯的有机物在此溶剂中的溶解度受温度影响较大,能够冷却结晶。
【问题】某粗苯甲酸样品中含有少量氯化钠和泥沙,提纯苯甲酸需要经过哪些步骤?
【资料卡片】
1、纯净的苯甲酸为无色结晶,其结构可表示为 ,
2、熔点122℃,沸点249℃。
3、苯甲酸微溶于水,易溶于乙醇、乙醚等有机溶剂。苯甲酸在水中的溶解度如下:
温度/℃ 25 50 75
溶解度/g 0.34 0.85 2.2
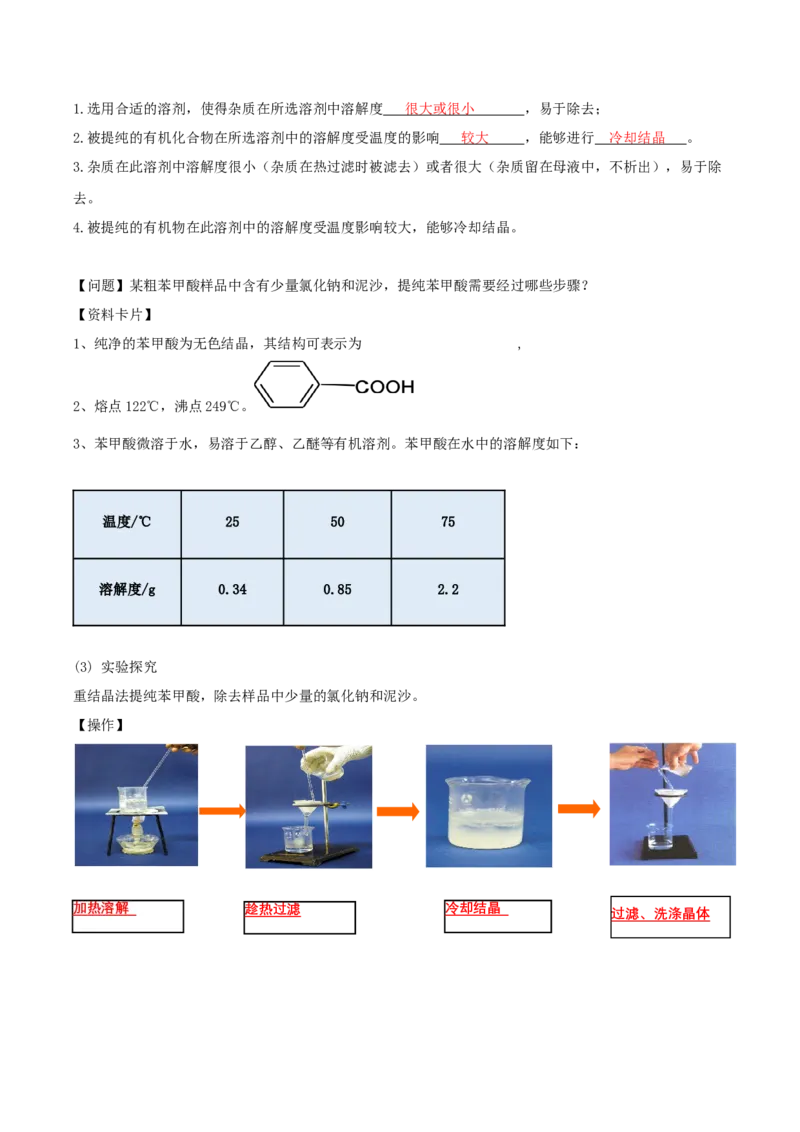
(3) 实验探究
重结晶法提纯苯甲酸,除去样品中少量的氯化钠和泥沙。
【操作】
加热溶解 趁热过滤 冷却结晶
过滤、洗涤晶体边加热边搅拌 ,
一贴,二低,三靠; ( 缓慢冷却结晶 , 晶形好 ) 白色片状晶体
至固体溶解
避免烫伤
流程简笔图:
【问题讨论】
①重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
提示 苯甲酸在不同温度的蒸馏水中溶解度不同。加热溶解、趁热过滤、冷却结晶、过滤洗涤、干燥称量 。
②溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
提示 加热是为了增大苯甲酸的溶解度,使苯甲酸充分溶解。趁热过滤是为了防止苯甲酸提前结晶析出。
③实验操作中多次用到了玻璃棒,分别起到了哪些作用?
提示 搅拌和引流。
④如何检验提纯后的苯甲酸中氯化钠已被除净?
提示 用适量蒸馏水洗涤过滤器中的苯甲酸晶体,取少量第 n 次洗涤后的液体,滴加几滴硝酸银溶液,观
察是否有沉淀产生。若无沉淀产生,则氯化钠被除净。
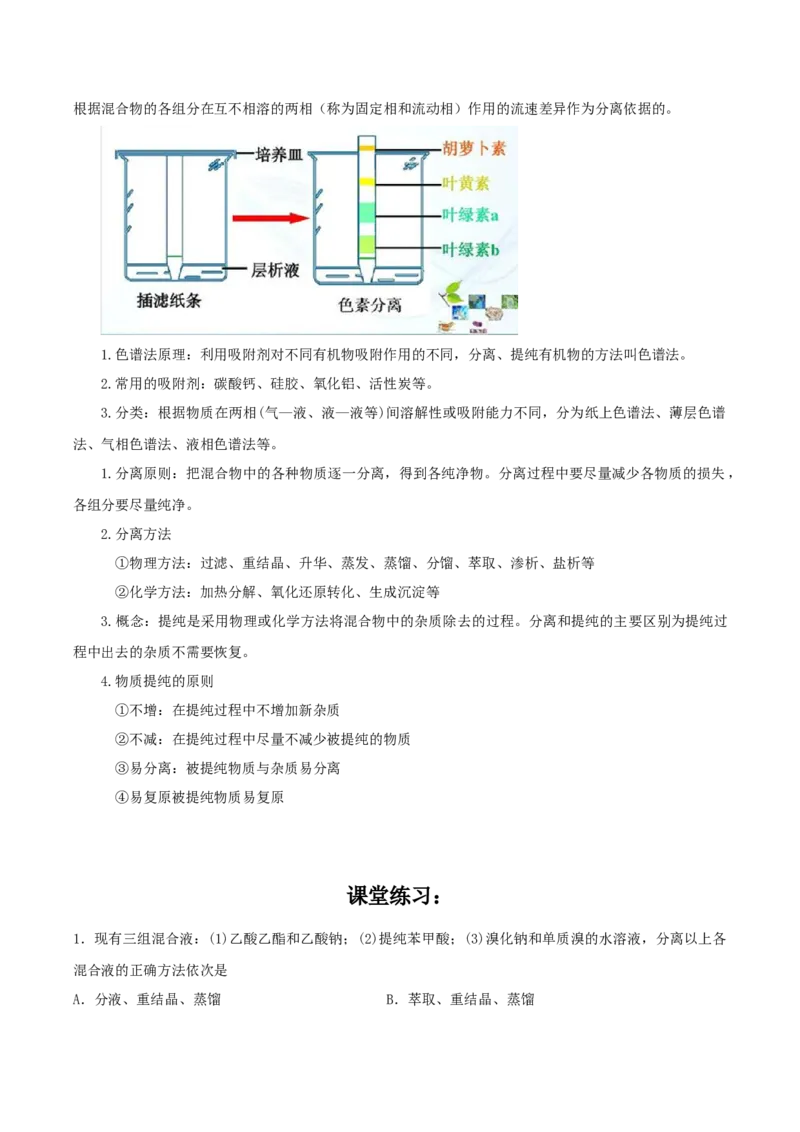
科学阅读:1906年Tswett 研究植物色素分离时提出色谱法概念;他在研究植物叶的色素成分时,将植物
叶子的萃取物倒入填有碳酸钙的直立玻璃管内,然后加入石油醚使其自由流下,结果色素中各组分互相分
离形成各种不同颜色的谱带。溶有绿色植物叶子色素的石油醚溶液自上而下地通过。结果植物色素便被碳
酸钙吸附,分成三段不同颜色:绿色、黄色、黄绿色。再将碳酸钙吸附柱取出,并用乙醇洗脱,即得色素
的溶液:叶绿素、叶黄素、胡萝卜素。
按光谱的命名方式,这种方法因此得名为色谱法。以后此法逐渐应用于无色物质的分离,“色谱”二
字虽已失去原来的含义,但仍被人们沿用至今。
色谱法
又称层析法或色层法,是一种利用物质的溶解性、吸附性等特性的物理化学分离方法。其分离原理是根据混合物的各组分在互不相溶的两相(称为固定相和流动相)作用的流速差异作为分离依据的。
1.色谱法原理:利用吸附剂对不同有机物吸附作用的不同,分离、提纯有机物的方法叫色谱法。
2.常用的吸附剂:碳酸钙、硅胶、氧化铝、活性炭等。
3.分类:根据物质在两相(气—液、液—液等)间溶解性或吸附能力不同,分为纸上色谱法、薄层色谱
法、气相色谱法、液相色谱法等。
1.分离原则:把混合物中的各种物质逐一分离,得到各纯净物。分离过程中要尽量减少各物质的损失,
各组分要尽量纯净。
2.分离方法
①物理方法:过滤、重结晶、升华、蒸发、蒸馏、分馏、萃取、渗析、盐析等
②化学方法:加热分解、氧化还原转化、生成沉淀等
3.概念:提纯是采用物理或化学方法将混合物中的杂质除去的过程。分离和提纯的主要区别为提纯过
程中出去的杂质不需要恢复。
4.物质提纯的原则
①不增:在提纯过程中不增加新杂质
②不减:在提纯过程中尽量不减少被提纯的物质
③易分离:被提纯物质与杂质易分离
④易复原被提纯物质易复原
课堂练习:
1.现有三组混合液:(1)乙酸乙酯和乙酸钠;(2)提纯苯甲酸;(3)溴化钠和单质溴的水溶液,分离以上各
混合液的正确方法依次是
A.分液、重结晶、蒸馏 B.萃取、重结晶、蒸馏C.萃取、蒸馏、分液 D.分液、重结晶、萃取
【答案】D
【详解】(1)乙酸乙酯不溶于水,乙酸钠溶于水,可用分液的方法分离;
(2)提纯粗苯甲酸用重结晶法,主要步骤为:加热溶解,趁热过滤,冷却结晶,过滤,洗涤;
(3)向溴化钠和单质溴的水溶液中加入萃取剂四氯化碳后,溴单质会溶解在四氯化碳中,四氯化碳和水互
不相溶而分层,然后分液即可实现二者的分离;
故选D。
2.下列玻璃仪器在相应实验中选用合理的是
A.重结晶法提纯苯甲酸:①⑥⑦
B.蒸馏法分离CHCl 和CCl:②⑤⑥
2 2 4
C.分离苯和四氯化碳:③⑦
D.用盐酸滴定NaOH溶液:④⑥
【答案】D
【详解】
A.利用重结晶来提纯苯甲酸,具体操作为加热溶解、趁热过滤和冷却结晶,用到的玻璃仪器有漏斗、烧
杯、玻璃棒、酒精灯,用不到锥形瓶,故A错误;
B.蒸馏法分离CHCl 和CCl 需要用到酒精灯、蒸馏烧瓶、温度计、锥形瓶、直形冷凝管等,图示中的②
2 2 4
为球形冷凝管,故B错误;
C.苯和四氯化碳是互溶的,不能用分液法分离,故C错误;
D.酸碱滴定法测定NaOH溶液浓度,需要用到酸式滴定管和锥形瓶,用到图示中的④⑥,故D正确;
答案选D。
3.现有一瓶A和B的混合液,已知A和B的某些性质如下:
由此推知分离A和B的最佳方法是
密 度 /
物质 分子式 熔点/℃ 沸点/℃ 水溶性
(g·cm-3)A CHO -24 141 0.99 可溶
3 6 2
B CHO -84 77 0.90 可溶
4 8 2
A.萃取 B.结晶 C.蒸馏 D.分液
【答案】C
【详解】A.观察表中数据,得知A、B两种物质都是有机物,都溶于水,不能用萃取方法进行分离,故 A
不选;
B.观察表中数据,得知A、B两种物质的熔点都比较低,常温下为液体,不能结晶方法析出,故B不选;
C.观察表中数据,得知A、B两种物质的沸点相差较大,故可以用蒸馏的方法将A、B分离,故C选;
D.观察表中数据,得知A、B两种物质都是有机物,都溶于水,不能用分液方法进行分离,故D不选;
故选:C。
4.用分液漏斗可以分离的一组液体混合物是( )
A.溴和CCl B.溴苯和水 C.苯和硝基苯 D.汽油和苯
4
【分析】能用分液漏斗分离的物质必须是两种相互不溶的液体,一般来说:有机溶质易溶于有机溶剂,无
机溶质易溶于无机溶剂;
【详解】A.溴易溶于有机物CCl,所以不能用分液漏斗分离,A错误;
4
B.溴苯是有机物,水是无机物,溴苯和水不互溶,所以能用分液漏斗分离,B正确;
C.苯和硝基苯都是有机物,所以苯和硝基苯能相互溶解,不能用分液漏斗分离,C错误;
D.汽油和苯都是有机物能互溶,不能用分液漏斗分离,D错误;
故选B。
5.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
A.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
B.用95.6%的工业酒精制取无水乙醇、可采用的方法是加生石灰,再蒸馏
C.用图1所示装置可以分离二氯甲烷、三氯甲烷和四氯化碳的混合物
D.用图2所示装置可以用乙醇提取溴水中的溴【答案】B
【详解】A.苯甲酸的溶解度随温度降低而减小,冷却后若降到常温会有苯甲酸析出损失,应趁热过滤,A
错误;
B.水和乙醇会形成共沸物,直接蒸馏得不到无水乙醇,生石灰和水反应生成高沸点的氢氧化钙,用95.6%
的工业酒精制取无水乙醇、可采用的方法是加生石灰,再蒸馏,B正确;
C.二氯甲烷、三氯甲烷和四氯化碳互溶,用蒸馏的方法分离,但是图1圆底烧瓶应改为蒸馏烧瓶,再加个
温度计,C错误;
D.乙醇与水互溶,不能用乙醇提取溴水中的溴,D错误;