文档内容
第一章《有机化合物的结构特点》教学设计
第二节有机化合物的研究方法
第一课时 有机物的分离提纯
课题: 1.2.1 有机物的分离提纯 课时 1 授课年级 高二
1.通过学习蒸馏、萃取、重结品等实验原理与操作,了解科学探究步骤,学会设计科学探
课标
究方案,培养严谨科学态度与思维。
要求
2.能根据有机化合物性质差异选择分离、提纯方法。
在高中化学教材的选择性必修三《有机化学基础》这一本书中,第一章第二节的内容集中探讨了有
机物的分离方法,包括但不限于萃取、蒸馏和重结晶等物理和化学分离技术。本节深入剖析了这些
分离方法背后的实验原理,让学生理解每种方法是如何基于物质特性的差异来实现有效分离的。
同时,也详细介绍了进行这些操作的基本步骤和注意事项,培养学生的动手能力和实验技巧。此
外,还通过实例分析,使学生认识到科学探究是一个系统性的过程,包括提出假设、设计实验、收
教材 集证据、分析结果等步骤,从而学会如何根据已知的科学原理和未知的问题设计合理的科学探究方
案。
分析
同时,通过对各种分离方法的实践操作,培养学生严谨的科学态度和科学的思维方式,使他们能够
根据物质的具体性质差异选择最适宜的分离和提纯方法。这一节的内容不仅有助于学生掌握有机物
的分离方法,更有助于他们培养科学探究能力和严谨的科学态度,为未来的科学研究和实践活动奠
定坚实的基础。
1.了解有机化合物结构测定的一般步骤和程序,能进行确定有机化合物分子式的简单计算,
形成宏观辨识与微观探析的化学学科核心素养。
教学 2.能利用官能团的化学检验方法鉴定官能团,培养证据推理与模型认知的化学学科核心素
目标 养。
3.初步了解一些测定有机化合物结构的现代手段,懂得有机化合物结构测定是有机化合物
合成的重要环节,培养科学态度与社会责任的化学学科核心素养。
教学 (1)、有机物分离方法的原理理解
重、 (2)、分离方法的实际应用
难点
高中有机化学学情分析:
(1) 掌握有机化合物结构测定的一般步骤和程序:学生需要熟悉有机化合物结构测定的基
本流程,包括样品准备、仪器选择、数据采集、数据分析等环节。同时,能够进行确定有机化
合物分子式的简单计算,形成宏观辨识与微观探析的化学学科核心素养。
(2) 能够利用官能团的化学检验方法鉴定官能团:学生应掌握常见官能团的化学检验方
法,如卤代烃的卤素鉴定、醛基的检验等。通过实践操作,培养学生证据推理与模型认知的化
学学科核心素养。同时,初步了解一些测定有机化合物结构的现代手段,如核磁共振、红外光
谱等。并懂得有机化合物结构测定是有机化合物合成的重要环节,培养科学态度与社会责任的
化学学科核心素养。
高中有机化学学情分析还应对学生进行以下方面的评估和指导:
学情
(1) 加强对有机化合物结构与性质关系的理解:在掌握有机化合物结构测定的方法和程序
分析
的基础上,引导学生理解有机化合物结构与其物理性质、化学性质之间的密切关系。通过实践
操作和案例分析,培养学生的宏观辨识与微观探析的化学学科核心素养。
(2) 注重实验实践和创新能力培养:除了理论学习,还应组织学生进行有机化合物结构测
定的实验操作。让学生亲手进行样品处理、仪器使用、数据记录和分析等环节,培养学生的实
验实践能力和创新能力。同时,鼓励学生参与科研项目或实践活动,提高他们的动手能力和问
题解决能力。
(3) 引导阅读相关科研文献和进展:适当引导学生阅读有机化学领域的科研文献和进展,
了解有机化合物结构测定的最新技术和方法,以及在科学研究中的应用。通过拓宽学生的视
野,培养他们的科学探究精神。同时,鼓励学生关注学科前沿,培养他们的创新思维和批判性
思维教学过程
教学 设计意
教学活动
环节 图
【新课导入】
环
节
一
生
、
活
情
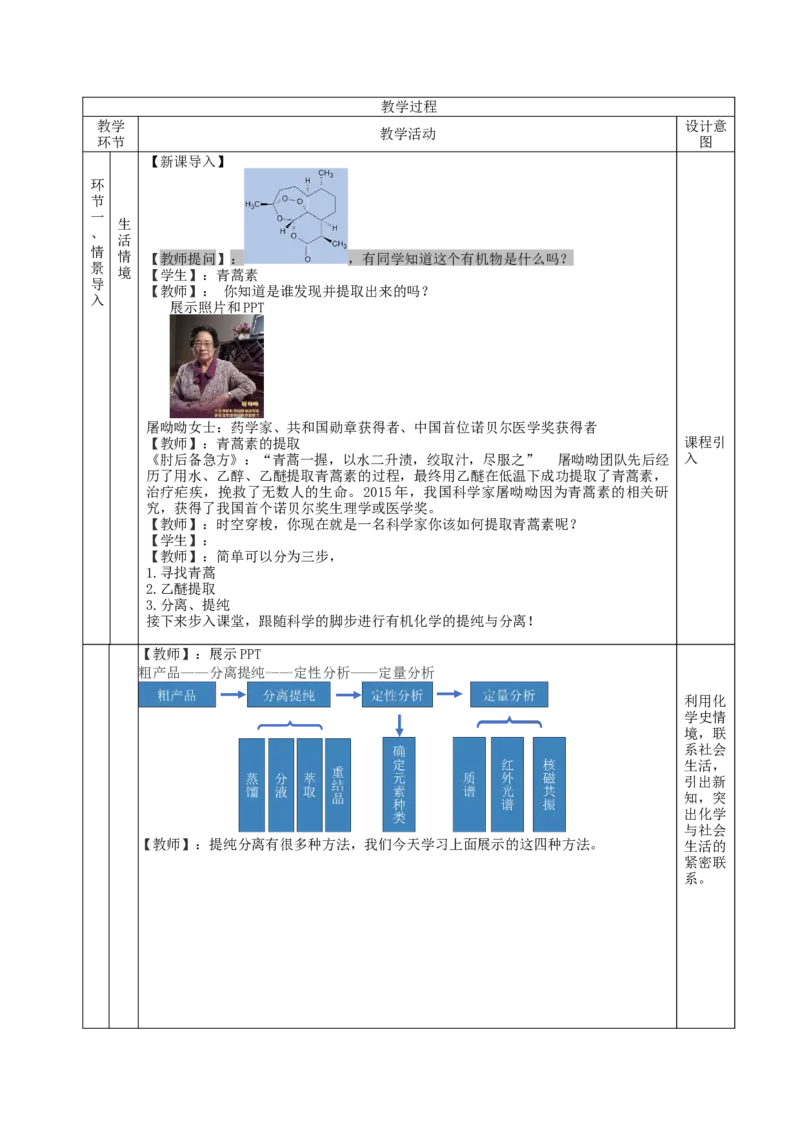
情 【教师提问】: ,有同学知道这个有机物是什么吗?
景
境 【学生】:青蒿素
导
【教师】: 你知道是谁发现并提取出来的吗?
入
展示照片和PPT
屠呦呦女士:药学家、共和国勋章获得者、中国首位诺贝尔医学奖获得者
【教师】:青蒿素的提取 课程引
《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之” 屠呦呦团队先后经 入
历了用水、乙醇、乙醚提取青蒿素的过程,最终用乙醚在低温下成功提取了青蒿素,
治疗疟疾,挽救了无数人的生命。2015年,我国科学家屠呦呦因为青蒿素的相关研
究,获得了我国首个诺贝尔奖生理学或医学奖。
【教师】:时空穿梭,你现在就是一名科学家你该如何提取青蒿素呢?
【学生】:
【教师】:简单可以分为三步,
1.寻找青蒿
2.乙醚提取
3.分离、提纯
接下来步入课堂,跟随科学的脚步进行有机化学的提纯与分离!
【教师】:展示PPT
粗产品——分离提纯——定性分析——定量分析
利用化
学史情
境,联
系社会
生活,
引出新
知,突
出化学
与社会
【教师】:提纯分离有很多种方法,我们今天学习上面展示的这四种方法。 生活的
紧密联
系。有 检测与
蒸馏
机 评价,
物 发现问
的 题,调
分 分液 控课
离 分离提纯 堂,提
提 高效
纯 萃取 率。
重结晶
环 【教师】:1. 适用范围:提纯互溶且 不同的液态有机物。
节 2. 适用条件:
二 有机物与杂质的沸点相差较大,一般差 以上。
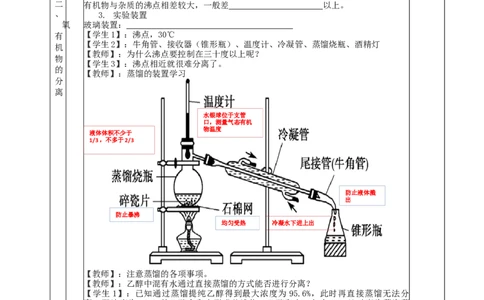
、 3. 实验装置
氧 玻璃装置:
有 【学生1】:沸点,30℃
【学生2】:牛角管、接收器(锥形瓶)、温度计、冷凝管、蒸馏烧瓶、酒精灯
机
【教师】:为什么沸点要控制在三十度以上呢?
物
【学生3】:沸点相近就很难分离了。
的
【教师】:蒸馏的装置学习
分
离
水银球位于支管
口,测量气态有机
物温度
液体体积不少于
1/3,不多于2/3
防止液体溅
出
防止暴沸
均匀受热 冷凝水下进上出
【教师】:注意蒸馏的各项事项。
【教师】:乙醇中混有水通过直接蒸馏的方式能否进行分离?
【学生1】:已知通过蒸馏提纯乙醇得到最大浓度为 95.6%,此时再直接蒸馏无法分
离。即浓度为95.5%的乙醇会和水形成共沸物,乙醇和水一起在78.1℃时变为蒸汽蒸
出,得到的还是95.6%的乙醇。
【教师】:补充;补充知识:共沸是指两组分或多组分的液体混合物以特定比例组成
时,在恒定压力下沸腾,其蒸气组成比例与溶液相同的现象。这实际是表明,此时沸腾
产生的蒸气与液体本身有着完全相同的组成。
【教师】:提问2:若想得到无水乙醇,应使用什么方法呢?
【学生2】向乙醇中加入生石灰,再进行蒸馏。
教师展示PPT和图片【教师】:这三种有什么用途呢?
球形冷凝管: 内管为若干个玻璃球连接起来,用于有机制备的回流,适用于各种沸点
的液体。
直形冷凝管:由内外组合的直玻璃管构成,多用于蒸馏蒸汽温度小于 140摄氏度的操
作,不用于回流。在其外管的上下两侧分别有连接管接头,用作出水口和进水口。
蛇形冷凝管:用于有机制备的回流,适用于沸点较低的液体。
【教师】:同学们还知道什么分离方法?
【教师】:1. 分液
(1)适用范围:分离两种 的液体的操作方法。
(2)实验装置:分液使用的仪器是 ,另外还需要烧杯与铁架台进行辅
助。
【学生1】:互不相容
【学生2】:分液漏斗
【教师】:注意事项:
①分液漏斗使用前要 ;
②分液时,先把下层液体从 放出,再把上层液体从 倒出。
【学生3】:检漏
【学生4】:下口上口
【教师】:(3)萃取
液-液萃取是利用溶质在两种互不相容的溶剂里溶解能力的不同,用一种溶剂(萃取
剂)将其从原溶剂中提取出来的方法。
萃取剂的要求
①萃取剂与原溶剂 ;
②溶质在萃取剂中的溶解度 在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应。
常用萃取剂: 等。
【学生1】:不互溶
【学生2】:远大于
【学生3】:乙醚 、 乙酸乙酯 、 二氯甲烷
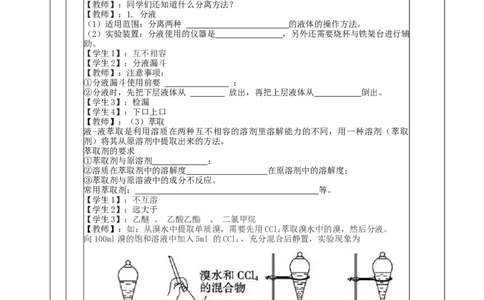
【教师】:如:从溴水中提取单质溴,需要先用CCl 萃取溴水中的溴,然后分液。
4
向100ml溴的饱和溶液中加入5ml 的CCl ,充分混合后静置,实验现象为
4
【学生1】:液体分层,下层橙红色,上层趋于无色。
【教师】:(4)重结晶
(1) 实验原理:是利用被提纯物质与杂质在同一溶剂中的 不同而将杂质除去
的方法。
(2) 溶剂的选择
①选用合适的溶剂,使得杂质在所选溶剂中溶解度 ,易于除去;②被提纯的有机化合物在所选溶剂中的溶解度受温度的影响 较大 ,能够进行
。
(3)溶剂要求: 。
【学生1】:溶解度
【学生2】:很大或很小
【学生3】:冷却结晶
固态有机混合物
【教师】①杂质在此溶剂中溶解度很小或者很大,易于除去。
②被提纯的有机物在此溶剂中的溶解度受温度影响较大,能够冷却结晶。
3.杂质在热过滤时被滤去,杂质留在母液中,不析出
【教师】:实例展示——重结晶法提纯苯甲酸
【问题】某粗苯甲酸样品中含有少量氯化钠和泥沙,提纯苯甲酸需要经过哪些步骤?
【资料卡片】
1、纯净的苯甲酸为无色结晶,其结构可表示为 ,
2、熔点122℃,沸点249℃。
3、苯甲酸微溶于水,易溶于乙醇、乙醚等有机溶剂。苯甲酸在水中的溶解度如下:
温度/℃ 25 50 75
溶解度/g 0.34 0.85 2.2
【教师】:【问题讨论】
① 重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
【学生1】: 苯甲酸在不同温度的蒸馏水中溶解度不同。加热溶解、趁热过滤、冷却
结晶、过滤洗涤、干燥称量。
【教师】:②溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
【学生2】:加热是为了增大苯甲酸的溶解度,使苯甲酸充分溶解。趁热过滤是为了防
止苯甲酸提前结晶析出。
【教师】:③实验操作中多次用到了玻璃棒,分别起到了哪些作用?
【学生3】:提示 搅拌和引流。
【教师】:④如何检验提纯后的苯甲酸中氯化钠已被除净
【学生4】:提示 用适量蒸馏水洗涤过滤器中的苯甲酸晶体,取少量第n次洗涤后的
液体,滴加几滴硝酸银溶液,观察是否有沉淀产生。若无沉淀产生,则氯化钠被除净。
【教师】:进行课堂练习
1、乙酰苯胺是一种具有解热镇痛作用的白色晶体,20 ℃时在乙醇中的溶解度为
36.9 g,在水中的溶解度如下表:
温 10
25 50 80
度/℃ 0
溶 0. 0. 3. 5.
解度/g 56 84 5 5
某种乙酰苯胺样品中混入了少量氯化钠杂质,下列提纯乙酰苯胺的方法正确的()A、用水溶解后分液 B、用乙醇溶解后过滤
C、用水作溶剂进行重结晶 D、用乙醇作溶剂进行重结晶
其 科学阅读:1906年Tswett 研究植物色素分离时提出色谱法概念;他在研究 利用已
他 植物叶的色素成分时,将植物叶子的萃取物倒入填有碳酸钙的直立玻璃管内,然后加 有知
常 识,预
入石油醚使其自由流下,结果色素中各组分互相分离形成各种不同颜色的谱带。溶有
见 测物质
绿色植物叶子色素的石油醚溶液自上而下地通过。结果植物色素便被碳酸钙吸附,分
分 的性
成三段不同颜色:绿色、黄色、黄绿色。再将碳酸钙吸附柱取出,并用乙醇洗脱,即
离 质,培
方 得色素的溶液:叶绿素、叶黄素、胡萝卜素。 养利用
法 按光谱的命名方式,这种方法因此得名为色谱法。以后此法逐渐应用于无色物质的分 所学解
( 离,“色谱”二字虽已失去原来的含义,但仍被人们沿用至今。 决实际
扩 【教师】:色谱法 问题的
展 能力。
又称层析法或色层法,是一种利用物质的溶解性、吸附性等特性的物理化学分离方
)
法。其分离原理是根据混合物的各组分在互不相溶的两相(称为固定相和流动相)作
用的流速差异作为分离依据的。
1.色谱法原理:利用吸附剂对不同有机物吸附作用的不同,分离、
提纯有机物的方法叫色谱法。色谱法是化学家分离、提纯有机物不可
实验探
缺少的方法。
究(验
证)预
测(猜
想),
2.常用的吸附剂:碳酸钙、硅胶、氧化铝、活性炭等。 培养观
察、分
析能
3.分类:根据物质在两相(气—液、液—液等)间溶解性或吸附能力不
力,体
同,分为纸上色谱法、薄层色谱法、气相色谱法、液相色谱法等。
验科学
研究的
基本方
【教师】:总结1.分离原则:把混合物中的各种物质逐一分离,得到 法。
各纯净物。分离过程中要尽量减少各物质的损失,各组分要尽量纯净。
2.分离方法
①物理方法:过滤、重结晶、升华、蒸发、蒸馏、分馏、萃取、渗析、盐析等
② 化学方法:加热分解、氧化还原转化、生成沉淀等
3.概念:提纯是采用物理或化学方法将混合物中的杂质除去的过程。分离和提纯的主
要区别为提纯过程中出去的杂质不需要恢复。 检测与
4.物质提纯的原则 评价,
通过反
①不增:在提纯过程中不增加新杂质
馈,发
②不减:在提纯过程中尽量不减少被提纯的物质
现问
③易分离:被提纯物质与杂质易分离
题,调
④易复原:被提纯物质易复原 控课
堂,提
高效
率。
【教师】
1.现有三组混合液:(1)乙酸乙酯和乙酸钠;(2)提纯苯甲酸;(3)溴化钠和单质溴
通过知
的水溶液,分离以上各混合液的正确方法依次是
识拓
A.分液、重结晶、蒸馏 B.萃取、重结晶、蒸馏 展,完
C.萃取、蒸馏、分液 D.分液、重结晶、萃取 善知识
【答案】D 建构,
【详解】(1)乙酸乙酯不溶于水,乙酸钠溶于水,可用分液的方法分离; 实现深
习 (2)提纯粗苯甲酸用重结晶法,主要步骤为:加热溶解,趁热过滤,冷却结晶,过滤, 度学
题 洗涤; 习。
专 (3)向溴化钠和单质溴的水溶液中加入萃取剂四氯化碳后,溴单质会溶解在四氯化碳题 中,四氯化碳和水互不相溶而分层,然后分液即可实现二者的分离;
练 故选D。
利用已
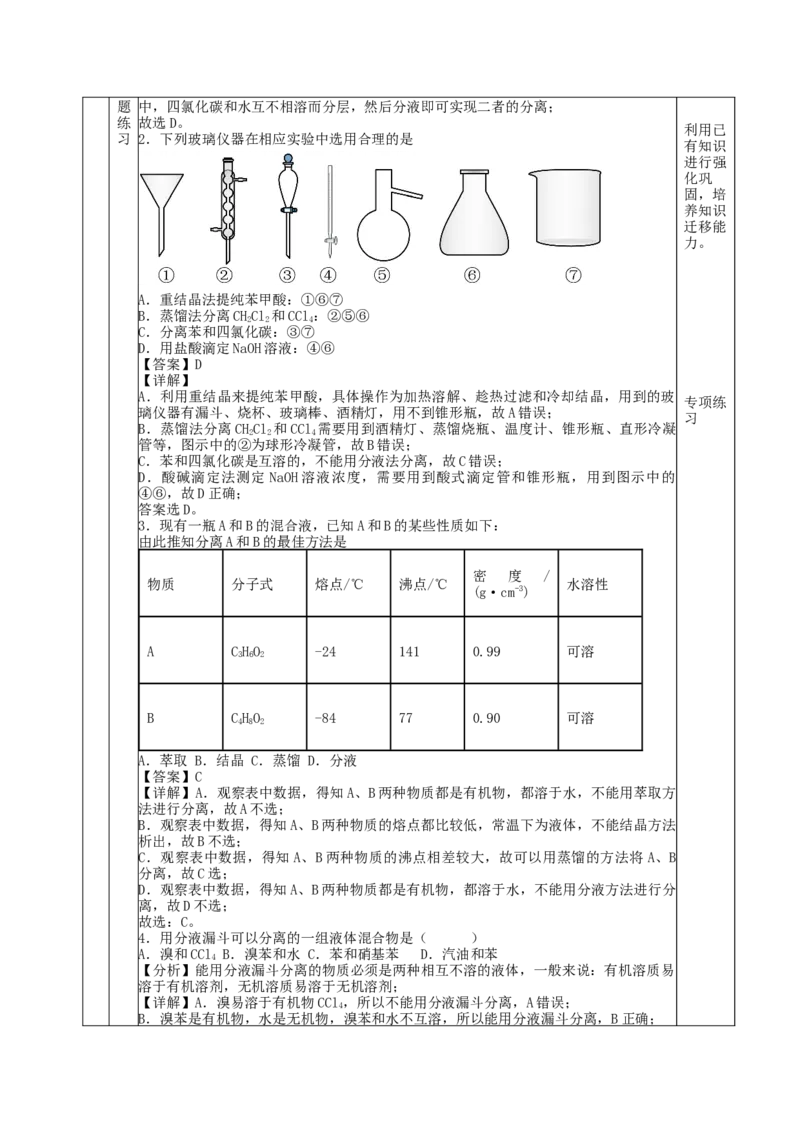
习 2.下列玻璃仪器在相应实验中选用合理的是
有知识
进行强
化巩
固,培
养知识
迁移能
力。
A.重结晶法提纯苯甲酸:①⑥⑦
B.蒸馏法分离CHCl 和CCl:②⑤⑥
2 2 4
C.分离苯和四氯化碳:③⑦
D.用盐酸滴定NaOH溶液:④⑥
【答案】D
【详解】
A.利用重结晶来提纯苯甲酸,具体操作为加热溶解、趁热过滤和冷却结晶,用到的玻
专项练
璃仪器有漏斗、烧杯、玻璃棒、酒精灯,用不到锥形瓶,故A错误;
习
B.蒸馏法分离CHCl 和CCl 需要用到酒精灯、蒸馏烧瓶、温度计、锥形瓶、直形冷凝
2 2 4
管等,图示中的②为球形冷凝管,故B错误;
C.苯和四氯化碳是互溶的,不能用分液法分离,故C错误;
D.酸碱滴定法测定 NaOH溶液浓度,需要用到酸式滴定管和锥形瓶,用到图示中的
④⑥,故D正确;
答案选D。
3.现有一瓶A和B的混合液,已知A和B的某些性质如下:
由此推知分离A和B的最佳方法是
密 度 /
物质 分子式 熔点/℃ 沸点/℃ 水溶性
(g·cm-3)
A CHO -24 141 0.99 可溶
3 6 2
B CHO -84 77 0.90 可溶
4 8 2
A.萃取 B.结晶 C.蒸馏 D.分液
【答案】C
【详解】A.观察表中数据,得知A、B两种物质都是有机物,都溶于水,不能用萃取方
法进行分离,故A不选;
B.观察表中数据,得知A、B两种物质的熔点都比较低,常温下为液体,不能结晶方法
析出,故B不选;
C.观察表中数据,得知A、B两种物质的沸点相差较大,故可以用蒸馏的方法将 A、B
分离,故C选;
D.观察表中数据,得知A、B两种物质都是有机物,都溶于水,不能用分液方法进行分
离,故D不选;
故选:C。
4.用分液漏斗可以分离的一组液体混合物是( )
A.溴和CCl B.溴苯和水 C.苯和硝基苯 D.汽油和苯
4
【分析】能用分液漏斗分离的物质必须是两种相互不溶的液体,一般来说:有机溶质易
溶于有机溶剂,无机溶质易溶于无机溶剂;
【详解】A.溴易溶于有机物CCl,所以不能用分液漏斗分离,A错误;
4
B.溴苯是有机物,水是无机物,溴苯和水不互溶,所以能用分液漏斗分离,B正确;C.苯和硝基苯都是有机物,所以苯和硝基苯能相互溶解,不能用分液漏斗分离,C错
误;
D.汽油和苯都是有机物能互溶,不能用分液漏斗分离,D错误;
故选B。
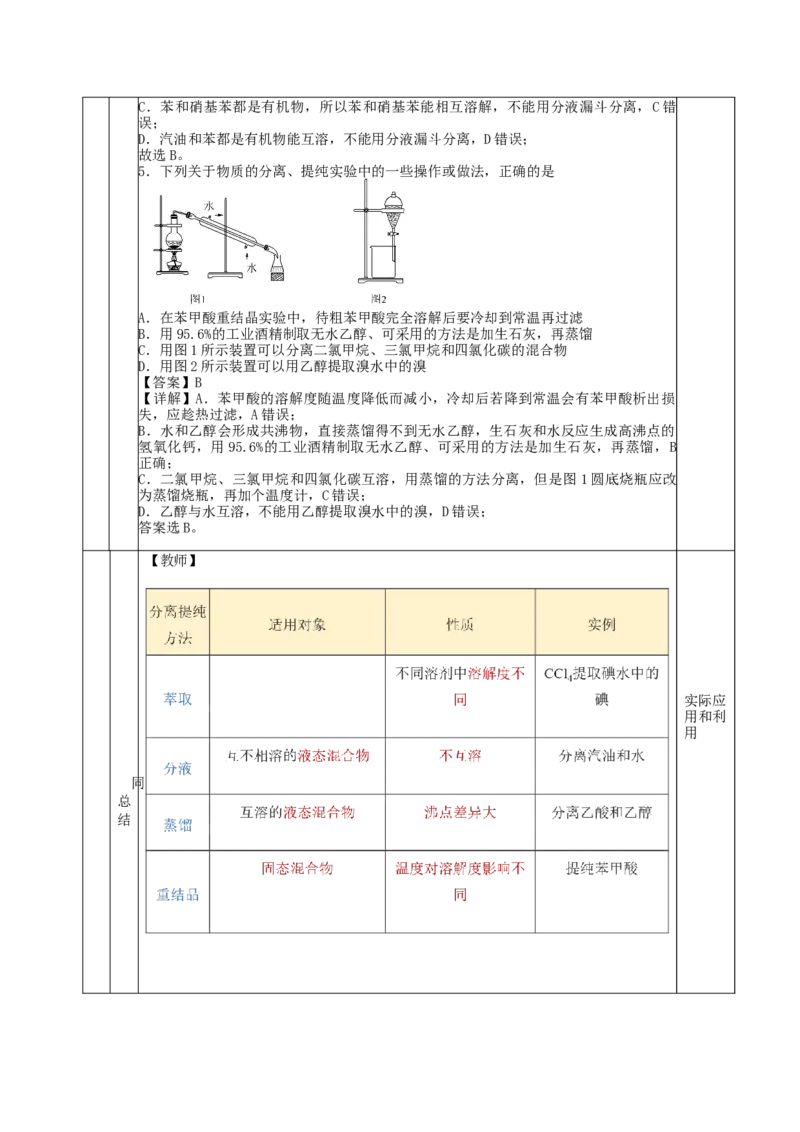
5.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
A.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
B.用95.6%的工业酒精制取无水乙醇、可采用的方法是加生石灰,再蒸馏
C.用图1所示装置可以分离二氯甲烷、三氯甲烷和四氯化碳的混合物
D.用图2所示装置可以用乙醇提取溴水中的溴
【答案】B
【详解】A.苯甲酸的溶解度随温度降低而减小,冷却后若降到常温会有苯甲酸析出损
失,应趁热过滤,A错误;
B.水和乙醇会形成共沸物,直接蒸馏得不到无水乙醇,生石灰和水反应生成高沸点的
氢氧化钙,用95.6%的工业酒精制取无水乙醇、可采用的方法是加生石灰,再蒸馏,B
正确;
C.二氯甲烷、三氯甲烷和四氯化碳互溶,用蒸馏的方法分离,但是图1圆底烧瓶应改
为蒸馏烧瓶,再加个温度计,C错误;
D.乙醇与水互溶,不能用乙醇提取溴水中的溴,D错误;
答案选B。
【教师】
实际应
用和利
用
同
总
结