文档内容
2.1.1 钠和钠的氧化物
知识点一 钠的物理性质
【例1】(2020·全国高一课时练习)下列有关钠的物理性质的叙述正确的有( )
①银白色金属 ②质软,可以用小刀切 ③熔点低于100℃ ④密度比水小 ⑤热和电的良导体
A.仅①②④⑤ B.仅①②③④
C.仅①③④⑤ D.①②③④⑤
【答案】D
【解析】①钠是I A族元素,为银白色金属单质,有金属光泽;②质地较软,可以用小刀切割;③将钠放
入水中,钠会立即熔成小球,说明熔点较低;④钠能浮于水面上,说明钠的密度比水的小;⑤钠是金属,
含有自由移动的电子,所以是热和电的良导体;故选D。
【一隅三反】
1.(2020·巩义市第四高级中学月考)实验室中对于少量金属钠的保存方法,正确的是
A.保存在水中 B.密封,保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中 D.密封,保存在煤油中
【答案】D
【解析】金属钠是活泼金属,可以和水、空气中O 等物质反应,因此少量的钠保存在煤油中,故选项D正
2
确。
2、关于钠的叙述中,正确的是( )
A.钠是银白色金属,熔点低,硬度大 B.钠与氧气反应时,产物是由O 的用量决定的
2
C.加热时,金属钠剧烈燃烧,产生黄色火焰 D.金属钠着火可以用泡沫灭火器或用干燥的沙土灭火
【答案】C
【解析】钠是银白色金属,密度小于水,熔点低,质软,性质活泼,在氧气中燃烧生成过氧化钠,过氧化钠与二氧化碳、水都反应,则不能用泡沫灭火器、干粉灭火器、水灭火。故选C。
3.(2020·全国高一单元测试)金属钠是实验室里常用的一种化学试剂,请回答下列问题:
(1)在实验室里,取用沉浸在煤油中的金属钠的操作方法是__________________。
(2)在空气中切开一块金属钠,可看到断面呈________色,具有金属光泽,但断面很快变____________,
主要是由于生成一薄层____________。
(3)若把钠放在石棉网上加热可观察到____________________________________,反应的化学方程式是
______________________________。
【答案】(1)用镊子夹取一小块钠,用滤纸吸干表面的煤油,放在玻璃片上,用小刀切下黄豆粒大小的
一小块钠,剩余的立刻放回原瓶
(2) 银白 暗 氧化钠
(3) 先熔化成光亮的银白色小球,后剧烈燃烧,发出黄色火焰,生成淡黄色固体 2Na+O
2
NaO
2 2
【解析】(1)钠质地软,易氧化,密度比煤油大,在实验室里,取用沉浸在煤油中的金属钠的操作方法
是:用镊子夹取一小块钠,用滤纸吸干表面的煤油,放在玻璃片上,用小刀切下黄豆粒大小的一小块钠,
剩余的立刻放回原瓶;
故答案为:用镊子夹取一小块钠,用滤纸吸干表面的煤油,放在玻璃片上,用小刀切下黄豆粒大小的一小
块钠,剩余的立刻放回原瓶;
(2)钠是银白色易氧化的金属,在空气中切开一块金属钠,可看到断面呈银白色,具有金属光泽,但断
面很快变暗,主要是由于生成一薄层氧化钠;
故答案为:银白; 暗 ; 氧化钠;
(3)钠在氧气中燃烧,生成过氧化钠,若把钠放在石棉网上加热可观察到先熔化成光亮的银白色小球,
后剧烈燃烧,发出黄色火焰,生成淡黄色固体,反应的化学方程式是2Na+O NaO;
2 2 2
故答案为:先熔化成光亮的银白色小球,后剧烈燃烧,发出黄色火焰,生成淡黄色固体 ;2Na+O
2
NaO。
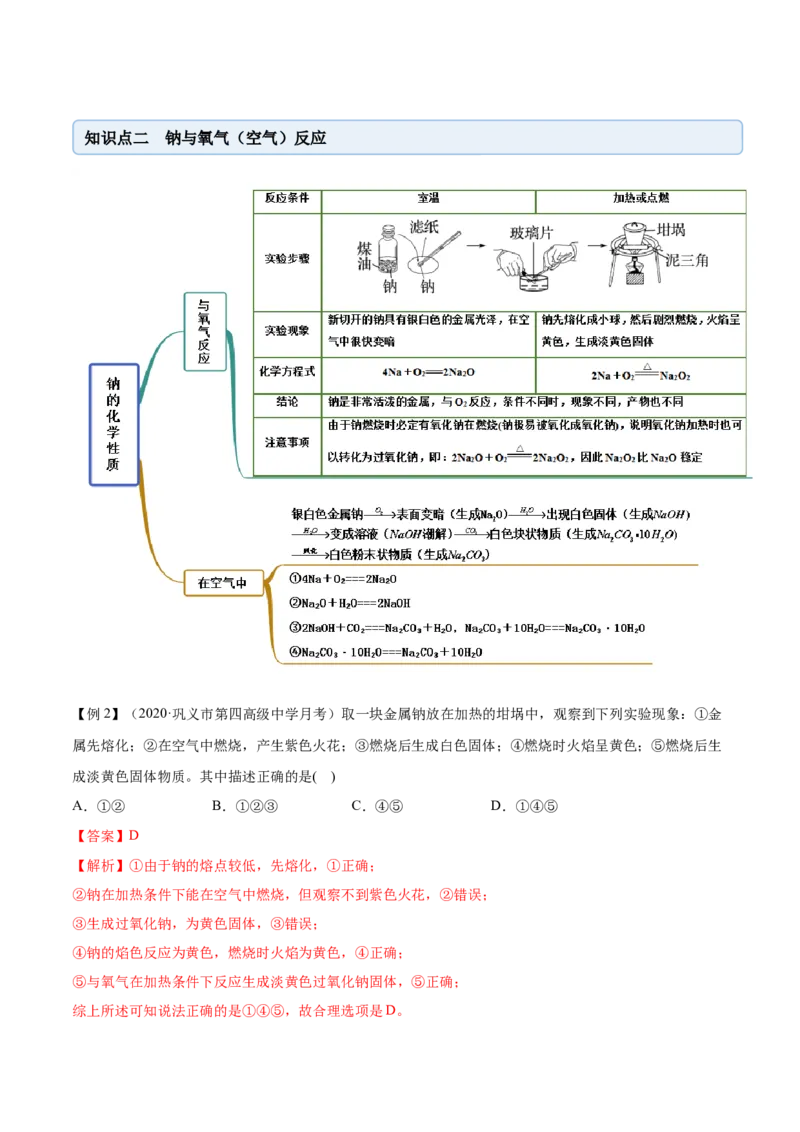
2 2知识点二 钠与氧气(空气)反应
【例2】(2020·巩义市第四高级中学月考)取一块金属钠放在加热的坩埚中,观察到下列实验现象:①金
属先熔化;②在空气中燃烧,产生紫色火花;③燃烧后生成白色固体;④燃烧时火焰呈黄色;⑤燃烧后生
成淡黄色固体物质。其中描述正确的是( )
A.①② B.①②③ C.④⑤ D.①④⑤
【答案】D
【解析】①由于钠的熔点较低,先熔化,①正确;
②钠在加热条件下能在空气中燃烧,但观察不到紫色火花,②错误;
③生成过氧化钠,为黄色固体,③错误;
④钠的焰色反应为黄色,燃烧时火焰为黄色,④正确;
⑤与氧气在加热条件下反应生成淡黄色过氧化钠固体,⑤正确;
综上所述可知说法正确的是①④⑤,故合理选项是D。1. 钠在加热条件下能在空气中燃烧,观察到黄色火焰,观察不到黄色火花
2.银白色金属钠在空气中被氧气氧化,生成白色固体Na O,颜色变暗,生成的Na O与空气中的水分结合
2 2
生成氢氧化钠,表面变白,氢氧化钠潮解,表面出现了液滴,氢氧化钠继续与空气中的CO 反应生成碳酸
2
钠晶体,失水后变为白色粉末,据此分析判断。
【一隅三反】
1.(2020·陕西榆阳·榆林十二中月考)下列关于金属 的叙述中,说法正确的是( )
A. 在空气中燃烧,发出黄色火焰 B. 在空气中燃烧,产物是
C. 是银白色金属,硬度大,熔点高 D. 常温和加热时与氧气反应,产物一样
【答案】A
【解析】A. 钠在空气中燃烧,发出黄色火焰,A项正确;
B. 钠在空气中燃烧生成的是过氧化钠,B项错误;
C. 钠的硬度小,熔点低,C项错误;
D. 在空气中放置生成氧化钠,在空气中燃烧生成过氧化钠,D项错误。答案选A。
2.(2020·全国课时练习)金属钠长期放置在空气中,在反应过程中不能生成的物质是( )
A. B.NaOH C.NaCl D.
【答案】C
【解析】金属钠长期放置在空气中,金属钠与空气中氧气反应生成氧化钠变暗,氧化钠与空气中的水反应
生成氢氧化钠白色固体,氢氧化钠吸收空气中的水蒸气变成NaOH小液滴,氢氧化钠小液滴吸收空气中的
二氧化碳生成NaCO·10H O晶体,NaCO·10H O风化变成NaCO 固体,在反应过程中不能生成NaCl,
2 3 2 2 3 2 2 3
故选C。
3.(2020·全国课时练习)某同学将一小块金属钠置于表面皿上,并露置于空气中,观察到下列现象:
银白色 变灰暗 变白 表面出现液滴 白色固体 白色粉末,下列说法正确的是
( )
A.过程①钠转化为过氧化钠
B.过程③是碳酸钠吸收空气中的水蒸气形成溶液C.过程④只发生了物理变化
D.如果时间足够长,最后得到的白色粉末是NaCO
2 3
【答案】D
【解析】A. 过程①钠与氧气常温下反应,生成了白色固体氧化钠,A项错误;
B. 过程③是生成的NaO与空气中的水分结合生成氢氧化钠,表面变白,氢氧化钠潮解,表面出现了液滴,
2
B项错误;
C. 过程④氢氧化钠继续与空气中的CO 反应生成碳酸钠晶体,发生了化学变化,C项错误;
2
D. 如果时间足够长,碳酸钠晶体失水,最后得到的白色粉末是NaCO,D项正确;答案选D。
2 3
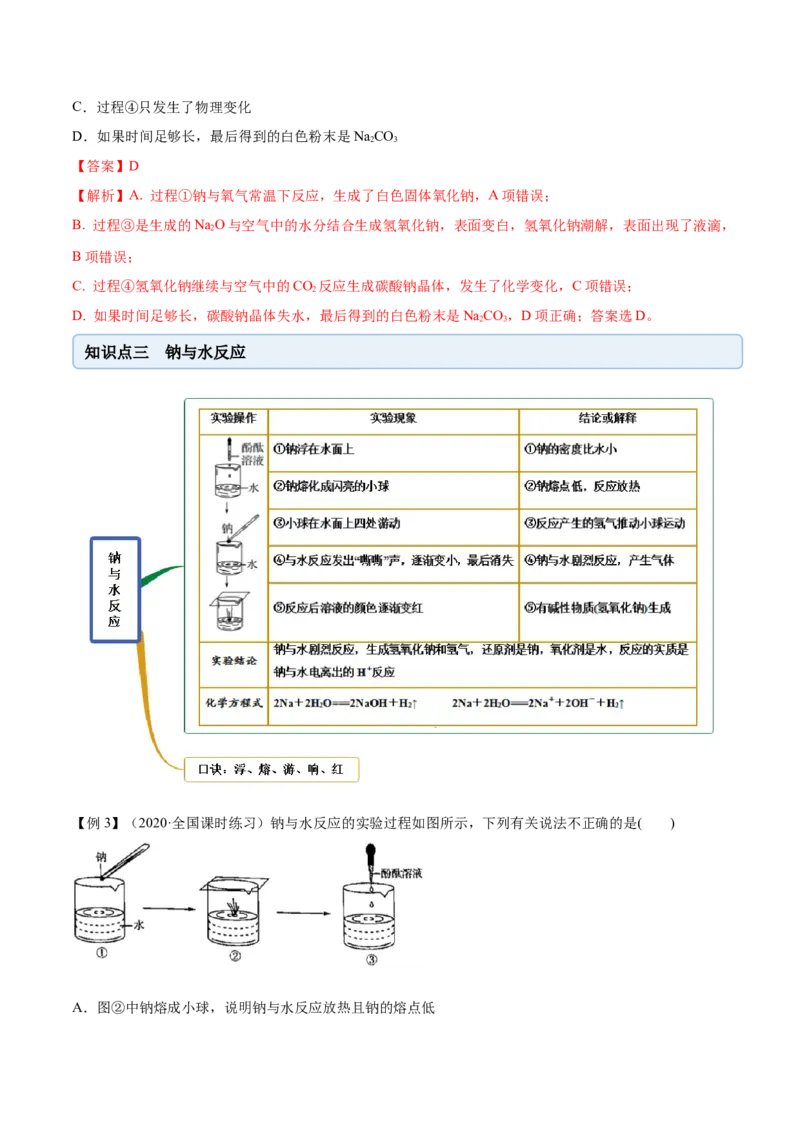
知识点三 钠与水反应
【例3】(2020·全国课时练习)钠与水反应的实验过程如图所示,下列有关说法不正确的是( )
A.图②中钠熔成小球,说明钠与水反应放热且钠的熔点低B.图②中钠球四处游动,说明钠的密度比水的小
C.图③中滴加酚酞溶液后溶液变红,说明有碱性物质生成
D.钠与水反应的化学方程式是2Na+2HO=2NaOH+H ↑
2 2
【答案】B
【解析】A.图②中钠熔成小球所需热量是由钠与水反应放出的,此时水未沸腾,说明钠的熔点低,A正
确;
B.图②中钠球四处游动是因为钠与水反应产生了气体,气体推动钠球运动,B错误;
C.图③中滴加酚酞溶液后溶液变红,说明有碱性物质生成,C正确;
D.钠与水反应的化学方程式是2Na+2HO=2NaOH+H ↑,D正确;故选B。
2 2
【一隅三反】
1.(2020·全国课时练习)钠与水反应时产生如下现象,其中正确的一组是( )
①钠浮在水面上 ②钠沉入水底 ③钠熔化成闪亮的小球 ④钠球在水面上四处游动 ⑤发出“嘶嘶”的
响声 ⑥滴入酚酞后溶液显红色
A.①②③④⑤ B.全部 C.①③④⑤⑥ D.①③④⑥
【答案】C
【解析】①钠的密度小于水的密度,钠与水反应时,钠浮在水面上,故正确;
②钠的密度小于水的密度,钠与水反应时,钠浮在水面上,故错误;
③钠与水的反应为放热反应,钠的熔点低,放出的热量使钠熔化成闪亮的小球,故正确;
④钠与水反应生成氢氧化钠和氢气,反应生成的氢气使钠球在水面上四处游动,故正确;
⑤钠与水反应生成氢氧化钠和氢气,反应生成的氢气与水面摩擦发出“嘶嘶”响声,故正确;
⑥钠与水反应生成氢氧化钠和氢气,反应生成的氢氧化钠使酚酞溶液变红,故正确;
①③④⑤⑥正确,故答案为:C。
2.(2020·全国课时练习)某化学研究性学习小组设计了如图所示的实验装置,目的是做钠与水反应的实
验并验证钠的物理性质。请回答下列问题:
(1)实验开始时,欲使钠与水接触发生反应,应如何操作?_____________________________________。
(2)反应开始后,试管中能观察到的实验现象是__________(填标号)。A.钠在水层中反应,熔成小球并四处游动
B.钠在两液体界面处反应,熔成小球并上下跳动
C.钠块不断减小直至消失
D.钠停留在煤油层中不反应
E.煤油中有气泡产生
(3)通过上述现象,能够验证钠的哪些物理性质?__________________________________________。
【答案】(1)按住橡皮塞,将大头针拔出,使钠块落入液体中
(2) BCE
(3) 熔点低,密度比水的小、比煤油的大
【解析】(1)钠的密度比煤油大,比水小,实验开始时,欲使钠与水接触,应该按住橡皮塞,将大头针
拔出,使钠块落入液体中,钠沉入煤油中,在两液体界面处与水接触,故答案为:按住橡皮塞,将大头针
拔出,使钠块落入液体中;
(2)A.钠的密度比水的小、比煤油的大,钠在两液体界面处反应,熔成小球并上下跳动,故A错误;
B.钠的密度比水的小、比煤油的大,钠在两液体界面处反应,熔成小球并上下跳动,故B正确;
C.钠和水反应生成氢氧化钠和氢气,钠块不断反应,减小直至消失,故C正确;
D.钠的密度比水的小、比煤油的大,钠在两液体界面处反应,熔成小球并上下跳动,故D错误;
E.钠和水反应生成的氢气不溶于水和煤油,煤油中有气泡产生,故E正确;
BCE正确,故答案为:BCE;
(3)钠熔成小球、在两液体界面处反应,说明钠的密度比水的小、比煤油的大,熔点低,故答案为:熔
点低,密度比水的小、比煤油的大。
3.用如图所表示的方法研究金属钠与水反应的性质,其中A是用带孔的铝箔包着的小块的金属钠.
(1)从大块钠上取下的小块钠要用滤纸擦一擦,这样做的目的是_______________.
(2)包裹钠块的铝箔要预先扎上足够多的小孔,若孔数不够,可能出现的不良后果是________.假如在实验
刚开始就将镊子松开拿出水面,A表现出的现象是________,出现这种现象的原因是___________
(3)据预测,钠与水反应生成氢气和氢氧化钠.
①证明生成的气体是氢气的实验方法是____________________________;
②证明生成氢氧化钠的实验方法和相应的现象是______________________________;
(4)如果用饱和碳酸钠溶液代替水做钠的性质实验的研究.①有金属钠参加的化学反应的方程式是______________________________________;
②其他化学反应的方程式是(假设溶液的温度保持不变)_________________________;
③再向烧杯中加入足量的稀盐酸,化学反应的化学方程式是_____________________.
【答案】(1)擦去钠表面上的煤油,避免影响实验效果
(2)发生爆炸 A浮在水面上 钠的密度小于水的密度,反应生成的氢气增大了A所受的浮力
(3)①在气体充满试管时,在水中单手握管、拇指封口,管口朝下拿出水面.在火焰的近处横置试管,
管口靠近火焰,松开拇指点燃气体
②向烧杯内的溶液中滴入3滴酚酞试液,溶液显红色
(4)①2Na+2HO===2NaOH+H↑
2 2
② NaCO+10HO===Na CO·10H O
2 3 2 2 3 2
③NaOH+HCl===NaCl+HO,NaCO+2HCl===2NaCl+HO+CO↑
2 2 3 2 2
【解析】(1)为了防止金属钠与氧气、水等反应,实验室中一般将金属钠保存在煤油中.在使用金属钠时,
为了不影响实验效果,一般要用滤纸擦净其表面上的煤油.
(2)金属钠具有很强的还原性.常温下钠和水剧烈反应生成氢氧化钠和氢气,并放出大量的热,在封闭的空
间内极易发生爆炸;金属钠的密度小于水的密度,在水中浮于水面上;钠与水反应生成的氢气更增大了A
所受的浮力.
(3)①收集氢气以及氢气的检验方法为:在气体集满试管时,在水中单手握试管、拇指堵住试管口,管
口朝下拿出水面,在管口的近处横置试管,管口靠近火焰,松开拇指;
②氢氧化钠是碱,遇酚酞变红色,故答案为向烧杯内的溶液中滴入3滴酚酞,溶液变红色;
(4)在饱和碳酸钠溶液中加入钠后,钠与水反应生成氢气和氢氧化钠,再加盐酸,盐酸分别与氢氧化钠、碳
酸钠发生反应,反应方程式分别为:2Na+2HO=2NaOH+H ↑;NaCO+10H O=Na CO·10H O;NaOH+
2 2 2 3 2 2 3 2
HCl===NaCl+HO,NaCO+2HCl=2NaCl+CO ↑+H O.
2 2 3 2 2
知识点四 钠与酸碱盐反应【例4】(2020·全国课时练习)将金属钠分别投入下列物质的溶液中,有气体放出,且溶液质量减轻的是
A.稀盐酸 B.KSO C.CuCl D.NaOH 溶液
2 4 2
【答案】C
【解析】A、钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H ↑,根据方程式知,溶液增加的质量=m
2
(Na)-m(H),A错误;
2
B、钠与硫酸钾溶液反应的实质是钠与水的反应,钠和水的反应方程式为:2Na+2HO═2NaOH+H↑,所以
2 2
溶液质量增加,溶液增加的质量=m(Na)-m(H),B错误;
2
C、钠先和水的反应方程式为:2Na+2HO═2NaOH+H↑,生成的氢氧化钠和氯化铜反应,方程式为:
2 2
2NaOH+CuCl ═2NaCl+Cu(OH)↓,将两个方程式相加:2Na+2HO+CuCl ═H ↑+2NaCl+Cu(OH)↓,由
2 2 2 2 2 2
方程式知,溶液的质量减轻, C正确;
D、钠与NaOH溶液反应的实质是钠与水的反应,钠和水的反应方程式为:2Na+2HO═2NaOH+H↑,所以
2 2
溶液质量增加,溶液增加的质量=m(Na)-m(H),D错误。
2
答案选C。
【一隅三反】
1.(2019·渭南高级中学月考)将一小块钠放入下列溶液时,既能产生气体又不会出现浑浊的是( )
A.硫酸钠溶液 B.氯化铁溶液 C.硫酸铜溶液 D.氯化镁溶液
【答案】A
【解析】A.钠和硫酸钠溶液的反应为:2Na+2HO=2NaOH+H ↑,NaOH与硫酸钠不反应,无沉淀生成,
2 2
不会出现浑浊,A符合题意;
B.钠和水生成的NaOH和H,NaOH再与氯化铁溶液反应,Fe3++3OH-=Fe(OH) ↓,生成红褐色沉淀,B不
2 3
符合题意;
C.钠和水生成的NaOH和H,再与硫酸铜溶液反应,Cu2++2OH-=Cu(OH) ↓,生成蓝色沉淀,C不符合题
2 2意;
D.钠和水生成的NaOH和H,再与氯化镁溶液反应,Mg2++2OH-=Mg(OH) ↓,生成白色沉淀,D不符合题
2 2
意;答案选A。
2.(2020·南昌县莲塘第二中学期末)下列实验产生白色沉淀的是
①将一小块金属钠投入CuSO 溶液中②向足量NaOH 溶液中滴加少量硫酸铝溶液③隔绝空气向FeCl 溶液
4 2
中滴加NaOH 溶液④ 向NaHCO 溶液中投入少量熟石灰
3
A.②③ B.③④ C.①② D.①②③④
【答案】B
【解析】①将一小块金属钠投入CuSO 溶液中生成蓝色的氢氧化铜沉淀,错误;
4
②向足量NaOH 溶液中滴加少量硫酸铝溶液,反应生成偏铝酸钠,无沉淀生成,错误;
③隔绝空气向FeCl 溶液中滴加NaOH 溶液生成白色的氢氧化亚铁沉淀,正确;
2
④ 向NaHCO 溶液中投入少量熟石灰反应生成碳酸钙白色沉淀,正确。
3
故选B。
3.(2020·全国课时练习)向分别盛有100mL水、100mL盐酸、100mL 溶液的X、Y、Z三个烧
杯中分别投入1.15g Na,Na完全反应,下列说法正确的是( )
A.三个烧杯中一定均会发生反应:
B.三个烧杯中的反应,相比而言,X中的反应最剧烈
C.Z烧杯中一定会有 沉淀生成
D.三个烧杯中生成的气体的质量不相同
【答案】C
【解析】A.钠投入溶液中,发生的反应实质是钠与酸或者水电离产生的氢离子的反应,当酸反应完后才
与溶剂水反应,当酸足量时,钠只与酸反应,离子方程式为:2Na+2H+=2Na++H ↑,故A错误;
2
B.盐酸为酸,硫酸铜为强酸弱碱盐水解显酸性,所以X、Y、Z三种溶液中,氢离子浓度由大到小的顺序
为:Y> Z> X,氢离子浓度越大,反应越剧烈,水中氢离子浓度最小,所以反应最缓和,故B错误;
C.钠与硫酸铜溶液反应方程式为:2Na+2HO=2NaOH+H ↑,2NaOH+CuSO =Cu(OH) ↓+Na SO 故C正确;
2 2 4 2 2 4
D.依据得失电子守恒,可知相同量的钠失去电子数相同,生成氢气的量相同,故D错误;故选C。
知识点五 氧化钠与过氧化钠【例5】(2019·渭南高级中学月考)NaO和NaO 在下列哪些性质上是相同的( )
2 2 2
A.NaO和NaO 中氧元素化合价
2 2 2
B.与盐酸反应所观察到现象
C.长期置放在空气中的最终产物
D.与水反应后滴加酚酞所观察到的现象
【答案】C
【解析】A.NaO中O的化合价为-2价,NaO 中O的化合价为-1价,氧元素化合价不同,故A不选;
2 2 2
B.氧化钠与盐酸反应生成氯化钠、水,没有气体放出;过氧化钠与盐酸反应生成氯化钠、水和氧气,产
生气泡,现象不相同,故B不选;
C.氧化钠和过氧化钠长期置放在空气,都会变质,最终都生成碳酸钠,最终产物相同,故C选;
D.氧化钠和水反应生成氢氧化钠,滴加酚酞后,溶液变红色;过氧化钠和水反应生成氢氧化钠和氧气,
滴加酚酞溶液都变红,随后又褪色,现象不同,故D不选;故选C。
【一隅三反】
1.(2020·全国课时练习)下列关于 和 的叙述正确的是( )A.利用加热法可除去 中少量的 杂质
B. 和 均为白色固体
C. 、 中阳离子与阴离子的数目比分别为2∶1和1∶1
D.将含等质量钠元素的 和 固体加入等量且足量的水中,充分反应后所得溶液中溶质的质量
分数相等
【答案】D
【解析】A.加热时NaO与O 会反应生成NaO,无法除去NaO中少量的NaO 杂质,A错误;
2 2 2 2 2 2 2
B. 为淡黄色固体,B错误;
C.NaO是离子化合物,由Na+和O2-通过离子键结合而成,阳离子与阴离子的数目比是2∶1;NaO 也是
2 2 2
离子化合物,是由Na+和 通过离子键结合而成,阳离子与阴离子的数目比也是2∶1,C错误;
D.由反应方程式NaO+HO=2NaOH、2NaO+2H O=4NaOH+O ↑可知:钠元素的质量相同时,NaO、
2 2 2 2 2 2 2
NaO 与足量水反应生成的溶质(NaOH)的质量相同,且反应后所得溶液的质量也相同,故最终所得溶液中
2 2
溶质的质量分数相等,D正确;故答案为D。
2.(2020·全国课时练习)无色的混合气体甲,可能含NO、CO、NO 、N 中的几种,将一定量的甲气体
2 2 2
经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
A.NO 、N B.NO、CO
2 2 2
C.NO 、CO D.NO、CO、N
2 2 2 2
【答案】B
【解析】二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮;二氧化碳可以和过氧化
钠反应生成碳酸钠和氧气,反应的化学方程式为:2NaO+2CO =2Na CO+O ,一氧化氮无色,与氧气立
2 2 2 2 3 2
即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有NO、CO,排水法收集气体,
2
广口瓶被上升的水注满,说明没有N,所以甲气体的组成为:NO、CO,故答案为B。
2 2
3.(2020·全国高一课时练习)有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示
的装置进行实验。通入SO 气体,将带火星的木条插入试管C中,木条复燃。
2请回答下列问题:
(1)第1小组同学认为NaO 与SO 反应生成了NaSO 和O,该反应的化学方程式是__。
2 2 2 2 3 2
(2)请设计一种实验方案,证明NaO 与SO 反应生成的白色固体中含有NaSO :__。
2 2 2 2 3
(3)第2小组同学认为NaO 与SO 反应除了能生成NaSO 与O 外,还有NaSO 生成。提出有NaSO 生成
2 2 2 2 3 2 2 4 2 4
这一猜想的理由是__。为检验是否有NaSO 生成,他们设计了如下方案:
2 4
上述方案是否合理?__(填“合理”或“不合理”)。请简要说出两点理由:①__;②__。
【答案】(1)2NaO+2SO=2Na SO +O
2 2 2 2 3 2
(2)取少量反应后的白色固体,加入足量稀硫酸(或稀盐酸),将产生的气体通入品红溶液,若品红溶液褪
色,说明白色固体中含有NaSO
2 3
(3) 过氧化钠具有强氧化性 不合理 稀硝酸能BaSO 将氧化为BaSO 若反应后的固体中还残
3 4
留NaO,它溶于水后能将SO 氧化成SO
2 2
【解析】(1)第1小组同学认为NaO 与SO 反应生成了NaSO 和O,该反应的化学方程式是2NaO +
2 2 2 2 3 2 2 2
2SO = 2Na SO +O ;故答案为:2NaO+2SO=2Na SO +O 。
2 2 3 2 2 2 2 2 3 2
(2)证明含有 即证明含有 , 与 反应生成能使品红溶液褪色的有刺激性气味的无色气体
;故答案为:取少量反应后的白色固体,加入足量稀硫酸(或稀盐酸),将产生的气体通入品红溶液,
若品红溶液褪色,说明白色固体中含有NaSO 。
2 3
(3)过氧化钠具有强氧化性,因此二氧化硫可能被过氧化钠氧化生成硫酸钠,该项实验的目的是检验是否有
生成,即检验是否存在 。但 易被反应后固体中残留的 或加入的稀 氧化为 ,所以该实验方案不合理;故答案为:过氧化钠具有强氧化性;不合理;稀硝酸能BaSO 将
3
氧化为BaSO;若反应后的固体中还残留NaO,它溶于水后能将SO 氧化成SO 。
4 2 2
知识点六 过氧化钠与水反应
【例6】(2020·全国课时练习)如图装置,试管中盛有水,气球a中盛有干燥的NaO 颗粒。U形管中注
2 2
有浅红色的水。将气球用橡皮筋紧缚在试管口。实验时将气球中的NaO 抖落到试管b的水中,将发现的
2 2
现象是( )A.U形管内浅红色退去 B.试管内溶液变红
C.U形管水位dc
【答案】C
【解析】A、NaO 与水反应:2NaO+2HO=4NaOH+O↑,气球a被吹大,A不符合题意;B、NaO 与
2 2 2 2 2 2 2 2
水反应生成NaOH,溶液变红,因为NaO 具有强氧化性,能把有色物质氧化成无色物质,有可能发生,B
2 2
不符合题意;C、U形管不是试管,因此U形管中红色不会退去,此实现现象不会发生,C符合题意;D、
NaO 与HO反应是放热反应,广口瓶中气体受热膨胀,因此U形管中d的水位高于c,此实验现象能够发
2 2 2
生,D不符合题意。知识点七 过氧化钠与H 、CO燃烧产物反应的计算
2
【例7】(2020·全国课时练习)在一密闭容器中有CO、H、O 共16.5g和足量的NaO,用电火花引燃,
2 2 2 2
使其完全反应,NaO 增重7.5g,则原混合气体中O 的质量分数是( )
2 2 2
A.33.3% B.40% C.36% D.54.5%
【答案】D
【解析】CO燃烧生成二氧化碳,反应方程式为2CO+O═2CO ,二氧化碳与过氧化钠发生反应
2 2
2CO+2Na O=2Na CO+O ,方程式相加的CO+Na O=Na CO,固体增加的质量为相当于CO的质量,氢
2 2 2 2 3 2 2 2 2 3
气燃烧生成水,反应方程式为2H+O ═2H O,水与过氧化钠发生反应2HO+2Na O=4NaOH+O,二者相加
2 2 2 2 2 2 2
可得H+Na O=2NaOH,固体增加的质量为相当于H 的质量,CO、H、O 用电火花引燃,使其完全反应,
2 2 2 2 2 2
NaO 增重7.5g就是原混合气体中CO、H 的质量和,所以混合气体中氧气的质量为16.5g-7.5g=9g,氧气
2 2 2
的质量分数为 9g/16.5g×100%=54.5%. D项正确;答案选D。
【一隅三反】
1.(2020·全国课时练习)(1)将ag CO、H 的混合气体在足量O 中充分燃烧,把产生的气体
2 2
(>100℃)通入足量的NaO 固体中,完全反应后,NaO 的质量增加___________g。
2 2 2 2
(2)30g甲醛(HCHO)在足量的O 中充分燃烧,把产生的气体(>100℃)通入足量的NaO 固体中,完
2 2 2
全反应后,NaO 的质量增加___________g。
2 2
【答案】(1)a (2) 30【解析】(1)由下列反应方程式:2CO+O 2CO,2NaO+2CO =2Na CO+O ,可得CO+
2 2 2 2 2 2 3 2
NaO=Na CO,同理,2H+O =2H O,2NaO+2H O=4NaOH+O ↑,H+ Na O=2NaOH,所以NaO 与
2 2 2 3 2 2 2 2 2 2 2 2 2 2 2 2
CO、HO反应后增加的质量与原混合气体CO、H 的质量相同。
2 2 2
(2)甲醛(HCHO)可以看成是(CO) (H ),充分燃烧后的气体与足量的NaO 完全反应,NaO 增加的质量与
m 2 n 2 2 2 2
原甲醛的质量相同。
2.(2019·夏津县双语中学高一月考)将2.8 g CO和0.2 g H 在足量的氧气中充分燃烧,使生成的CO 和水
2 2
蒸气通过过量的过氧化钠,完全反应后固体的质量变化量是( )
A.增加了3.0 g B.减少了3.0 g C.增加了2.6 g D.减少了2.6 g
【答案】A
【解析】H 燃烧生成水,水再与过氧化钠反应,反应方程式为2H+O 2HO、2NaO+2HO=4NaOH
2 2 2 2 2 2 2
+O↑,可认为总反应方程式为H+NaO=2NaOH,固体增加的质量即为H 的质量;CO燃烧生成CO,
2 2 2 2 2 2
CO 再与过氧化钠反应,反应方程式为2CO+O 2CO、2NaO+2CO=2Na CO+O,可认为总反应
2 2 2 2 2 2 2 3 2
方程式为CO+NaO=Na CO,固体增加的质量即为CO的质量。综上分析可知,最终固体增加的质量为
2 2 2 3
H、CO的质量和,即为2.8 g+0.2 g=3.0g。答案选A。
2
3.(2019·上饶中学高一月考)在一定条件下,使CO和O 的混合气体26克充分反应,所得混合物在常温
2
下与足量的NaO 固体反应,结果固体增重14克,则原混合气体中的CO和O 的质量比是( )
2 2 2
A.4 :9 B.7 :4 C.7 :6 D.6 :7
【答案】C
【解析】由反应2NaO+2CO =2Na CO+O ,可知混合物在常温下跟足量的NaO 固体反应生成固体为
2 2 2 2 3 2 2 2
NaCO,1molNa O 生成1molNa CO,质量增加28g,恰好为CO的质量,
2 3 2 2 2 3
固体增重14g,说明混合气体中CO为14g,则O 为26g-14g=12g,
2
原混合气体中CO和O 的质量比为14g:12g=7:6,故选C。
2