文档内容
第二章 《化学平衡》教学设计
第二节
第四课时 化学平衡图像
课题: 2.2.4 化学平衡图像 课时 1 授课年级 高二
课标要 能运用浓度、压强、温度对化学平衡的影响规律,推测平衡 移动方向及浓度、转化率等相关
求 物理量的变化,能讨论化学反应条 件的选择和优化。
化学平衡图像是描述化学反应中物质浓度随时间变化的一种图形表示方法。在教材中,化学平
衡图像通常包括以下几种类型:
1. 反应速率与时间的关系图:这种图像表示了在一定条件下,反应物浓度随时间的变化情况。
通过观察图像,可以了解反应的快慢以及达到平衡所需的时间。
2. 反应速率与温度的关系图:这种图像表示了在一定压力下,反应速率随温度的变化情况。通
过观察图像,可以了解反应速率对温度的敏感性,以及反应的活化能。
3. 反应物浓度与时间的关系图:这种图像表示了在一定条件下,反应物浓度随时间的变化情
况。通过观察图像,可以了解反应物的消耗速度以及达到平衡所需的时间。
4. 生成物浓度与时间的关系图:这种图像表示了在一定条件下,生成物浓度随时间的变化情
教材 况。通过观察图像,可以了解生成物的生成速度以及达到平衡所需的时间。
分析 5. 反应物浓度与压力的关系图:这种图像表示了在一定温度下,反应物浓度随压力的变化情
况。通过观察图像,可以了解反应物浓度对压力的敏感性,以及反应的K值(平衡常数)。
6. 生成物浓度与压力的关系图:这种图像表示了在一定温度下,生成物浓度随压力的变化情
况。通过观察图像,可以了解生成物浓度对压力的敏感性,以及反应的K值(平衡常数)。
7. 反应物浓度与温度的关系图:这种图像表示了在一定压力下,反应物浓度随温度的变化情
况。通过观察图像,可以了解反应物浓度对温度的敏感性,以及反应的K值(平衡常数)。
8. 生成物浓度与温度的关系图:这种图像表示了在一定压力下,生成物浓度随温度的变化情
况。通过观察图像,可以了解生成物浓度对温度的敏感性,以及反应的K值(平衡常数)。
通过对这些化学平衡图像的分析,学生可以更好地理解化学反应的动态过程,掌握化学反应规
律,为进一步学习化学反应动力学、化学平衡计算等知识打下基础。
1.学会分析化学反应速率与化学平衡图像
教学目
2.由定性和定量结合的方式揭示化学平衡及移动的本质特征。
标
3.能运用相关的图像解答化学反应原理的相关问题。
教学 重点:化学平衡图像
重、难 难点:分析化学平衡图像
点
化学平衡图像的核心素养主要体现在学生对化学反应速率和化学平衡的深入理解和把握
上。这包括以下几个方面:
1. 变化观念与平衡思想:学习理解化学反应速率和化学平衡图像,需要掌握物质浓度、
核心素 反应速率、温度、压强等因素对反应进程的影响,以及如何通过这些因素的变化来预测反应的
进行状态。
养
2. 证据推理与模型认知:能够根据实验数据或理论推导,建立相应的化学平衡模型,并
通过对这些模型的分析,解决实际问题。
3. 知识运用能力:具备利用化学反应速率和化学平衡的知识,分析解决实际问题的能
力。例如,能够分析和解释恒压(温)曲线图象中物质的平衡浓度或反应物的转化率随温度或压强变化的情况。
以上核心素养有助于学生养成化学学科观念,提升他们的科学素养,为他们进一步学习
和研究化学反应动力学、化学平衡计算等知识打下坚实的基础。
在化学平衡图像的学习过程中,学生的情况各有不同。接触化学平衡及图像分析前,学生
对化学反应速率、可逆反应以及影响化学反应速率的因素已有一定的认识,并且已经具备一定
的图像分析能力。
然而,尽管他们可以解析和处理一些基本的图像信息,但他们仍然缺乏一个完整和系统的
知识结构来全面理解和掌握化学平衡图像分析这一复杂问题。例如,他们可能对如何解读恒压
学情分 (温)曲线图象中物质的平衡浓度或反应物的转化率随温度或压强变化的情况感到困惑。
为了帮助学生更好地理解和掌握化学平衡图像分析,教师需要采取有效的教学策略。首
析
先,可以通过复习基本要点让学生对平衡图像有个知识回顾;然后,系统复习图像分析的一般
方法,通过四种常见的化学平衡图像,给出具体的示例分析,从而帮助学生理解并掌握化学平
衡图像的意义,以及化学平衡图像题的一般解题方法。
总的来说,化学平衡图像的学习不仅需要学生具备一定的基础知识和技能,更需要他们发
展出系统的分析能力和深层次的理解。只有这样,他们才能真正把握化学反应速率和化学平衡
的本质,进一步提升他们的科学素养
教学过程
教学环 设计
教学活动
节 意图
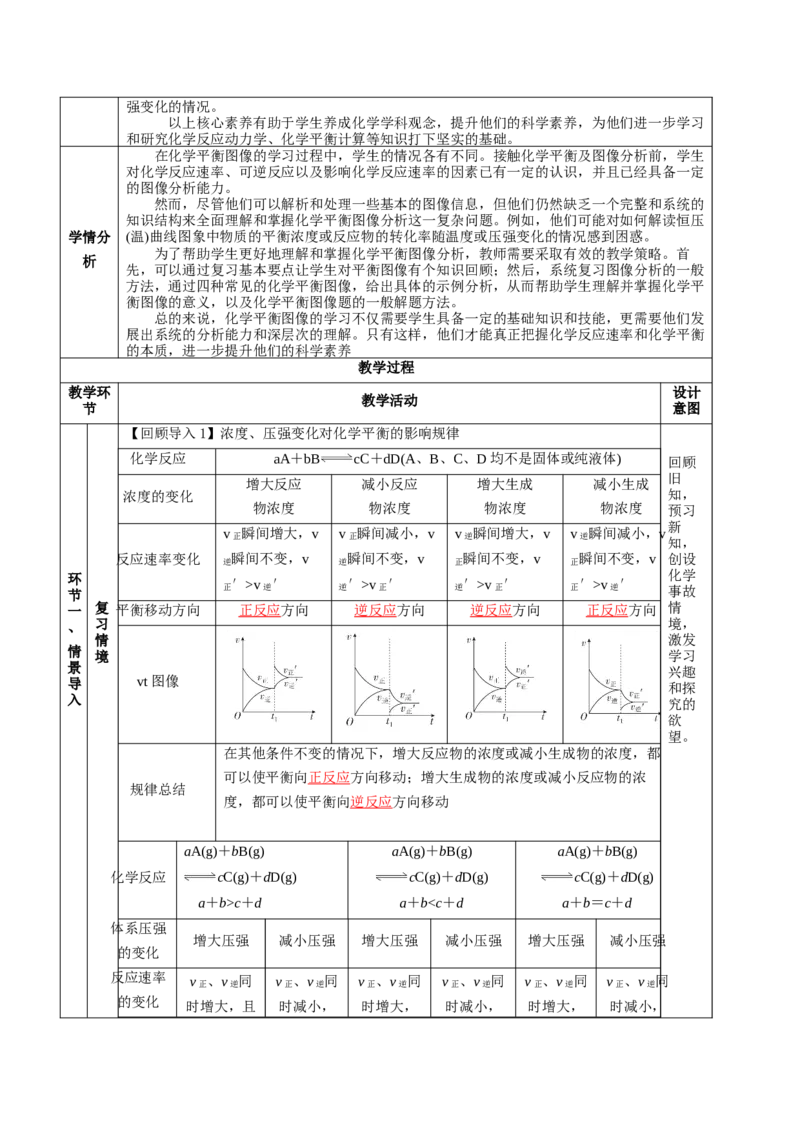
【回顾导入1】浓度、压强变化对化学平衡的影响规律
化学反应 aA+bB cC+dD(A、B、C、D均不是固体或纯液体) 回顾
旧
增大反应 减小反应 增大生成 减小生成
浓度的变化 知,
物浓度 物浓度 物浓度 物浓度 预习
新
v 瞬间增大,v v 瞬间减小,v v 瞬间增大,v v 瞬间减小,v
正 正 逆 逆 知,
反应速率变化 瞬间不变,v 瞬间不变,v 瞬间不变,v 瞬间不变,v 创设
逆 逆 正 正
环 化学
′>v ′ ′>v ′ ′>v ′ ′>v ′
节 正 逆 逆 正 逆 正 正 逆 事故
一 复 平衡移动方向 正反应方向 逆反应方向 逆反应方向 正反应方向 情
、 习 境,
情 激发
情
境 学习
景
兴趣
导 vt图像
和探
入
究的
欲
望。
在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都
可以使平衡向正反应方向移动;增大生成物的浓度或减小反应物的浓
规律总结
度,都可以使平衡向逆反应方向移动
aA(g)+bB(g) aA(g)+bB(g) aA(g)+bB(g)
化学反应 cC(g)+dD(g) cC(g)+dD(g) cC(g)+dD(g)
a+b>c+d a+bv 且v ′>v 且v ′>v 且v ′= 且v ′=
逆 逆 正 正 正
v ′>v ′
正 逆
′ ′ ′ v ′ v ′
正 正 逆 逆 逆
平衡移动 逆反应方 逆反应方 正反应方
正反应方向 不移动 不移动
方向 向 向 向
vt图像
在其他条件不变的情况下,增大压强,平衡向气态物质分子数减小的反应方向
规律总结 移动;减小压强,平衡向气态物质分子数增大的反应方向移动;反应物与生成
物的气体分子数相等时,改变压强平衡不移动
【回顾导入1】温度对化学平衡移动的影响规律
1.任何化学反应都伴随着能量的变化(放热或吸热),所以任意可逆反应的化学平衡状
态都受温度的影响。
2.升高温度,v 、v 均增大,但v 增大程度大;
放 吸 吸
降低温度,v 、v 均减小,但v 减小程度大。
放 吸 吸
3.当其他条件不变时
温度升高,平衡向吸热反应方向移动;
温度降低,平衡向放热反应方向移动。
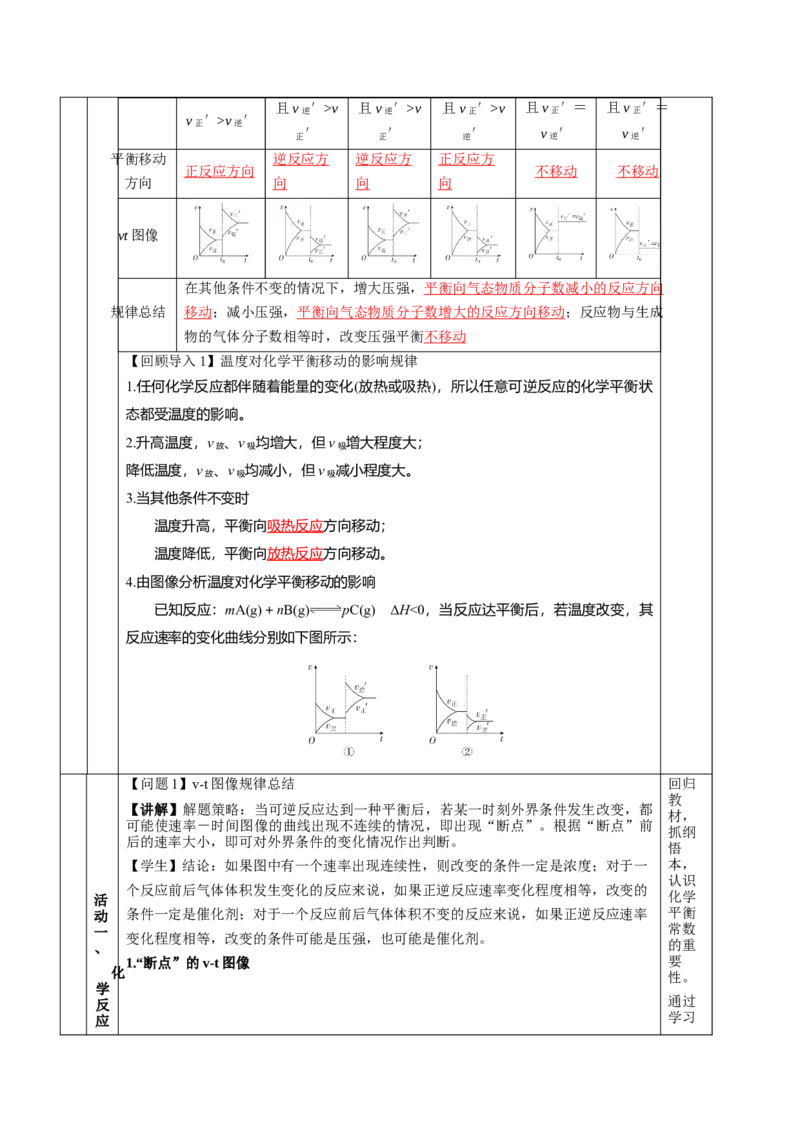
4.由图像分析温度对化学平衡移动的影响
已知反应:mA(g)+nB(g) pC(g) ΔH<0,当反应达平衡后,若温度改变,其
反应速率的变化曲线分别如下图所示:
【问题1】v-t图像规律总结 回归
教
【讲解】解题策略:当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都
材,
可能使速率-时间图像的曲线出现不连续的情况,即出现“断点”。根据“断点”前
抓纲
后的速率大小,即可对外界条件的变化情况作出判断。
悟
【学生】结论:如果图中有一个速率出现连续性,则改变的条件一定是浓度;对于一 本,
认识
个反应前后气体体积发生变化的反应来说,如果正逆反应速率变化程度相等,改变的
活 化学
动 条件一定是催化剂;对于一个反应前后气体体积不变的反应来说,如果正逆反应速率 平衡
一 常数
变化程度相等,改变的条件可能是压强,也可能是催化剂。
、 的重
1.“断点”的v-t图像 要
化
性。
学
反 通过
应 学习速 平衡
率 表达
图 式为
图像
像 之后
(vt 的学
图 习打
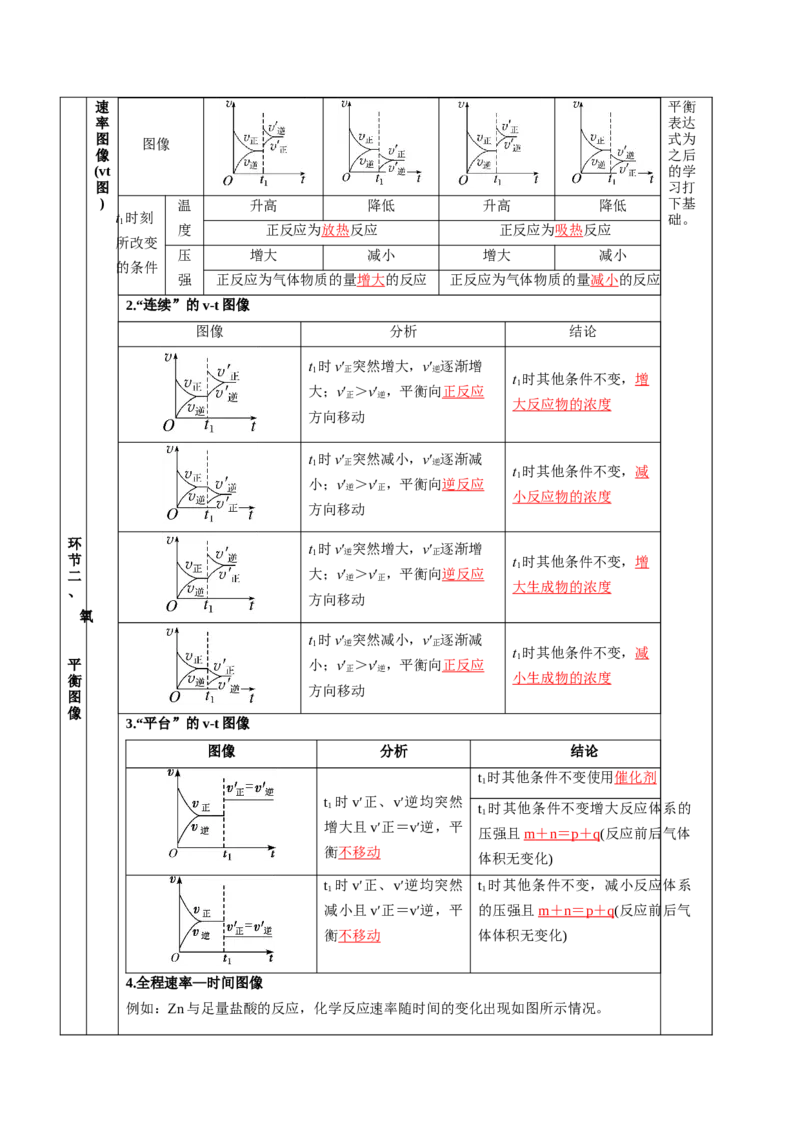
) 温 升高 降低 升高 降低 下基
t 时刻 础。
1
度 正反应为放热反应 正反应为吸热反应
所改变
压 增大 减小 增大 减小
的条件
强 正反应为气体物质的量增大的反应 正反应为气体物质的量减小的反应
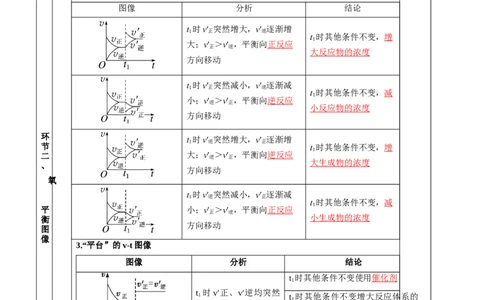
2.“连续”的v-t图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增
1 正 逆
t 时其他条件不变,增
1
大;v′ >v′ ,平衡向正反应
正 逆
大反应物的浓度
方向移动
t 时v′ 突然减小,v′ 逐渐减
1 正 逆
t 时其他条件不变,减
1
小;v′ >v′ ,平衡向逆反应
逆 正
小反应物的浓度
方向移动
环
t 时v′ 突然增大,v′ 逐渐增
节 1 逆 正 t 时其他条件不变,增
1
二 大;v′ >v′ ,平衡向逆反应
逆 正
大生成物的浓度
、
方向移动
氧
t 时v′ 突然减小,v′ 逐渐减
1 逆 正
t 时其他条件不变,减
1
平 小;v′ >v′ ,平衡向正反应
正 逆
衡 小生成物的浓度
方向移动
图
像
3.“平台”的v-t图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 时v′正、v′逆均突然
1 t 时其他条件不变增大反应体系的
1
增大且v′正=v′逆,平
压强且 m + n = p + q (反应前后气体
衡不移动
体积无变化)
t 时v′正、v′逆均突然 t 时其他条件不变,减小反应体系
1 1
减小且v′正=v′逆,平 的压强且 m + n = p + q (反应前后气
衡不移动 体体积无变化)
4.全程速率—时间图像
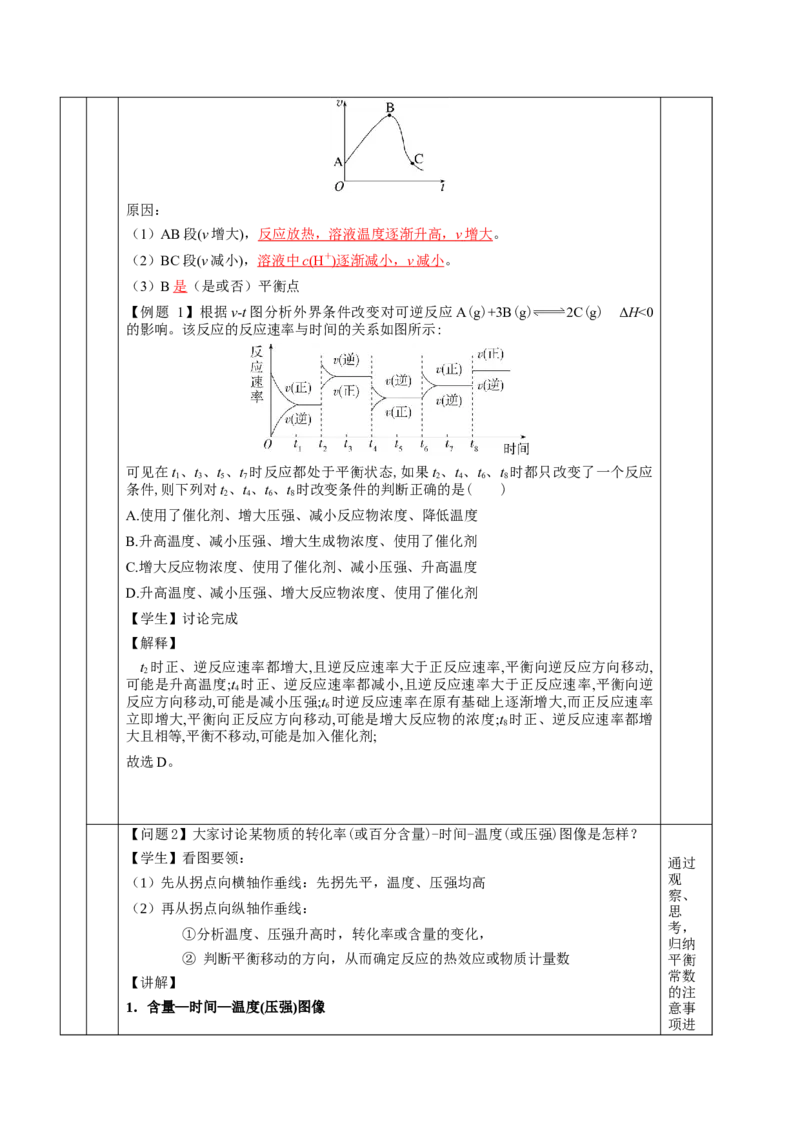
例如:Zn与足量盐酸的反应,化学反应速率随时间的变化出现如图所示情况。原因:
(1)AB段(v增大), 反应放热,溶液温度逐渐升高, v 增大 。
(2)BC段(v减小), 溶液中 c (H + ) 逐渐减小, v 减小 。
(3)B是(是或否)平衡点
【例题 1】根据v-t图分析外界条件改变对可逆反应A(g)+3B(g) 2C(g) ΔH<0
的影响。该反应的反应速率与时间的关系如图所示:
可见在t 、t 、t 、t 时反应都处于平衡状态,如果t 、t 、t 、t 时都只改变了一个反应
1 3 5 7 2 4 6 8
条件,则下列对t、t、t、t 时改变条件的判断正确的是( )
2 4 6 8
A.使用了催化剂、增大压强、减小反应物浓度、降低温度
B.升高温度、减小压强、增大生成物浓度、使用了催化剂
C.增大反应物浓度、使用了催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
【学生】讨论完成
【解释】
t 时正、逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动,
2
可能是升高温度;t 时正、逆反应速率都减小,且逆反应速率大于正反应速率,平衡向逆
4
反应方向移动,可能是减小压强;t 时逆反应速率在原有基础上逐渐增大,而正反应速率
6
立即增大,平衡向正反应方向移动,可能是增大反应物的浓度;t 时正、逆反应速率都增
8
大且相等,平衡不移动,可能是加入催化剂;
故选D。
【问题2】大家讨论某物质的转化率(或百分含量)-时间-温度(或压强)图像是怎样?
【学生】看图要领:
通过
(1)先从拐点向横轴作垂线:先拐先平,温度、压强均高 观
察、
(2)再从拐点向纵轴作垂线: 思
考,
①分析温度、压强升高时,转化率或含量的变化,
归纳
② 判断平衡移动的方向,从而确定反应的热效应或物质计量数 平衡
常数
【讲解】
的注
1.含量—时间—温度(压强)图像 意事
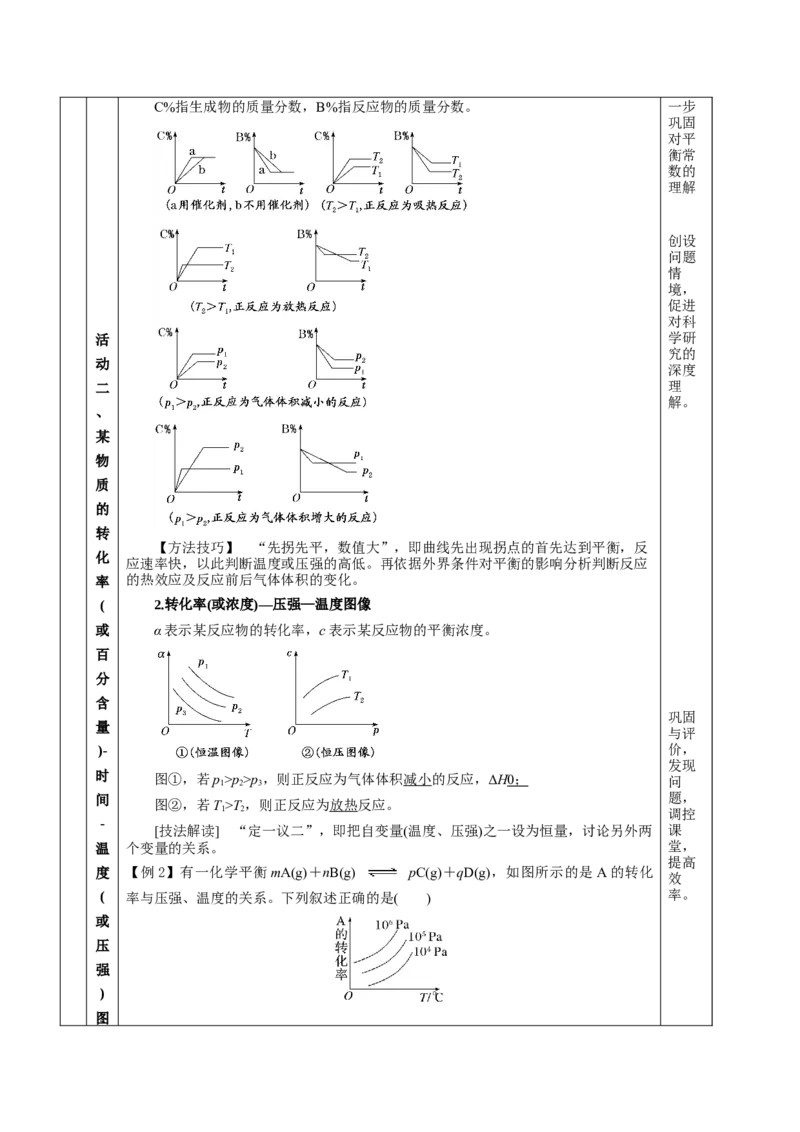
项进C%指生成物的质量分数,B%指反应物的质量分数。 一步
巩固
对平
衡常
数的
理解
创设
问题
情
境,
促进
对科
活 学研
究的
动
深度
二 理
解。
、
某
物
质
的
转
【方法技巧】 “先拐先平,数值大”,即曲线先出现拐点的首先达到平衡,反
化
应速率快,以此判断温度或压强的高低。再依据外界条件对平衡的影响分析判断反应
率 的热效应及反应前后气体体积的变化。
( 2.转化率(或浓度)—压强—温度图像
或 α表示某反应物的转化率,c表示某反应物的平衡浓度。
百
分
含
巩固
量
与评
)- 价,
发现
时 图①,若p>p>p,则正反应为气体体积减小的反应,ΔH 0 ; 问
1 2 3
间 题,
图②,若T>T,则正反应为放热反应。
1 2 调控
-
[技法解读] “定一议二”,即把自变量(温度、压强)之一设为恒量,讨论另外两 课
温 个变量的关系。 堂,
提高
度 【例2】有一化学平衡mA(g)+nB(g) pC(g)+qD(g),如图所示的是A的转化
效
( 率与压强、温度的关系。下列叙述正确的是( ) 率。
或
压
强
)
图像 A.正反应是放热反应;m+n>p+q
B.正反应是吸热反应;m+np+q
【答案】 D
【解析】 同一压强下,温度越高,A的转化率越高,说明正反应是吸热反应;同一
温度下,压强越大,A的转化率越高,说明正反应是气体体积减小的反应,即m+
n>p+q。
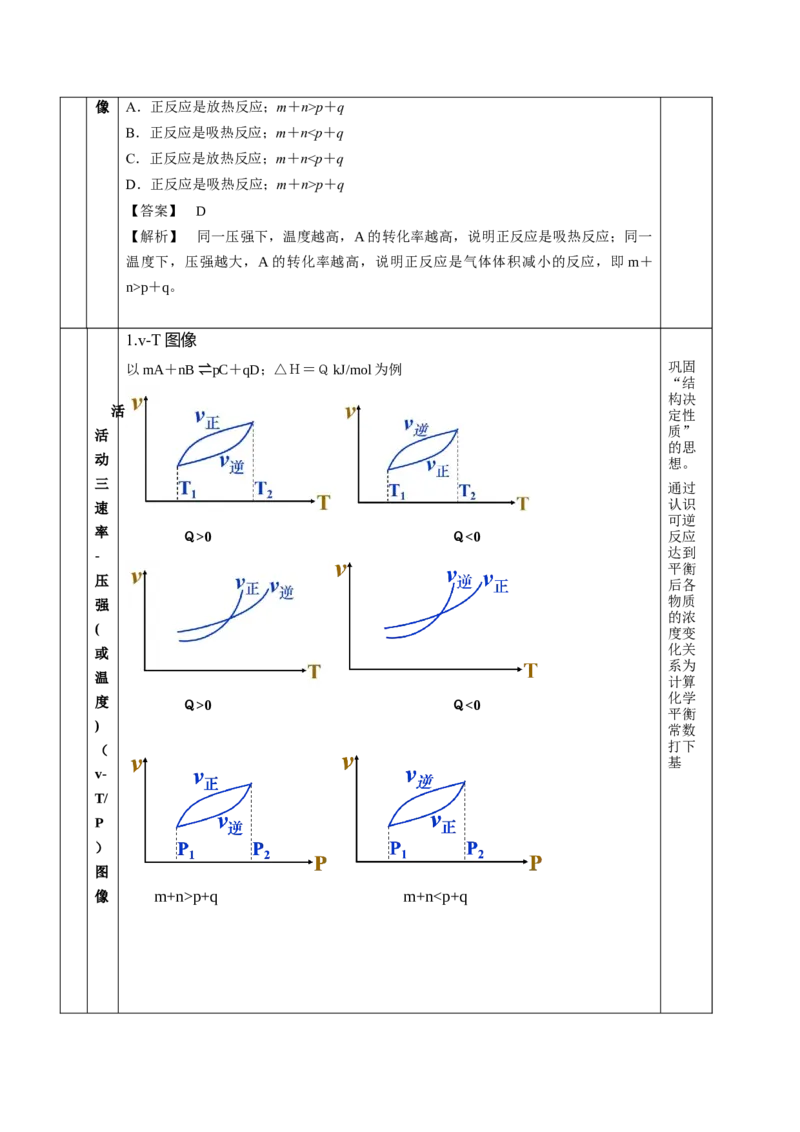
1.v-T图像
以mA+nB ⇌pC+qD;△H=QkJ/mol为例 巩固
“结
构决
活
定性
活 质”
的思
动
想。
三
通过
速 认识
可逆
率
Q>0 Q<0 反应
- 达到
平衡
压
后各
强 物质
的浓
( 度变
化关
或
系为
温 计算
化学
度 Q>0 Q<0
平衡
) 常数
打下
(
基
v-
T/
P
)
图
像 m+n>p+q m+np+q m+n