文档内容
第二节 化学平衡
一、化学平衡状态
(一)研究对象:可逆反应
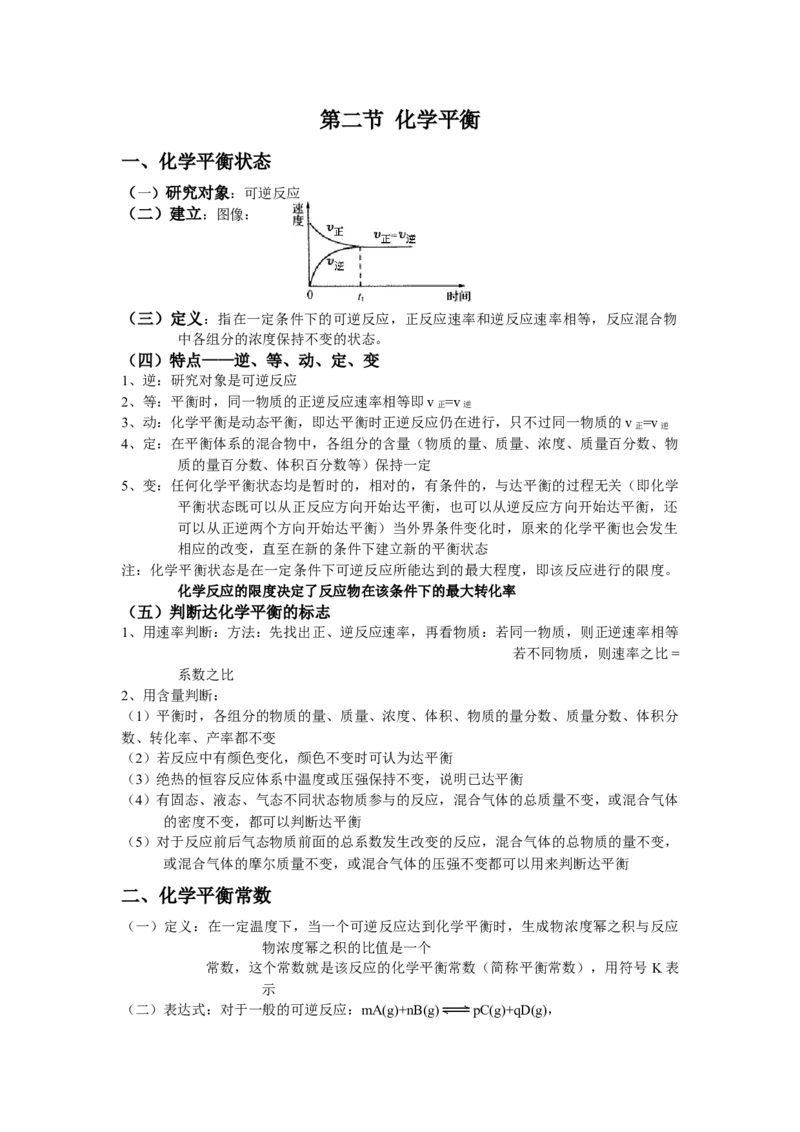
(二)建立:图像:
(三)定义:指在一定条件下的可逆反应,正反应速率和逆反应速率相等,反应混合物
中各组分的浓度保持不变的状态。
(四)特点——逆、等、动、定、变
1、逆:研究对象是可逆反应
2、等:平衡时,同一物质的正逆反应速率相等即v =v
正 逆
3、动:化学平衡是动态平衡,即达平衡时正逆反应仍在进行,只不过同一物质的v =v
正 逆
4、定:在平衡体系的混合物中,各组分的含量(物质的量、质量、浓度、质量百分数、物
质的量百分数、体积百分数等)保持一定
5、变:任何化学平衡状态均是暂时的,相对的,有条件的,与达平衡的过程无关(即化学
平衡状态既可以从正反应方向开始达平衡,也可以从逆反应方向开始达平衡,还
可以从正逆两个方向开始达平衡)当外界条件变化时,原来的化学平衡也会发生
相应的改变,直至在新的条件下建立新的平衡状态
注:化学平衡状态是在一定条件下可逆反应所能达到的最大程度,即该反应进行的限度。
化学反应的限度决定了反应物在该条件下的最大转化率
(五)判断达化学平衡的标志
1、用速率判断:方法:先找出正、逆反应速率,再看物质:若同一物质,则正逆速率相等
若不同物质,则速率之比=
系数之比
2、用含量判断:
(1)平衡时,各组分的物质的量、质量、浓度、体积、物质的量分数、质量分数、体积分
数、转化率、产率都不变
(2)若反应中有颜色变化,颜色不变时可认为达平衡
(3)绝热的恒容反应体系中温度或压强保持不变,说明已达平衡
(4)有固态、液态、气态不同状态物质参与的反应,混合气体的总质量不变,或混合气体
的密度不变,都可以判断达平衡
(5)对于反应前后气态物质前面的总系数发生改变的反应,混合气体的总物质的量不变,
或混合气体的摩尔质量不变,或混合气体的压强不变都可以用来判断达平衡
二、化学平衡常数
(一)定义:在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应
物浓度幂之积的比值是一个
常数,这个常数就是该反应的化学平衡常数(简称平衡常数),用符号 K表
示
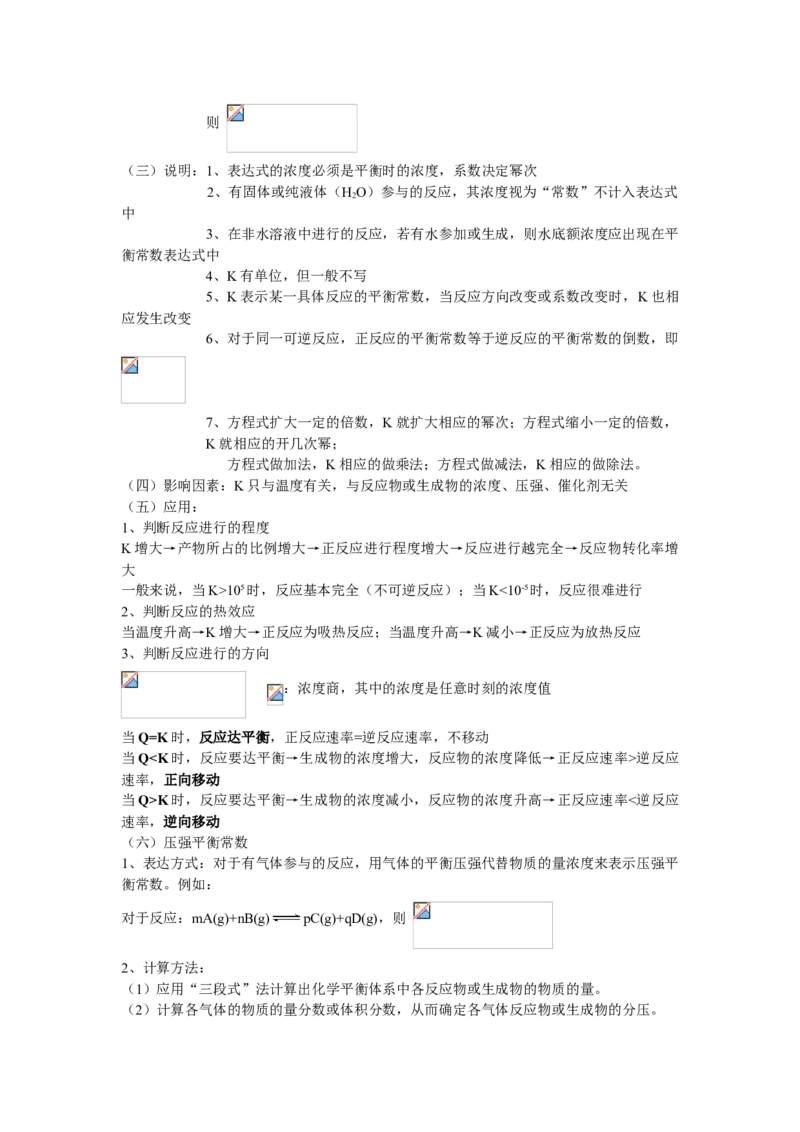
(二)表达式:对于一般的可逆反应:mA(g)+nB(g) pC(g)+qD(g),则
(三)说明:1、表达式的浓度必须是平衡时的浓度,系数决定幂次
2、有固体或纯液体(HO)参与的反应,其浓度视为“常数”不计入表达式
2
中
3、在非水溶液中进行的反应,若有水参加或生成,则水底额浓度应出现在平
衡常数表达式中
4、K有单位,但一般不写
5、K表示某一具体反应的平衡常数,当反应方向改变或系数改变时,K也相
应发生改变
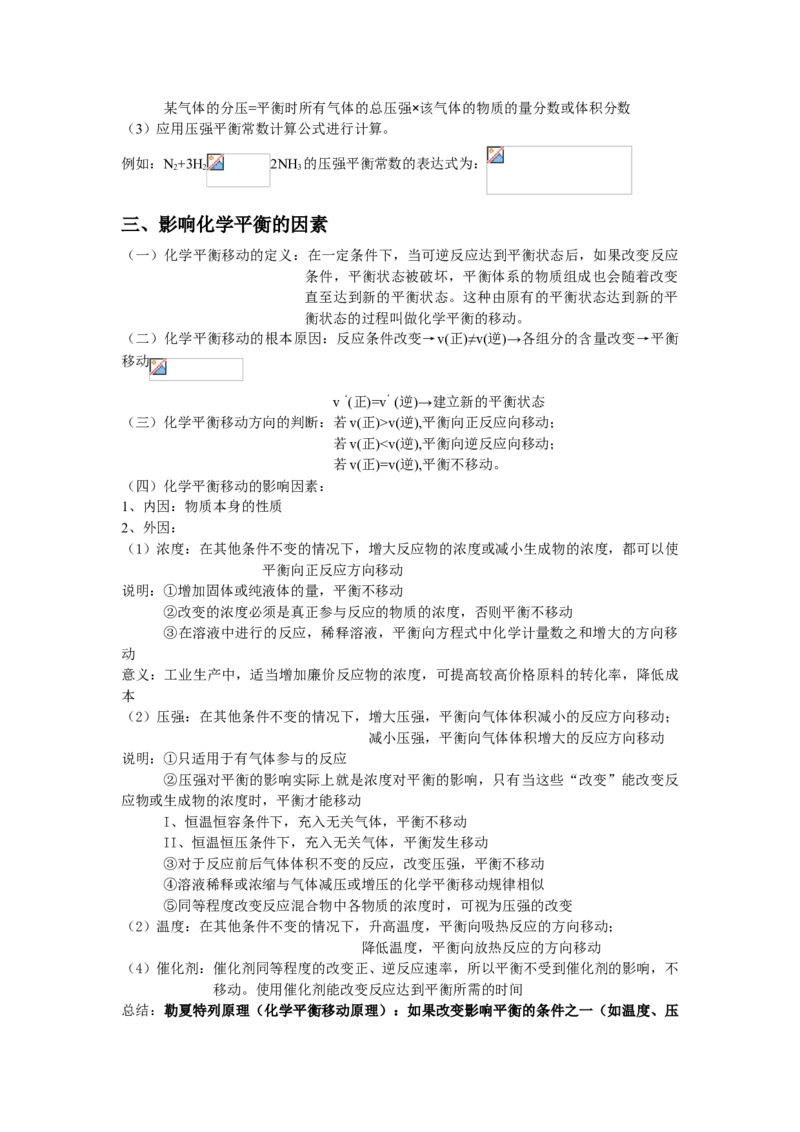
6、对于同一可逆反应,正反应的平衡常数等于逆反应的平衡常数的倒数,即
7、方程式扩大一定的倍数,K就扩大相应的幂次;方程式缩小一定的倍数,
K就相应的开几次幂;
方程式做加法,K相应的做乘法;方程式做减法,K相应的做除法。
(四)影响因素:K只与温度有关,与反应物或生成物的浓度、压强、催化剂无关
(五)应用:
1、判断反应进行的程度
K增大→产物所占的比例增大→正反应进行程度增大→反应进行越完全→反应物转化率增
大
一般来说,当K>105时,反应基本完全(不可逆反应);当K<10-5时,反应很难进行
2、判断反应的热效应
当温度升高→K增大→正反应为吸热反应;当温度升高→K减小→正反应为放热反应
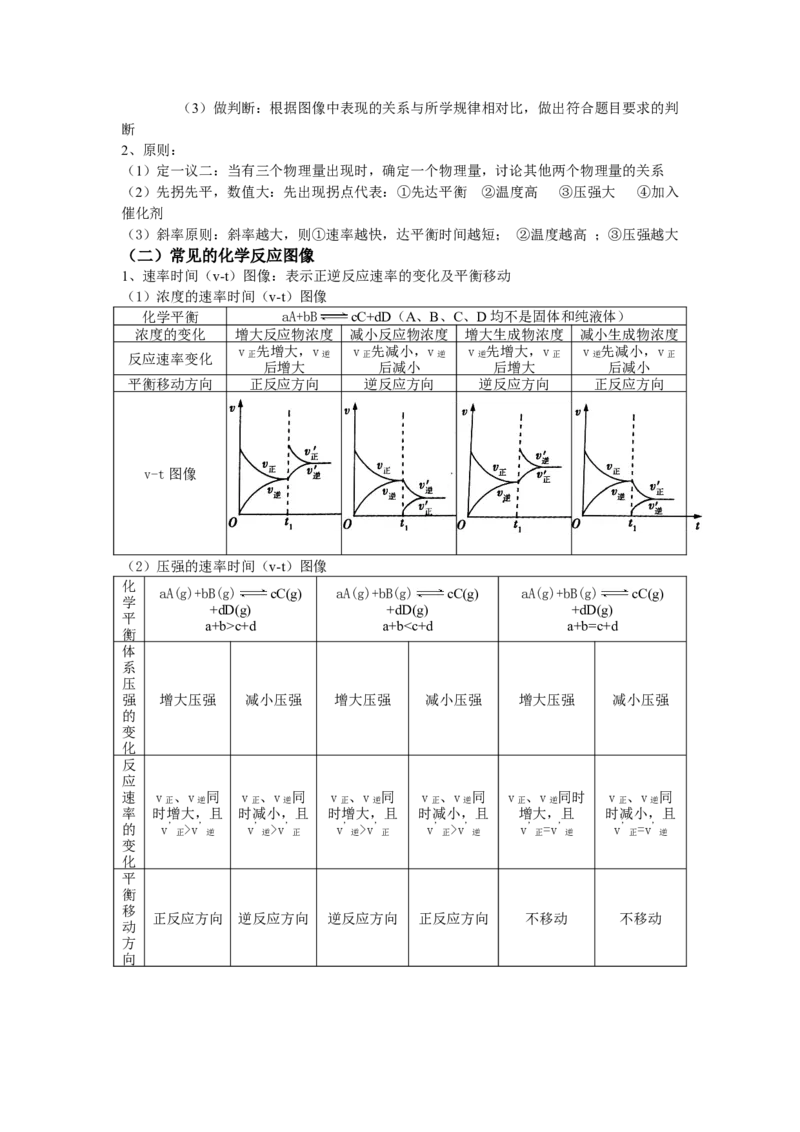
3、判断反应进行的方向
:浓度商,其中的浓度是任意时刻的浓度值
当Q=K时,反应达平衡,正反应速率=逆反应速率,不移动
当Q逆反应
速率,正向移动
当Q>K时,反应要达平衡→生成物的浓度减小,反应物的浓度升高→正反应速率<逆反应
速率,逆向移动
(六)压强平衡常数
1、表达方式:对于有气体参与的反应,用气体的平衡压强代替物质的量浓度来表示压强平
衡常数。例如:
对于反应:mA(g)+nB(g) pC(g)+qD(g),则
2、计算方法:
(1)应用“三段式”法计算出化学平衡体系中各反应物或生成物的物质的量。
(2)计算各气体的物质的量分数或体积分数,从而确定各气体反应物或生成物的分压。某气体的分压=平衡时所有气体的总压强×该气体的物质的量分数或体积分数
(3)应用压强平衡常数计算公式进行计算。
例如:N+3H 2NH 的压强平衡常数的表达式为:
2 2 3
三、影响化学平衡的因素
(一)化学平衡移动的定义:在一定条件下,当可逆反应达到平衡状态后,如果改变反应
条件,平衡状态被破坏,平衡体系的物质组成也会随着改变
直至达到新的平衡状态。这种由原有的平衡状态达到新的平
衡状态的过程叫做化学平衡的移动。
(二)化学平衡移动的根本原因:反应条件改变→v(正)≠v(逆)→各组分的含量改变→平衡
移动
v‘(正)=v’(逆)→建立新的平衡状态
(三)化学平衡移动方向的判断:若v(正)>v(逆),平衡向正反应向移动;
若v(正)b+c时,A的转化率增大;
ac+d时,A、B的转化率增大; 总结:平衡移动方向看浓度,转化率看压强
a+bc+d a+bv’ v’ >v’ v’ >v’ v’ >v’ v’ =v’ v’ =v’
正 逆 逆 正 逆 正 正 逆 正 逆 正 逆
变
化
平
衡
移
正反应方向 逆反应方向 逆反应方向 正反应方向 不移动 不移动
动
方
向v-
t
图
像
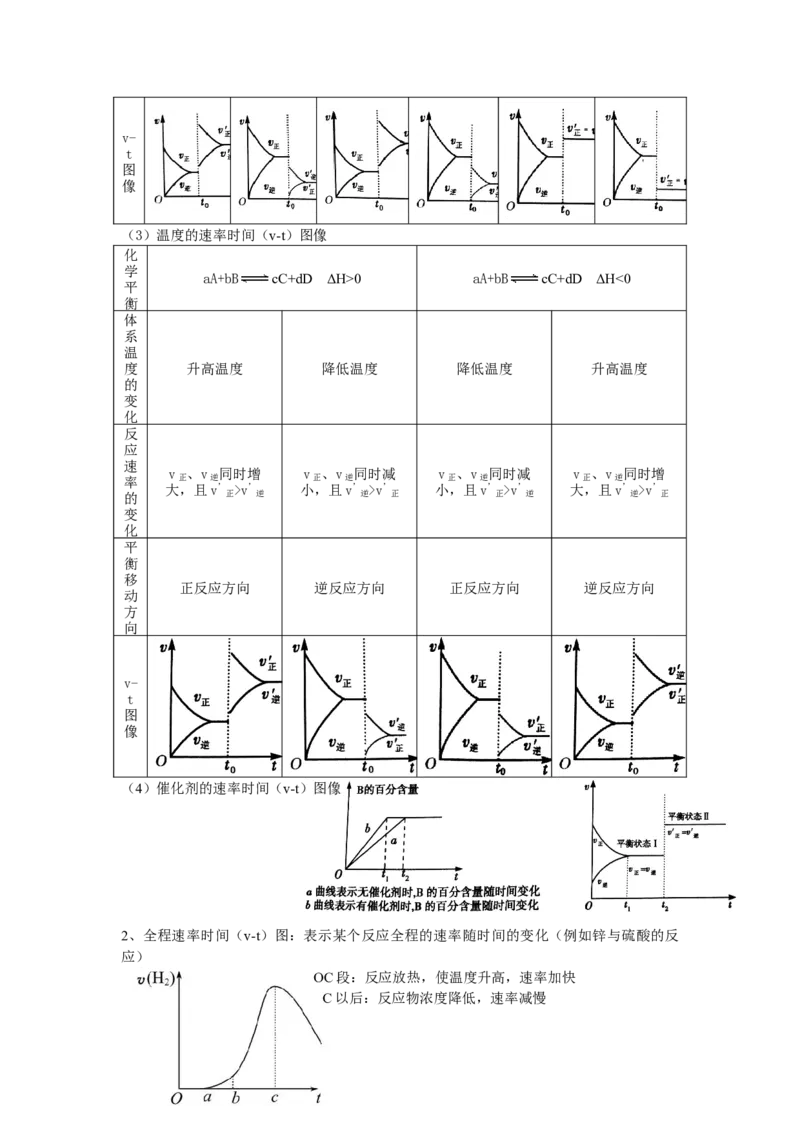
(3)温度的速率时间(v-t)图像
化
学
aA+bB cC+dD ΔH>0 aA+bB cC+dD ΔH<0
平
衡
体
系
温
度 升高温度 降低温度 降低温度 升高温度
的
变
化
反
应
速
v 、v 同时增 v 、v 同时减 v 、v 同时减 v 、v 同时增
率 正 逆 正 逆 正 逆 正 逆
大,且v’ >v’ 小,且v’ >v’ 小,且v’ >v’ 大,且v’ >v’
的 正 逆 逆 正 正 逆 逆 正
变
化
平
衡
移
正反应方向 逆反应方向 正反应方向 逆反应方向
动
方
向
v-
t
图
像
(4)催化剂的速率时间(v-t)图像
2、全程速率时间(v-t)图:表示某个反应全程的速率随时间的变化(例如锌与硫酸的反
应)
OC段:反应放热,使温度升高,速率加快
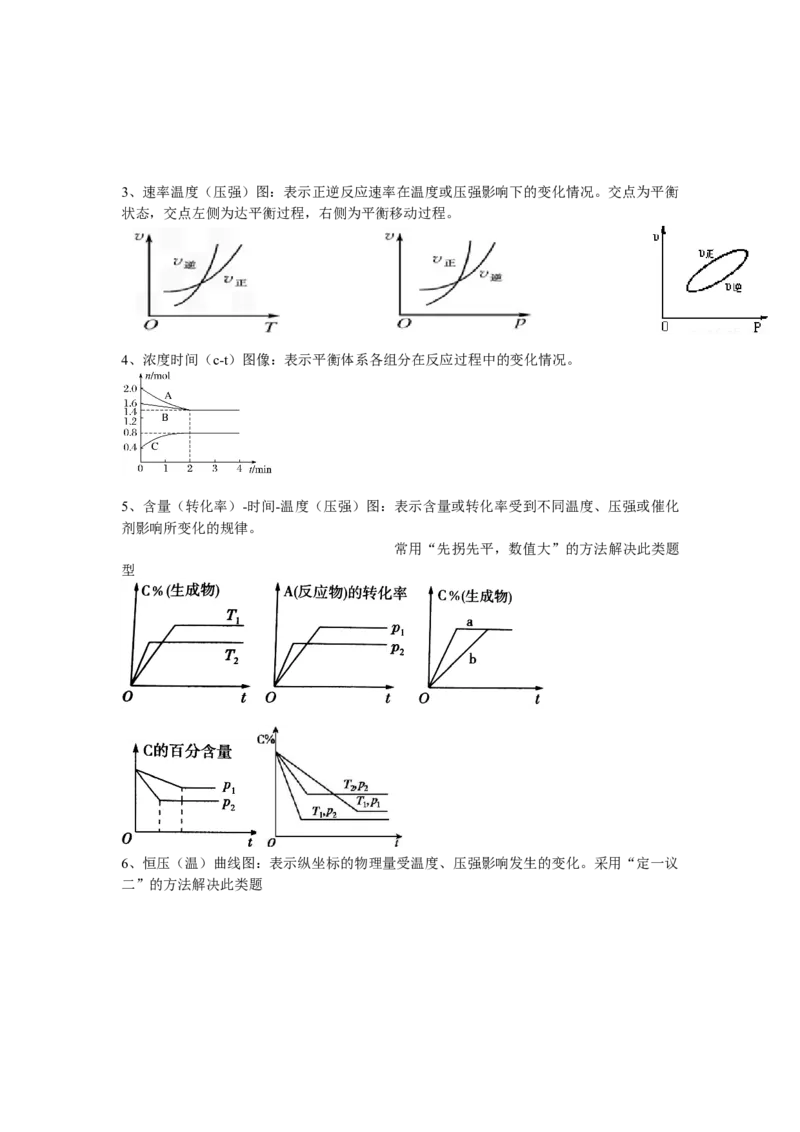
C以后:反应物浓度降低,速率减慢3、速率温度(压强)图:表示正逆反应速率在温度或压强影响下的变化情况。交点为平衡
状态,交点左侧为达平衡过程,右侧为平衡移动过程。
4、浓度时间(c-t)图像:表示平衡体系各组分在反应过程中的变化情况。
5、含量(转化率)-时间-温度(压强)图:表示含量或转化率受到不同温度、压强或催化
剂影响所变化的规律。
常用“先拐先平,数值大”的方法解决此类题
型
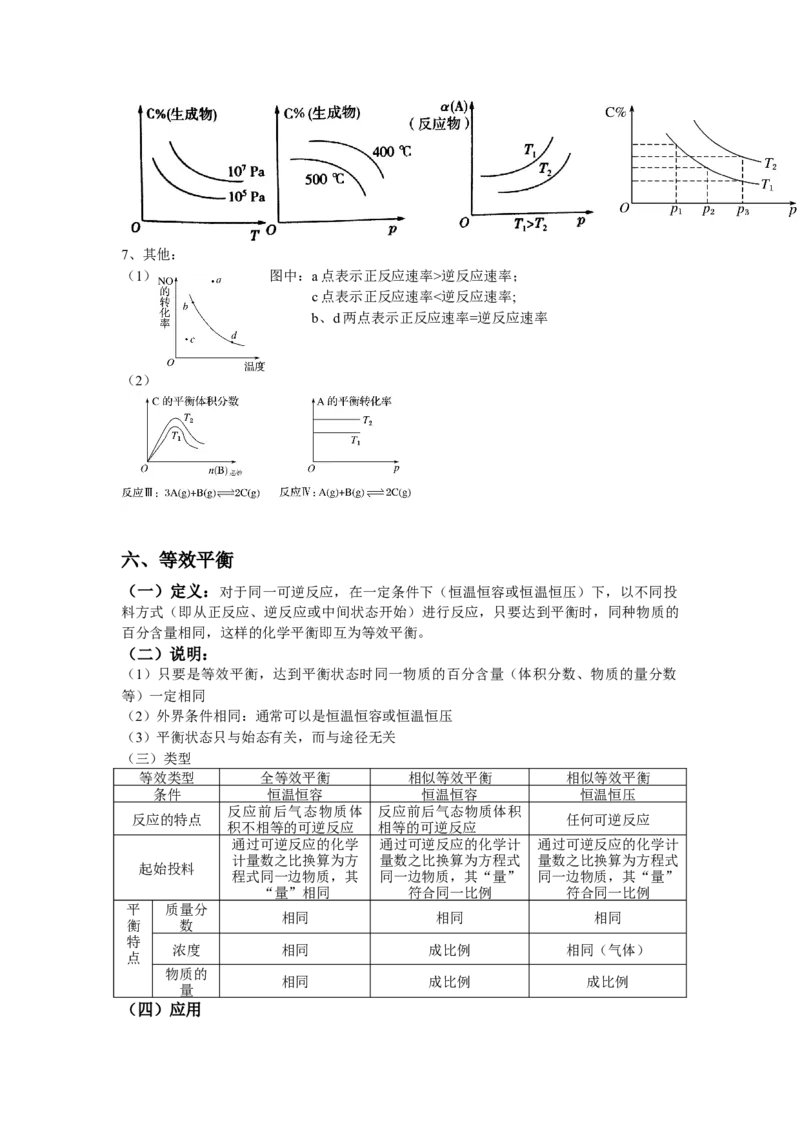
6、恒压(温)曲线图:表示纵坐标的物理量受温度、压强影响发生的变化。采用“定一议
二”的方法解决此类题7、其他:
(1) 图中:a点表示正反应速率>逆反应速率;
c点表示正反应速率<逆反应速率;
b、d两点表示正反应速率=逆反应速率
(2)
六、等效平衡
(一)定义:对于同一可逆反应,在一定条件下(恒温恒容或恒温恒压)下,以不同投
料方式(即从正反应、逆反应或中间状态开始)进行反应,只要达到平衡时,同种物质的
百分含量相同,这样的化学平衡即互为等效平衡。
(二)说明:
(1)只要是等效平衡,达到平衡状态时同一物质的百分含量(体积分数、物质的量分数
等)一定相同
(2)外界条件相同:通常可以是恒温恒容或恒温恒压
(3)平衡状态只与始态有关,而与途径无关
(三)类型
等效类型 全等效平衡 相似等效平衡 相似等效平衡
条件 恒温恒容 恒温恒容 恒温恒压
反应前后气态物质体 反应前后气态物质体积
反应的特点 任何可逆反应
积不相等的可逆反应 相等的可逆反应
通过可逆反应的化学 通过可逆反应的化学计 通过可逆反应的化学计
计量数之比换算为方 量数之比换算为方程式 量数之比换算为方程式
起始投料
程式同一边物质,其 同一边物质,其“量” 同一边物质,其“量”
“量”相同 符合同一比例 符合同一比例
平 质量分
相同 相同 相同
衡 数
特
浓度 相同 成比例 相同(气体)
点
物质的
相同 成比例 成比例
量
(四)应用(1)判断同一可逆反应在相同的反应条件下是否为相同的平衡状态
(2)求要达到等效平衡,两种不同的状态下起始量之间的关系式
(3)求属于等效平衡状态下的反应方程式的化学计量数
(五)解题方法
起始量 转化量(同侧物质) 新起始量→与原标准量对照→符
合条件,互为等效平衡