文档内容
2.3.1 摩尔与气体摩尔体积
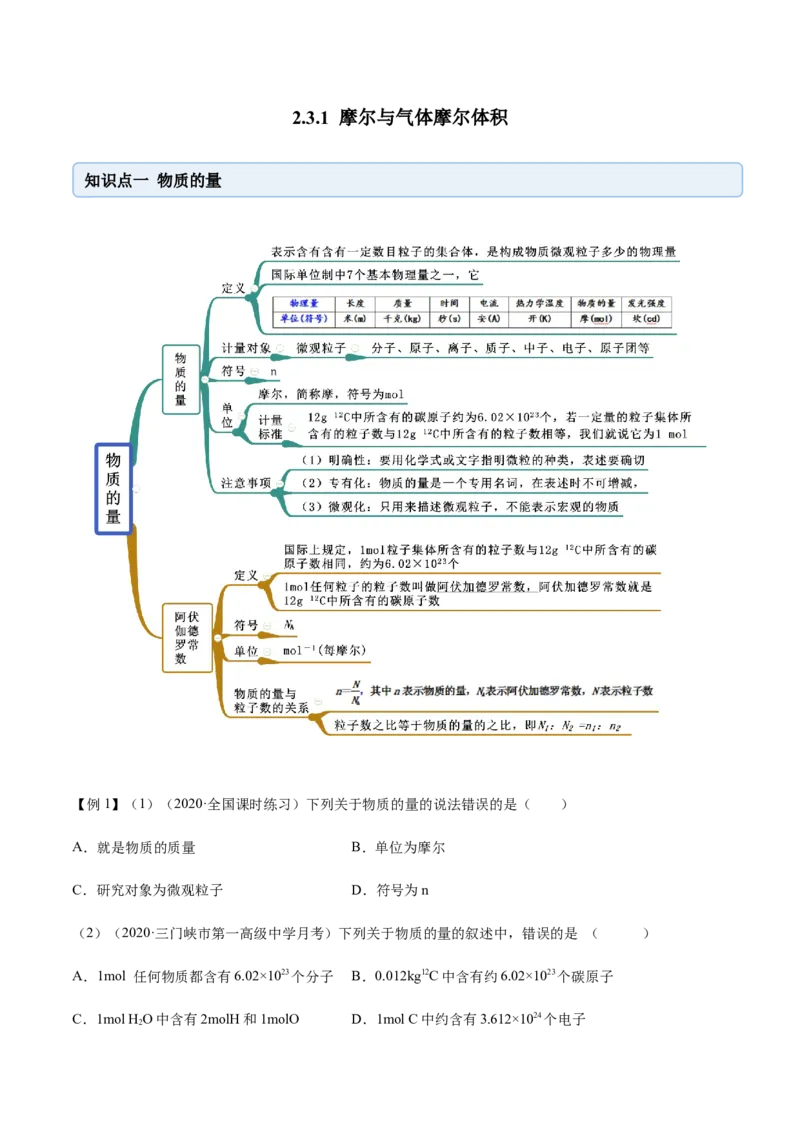
知识点一 物质的量
【例1】(1)(2020·全国课时练习)下列关于物质的量的说法错误的是( )
A.就是物质的质量 B.单位为摩尔
C.研究对象为微观粒子 D.符号为n
(2)(2020·三门峡市第一高级中学月考)下列关于物质的量的叙述中,错误的是 ( )
A.1mol 任何物质都含有6.02×1023个分子 B.0.012kg12C中含有约6.02×1023个碳原子
C.1mol HO中含有2molH和1molO D.1mol C中约含有3.612×1024个电子
2【答案】(1)A(2)A
【解析】(1)物质的量是表示含有一定数目粒子的集合体的物理量,符号为n,单位为摩尔,研究的对象
为微观粒子,综上所述,答案为A。
(2)A、不是任何物质都由分子构成,构成物质的微粒还有原子和离子,故A错误;
B、0.012kg 12C的物质的量为 =1mol,含有约6.02×1023个碳原子,故B正确;
C、一个水分子中含两个氢原子和一个氧原子,因此1molH O中含有2molH和1molO,故C正确;
2
D、一个C原子有6个电子,1molC就有6mol电子,所以1mol C中约含有3.612×1024个电子,故D正确;
故选A。
【一隅三反】
1.(2020·长葛市第一高级中学月考)下列关于物质的量的表述中错误的是( )
A.0.3 mol硝酸 B.1.5 mol氧气 C.1 mol氮 D.0.5 mol氦原子
【答案】C
【解析】用摩尔表示物质的量单位时,要指明微粒的种类。“1 mol氮”没有指明是氮分子还是氮原子。
故C错误。故选C。
2.(2020·西华县第一高级中学月考)下列叙述错误的是( )
A.1mol任何物质都含有6.02×1023个原子
B.0.012kg12C 含有阿伏加德罗常数个碳原子
C.在使用摩尔表示物质的量的单位时,应指明粒子的种类
D.物质的量是国际单位制中七个基本物理量之一
【答案】A
【解析】A.1mol任何物质都含有6.02×1023个微粒,可能是分子,也可能是原子,故A错误;B.国际上规定,1mol粒子集体所含的粒子数与0.012kg12C中所含的碳原子数相同,把1mol任何粒子的粒
子数叫做阿伏加德罗常数,所以0.012kg12C 含有阿伏加德罗常数个碳原子,故B正确;
C.在使用摩尔表示物质的量的单位时,应指明粒子的种类,故C正确;
D.物质的量是国际单位制中七个基本物理量之一,故D正确;故选A。
3.(2020·商水县实验高级中学月考)1 mol CO和1 mol CO 具有相同的( )
2
①分子数 ②原子数 ③C原子数 ④O原子数
A.②④ B.①③ C.①④ D.①②
【答案】B
【解析】二者物质的量相同,所以具有相同的分子数,碳原子角标一样,所以C原子数 相同
4.(2020·全国课时练习)下列关于阿伏加德罗常数的叙述错误的是( )
A.物质的量越大,阿伏加德罗常数就越大B.1mol任何粒子的数目都约等于6.02×1023
C.符号为N ,约为6.02×1023mol-1D.在数值上约等于12g12C所含的碳原子数
A
【答案】A
【解析】A.12g12C中含有的碳原子数称为阿伏伽德罗常数,其数值与物质的量的多少无关,选项A错误;
B.将阿伏伽德罗常数个微粒看做一个整体,即1mol,故1mol任何粒子的数目都约等于6.02×1023,选项B
正确;C.阿伏加德罗常数的符号为 ,近似值为 ,约为 ,C
正确;D.12g12C中含有的碳原子数称为阿伏伽德罗常数,故阿伏伽德罗常数在数值上等于12g12C中所含
的碳原子数,选项D正确;答案选A。
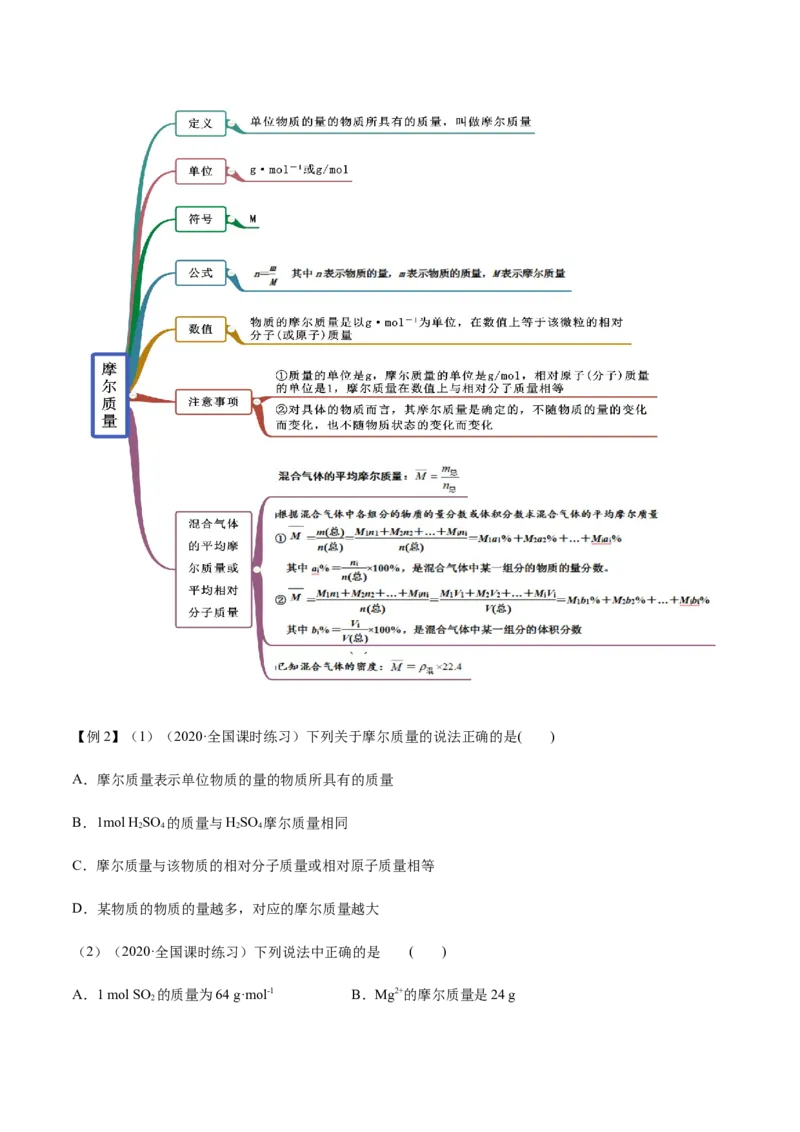
知识点二 摩尔质量【例2】(1)(2020·全国课时练习)下列关于摩尔质量的说法正确的是( )
A.摩尔质量表示单位物质的量的物质所具有的质量
B.1mol HSO 的质量与HSO 摩尔质量相同
2 4 2 4
C.摩尔质量与该物质的相对分子质量或相对原子质量相等
D.某物质的物质的量越多,对应的摩尔质量越大
(2)(2020·全国课时练习)下列说法中正确的是 ( )
A.1 mol SO 的质量为64 g·mol-1 B.Mg2+的摩尔质量是24 g
2C.CO的摩尔质量是28 g·mol-1 D.氮的摩尔质量是28 g·mol-1
【答案】(1)A(2)C
【解析】(1)A.单位物质的量的物质所具有的质量称为摩尔质量,用符号M表示,A说法正确;
B.1mol HSO 的质量与HSO 摩尔质量的数值相同,但单位分别为g和g/mol,B说法错误;
2 4 2 4
C.摩尔质量的数值与该物质的相对分子质量或相对原子质量相等,C说法错误;
D.物质的摩尔质量为定值,不随物质的物质的量发生变化,D说法错误;答案为A。
(2)质量的常用单位之一是g,g·mol-1是摩尔质量的单位,故A、B项错误。D项中的氮所指的对象不明
确,不能确定是氮分子还是氮原子,错误。C正确。故选C。
【一隅三反】
1.(2020·全国课时练习)下列叙述错误的个数是
①摩尔是国际单位制中七个基本物理量之一
②1 mol任何物质都含有约6.02×1023个分子
③6.02×1023就是阿伏加德罗常数
④氢原子的摩尔质量是1 g
⑤HCl的摩尔质量等于1 mol HCl分子的质量
⑥1 mol H O中含有1 mol氢分子和1mol氧原子
2
A.3 B.4 C.5 D.6
【答案】D
【解析】①物质的量是国际单位制中七个基本物理量之一,而摩尔是物质的量单位,故①错误;
②有些物质是由原子组成的,不含有分子,如金刚石是由碳原子组成,应说成是1mol任何微粒的集合体
含有约6.02×1023个粒子,故②错误;
③6.02×1023是实验值,阿伏加德罗常数是N ,故③错误;
A④摩尔质量的单位是g·mol-1,故④错误;
⑤摩尔质量单位是g·mol-1,质量的单位是g。故⑤错误;
⑥H O中不含有氢分子,应是1molH O中含有2mol氢原子和1mol氧原子,故⑥错误;
2 2
综上所述,选项D符合题意。
2.(2020·全国课时练习)已知3.2 g某气体中所含的分子数约为3.01×1022,此气体的摩尔质量为( )
A.64 g·mol-1 B.64 mol C.64 g D.32 g·mol-1
【答案】A
【解析】气体中所含的分子数目约为3.01×1022,则物质的量为 =0.05mol,则此气体的摩
尔质量为3.2g÷0.05mol=64g/mol,答案选A。
3(2020·全国课时练习)已知12.3 g A与4.6 g B恰好完全反应生成了3.2 g C、4.5 g D和0.2 mol E,则E的
摩尔质量是( )
A.46 B.46 g·mol-1
C.64 g·mol-1 D.64
【答案】B
【解析】由于A与B恰好完全反应生成了C、D和E,则根据质量守恒定律可知m(E)=(12.3 g+4.6 g)-(3.2
g+4.5 g)=9.2 g,则E的摩尔质量M(E)= =46 g·mol-1。故选B。
4.(2021·赣榆智贤中学月考)填充表格_____
指定的微粒 质量(m) 物质的量(n) 摩尔质量(M)(g/
物质
(个) (g) (mol) mol)
O 0.2
2S 1.204×1023
NaCO 53
2 3
【答案】
指定的微粒 质量(m) 物质的量(n) 摩尔质量(M)(g/
物质
(个) (g) (mol) mol)
O 1.204×1023 6.4 0.2 32
2
S 1.204×1023 6.4 0.2 32
NaCO 3.01×1023 53 0.5 106
2 3
【解析】0.2mol O 的分子数目为0.2mol×6.02×1023mol-1=1.204×1023,摩尔质量为32g/mol,其质量为
2
0.2mol×32g/mol=6.4g;1.204×1023个S原子物质的量为 =0.2mol,其摩尔质量为32g/mol,
质量为0.2mol×32g/mol=6.4g;M(NaCO)=106g/mol;n(NaCO)= =0.5mol,N(NaCO)
2 3 2 3 2 3
=0.5mol×6.02×1023mol-1=3.01×1023;故答案为
指定的微粒 质量(m) 物质的量(n) 摩尔质量(M)(g/
物质
(个) (g) (mol) mol)
O 1.204×1023 6.4 0.2 32
2
S 1.204×1023 6.4 0.2 32
NaCO 3.01×1023 53 0.5 106
2 3
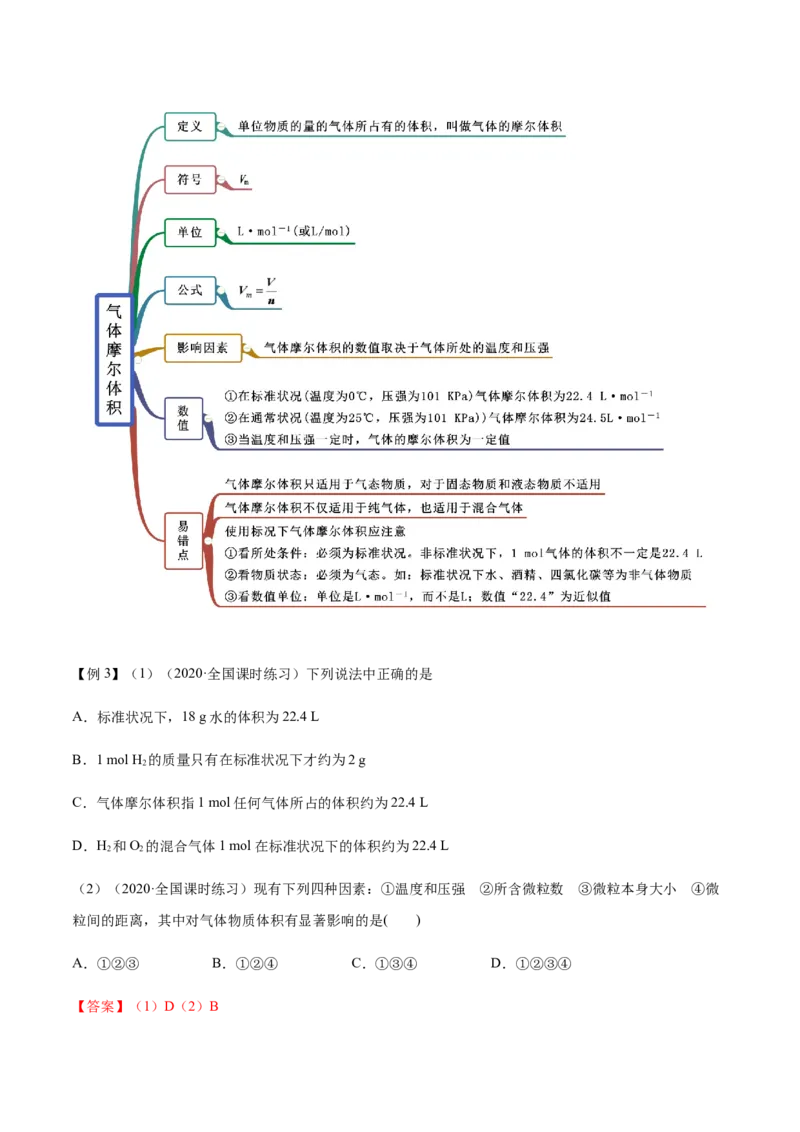
知识点三 气体摩尔体积【例3】(1)(2020·全国课时练习)下列说法中正确的是
A.标准状况下,18 g水的体积为22.4 L
B.1 mol H 的质量只有在标准状况下才约为2 g
2
C.气体摩尔体积指1 mol任何气体所占的体积约为22.4 L
D.H 和O 的混合气体1 mol在标准状况下的体积约为22.4 L
2 2
(2)(2020·全国课时练习)现有下列四种因素:①温度和压强 ②所含微粒数 ③微粒本身大小 ④微
粒间的距离,其中对气体物质体积有显著影响的是( )
A.①②③ B.①②④ C.①③④ D.①②③④
【答案】(1)D(2)B【解析】A、标准状况下,水不是气体,不能用22.4L·mol-1计算,故A错误;
B、质量与条件无关,1molH 的质量就是2g,故B错误;
2
C、气体摩尔体积为1mol任何气体所占的体积,在标准状况下,1mol气体所占有的体积约为22.4L,故C
错误;
D、标况下,1mol任何气体所占有的体积约为22.4L,该气体可以是混合气体也可以是单一气体,故D正
确;
答案选D。
(2)对于气体来说,温度和压强不同,气体分子之间的距离不同,而微粒本身大小远小于微粒间的距离,
所以微粒本身大小可忽略不计;微粒数目越多,则体积越大,所以影响气体体积的因素主要有:温度和压
强、所含微粒数以及微粒间的距离;①②④可选;综上所述,本题答案选B。
【一隅三反】
1.(2020·全国课时练习)下列有关气体体积的叙述中,正确的是
A.不同的气体,若体积不同,则它们所含的分子数也不同
B.一定温度和压强下,气体体积由构成气体的分子数决定
C.一定温度和压强下,气体体积由构成气体的分子大小决定
D.气体摩尔体积是指1 mol任何气体所占的体积约为22.4 L
【答案】B
【解析】A、根据分子数N=N V/V 可以知道,不同的气体,当体积不同时,因为气体所处的状态的气体
A m
摩尔体积未知,故分子数N可能相同,故A错误;
B、一定温度和压强下,气体摩尔体积的数值确定,而气体体积V=nV ,故此时气体体积的大小取决于气
m
体的物质的量即分子个数,故B正确;
C、由于气体分子在很大的空间运动,分子本身相对于分子间隔很小,可以忽略不计,所以温度压强确定,
则分子间距离确定,故气体摩尔体积的数值确定,而气体体积V=nV ,故此时气体体积的大小取决于气体
m
的物质的量即分子个数,故C错误;D、气体摩尔体积是指单位物质的量的气体所占据的体积,数值和气体所处的状态有关,不一定为22.4L/
mol,故D错误;综上所述,本题选B。
2.(2020·全国课时练习)下列物质的体积一定是 的是( )
A. 氯气 B. 氨气
C.标准状况下 二氧化碳 D. 、 时 氢气
【答案】C
【解析】A. 氯气不一定是在标准状况下,所以体积不一定是 ,A错误;
B. 氨气的物质的量 ,温度、压强不确定,不能确定气体的体积,B错误;
C. 二氧化碳的物质的量为 ,所以标准状况下 二氧化碳气体的体积为 ,
C正确;
D. 氢气的物质的量是 ,但 、 不是标准状况,所以 氢气的体积不是 ,D
错误;故选C。
3.(2020·全国课时练习)用 表示阿伏加德罗常数的值,下列叙述正确的是
A.非标准状况下,1mol 的体积不可能是22.4L
B.含有 个氦原子的氦气在标准状况下的体积为11.2L
C.11.2L 含有的分子数为D.标准状况下,11.2L 中含有的分子数为
【答案】D
【解析】A.改变温度与压强,在非标准状况下,1mol 的体积也可能是22.4L,故A错误;
B.氦气为单原子分子,故含有 个氦原子的氦气的物质的量为1mol,在标准状况下的体积为22.4L,故
B错误;
C.未指明气体所处状态,不能确定11.2L 的物质的量,故C错误;
D.标准状况下,11.2L 的物质的量为0.5mol,含分子数为 ,故D正确;
故答案为D。
4.(2020·张家口市宣化第一中学高一月考)下列有关气体摩尔体积的描述中正确的是( )
A.气体摩尔体积的数值是固定不变的,都约为22.4L
B.通常状况下的气体摩尔体积约为22.4L
C.标准状况下的气体的摩尔体积约为22.4L
D.标准状况下,气体的摩尔体积约为22.4L/mol
【答案】D
【解析】A.气体的摩尔体积由温度和压强共同决定的,温度、压强改变,气体摩尔体积就变,故A错误;
B.通常状况为25度,101kPa,1mol气体体积大于22.4L,故B错误;
C.标准状况下的气体的摩尔体积约为22.4L/mol,故C错误;
D.标准状况下,气体的摩尔体积约为22.4L/mol,故D正确;故选D。
5.(2020·全国课时练习)标准状况下,有:① ,② ,③ ,④个 分子,下列对这四种气体关系的描述不正确的是( )
A.体积:④<①<②<③ B.质量:①<④<③<②
C.密度:④<②<③<① D.氢原子数:④<②<①<③
【答案】C
【解析】A.① 是 ,② 的物质的量为 ,③中 的
物质的量是 ,④ 个 分子的物质的量是 ,同温同压条件下,气体的体积之
比等于物质的量之比,所以体积:④<①<②<③,A正确;
B.①中 的质量为 ,②中 质量为 ,③中 质量为
,④中 的质量为 ,所以质量:①<④<③
<②,B正确;
C.依据 可知,同温同压条件下,密度与 成正比,①甲烷的摩尔质量为 ,②硫
化氢的摩尔质量为 ,③氨气的摩尔质量为 ,④氯化氢的摩尔质量为 ,
所以密度:①<③<②<④,C错误;
D.①②③④中 原子的物质的量分别是 、 、 、 ,氢原子数:④<②<①
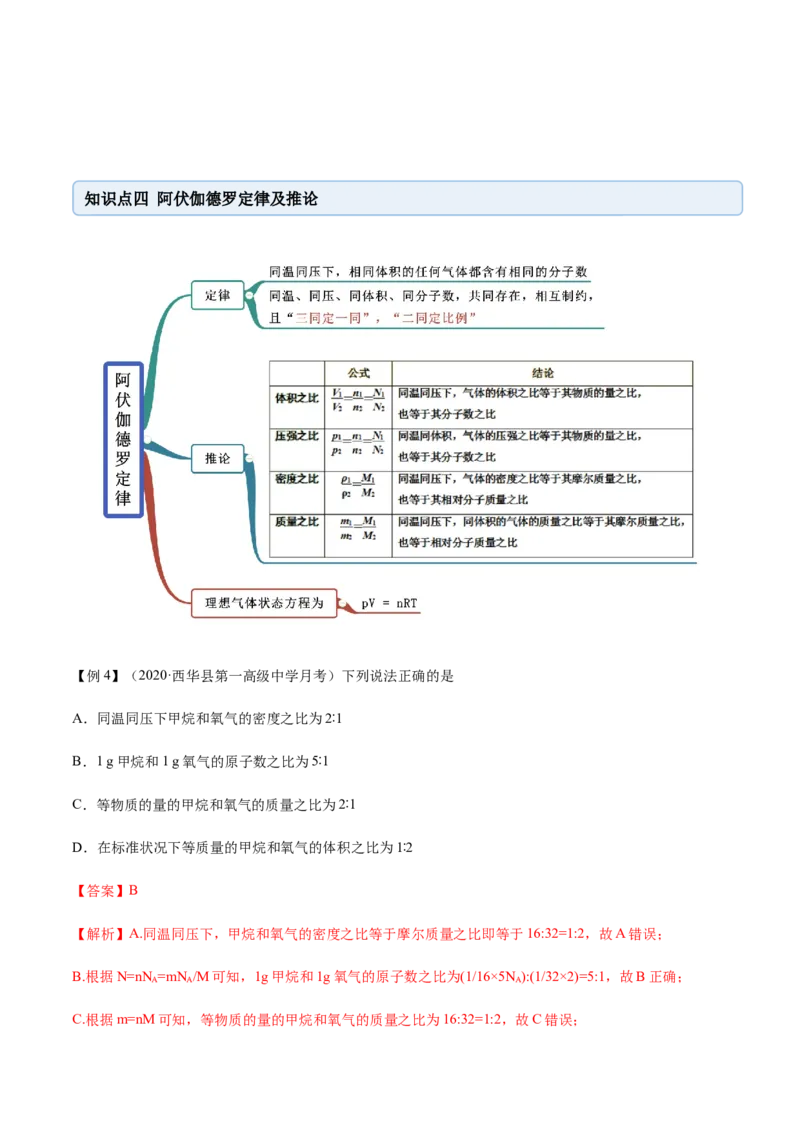
<③,D正确;故选C。知识点四 阿伏伽德罗定律及推论
【例4】(2020·西华县第一高级中学月考)下列说法正确的是
A.同温同压下甲烷和氧气的密度之比为2∶1
B.1 g甲烷和1 g氧气的原子数之比为5∶1
C.等物质的量的甲烷和氧气的质量之比为2∶1
D.在标准状况下等质量的甲烷和氧气的体积之比为1∶2
【答案】B
【解析】A.同温同压下,甲烷和氧气的密度之比等于摩尔质量之比即等于16:32=1:2,故A错误;
B.根据N=nN =mN /M可知,1g甲烷和1g氧气的原子数之比为(1/16×5N ):(1/32×2)=5:1,故B正确;
A A A
C.根据m=nM可知,等物质的量的甲烷和氧气的质量之比为16:32=1:2,故C错误;D.根据公式V=nV =mV /M可知,在标准状况下等质量的甲烷和氧气的体积之比=(mV /16):(mV /
m m m m
32)=2:1,故D错误;故答案选B。
【一隅三反】
1.(2020·全国课时练习)下列条件下,两种气体所含原子数一定相同的是( )
A.同体积、同密度的CO和 B.同温度、同体积的CO和
C.同质量、同密度的 和 D.同压强、同密度的 和
【答案】A
【解析】A.同体积、同密度的 和CO,二者的质量相同,因其摩尔质量也相同,则其物质的量相同,
故二者所含原子数相同,A符合题意;
B.同温度、同体积的CO和 ,压强可能不同,即二者物质的量可能不同,所含原子数可能不同,B不
合题意;
C.二者的质量相同,设其质量均为m g, 代表阿伏加德罗常数的值,则 中含有的原子数为
,而 中含有的原子数为 ,C不合题意;
D.同压强、同密度的 和 ,二者的质量不一定相同,物质的量不一定相同,所含原子数不一定
相同,D不合题意;
故选A。
2.(2020·全国课时练习)向三个密闭容器中分别充入Ne、H、O,下列有关这三种气体的叙述正确的是
2 2
A.同温、同压时,三种气体的密度关系:B.温度、密度相同时,三种气体的压强关系:
C.质量、温度、压强均相同时,三种气体的体积关系:
D.温度、压强、体积均相同时,三种气体的质量关系:
【答案】B
【解析】A.根据阿伏加德罗定律的推论,同温、同压时,气体的密度与其摩尔质量成正比,故A不选;
B.温度、密度相同时,气体的压强与其摩尔质量成反比,故选B;
C.质量、温度、压强均相同时,气体的体积与其摩尔质量成反比,故C不选;
D.温度、压强、体积均相同时,气体的质量与其摩尔质量成正比,故D不选。
答案选B
3.(2020·全国课时练习)在一定温度和压强下,分别用质量均为mg的CH、CO、O 和SO 四种气体吹
4 2 2 2
出的气球体积大小不同,下列说法中正确的是( )
A.气球②中装的是O B.气球①和③中气体分子数相等
2
C.气球①和④中气体物质的量之比为4∶1 D.气球③和④中气体密度之比为2:1
【答案】D
【解析】A.一定温度压强下,气体的V 是相等的,用mg的CH、CO、O、SO 四种气体分别吹出四个
m 4 2 2 2体积大小不同的气球,根据V=nV = V ,体积和相对分子质量成反比,所以体积的大小顺序是:CH>
m m 4
O>CO>SO ,③中装的是氧气,故A错误;
2 2 2
B.根据A的分析,④、③、②、①四个球中分别是CH、O、CO、SO ,气球①和气球③中气体分子数
4 2 2 2
之比等于体积之比,等于相对分子质量M的倒数之比,则气球①和③中气体分子数之比=32∶64=1∶2,故B
错误;
C.气球①和气球④中气体物质的量之比等于体积之比等于M的倒数之比,则气球①和④中气体物质的量
之比=16∶64=1∶4,故C错误;
D.气球③和气球④中气体密度之比等于摩尔质量之比=32∶16=2∶1,故D正确;
故选D。
知识点五 综合运用
【例5】(2020·贵溪市实验中学月考)现有14.4gCO和CO 的混合气体,在标准状况下其体积为8.96L。
2
(1)该混合气体的平均摩尔质量为____。
(2)混合气体中碳原子的个数为____(用N 表示阿伏加德罗常数)。
A
(3)将混合气体依次通过下列装置,最后收集在气球中(实验在标准状况下测定)。①气球中收集到的气体的摩尔质量为____。
②气球的体积为____L。
【答案】(1)36g·mol-1 (2)0.4N (3)28g·mol-1 4.48
A
【解析】设CO和CO 的物质的量分别为xmol、ymol,则列方程组:28x+44y=14.4,x+y= mol,解之
2
得x=0.2,y=0.2,气体共为0.4mol,则
(1)根据M=m/n可知,该混合气体的平均摩尔质量为14.4g÷0.4mol=36g/mol;
答案是:36g/mol;
(2)CO和CO 中碳原子的物质的量为0.2mol×1+0.2mol×1=0.4mol,碳原子的个数为0.4mol×N =0.4N ;
2 A A
故答案是:0.4N ;
A
(3)将混合气体依次通过如图所示装置,二氧化碳与氢氧化钠反应,经浓硫酸干燥,得到的气体为CO,
①气球中收集到的气体为CO,摩尔质量为28g/mol;
故答案是:28g/mol;
②气球中收集到的气体为CO,标况下体积V=0.2mol×22.4L/mol=4.48L;
故答案是:4.48。
【一隅三反】
1.(2020·东莞市东莞中学松山湖学校期中)设N 为阿伏加德罗常数,下列说法正确的是( )
A
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为N
A
②体积相同的氢气和氩气所含的分子数相等③2mol·L-1的AlCl 溶液中含氯离子为6N
3 A
④标准状况下,22.4LH O中分子数为N
2 A
⑤32gO 和O 混合气体中含有原子数为2N
2 3 A
A.①⑤ B.①②③ C.①③④ D.③④
【答案】A
【解析】①标况下,11.2L气体的物质的量为0.5mol,0.5mol氮气和氧气的混合气体中含有1mol原子,所
含的原子数为N ,故①正确;
A
②没有明确是否为相同条件,无法确定体积相同的氢气和氩气的物质的量是否相同,则所含的分子数不一
定相等,故②错误;
③没有告诉2mol/L的氯化铝溶液的体积,无法计算溶液中溶质氯化铝的物质的量及氯离子的数目,故③错
误;
④标况下水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故④错误;
⑤32g氧气和臭氧的混合物中含有32g氧原子,故含有2mol氧原子,含有原子数为2N ,故⑤正确;
A
①⑤正确,故选A。
2.(2020·全国课时练习)(1)标准状况下, 气体 的体积为 ,则此气体的相对分子质量为
_____。
(2)在 、 的条件下,相同质量的 和 气体的体积之比是 ,则 的摩尔质量为______。
(3)两个容积相同的密闭容器 、 ,在 下, 中充入 气体, 中充入 气体, 与
的压强之比是 ,则 的摩尔质量为_____。
(4)相同条件下,体积比为 和质量比为 的H 和O 的混合气体,其平均摩尔质量分别是______和
2 2
______。【答案】(1)64 (2) (3) (4)
【解析】(1) , ,则其相对分子质量为64。答
案为:64;
(2)温度、压强相同时,气体体积之比等于其物质的量之比,则 ,
。答案为: ;
(3)温度、体积相同时,气体压强之比等于其物质的量之比,则 ,
。答案为: ;
(4)体积比为 的H 和O 的混合气体的平均摩尔质量
2 2
;质量比为 的H 和O 的混合气体的平均
2 2
摩尔质量 。答案为: ; 。
3.(2020·上海期中)(1)2molO 和3molO 的质量之比_______,分子数之比______,同温同压下密度之比
3 2
________,含氧原子数之比______,体积之比______。
(2)O 与Cl 具有相似的性质,均可用于自来水的消毒。已知二者在消毒时均被还原为最低价态,则相同状
3 2
况下10LO 与______LCl 的消毒能力相当。
3 2(3)气体化合物A分子式可表示为OF,已知同温同压下10mLA受热分解生成15mLO 和10mLF ,则A的
x y 2 2
化学式为_________。
【答案】(1)1:1 2:3 3:2 1:1 2:3 (2)30 (3) OF
3 2
【解析】(1)2mol O 与3mol O 中都含有6mol氧原子,所以二者质量相等,质量之比为1:1;分子数之
3 2
比等于二者物质的量之比,分子数之比为2:3;同温同压下,气体的密度之比=摩尔质量之比,所以臭氧
和氧气的密度之比为:48:32=3:2;二者中都含有6mol氧原子,氧原子数之比为1:1;体积之比等于物
质的量之比,体积之比为2:3,故答案为1:1;2:3;3:2;1:1;2:3;
(2)O 与Cl 都具有强氧化性,因此二者消毒原理相同,消毒时二者均被还原为最低价态(O为-2价,F
3 2
为-1价),且相同条件下,气体的体积之比=物质的量之比,若消毒能力相当,说明转移的电子数相等,
有O~6e-~3Cl ,所以若10L臭氧参与消毒,则需要氯气的体积为: L=30L,故答案为30;
3 2
(3)根据质量守恒定律和阿伏伽德罗定律,相同条件下,气体的物质的量之比=体积之比,则同温同压下
10mL A受热分解生成15mL O 和10mL F ,分子的组成为:N(O)= =3,N(F)= =2,
2 2
则A的化学式为:OF,故答案为OF。
3 2 3 2