文档内容
期中备考试卷(二)
时间:90分钟 满分:100分
一、选择题(本题共14小题,每小题3分,共42分,每小题仅有一个选项符合题
意)
1.化学在生产和日常生活中有着重要的应用。下列说法正确的是( )
A.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N 和
2
CO
2
B.向煤中加入适量石灰石,使煤燃烧产生的SO 最终生成CaSO ,可减少对大
2 3
气的污染
C.高纯度的硅单质广泛用于制作光导纤维
D.大量燃烧化石燃料排放的废气中含CO 、SO ,从而使雨水的pH=5.6即形
2 2
成酸雨
答案 A
解析 煤中加入适量石灰石,使煤燃烧产生的SO 转化为CaSO ,再氧化生成
2 3
CaSO ,B错误;制作光导纤维的是二氧化硅,C错误;雨水的pH<5.6才形成酸雨,
4
D错误。
2.自然界存在NaIO ,可利用NaIO 与NaHSO 溶液来制取单质碘。反应分两步
3 3 3
进行:IO+3HSO===I-+3SO+3H+;IO+5I-+6H+===3I +3H O。下列说法错误
2 2
的是( )
A.NaIO 是氧化剂, HSO是还原剂
3
B.生产中可得到副产物H SO 和Na SO
2 4 2 4
C.I 既是氧化产物又是还原产物
2
D.HSO的还原性比I-弱
答案 D
解析 在反应IO+3HSO===I-+3SO+3H+中,HSO是还原剂,I-是还原产物
还原剂的还原性强于还原产物的还原性,故D错误。
3.已知NH NO 爆炸时的反应为4NH NO =====3N ↑+2NO ↑+8H O↑。下
4 3 4 3 2 2 2
列说法不正确的是( )
A.NH NO 在高温下爆炸时可以看到红棕色的烟雾
4 3
B.NH NO 的含氮量小于氯化铵
4 3
C.实验室不能用NH NO 固体与Ca(OH) 固体混合加热制备NH
4 3 2 3
D.乘坐火车时不能携带NH NO 固体
4 3
答案 B
解析 选项A,根据NH NO 的爆炸反应可知生成的NO 为红棕色,爆炸时,
4 3 2
NO 、粉尘、H O等形成了红棕色的烟雾;选项B,NH NO 的含氮量为35%,NH Cl
2 2 4 3 4
的含氮量约为26.2%;选项C,由于NH NO 固体受热可能爆炸,故实验室不能用其
4 3制备NH ;选项D,NH NO 属于易爆炸物,不能带上火车。
3 4 3
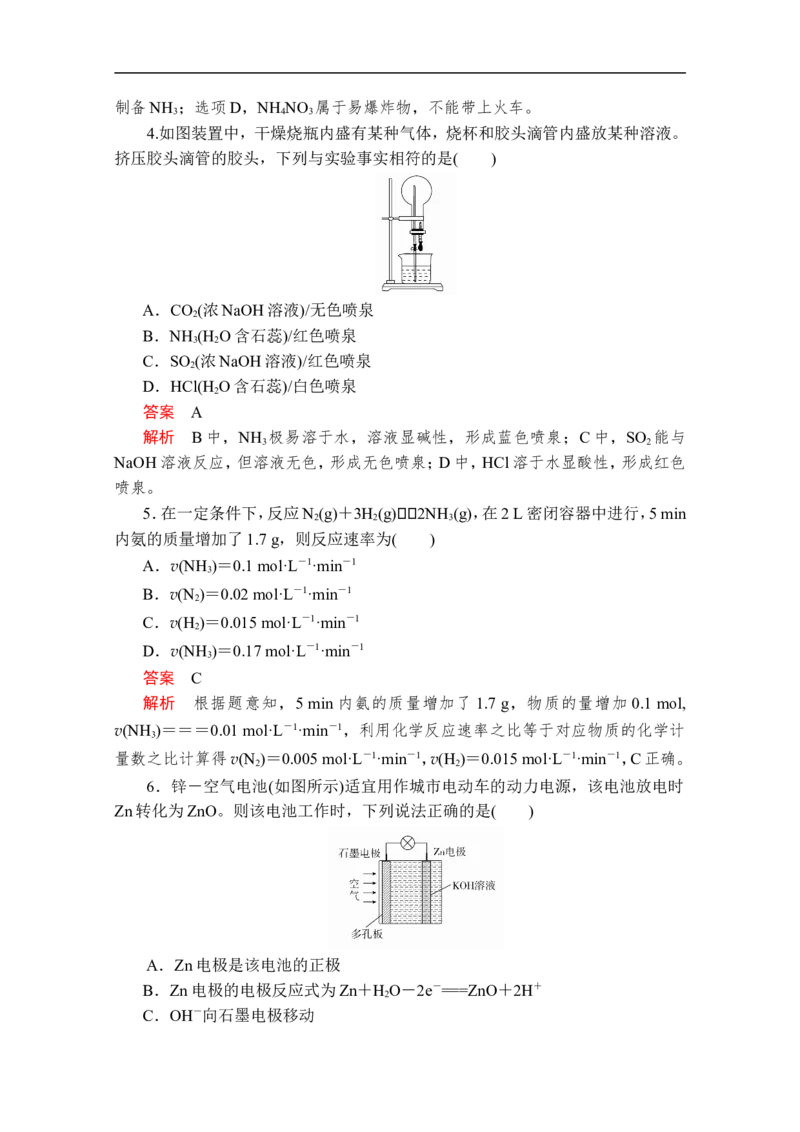
4.如图装置中,干燥烧瓶内盛有某种气体,烧杯和胶头滴管内盛放某种溶液。
挤压胶头滴管的胶头,下列与实验事实相符的是( )
A.CO (浓NaOH溶液)/无色喷泉
2
B.NH (H O含石蕊)/红色喷泉
3 2
C.SO (浓NaOH溶液)/红色喷泉
2
D.HCl(H O含石蕊)/白色喷泉
2
答案 A
解析 B中,NH 极易溶于水,溶液显碱性,形成蓝色喷泉;C中,SO 能与
3 2
NaOH溶液反应,但溶液无色,形成无色喷泉;D中,HCl溶于水显酸性,形成红色
喷泉。
5.在一定条件下,反应N (g)+3H (g)2NH (g),在2 L密闭容器中进行,5 min
2 2 3
内氨的质量增加了1.7 g,则反应速率为( )
A.v(NH )=0.1 mol·L-1·min-1
3
B.v(N )=0.02 mol·L-1·min-1
2
C.v(H )=0.015 mol·L-1·min-1
2
D.v(NH )=0.17 mol·L-1·min-1
3
答案 C
解析 根据题意知,5 min 内氨的质量增加了 1.7 g,物质的量增加 0.1 mol,
v(NH )===0.01 mol·L-1·min-1,利用化学反应速率之比等于对应物质的化学计
3
量数之比计算得v(N )=0.005 mol·L-1·min-1,v(H )=0.015 mol·L-1·min-1,C正确。
2 2
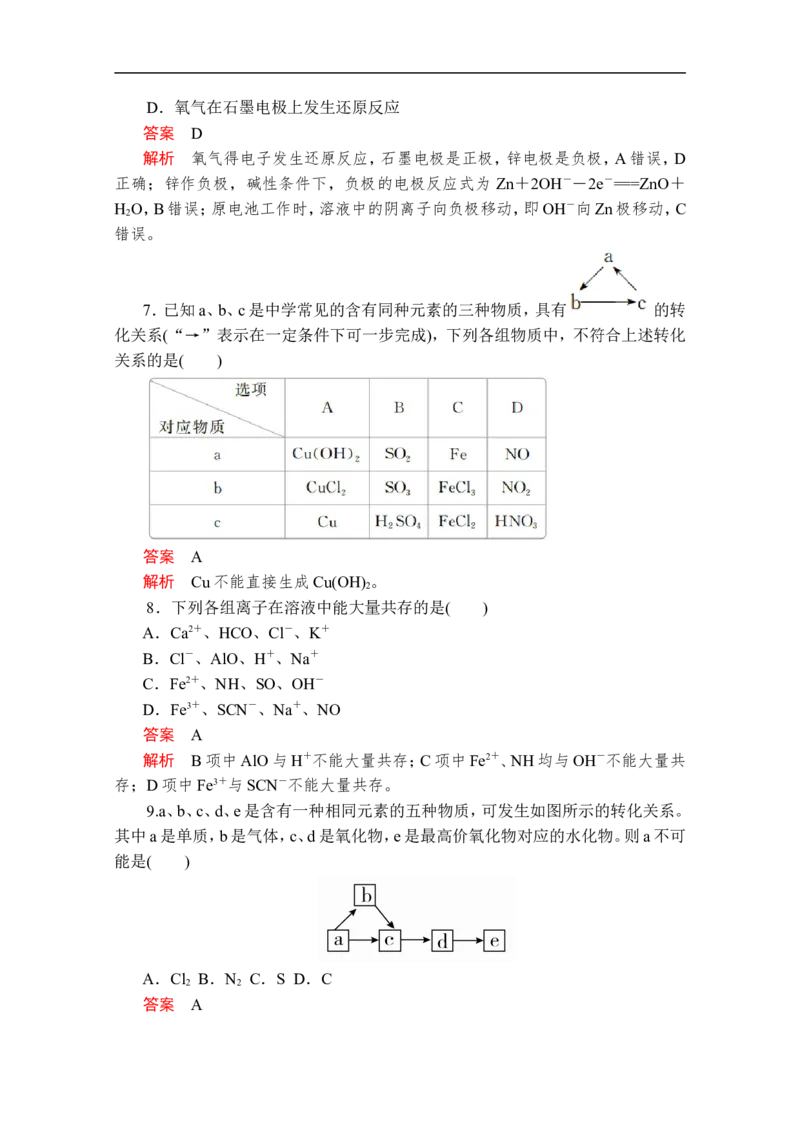
6.锌-空气电池(如图所示)适宜用作城市电动车的动力电源,该电池放电时
Zn转化为ZnO。则该电池工作时,下列说法正确的是( )
A.Zn电极是该电池的正极
B.Zn电极的电极反应式为Zn+H O-2e-===ZnO+2H+
2
C.OH-向石墨电极移动D.氧气在石墨电极上发生还原反应
答案 D
解析 氧气得电子发生还原反应,石墨电极是正极,锌电极是负极,A错误,D
正确;锌作负极,碱性条件下,负极的电极反应式为 Zn+2OH--2e-===ZnO+
H O,B错误;原电池工作时,溶液中的阴离子向负极移动,即OH-向Zn极移动,C
2
错误。
7.已知a、b、c是中学常见的含有同种元素的三种物质,具有 的转
化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化
关系的是( )
答案 A
解析 Cu不能直接生成Cu(OH) 。
2
8.下列各组离子在溶液中能大量共存的是( )
A.Ca2+、HCO、Cl-、K+
B.Cl-、AlO、H+、Na+
C.Fe2+、NH、SO、OH-
D.Fe3+、SCN-、Na+、NO
答案 A
解析 B项中AlO与H+不能大量共存;C项中Fe2+、NH均与OH-不能大量共
存;D项中Fe3+与SCN-不能大量共存。
9.a、b、c、d、e是含有一种相同元素的五种物质,可发生如图所示的转化关系。
其中a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物。则a不可
能是( )
A.Cl B.N C.S D.C
2 2
答案 A解析 符合图示转化关系的有:
10.向CuSO 溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液
4
变为棕色。再向反应后的混合物中不断通入SO 气体,溶液逐渐变成无色。下列分
2
析正确的是( )
A.滴加KI溶液时,转移2 mol e-时生成1 mol白色沉淀
B.通入SO 后溶液逐渐变成无色,体现了SO 的漂白性
2 2
C.通入SO 时,SO 与I 反应,I 作还原剂
2 2 2 2
D.上述实验条件下,物质的氧化性:Cu2+>I >SO
2 2
答案 D
解析 KI与CuSO 发生反应2Cu2++ 4I-===2CuI↓+I ,铜元素由+2价降为
4 2
+1价,则转移2 mol e-时生成2 mol白色沉淀,A错误;通入SO 时发生的反应为
2
SO +I +2H O===H SO +2HI,体现了SO 的还原性,B错误;通入SO 时,SO 作
2 2 2 2 4 2 2 2
还原剂,I 作氧化剂,C错误;氧化剂的氧化性大于氧化产物的氧化性,则物质的氧
2
化性:Cu2+>I >SO ,D正确。
2 2
11.国际上已禁止民用产品使用石棉制品,避免吸入石棉纤维而诱发肺病。某
石棉(硅酸盐)的化学式可表示为Ca Mg Si O (OH) ,式中的x、y的值分别为( )
2 x y 22 2
A.8,3 B.5,8 C.3,8 D.8,5
答案 B
解析 根据化合物中各元素的正、负化合价代数和为零可得 2×2+2x+4y-
2×22-1×2=0。则x+2y=21,只有B项符合。
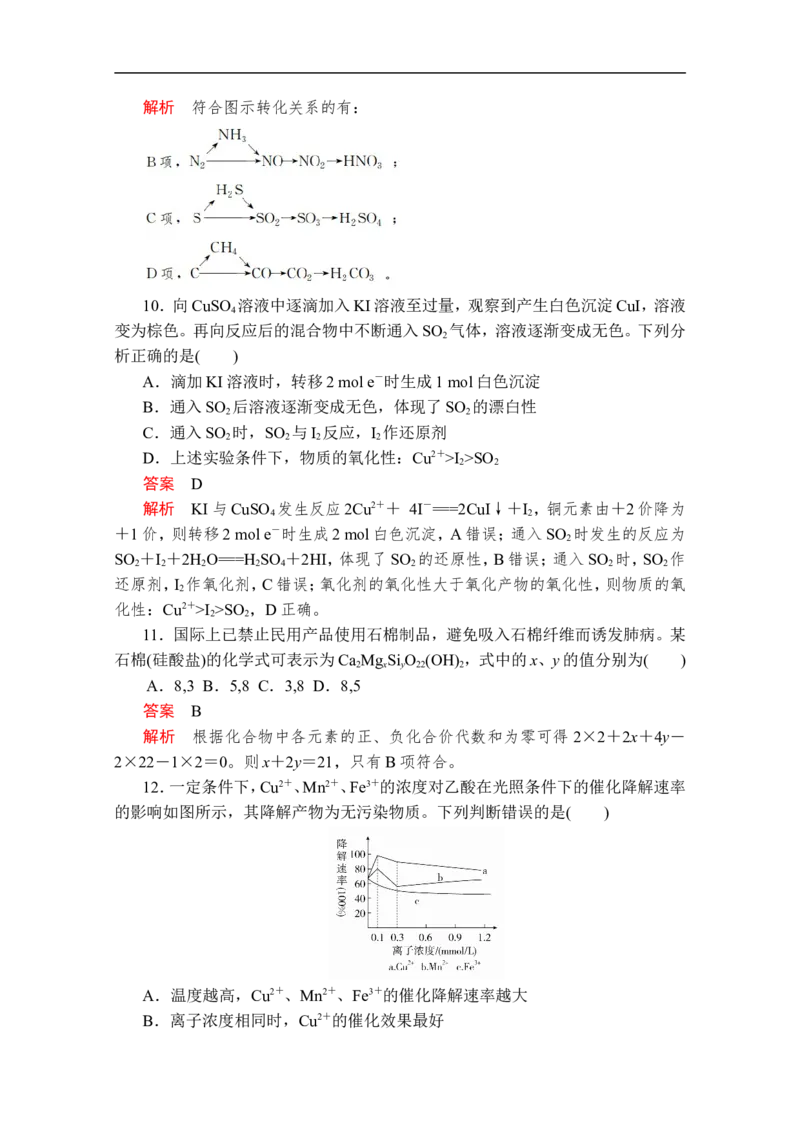
12.一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照条件下的催化降解速率
的影响如图所示,其降解产物为无污染物质。下列判断错误的是( )
A.温度越高,Cu2+、Mn2+、Fe3+的催化降解速率越大
B.离子浓度相同时,Cu2+的催化效果最好C.Fe3+的浓度对乙酸降解速率的影响不大
D.乙酸的降解产物可能是CO 和H O
2 2
答案 A
解析 Cu2+、Mn2+、Fe3+均可作乙酸降解的催化剂,要使催化剂达到最佳催化
效果,需在一定温度下进行,并不是温度越高越好,A错误。根据图示可知,相同浓
度下,a线(Cu2+)表示的降解速率最大,B正确;根据图示可知,Fe3+的浓度增加,乙
酸的降解速率变化不是很大,所以Fe3+的浓度对乙酸降解速率的影响不大,C正确;
乙酸的降解产物为无污染物质,其产物可能为CO 、H O,D正确。
2 2
13.一定质量的铜分别与足量的稀硝酸和浓硝酸完全反应,在相同条件下用排
水法收集反应产生的气体,下列叙述正确的是( )
A.硝酸浓度越大,硝酸被还原之后的生成物的价态越低,对应的硝酸的氧化
性越弱
B.硝酸浓度不同,生成Cu(NO ) 的物质的量不同
3 2
C.硝酸浓度越大,产生的气体越少
D.两者用排水法收集到的气体体积相等
答案 D
解析 硝酸的浓度越大氧化性越强,故A错误;等量的Cu与足量酸反应,生成
Cu(NO ) 的物质的量相同,故B错误;等量的Cu与足量酸反应,浓硝酸反应生成气
3 2
体多,故C错误;因3NO +H O===2HNO +NO,最终收集气体均为NO,由得失电
2 2 3
子守恒可知,收集NO的体积相等,故D正确。
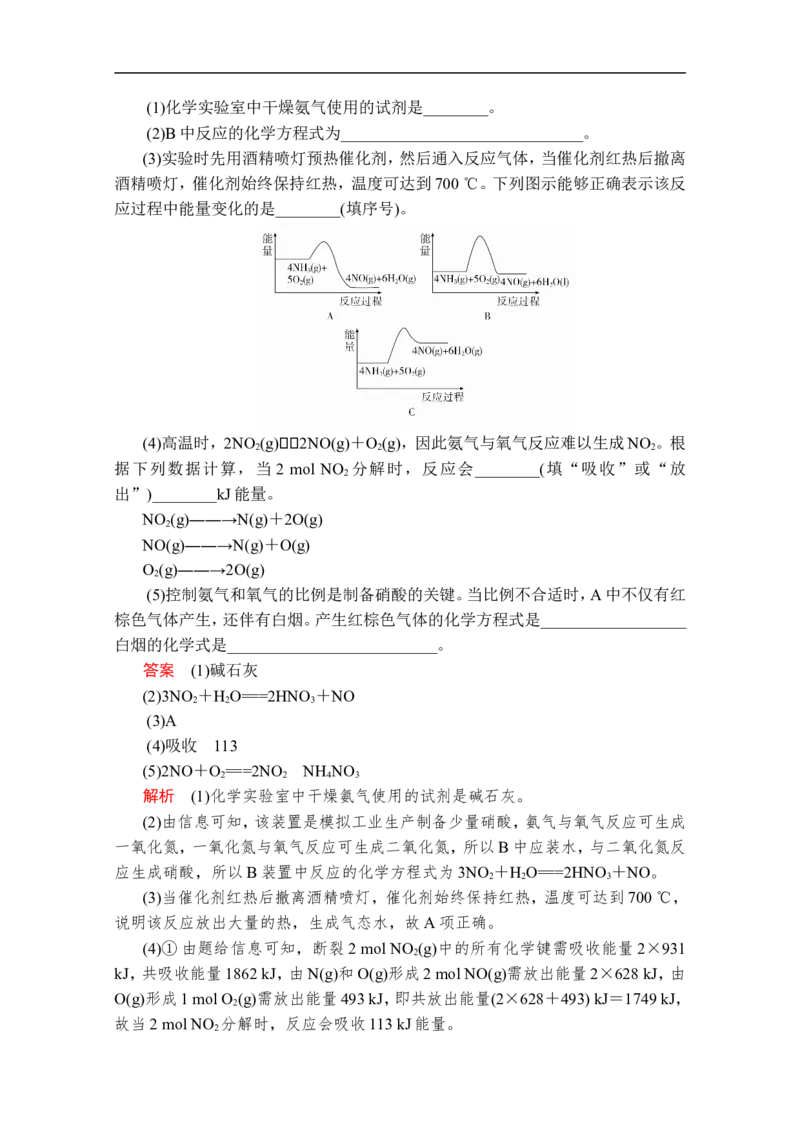
14.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体 Y同时通入
盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
答案 D
解析 在此过程中发生的反应有
C+2H SO (浓)=====CO ↑+2SO ↑+2H O
2 4 2 2 2
Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O
3 3 2 2 2
3NO +H O===2HNO +NO
2 2 3
2HNO +3SO +2H O===3H SO +2NO
3 2 2 2 42NO+O ===2NO
2 2
Ba2++SO===BaSO ↓
4
生成的沉淀是BaSO ,A、C错误;CO 不参与后续反应,所以从Z导管出来的气
4 2
体中有CO ,B错误。
2
二、非选择题(本题共4小题,共58分)
15.(14分)盐酸、硫酸和硝酸是中学阶段常见的“三大强酸”。现就硫酸、硝酸
与金属铜反应的情况,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有
关的化学方程式是________________________________________。不采用铜跟浓
硫酸反应来制取硫酸铜的原因是____________________________。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原
的硫酸为 0.9 mol。则浓硫酸的实际体积______(填“大于”“等于”或“小
于”)180 mL。
(3)若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO 溶液),则该
3
反应的离子方程式为______________________________________。
(4)将8 g Fe O 投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,
2 3
收集到1.68 L H (标准状况),同时,Fe和Fe O 均无剩余,为了中和过量的硫酸,且
2 2 3
使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物
质的量浓度为________。
答案 (1)2Cu+O =====2CuO、CuO+H SO =====CuSO +H O 生成等量的
2 2 4 4 2
硫酸铜需硫酸较多,且生成的二氧化硫污染环境
(2)大于
(3)3Cu+2NO+8H+===3Cu2++2NO↑+4H O
2
(4)2 mol·L-1
解析 (4)铁元素完全沉淀后溶液中的溶质为Na SO ,Na SO 中的Na+来源于
2 4 2 4
NaOH,SO来源于H SO ,则得出如下关系式:
2 4
H SO ~2NaOH
2 4
1 2
n 150×10-3 L×4 mol·L-1=0.6 mol
则n=0.3 mol
c(H SO )==2 mol·L-1。
2 4
16.(10分)实验室利用如下装置模拟工业生产制备少量硝酸。(1)化学实验室中干燥氨气使用的试剂是________。
(2)B中反应的化学方程式为______________________________。
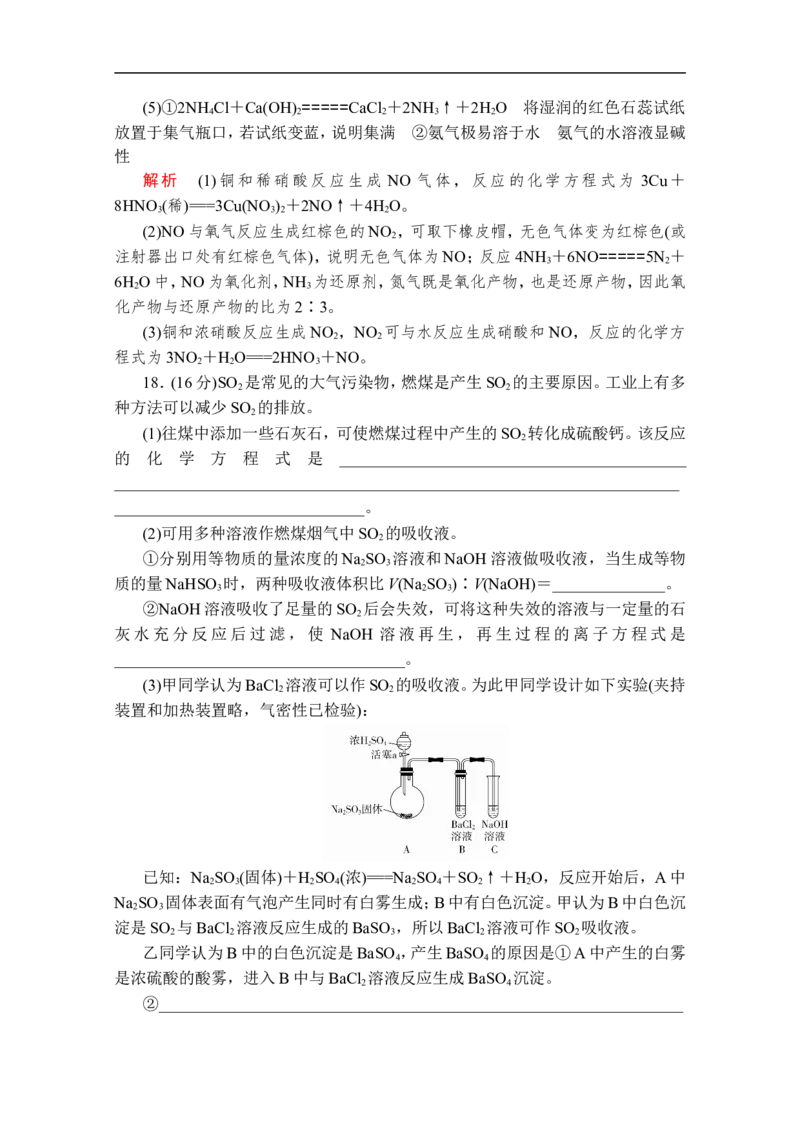
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离
酒精喷灯,催化剂始终保持红热,温度可达到700 ℃。下列图示能够正确表示该反
应过程中能量变化的是________(填序号)。
(4)高温时,2NO (g)2NO(g)+O (g),因此氨气与氧气反应难以生成NO 。根
2 2 2
据下列数据计算,当 2 mol NO 分解时,反应会________(填“吸收”或“放
2
出”)________kJ能量。
NO (g)――→N(g)+2O(g)
2
NO(g)――→N(g)+O(g)
O (g)――→2O(g)
2
(5)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红
棕色气体产生,还伴有白烟。产生红棕色气体的化学方程式是__________________
白烟的化学式是__________________________。
答案 (1)碱石灰
(2)3NO +H O===2HNO +NO
2 2 3
(3)A
(4)吸收 113
(5)2NO+O ===2NO NH NO
2 2 4 3
解析 (1)化学实验室中干燥氨气使用的试剂是碱石灰。
(2)由信息可知,该装置是模拟工业生产制备少量硝酸,氨气与氧气反应可生成
一氧化氮,一氧化氮与氧气反应可生成二氧化氮,所以B中应装水,与二氧化氮反
应生成硝酸,所以B装置中反应的化学方程式为3NO +H O===2HNO +NO。
2 2 3
(3)当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700 ℃,
说明该反应放出大量的热,生成气态水,故A项正确。
(4)①由题给信息可知,断裂2 mol NO (g)中的所有化学键需吸收能量2×931
2
kJ,共吸收能量1862 kJ,由N(g)和O(g)形成2 mol NO(g)需放出能量2×628 kJ,由
O(g)形成1 mol O (g)需放出能量493 kJ,即共放出能量(2×628+493) kJ=1749 kJ,
2
故当2 mol NO 分解时,反应会吸收113 kJ能量。
2(5)当比例不合适时,氨气与氧气反应生成的一氧化氮与过量的氧气反应可生
成红棕色的二氧化氮,反应的化学方程式为2NO+O ===2NO ;二氧化氮再与水蒸
2 2
气反应生成硝酸,硝酸与氨气反应有白烟生成,即生成硝酸铵,化学式为NH NO 。
4 3
17.(18分)某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO。
实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜
丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生。
(1) 请 写 出 铜 与 稀 硝 酸 反 应 的 化 学 方 程 式 :
______________________________________________________________________
______________________________________________________________________
____。
(2) 若 证 明 无 色 气 体 是 NO 的 实 验 操 作 和 现 象 是
________________________________。一氧化氮是大气污染物之一。目前有一种治
理方法是在400 ℃左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水
该反应的化学方程式为4NH +6NO=====5N +6H O,每有10 mol N 生成,氧化
3 2 2 2
产物与还原产物的比为________。
(3)若将上述稀硝酸换成浓硝酸,其生成的气体通入水中,发生反应的化学方程
式 为 _______________________________________________________________
______________________________________________________________________
_________。
(4)分别将等质量的铜片与等体积过量的浓、稀硝酸反应,所得溶液前者呈绿色
后者呈蓝色。某同学认为可能是 Cu2+浓度的差异引起的,你认为是否正确?
________( 填 “ 正 确 ” 或 “ 不 正 确 ” ) , 理 由 是
__________________________________________。
(5)① 写出实验室由 NH Cl 和 Ca(OH) 加热制取氨气的化学方程式:
4 2
__________________________________ ; 检 验 氨 气 已 收 集 满 的 方 法 是
__________________________________。
②进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两
个重要性质分别是________、____________。
答案 (1)3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O
3 3 2 2
(2)取下橡皮帽,注射器口处无色气体变为红棕色 2∶3
(3)3NO +H O===2HNO +NO
2 2 3
(4)不正确 等质量的铜与等体积过量的浓、稀硝酸反应后,所得溶液中Cu2+的
浓度相等(5)①2NH Cl+Ca(OH) =====CaCl +2NH ↑+2H O 将湿润的红色石蕊试纸
4 2 2 3 2
放置于集气瓶口,若试纸变蓝,说明集满 ②氨气极易溶于水 氨气的水溶液显碱
性
解析 (1)铜和稀硝酸反应生成 NO 气体,反应的化学方程式为 3Cu+
8HNO (稀)===3Cu(NO ) +2NO↑+4H O。
3 3 2 2
(2)NO与氧气反应生成红棕色的NO ,可取下橡皮帽,无色气体变为红棕色(或
2
注射器出口处有红棕色气体),说明无色气体为NO;反应4NH +6NO=====5N +
3 2
6H O中,NO为氧化剂,NH 为还原剂,氮气既是氧化产物,也是还原产物,因此氧
2 3
化产物与还原产物的比为2∶3。
(3)铜和浓硝酸反应生成NO ,NO 可与水反应生成硝酸和NO,反应的化学方
2 2
程式为3NO +H O===2HNO +NO。
2 2 3
18.(16分)SO 是常见的大气污染物,燃煤是产生SO 的主要原因。工业上有多
2 2
种方法可以减少SO 的排放。
2
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO 转化成硫酸钙。该反应
2
的 化 学 方 程 式 是 ___________________________________________
______________________________________________________________________
_______________________________。
(2)可用多种溶液作燃煤烟气中SO 的吸收液。
2
①分别用等物质的量浓度的Na SO 溶液和NaOH溶液做吸收液,当生成等物
2 3
质的量NaHSO 时,两种吸收液体积比V(Na SO )∶V(NaOH)=______________。
3 2 3
②NaOH溶液吸收了足量的SO 后会失效,可将这种失效的溶液与一定量的石
2
灰水充分反应后过滤,使 NaOH 溶液再生,再生过程的离子方程式是
____________________________________。
(3)甲同学认为BaCl 溶液可以作SO 的吸收液。为此甲同学设计如下实验(夹持
2 2
装置和加热装置略,气密性已检验):
已知:Na SO (固体)+H SO (浓)===Na SO +SO ↑+H O,反应开始后,A中
2 3 2 4 2 4 2 2
Na SO 固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲认为B中白色沉
2 3
淀是SO 与BaCl 溶液反应生成的BaSO ,所以BaCl 溶液可作SO 吸收液。
2 2 3 2 2
乙同学认为B中的白色沉淀是BaSO ,产生BaSO 的原因是①A中产生的白雾
4 4
是浓硫酸的酸雾,进入B中与BaCl 溶液反应生成BaSO 沉淀。
2 4
②________________________________________________________________________。
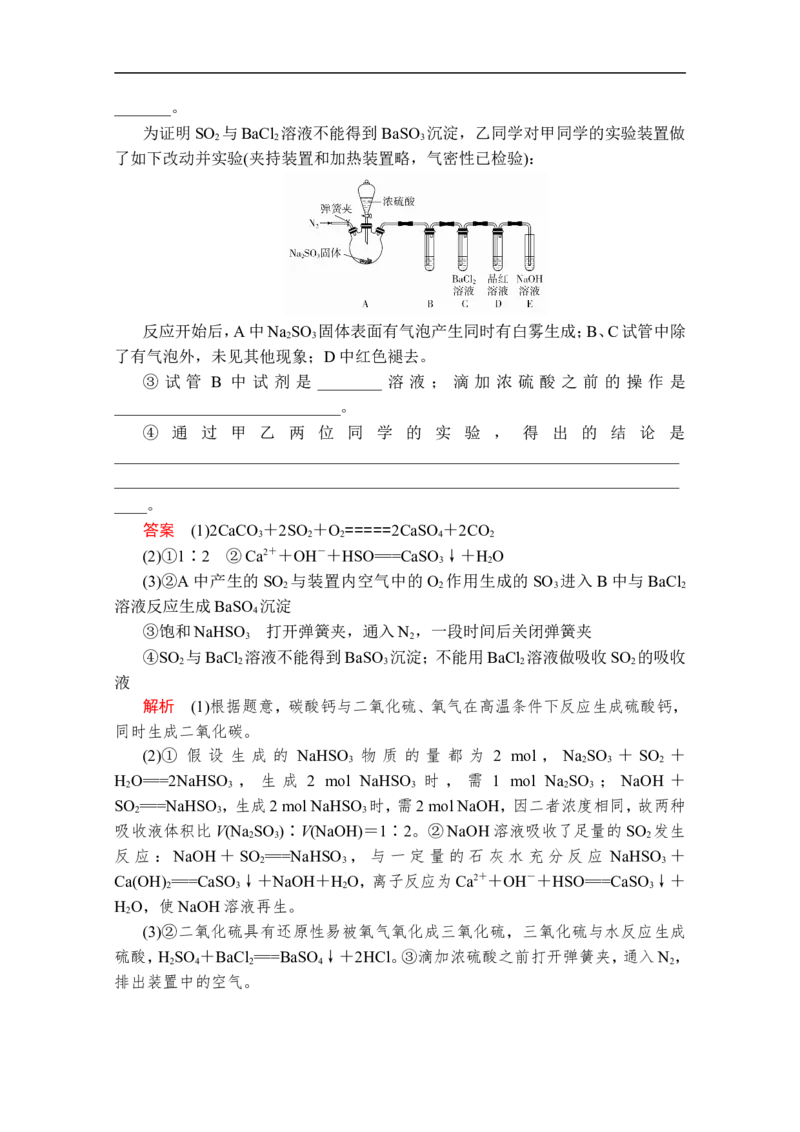
为证明SO 与BaCl 溶液不能得到BaSO 沉淀,乙同学对甲同学的实验装置做
2 2 3
了如下改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中Na SO 固体表面有气泡产生同时有白雾生成;B、C试管中除
2 3
了有气泡外,未见其他现象;D中红色褪去。
③ 试 管 B 中 试 剂 是 ________ 溶 液 ; 滴 加 浓 硫 酸 之 前 的 操 作 是
____________________________。
④ 通 过 甲 乙 两 位 同 学 的 实 验 , 得 出 的 结 论 是
______________________________________________________________________
______________________________________________________________________
____。
答案 (1)2CaCO +2SO +O =====2CaSO +2CO
3 2 2 4 2
(2)①1∶2 ②Ca2++OH-+HSO===CaSO ↓+H O
3 2
(3)②A中产生的SO 与装置内空气中的 O 作用生成的SO 进入B中与BaCl
2 2 3 2
溶液反应生成BaSO 沉淀
4
③饱和NaHSO 打开弹簧夹,通入N ,一段时间后关闭弹簧夹
3 2
④SO 与BaCl 溶液不能得到BaSO 沉淀;不能用BaCl 溶液做吸收SO 的吸收
2 2 3 2 2
液
解析 (1)根据题意,碳酸钙与二氧化硫、氧气在高温条件下反应生成硫酸钙,
同时生成二氧化碳。
(2)① 假 设 生 成 的 NaHSO 物 质 的 量 都 为 2 mol , Na SO + SO +
3 2 3 2
H O===2NaHSO , 生 成 2 mol NaHSO 时 , 需 1 mol Na SO ; NaOH +
2 3 3 2 3
SO ===NaHSO ,生成2 mol NaHSO 时,需2 mol NaOH,因二者浓度相同,故两种
2 3 3
吸收液体积比V(Na SO )∶V(NaOH)=1∶2。②NaOH溶液吸收了足量的SO 发生
2 3 2
反应:NaOH+SO ===NaHSO ,与一定量的石灰水充分反应 NaHSO +
2 3 3
Ca(OH) ===CaSO ↓+NaOH+H O,离子反应为Ca2++OH-+HSO===CaSO ↓+
2 3 2 3
H O,使NaOH溶液再生。
2
(3)②二氧化硫具有还原性易被氧气氧化成三氧化硫,三氧化硫与水反应生成
硫酸,H SO +BaCl ===BaSO ↓+2HCl。③滴加浓硫酸之前打开弹簧夹,通入N ,
2 4 2 4 2
排出装置中的空气。