文档内容
期中备考试卷(一)
时间:90分钟 满分:100分
一、选择题(本题共14小题,每小题3分,共42分,每小题仅有一个选项符合
题意)
1.化学与生产、生活息息相关,下列叙述错误的是( )
A.用活性炭去除冰箱中的异味
B.制饭勺、饭盒、高压锅的不锈钢是合金
C.工业生产玻璃、水泥和陶瓷,均需用石灰石作原料
D.人类超量排放氮氧化物和二氧化硫是形成酸雨的主要原因
答案 C
解析 生产陶瓷的原料是黏土。
2.下列物质的使用不涉及化学变化的是( )
A.明矾作净水剂 B.液氨用作制冷剂
C.氢氟酸刻蚀玻璃 D.生石灰作干燥剂
答案 B
解析 A项,明矾溶于水电离出的铝离子水解生成氢氧化铝胶体,胶体具有吸
附性,可用作净水剂,包含化学变化;B项,液氨汽化时吸热,使周围环境温度急剧
降低,因此可用作制冷剂,物质的三态变化属于物理变化;C项,氢氟酸能与玻璃中
的二氧化硅反应生成四氟化硅和水,因此可用于刻蚀玻璃,属于化学变化;D项,生
石灰与水反应生成氢氧化钙,可用作干燥剂,属于化学变化。
3.下列说法正确的是( )
A.硫粉在空气中燃烧生成SO ,在纯氧中燃烧生成SO
2 3
B.可以用品红溶液鉴别SO 和CO
2 2
C.SO 能使品红溶液、酸性KMnO 溶液褪色,褪色原理相同
2 4
D.SO 通入CaCl 溶液中,有白色沉淀生成
2 2
答案 B
解析 硫粉在过量的纯氧中燃烧只能生成SO ,A错误;SO 能使品红溶液褪
2 2
色是因为SO 具有漂白性;SO 能使酸性KMnO 溶液褪色,是因为SO 具有还原性,
2 2 4 2
二者褪色原理不同,C错误;亚硫酸酸性比盐酸弱,SO 与CaCl 溶液不反应,D错
2 2
误。
4.下列实验操作或事故处理方法错误的是( )
A.少量的金属钠应保存在煤油中B.不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
C.将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌
D.大量氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向低处跑
答案 D
解析 钠与空气中的水和氧气反应,少量的钠保存在煤油中,A正确;万一酸
液溅到眼睛里,如果立即揉眼睛会加重酸液对眼的腐蚀,B正确;浓硫酸比水重,且
溶于水放出大量的热,所以将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅
拌,C正确;氯气有毒,且氯气的密度比空气大,应该往高处跑,D错误。
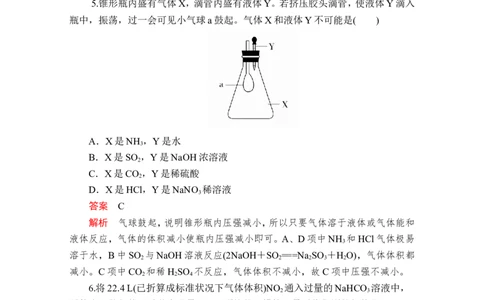
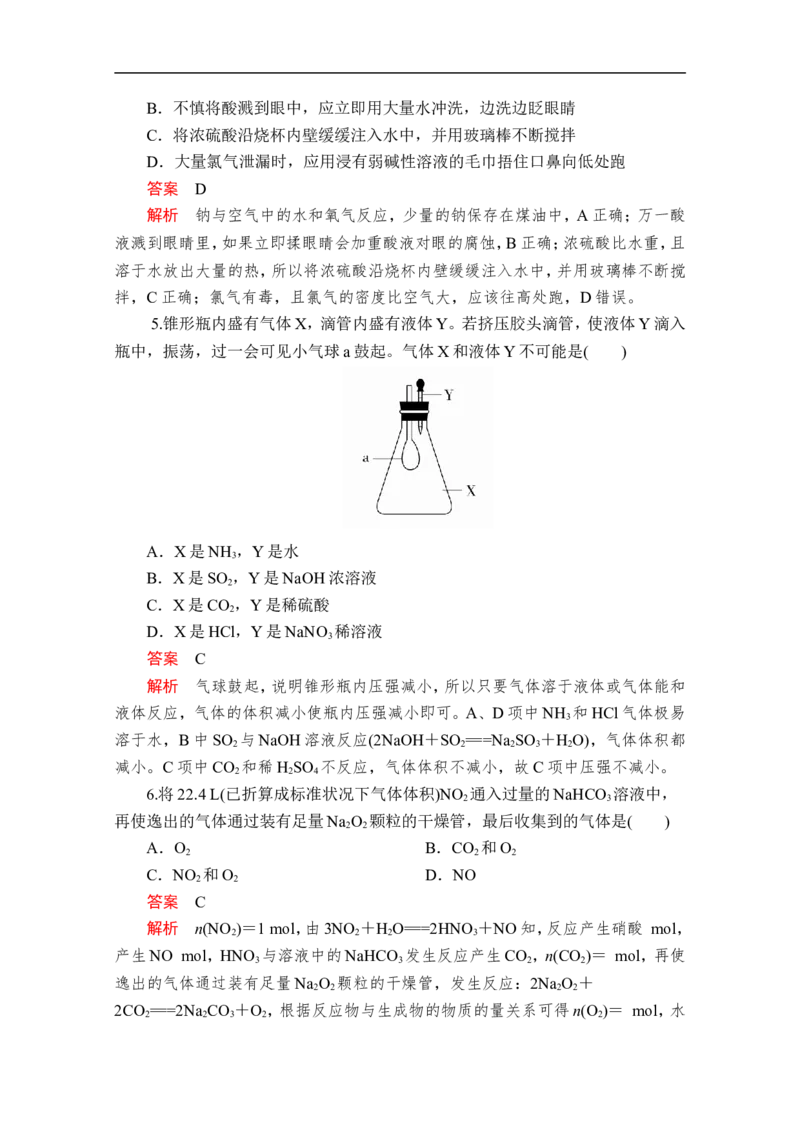
5.锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入
瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
A.X是NH ,Y是水
3
B.X是SO ,Y是NaOH浓溶液
2
C.X是CO ,Y是稀硫酸
2
D.X是HCl,Y是NaNO 稀溶液
3
答案 C
解析 气球鼓起,说明锥形瓶内压强减小,所以只要气体溶于液体或气体能和
液体反应,气体的体积减小使瓶内压强减小即可。A、D项中NH 和HCl气体极易
3
溶于水,B中SO 与NaOH溶液反应(2NaOH+SO ===Na SO +H O),气体体积都
2 2 2 3 2
减小。C项中CO 和稀H SO 不反应,气体体积不减小,故C项中压强不减小。
2 2 4
6.将22.4 L(已折算成标准状况下气体体积)NO 通入过量的NaHCO 溶液中,
2 3
再使逸出的气体通过装有足量Na O 颗粒的干燥管,最后收集到的气体是( )
2 2
A.O B.CO 和O
2 2 2
C.NO 和O D.NO
2 2
答案 C
解析 n(NO )=1 mol,由3NO +H O===2HNO +NO知,反应产生硝酸 mol,
2 2 2 3
产生NO mol,HNO 与溶液中的NaHCO 发生反应产生CO ,n(CO )= mol,再使
3 3 2 2
逸出的气体通过装有足量Na O 颗粒的干燥管,发生反应:2Na O +
2 2 2 2
2CO ===2Na CO +O ,根据反应物与生成物的物质的量关系可得n(O )= mol,水
2 2 3 2 2蒸气也和Na O 反应产生氧气,所以氧气大于 mol, NO与O 发生反应:2NO+
2 2 2
O ===2NO 。由于二者反应时物质的量之比是2∶1,而实际n(NO)= mol,n(O )>
2 2 2
mol,所以氧气过量,反应后气体为过量的氧气与反应产生的NO 的混合气体。
2
7.将一定量纯净的氨基甲酸铵(NH COONH )置于特制的密闭真空容器中(假设
2 4
容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH COONH (s)2NH (g)+CO (g)。下列可以判断该分解反应已经达到化学
2 4 3 2
平衡状态的是( )
A.v(NH )=2v(CO )
3 2
B.密闭容器中总压强不变
C.密闭容器中混合气体的平均相对分子质量不变
D.密闭容器中氨气的体积分数不变
答案 B
解析 未指明正、逆反应速率,A错误;反应前后气体体积变化的反应,密闭容
器中总压强不变,说明达到平衡状态,B正确;混合气体中NH 和CO 的物质的量
3 2
之比为定值(2∶1),其相对分子质量也为定值,故C、D两项不能作为达到平衡的标
志。
8.NO和CO都是汽车尾气中的物质,它们能很缓慢地反应生成N 和CO ,对
2 2
此反应有关的叙述中不正确的是( )
A.升高温度能加快化学反应速率
B.使用适当催化剂可以加快化学反应速率
C.降低压强能降低化学反应速率
D.增大压强对化学反应速率没有影响
答案 D
解析 升高温度,加入催化剂,能加快化学反应速率,降低压强,对有气体参加
的反应其反应速率降低,而增大压强,可增大有气体参加反应的反应速率。
9.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一
定有CO
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定
有NH
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
答案 C解析 A项可能含有HCO,B项可能含有Ag+,C项正确,D项可能含Ca2+。
10.利用实验器材(规格和数量不限),能完成相应实验的一项是( )
答案 D
解析 A项,缺少酒精灯,错误;B项,缺少过滤的漏斗,错误;C项,缺少称量
用的天平,错误;D项,用溴水置换碘后,用CCl 萃取除去过量的溴和反应得到的
4
碘,正确。
11.将2.56 g Cu和一定量的浓HNO 反应,随着Cu的不断减少,反应生成气体
3
的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况下),则反应中
消耗HNO 的物质的量为( )
3
A.0.05 mol B.1 mol
C.1.05 mol D.0.13 mol
答案 D
解析 反应消耗的硝酸包括起酸性作用的硝酸与起氧化作用的硝酸两部分,
其中起酸性作用的硝酸最终变为硝酸铜,n(HNO )=n[Cu(NO ) ]=2n(Cu)=2×0.04
3 3 2
mol=0.08 mol,作氧化剂的硝酸最终变为气体(NO+NO ),则n(HNO )=n(气体)=
2 3
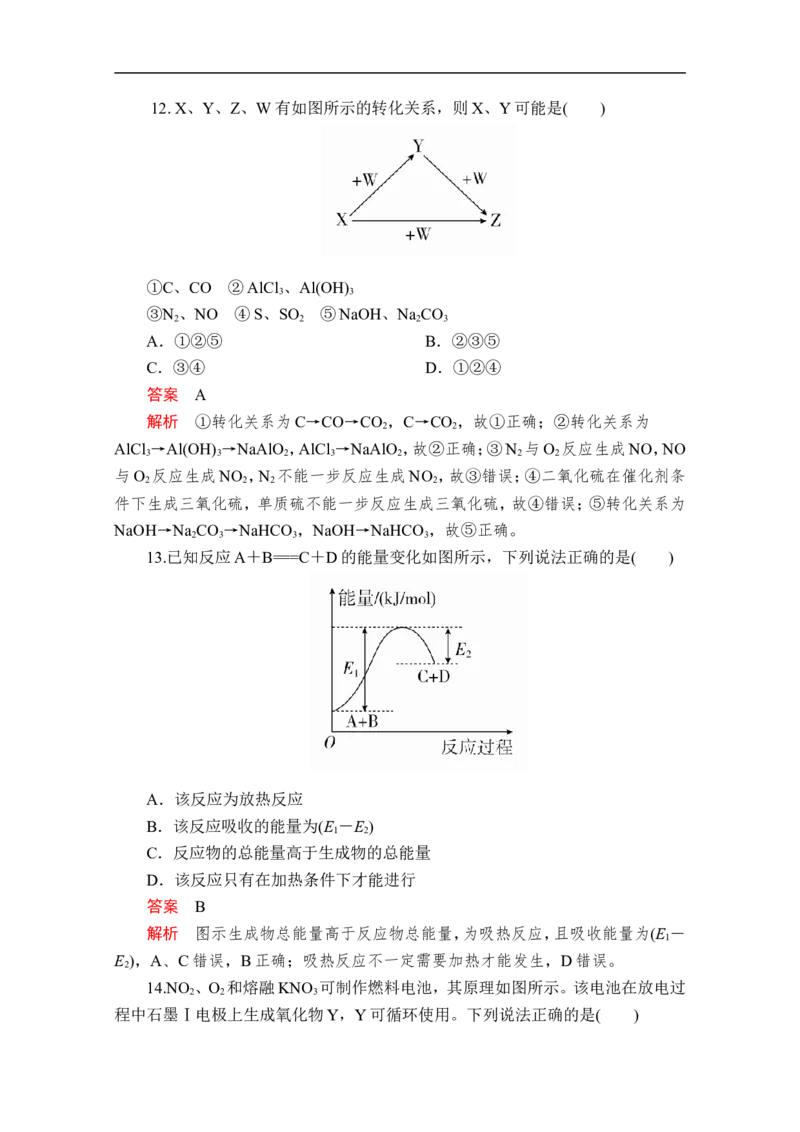
0.05 mol,反应消耗的硝酸总物质的量=0.08 mol+0.05 mol=0.13 mol。12. X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②AlCl 、Al(OH)
3 3
③N 、NO ④S、SO ⑤NaOH、Na CO
2 2 2 3
A.①②⑤ B.②③⑤
C.③④ D.①②④
答案 A
解析 ①转化关系为C→CO→CO ,C→CO ,故①正确;②转化关系为
2 2
AlCl →Al(OH) →NaAlO ,AlCl →NaAlO ,故②正确;③N 与O 反应生成NO,NO
3 3 2 3 2 2 2
与O 反应生成NO ,N 不能一步反应生成NO ,故③错误;④二氧化硫在催化剂条
2 2 2 2
件下生成三氧化硫,单质硫不能一步反应生成三氧化硫,故④错误;⑤转化关系为
NaOH→Na CO →NaHCO ,NaOH→NaHCO ,故⑤正确。
2 3 3 3
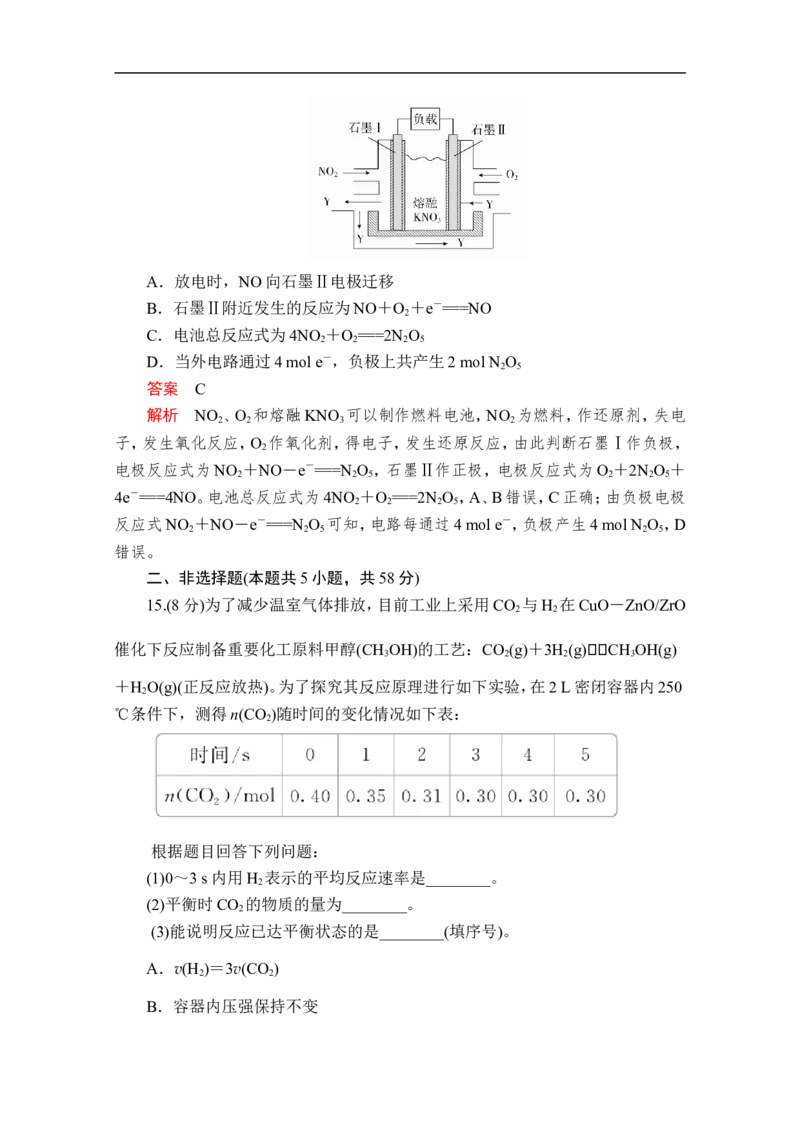
13.已知反应A+B===C+D的能量变化如图所示,下列说法正确的是( )
A.该反应为放热反应
B.该反应吸收的能量为(E -E )
1 2
C.反应物的总能量高于生成物的总能量
D.该反应只有在加热条件下才能进行
答案 B
解析 图示生成物总能量高于反应物总能量,为吸热反应,且吸收能量为(E -
1
E ),A、C错误,B正确;吸热反应不一定需要加热才能发生,D错误。
2
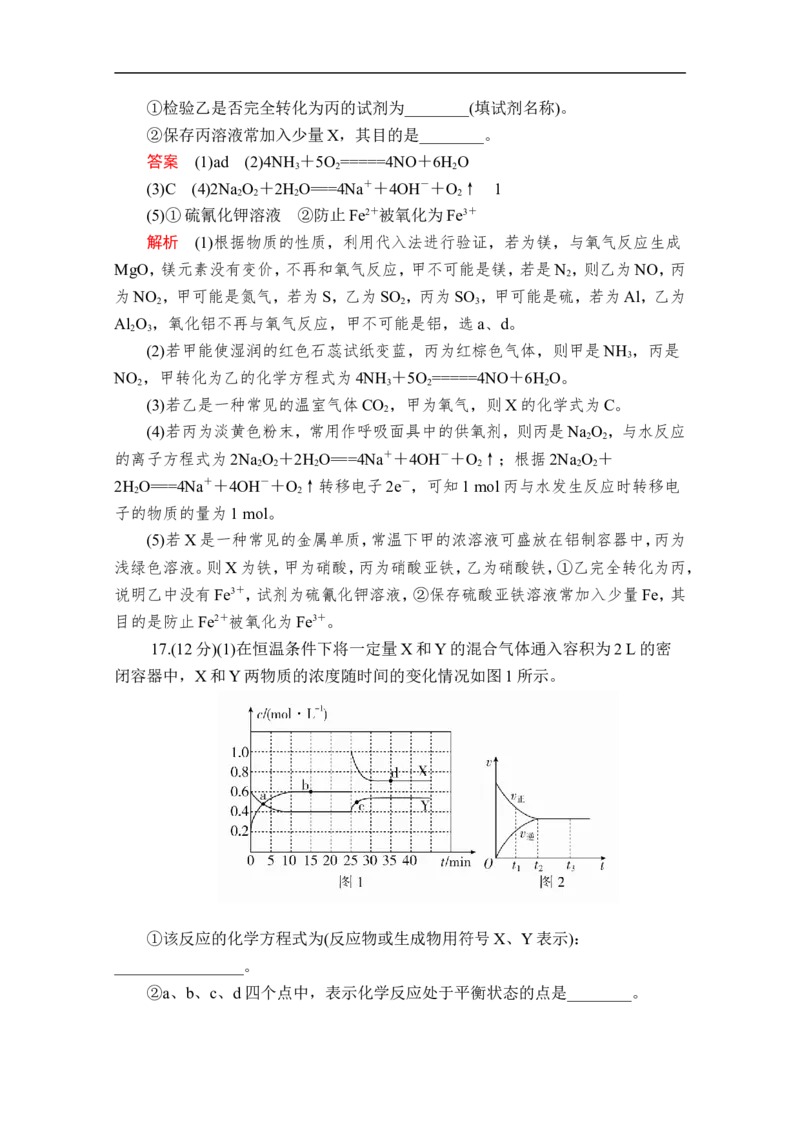
14.NO 、O 和熔融KNO 可制作燃料电池,其原理如图所示。该电池在放电过
2 2 3
程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用。下列说法正确的是( )A.放电时,NO向石墨Ⅱ电极迁移
B.石墨Ⅱ附近发生的反应为NO+O +e-===NO
2
C.电池总反应式为4NO +O ===2N O
2 2 2 5
D.当外电路通过4 mol e-,负极上共产生2 mol N O
2 5
答案 C
解析 NO 、O 和熔融KNO 可以制作燃料电池,NO 为燃料,作还原剂,失电
2 2 3 2
子,发生氧化反应,O 作氧化剂,得电子,发生还原反应,由此判断石墨Ⅰ作负极,
2
电极反应式为NO +NO-e-===N O ,石墨Ⅱ作正极,电极反应式为O +2N O +
2 2 5 2 2 5
4e-===4NO。电池总反应式为4NO +O ===2N O ,A、B错误,C正确;由负极电极
2 2 2 5
反应式NO +NO-e-===N O 可知,电路每通过4 mol e-,负极产生4 mol N O ,D
2 2 5 2 5
错误。
二、非选择题(本题共5小题,共58分)
15.(8分)为了减少温室气体排放,目前工业上采用CO 与H 在CuO-ZnO/ZrO
2 2
催化下反应制备重要化工原料甲醇(CH OH)的工艺:CO (g)+3H (g)CH OH(g)
3 2 2 3
+H O(g)(正反应放热)。为了探究其反应原理进行如下实验,在2 L密闭容器内250
2
℃条件下,测得n(CO )随时间的变化情况如下表:
2
根据题目回答下列问题:
(1)0~3 s内用H 表示的平均反应速率是________。
2
(2)平衡时CO 的物质的量为________。
2
(3)能说明反应已达平衡状态的是________(填序号)。
A.v(H )=3v(CO )
2 2
B.容器内压强保持不变C.v (CO )=v (CH OH)
逆 2 正 3
D.容器内密度保持不变
(4)为了提高经济效益,下列措施可行的是________(填序号)。
A.增大H 浓度,提升CO 的转化率
2 2
B.增大CO 浓度
2
C.选择适当的催化剂
答案 (1)0.05 mol·L-1·s-1 (2)0.30 mol
(3)BC (4)BC
解析 (1)v(H )=3v(CO )=3×=0.05 mol·L-1·s-1。
2 2
(2)3 s后,CO 浓度不随时间变化而变化,说明反应达到平衡,此时CO 为0.30
2 2
mol。
(3)选项A,任何时刻均有v(H )=3v(CO )。选项B,容器内压强不变,说明混合
2 2
体系中各种物质的含量恒定,反应达到平衡。选项C,v (CO )=v (CH OH)=v
逆 2 正 3 正
(CO ),说明CO 的消耗速率等于其生成速率,反应达到平衡。选项D,因气体的体
2 2
积及质量不变,任何时刻气体的密度不变。
(4)选项A,H 价格高,CO 价格低,增加H 浓度来提高CO 的转化率不能提高
2 2 2 2
经济效益。选项B,增加廉价CO 浓度正反应速率加快且增大H 转化率,有利于提
2 2
高经济效益。选项C,选用合适的催化剂能加快反应速率,有利于提高经济效益。
16.(14分)甲、乙、丙、X是中学化学中常见的物质,在一定条件下,它们之间的
转化关系如下图所示(部分产物已略去)。请回答下列问题:
――→――→
(1)若X是O ,则甲不可能是________(填代号)
2
a.Mg b.N c.S d.Al
2
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的
化学方程式:______________________________________。
(3)若乙是一种常见的温室气体,则X的化学式为________。
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与水反应的离子方
程式为__________________;1 mol丙与水发生反应时转移电子的物质的量为
________mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙
为浅绿色溶液。①检验乙是否完全转化为丙的试剂为________(填试剂名称)。
②保存丙溶液常加入少量X,其目的是________。
答案 (1)ad (2)4NH +5O =====4NO+6H O
3 2 2
(3)C (4)2Na O +2H O===4Na++4OH-+O ↑ 1
2 2 2 2
(5)①硫氰化钾溶液 ②防止Fe2+被氧化为Fe3+
解析 (1)根据物质的性质,利用代入法进行验证,若为镁,与氧气反应生成
MgO,镁元素没有变价,不再和氧气反应,甲不可能是镁,若是N ,则乙为NO,丙
2
为NO ,甲可能是氮气,若为S,乙为SO ,丙为SO ,甲可能是硫,若为Al,乙为
2 2 3
Al O ,氧化铝不再与氧气反应,甲不可能是铝,选a、d。
2 3
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体,则甲是NH ,丙是
3
NO ,甲转化为乙的化学方程式为4NH +5O =====4NO+6H O。
2 3 2 2
(3)若乙是一种常见的温室气体CO ,甲为氧气,则X的化学式为C。
2
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙是Na O ,与水反应
2 2
的离子方程式为2Na O +2H O===4Na++4OH-+O ↑;根据2Na O +
2 2 2 2 2 2
2H O===4Na++4OH-+O ↑转移电子2e-,可知1 mol丙与水发生反应时转移电
2 2
子的物质的量为1 mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为
浅绿色溶液。则X为铁,甲为硝酸,丙为硝酸亚铁,乙为硝酸铁,①乙完全转化为丙,
说明乙中没有Fe3+,试剂为硫氰化钾溶液,②保存硫酸亚铁溶液常加入少量Fe,其
目的是防止Fe2+被氧化为Fe3+。
17.(12分)(1)在恒温条件下将一定量X和Y的混合气体通入容积为2 L的密
闭容器中,X和Y两物质的浓度随时间的变化情况如图1所示。
①该反应的化学方程式为(反应物或生成物用符号X、Y表示):
________________。
②a、b、c、d四个点中,表示化学反应处于平衡状态的点是________。(2)如图2所示是可逆反应X +3Y 2Z的反应速率(v)与时间(t)的关系曲线,
2 2
下列叙述正确的是________。
A.t 时,只有正方向反应在进行
1
B.t 时,反应达到最大限度
2
C.t ~t ,反应不再进行
2 3
D.t ~t ,各物质的浓度不再发生变化
2 3
答案 (1)①Y2X ②bd (2)BD
解析 (1)从浓度变化趋势来看,X为生成物,Y为反应物。15 min时X增加了
0.4 mol·L-1,Y减小了0.2 mol·L-1,故X、Y的化学计量数之比为2∶1,10~25 min
内,X、Y的浓度不发生变化,达到化学平衡状态,则该反应为可逆反应,化学方程
式为Y2X。b、d两点处于化学平衡状态。
(2)对于可逆反应,反应开始后的任何时刻,正、逆反应均在进行。根据图像可
知,0~t 反应处于非平衡状态,t 后,正、逆反应速率相等,但不等于0;处于平衡状
2 2
态时,各物质的浓度不再发生变化,故B、D正确。
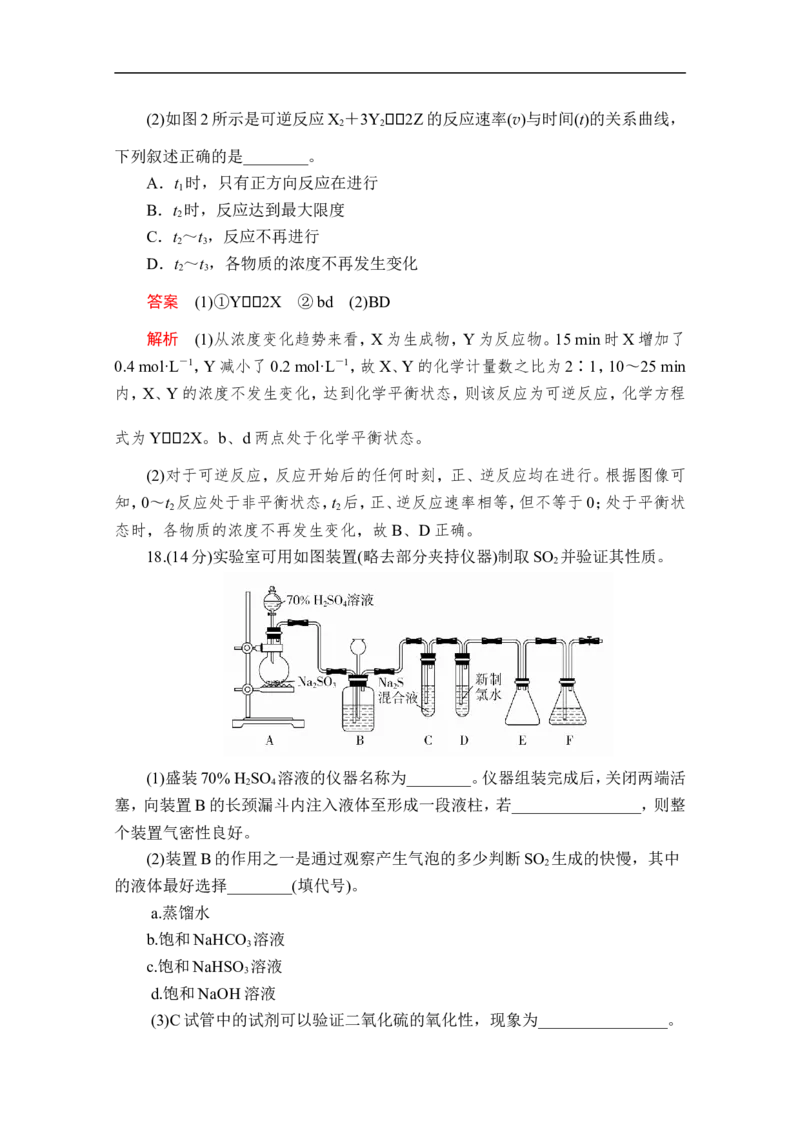
18.(14分)实验室可用如图装置(略去部分夹持仪器)制取SO 并验证其性质。
2
(1)盛装70% H SO 溶液的仪器名称为________。仪器组装完成后,关闭两端活
2 4
塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若________________,则整
个装置气密性良好。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO 生成的快慢,其中
2
的液体最好选择________(填代号)。
a.蒸馏水
b.饱和NaHCO 溶液
3
c.饱和NaHSO 溶液
3
d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为________________。(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别
进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO 溶液,有白色沉淀生成;
3
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl 溶液,产生白色沉淀。
2
上述方案合理的是方案________(填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反
应的离子方程式为__________________________________________。
(5)装置E的作用是________。装置F中为________溶液。
答案 (1)分液漏斗 液柱高度保持不变
(2)c
(3)有浅黄色沉淀生成
(4)Ⅲ SO +Cl +2H O===4H++SO+2Cl-
2 2 2
(5)防止倒吸 NaOH
解析 (1)根据仪器特点,该仪器名称为分液漏斗;液柱高度保持不变,说明气
密性良好。
(2)SO 易溶于水,能与NaOH溶液、NaHCO 溶液反应,但在NaHSO 溶液中溶
2 3 3
解度较小,c项正确。
(3)SO 能将S2-氧化,生成硫单质,所以现象为有浅黄色沉淀生成。
2
(4)方案Ⅰ,氯水中加入AgNO 溶液也可得到白色沉淀;方案Ⅱ中二氧化硫和
3
氯水均可使品红褪色;方案Ⅲ中产生沉淀可证明SO 与Cl 发生了氧化还原反应(因
2 2
溶液显酸性,不会产生BaSO 沉淀,而是BaSO 沉淀),选方案Ⅲ。
3 4
(5)E为安全瓶,防止倒吸;装置F起到吸收尾气中SO 、H S的作用,可选用
2 2
NaOH溶液。
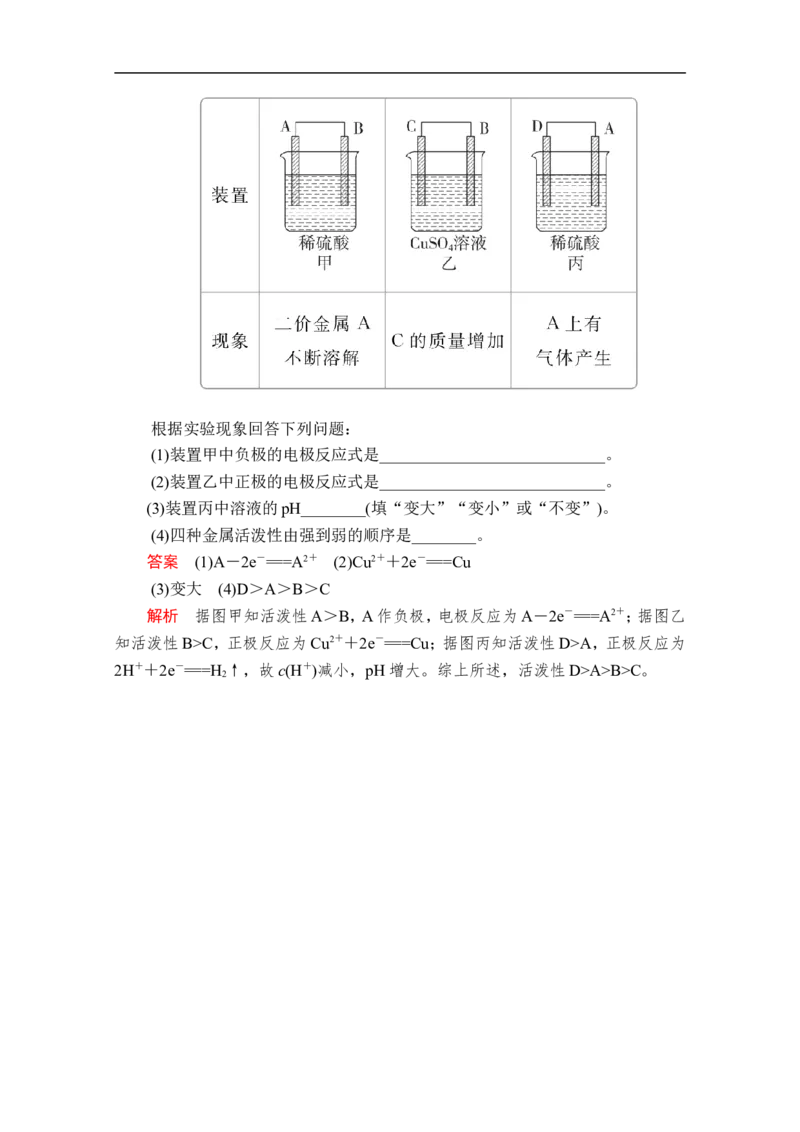
19.(10分)由A、B、C、D四种金属按表中装置进行实验。根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是____________________________。
(2)装置乙中正极的电极反应式是____________________________。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活泼性由强到弱的顺序是________。
答案 (1)A-2e-===A2+ (2)Cu2++2e-===Cu
(3)变大 (4)D>A>B>C
解析 据图甲知活泼性A>B,A作负极,电极反应为A-2e-===A2+;据图乙
知活泼性B>C,正极反应为Cu2++2e-===Cu;据图丙知活泼性D>A,正极反应为
2H++2e-===H ↑,故c(H+)减小,pH增大。综上所述,活泼性D>A>B>C。
2