文档内容
2.4化学反应的调控(分层作业)
1.在一定温度和压强下,在密闭容器中充入H、N、NH ,开始时其物质的量之比为3∶1∶1,反应达平衡后,
2 2 3
H、N、NH 的物质的量之比为9∶3∶4,则此时氮气的转化率为
2 2 3
A.10% B.20%
C.15% D.30%
2.一定温度下,向一恒容密闭容器中充入一定量的 和 ,测得容器中 的百分含量随时间的变化如图所
示,已知该条件下, 、 和 均为气体,下列说法正确的是
A.该温度和压强下, 和 一定不发生反应
B. 时刻与 时刻, 的百分含量也一定相同
C.若 时刻与 时刻的压强不同,则 %
D. 时刻与 时刻,反应均处于平衡状态
3.下列关于工业合成氨的叙述正确的是
A.合成氨工业温度选择为700 K左右,主要是为了提高NH 产率
3
B.使用催化剂和施加高压,都能提高反应速率,但对化学平衡状态无影响
C.合成氨生产过程中将NH 液化分离,可提高其自身的转化率
3
D.合成氨工业中为了提高氢气的利用率,可适当增加氮气浓度
4.接触法制硫酸生产中接触室的反应为2SO (g)+O(g) 2SO (g) ΔH=-196.6 kJ/mol,能提高SO 转化率的条
2 2 3 2
件是
A.400~500 ℃ B.常压 C.催化剂 D.过量的空气
5.工业合成氨: ,一般采用 左右的温度,其原因是:
①提高 的平衡转化率 ②适当提高氨的合成速率 ③提高氨的产率 ④催化剂在 左右时活性
最大
A.只有① B.②④ C.②③④ D.①②6.在固定容积的密闭容器中,进行如下反应:N(g)+3H(g)⇄2NH (g) ,其化学平衡常数 与温度的
2 2 3
关系如下表。下列说法正确的是
温度(℃) 25 125 225 …
平衡常
…
数
A. 能说明反应已达平衡
B.平衡常数
C.混合气体的平均摩尔质量不再改变不能说明反应已达平衡
D.为提高反应速率和平衡转化率,工业生产时通常选择400~500℃、10~30MPa的反应条件
7.对已达到平衡的反应 进行操作后发现:仅升高温度,X(g)的平衡转化率减小;
仅增大容器体积,混合体系中W(g)的质量分数减小。下列说法一定正确的是
A.
B.反应物的总能量小于生成物的总能量
C.恒容时,降低温度,当容器内压强不变时,反应达到了平衡
D.保持容器体积不变,再加入X(g),平衡正向移动,X(g)的平衡转化率增大
8.中国科学院天津工业生物技术研究所研究员马延和研究团队,采用一种类似“搭积木”的方式,以二氧化
碳、氢气为原料,首次在实验室实现了二氧化碳到淀粉的合成。回答下列问题:
(1)用CO 人工合成淀粉,其中前两步分别合成甲醇、甲醛,涉及的反应如下:
2
①CO(g)+3H(g) CHOH(g)+HO(g) ΔH
2 2 3 2 1
②CHOH(g)+O(g) HCHO(g)+HO(l) ΔH
3 2 2 2 2
③2HO(l) 2HO(g)+O(g) ΔH
2 2 2 2 3
已知反应④2H(g)+O(g)=2HO(g) ΔH,则反应CO(g)+2H(g) HCHO(g)+HO(g) ΔH= 。
2 2 2 4 2 2 2
(2)一定温度下,在一个刚性密闭容器中同时进行反应①和反应②,下列说法正确的是 (填标号)。
A.平衡时向容器中充入惰性气体,反应①的平衡正向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.选用合适的催化剂可以提高CHOH的平衡产率
3
D.增加HO 的量,可加快反应速率
2 2
E.体系达平衡后,若压缩容器容积,则反应②平衡正向移动
(3)CO 与CHOH反应可制备HCOOCH 和HCOOH,发生的主要反应如下:
2 3 3Ⅰ.CH OH(g)+CO(g) HCOOH(g)+HCHO(g) ΔH>0
3 2 5
Ⅱ.HCOOH(g)+CHOH(g) HCOOCH (g)+HO(g) ΔH>0
3 3 2 6
Ⅲ.2HCHO(g) HCOOCH (g) ΔH<0
3 7
一定温度下,在一装有压强传感器的2 L刚性密闭容器中,充入2.0 mol CH OH(g)和1.0 mol CO (g)发生反应Ⅰ、
3 2
Ⅱ、Ⅲ,测得压强变化如表:
时间/min 0 10 20 30 40 ∞
压强/kPa 60 57 55.5 54.5 54 54
达到平衡时,测得容器中HCOOH、HCHO的物质的量分别为0.10 mol、0.20 mol。
①0~20 min内,反应Ⅲ的平均反应速率v(HCHO)= mol·L-1·min-1。
②CO 的平衡转化率为 。
2
③该温度下,反应Ⅱ的压强平衡常数K= 。
p
④不同压强下,投入足量CHOH(g)和CO(g)发生反应Ⅰ、Ⅱ、Ⅲ,实验测定HCOOCH 的平衡产率随温度的变
3 2 3
化关系如图所示。随温度升高,HCOOCH 的平衡产率先升高后降低,其原因为 。
3
压强p、p、p 由大到小的顺序为 ;图中T 温度时,三条曲线几乎交于一点的原因是 。
1 2 3 1
9.利用CO 和H 合成甲醇时主要涉及以下反应:
2 2
CO(g)+3H(g) CHOH(g)+H O(g);ΔH=-58kJ·mol-1
2 2 3 2 1
CO(g)+H(g) CO(g)+HO(g);ΔH=41kJ·mol-1
2 2 2 2
向含有催化剂的密闭容器中充入充入物质的量之比为1∶3的CO 和H 混合气体,其他条件一定,反应相同时
2 2
间,测得CO 的转化率和CHOH的选择性[ ×100%]与温度的关系如图所示。下列说法正确的是
2 3A.反应CO(g)+2H(g) CHOH(g)的ΔH=+99kJ·mol-1
2 3
B.250℃时容器中CHOH的物质的量小于210℃时容器中
3
C.平衡时CO 的转化率为20%,CHOH的选择性为75%,则H 的转化率为33.4%
2 3 2
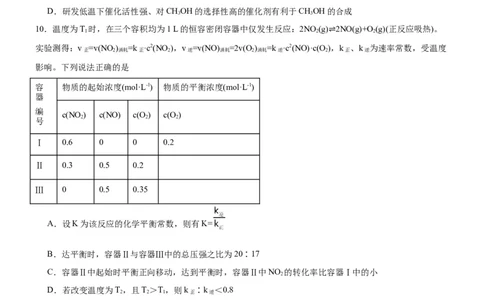
D.研发低温下催化活性强、对CHOH的选择性高的催化剂有利于CHOH的合成
3 3
10.温度为T 时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO (g) 2NO(g)+O (g)(正反应吸热)。
1 2 2
实验测得:v =v(NO) =k ·c2(NO ),v =v(NO) =2v(O ) =k ·c2(NO)·c(O)⇌,k 、k 为速率常数,受温度
正 2 消耗 正 2 逆 消耗 2 消耗 逆 2 正 逆
影响。下列说法正确的是
容 物质的起始浓度(mol·L-1) 物质的平衡浓度(mol·L-1)
器
编
c(NO ) c(NO) c(O) c(O)
2 2 2
号
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
Ⅲ 0 0.5 0.35
A.设K为该反应的化学平衡常数,则有K=
B.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C.容器Ⅱ中起始时平衡正向移动,达到平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小
2
D.若改变温度为T,且T>T,则k ∶k <0.8
2 2 1 正 逆
11.在t ℃时,向a L密闭容器中加入1.6 mol HI(g),发生反应2HI(g) H(g)+I(g) ΔH>0,H 的物质的量随
2 2 2
时间的变化如图所示,下列有关说法中正确的是A.平衡时,I 蒸气的体积分数为25%
2
B.若在1.5 min时降低温度,则反应将向左进行
C.平衡后若升高温度,υ 增大,υ 减小
正 逆
D.平衡后向容器中加入一定量的H 后,平衡向左移动,H 的体积分数减小
2 2
12.已知某化学反应的平衡常数表达式为K= ,在不同的温度下该反应的平衡常数如下表所示:
T/℃ 700 800 830 1 000 1 200
K 1.67 1.11 1.00 0.60 0.38
下列有关叙述不正确的是
A.该反应的化学方程式是CO(g)+HO(g) CO(g)+H(g)
2 2 2
B.升温,该反应进行的程度减小
C.如果在一定体积的密闭容器中充入CO 和H 各1 mol,5 min后温度升高到830 ℃,此时测得CO 为0.4
2 2 2
mol时,该反应达到平衡状态
D.某温度下,如果平衡浓度符合下列关系式: ,判断此时的温度是1000 ℃
13.镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi(s)+3H(g) LaNiH(s) ΔH<0,欲使LaNiH(s)释
5 2 5 6 5 6
放出气态氢,根据平衡移动原理,可改变的条件是
A.增加LaNiH(s)的量 B.降低温度
5 6
C.减小压强 D.使用催化剂
14.用CH 还原SO 不仅可以消除污染,而且可以得到单质S,反应如下:
4 2
t℃时,在容积为2L的恒容密闭容器中测的反应在不同时
刻各物质的物质的量如下表:
物质的量(mol)时间(min)
0 2 4 6 8 10
物质
SO 4.8 2.64 1.8 1.8 2.1 2.1
2
CO 0 1.08 1.5 1.5 1.75 1.75
2
下列说法不正确的是
A.前2min的平均反应速率v(CH)=0.27mol·L-1·min-1
4
B.6min时SO 的转化率等于10min时SO 的转化率
2 2
C.其它条件不变,在第10min后降低温度,可使容器中的CO 的浓度升高到1.4mol·L-1
2D.向容器内通入适量的HS,会使平衡逆向移动
2
15.在三种不同条件下,分别向容积为 的恒容密闭容器中充入 和 ,发生反应:
。相关条件和数据如表所示:
实验编号 Ⅰ Ⅱ Ⅲ
45
反应温度/℃ 450 500
0
有无催化剂 无 有 无
平衡时
1.5 1.5 1
下列说法正确的是
A.三种条件下,实验Ⅲ的平衡常数最大
B.催化剂降低了反应的活化能,使实验Ⅱ的平衡常数最大
C.实验Ⅰ条件下,若向容器中充入的是 ,达到平衡时 的转化率为25%
D.可以计算出实验Ⅲ的平衡常数为1
16.航天员呼吸产生的CO 用下列反应处理,可实现空间站中O 的循环利用。
2 2
Sabatier反应:CO(g)+4H(g) CH(g)+2HO(g)
2 2 4 2
水电解反应:2HO(g)=2H (g)+O(g)
2 2 2
一种新的循环利用方案是用Bosch反应CO(g)+2H(g) C(s)+2HO(g) ΔH<0代替Sabatier反应,再电解水实
2 2 2
现O 的循环利用。
2
回答下列问题:
(1)有关上述反应,下列说法正确的是 (填标号)。
A.室温下,2HO(g) 2H(g)+O(g)不能自发进行的原因为ΔS<0
2 2 2
B.可逆反应都有一定⇌的限度,限度越大反应物的转化率一定越高
C.可逆反应中,若反应物的总能量>生成物的总能量,则ΔH<0
(2)在Sabatier反应[反应Ⅰ:CO(g)+4H(g) CH(g)+2HO(g) K]体系中,还会发生副反应(反应Ⅱ):CO(g)
2 2 4 2 Ⅰ 2
+H (g) CO(g)+HO(g) K ;一定压强下,向某容积可变的密闭容器中通入CO 和H 的混合气体(其中CO 和
2 2 Ⅱ 2 2 2
H 的物质的量之比为1∶4),在某催化剂的作用下同时发生反应Ⅰ和反应Ⅱ,测得CO 的转化率、CH 的选择性、
2 2 4
CO的选择性随反应温度的变化情况如图所示。已知:CH 或CO的选择性指反应生成CH 或CO时所消耗的CO 的物质的量占参与反应的CO 总物质的量的百
4 4 2 2
分比。相同温度下,反应2CO(g)+2H(g) CO(g)+CH (g)的平衡常数为 (用含K、K 的式子表示);提高
2 2 4 Ⅰ Ⅱ
CH 的选择性的措施有 、 。 ⇌
4
(3)对于Bosch反应CO(g)+2H(g) C(s)+2HO(g) ΔH<0,下列关于各图像的解释或得出的结论正确的是
2 2 2
_____(填标号)。 ⇌
A.由甲图可知,反应在tmin时可能改变了压强或使用了催化剂
1
B.由乙图可知,反应在m点可能达到了平衡状态
C.由丙图可知,反应过程中v >v 的点是C点
正 逆
D.由丁图可知,交点A表示的反应一定处于平衡状态
(4)室温下,向体积为2L的恒容密闭容器中通入4molH 和1molCO 发生Sabatier反应:CO(g)+4H(g)
2 2 2 2
CH(g)+2HO(g)(不考虑副反应);若反应时保持温度恒定,测得反应过程中压强随时间的变化如下表所示:
4 2
时间/min 0 10 20 30 40 50 60
压强 5.00p 4.60p 4.30p 4.15p 4.06p 4.00p 4.00p
①0~10min内,v(CO)= mol·L-1·min-1,该温度下Sabatier反应的K= (K 为用气体的分压表示的平衡
2 p p
常数,分压=气体的体积分数×体系总压)。