文档内容
第1课时 羧酸 酯
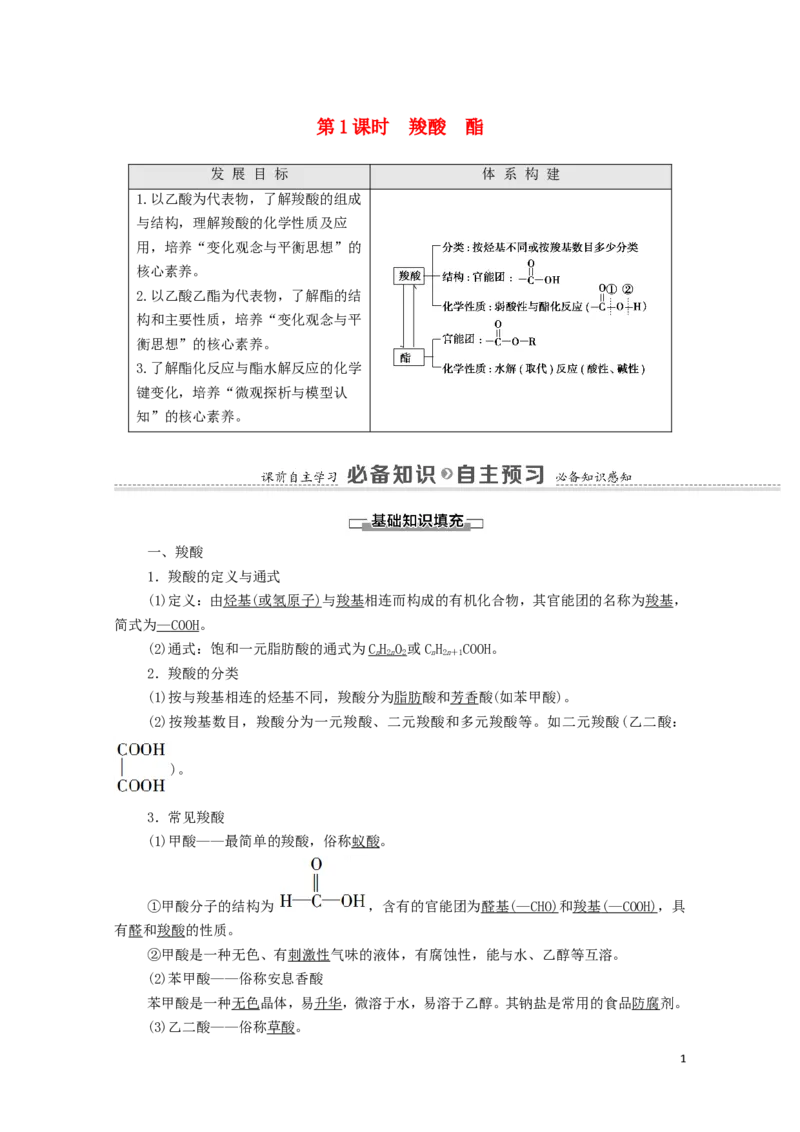
发 展 目 标 体 系 构 建
1.以乙酸为代表物,了解羧酸的组成
与结构,理解羧酸的化学性质及应
用,培养“变化观念与平衡思想”的
核心素养。
2.以乙酸乙酯为代表物,了解酯的结
构和主要性质,培养“变化观念与平
衡思想”的核心素养。
3.了解酯化反应与酯水解反应的化学
键变化,培养“微观探析与模型认
知”的核心素养。
一、羧酸
1.羧酸的定义与通式
(1)定义:由 烃基 ( 或氢原子 )与羧基相连而构成的有机化合物,其官能团的名称为羧基,
简式为 — COO H。
(2)通式:饱和一元脂肪酸的通式为CH O 或CH COOH。
n 2n 2 n 2n+1
2.羧酸的分类
(1)按与羧基相连的烃基不同,羧酸分为脂肪酸和芳香酸(如苯甲酸)。
(2)按羧基数目,羧酸分为一元羧酸、二元羧酸和多元羧酸等。如二元羧酸(乙二酸:
)。
3.常见羧酸
(1)甲酸——最简单的羧酸,俗称蚁酸。
①甲酸分子的结构为 ,含有的官能团为 醛基 (—CHO )和 羧基 (—COOH ),具
有醛和羧酸的性质。
②甲酸是一种无色、有刺激性气味的液体,有腐蚀性,能与水、乙醇等互溶。
(2)苯甲酸——俗称安息香酸
苯甲酸是一种无色晶体,易升华,微溶于水,易溶于乙醇。其钠盐是常用的食品防腐剂。
(3)乙二酸——俗称草酸。
1乙二酸是二元羧酸,无色晶体,可溶于水和乙醇。常用于化学分析的还原剂。
(4)羟基酸——具有羟基和羧基性质。
乳酸与柠檬酸是羟基酸,其结构简式分别为
4.饱和一元羧酸的物理性质变化规律
(1)随分子中碳原子数的增加,溶解度迅速减小,沸点逐渐升高。
(2)羧酸与相对分子质量相当的其他有机物相比,沸点较高,这与羧酸分子间可以形成氢
键有关。
5.羧酸的化学性质
羧酸反应时,羧基( )中①②号极性键断裂。
(1)酸性——弱酸,具有酸类的性质
写出下列化学方程式
①HCOOH与NaHCO 反应: HCOO H + NaHC O = = = HCOON a + C O ↑ + HO。
3 3 2 2
②苯甲酸与NaOH反应:
。
③乙二酸与NaOH反应: 。
(2)酯化反应(乙酸与乙醇反应)
①乙酸与乙醇的酯化反应方程式:
。
②原理:
用同位素示踪法探究酯化反应中的脱水方式。用含有示踪原子的CHCHOH与CHCOOH反应,
3 3
化学方程式为
,
说明酯化反应时,羧基脱—OH,醇羟基脱H。
微点拨:酯化反应是可逆反应,浓硫酸在此反应中作催化剂和吸水剂。
二、羧酸衍生物——酯
1.组成、结构和命名
22.酯的性质
(1)物理性质
低级酯是具有芳香气味的液体,密度一般小于水,难溶于水,易溶于乙醇、乙醚等有机溶
剂。
(2)化学性质——水解反应(以乙酸乙酯为例)
①酸性条件下水解
CHCOOCH+HO CH COO H + CHOH。
3 2 5 2 3 2 5
②碱性条件下水解
CHCOOCH+NaOH――→CH COON a + CHOH。
3 2 5 3 2 5
微点拨:①酯的酸性水解与酯化反应均为可逆反应和取代反应。
②酯的碱性水解,由于生成了羧酸盐,水解反应不可逆,也属于取代反应。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)含有—COOH的化合物一定是羧酸类。 ( )
(2)根据烃基的不同,羧酸可以分为饱和羧酸和不饱和羧酸。 ( )
(3)任何羧酸的酸性都比碳酸强。 ( )
(4)酯化反应与酯的水解反应均为取代反应。 ( )
(5)浓硫酸在酯化反应中起催化剂和脱水剂作用。 ( )
[答案] (1)× (2)√ (3)× (4)√ (5)×
2.下列物质与NaHCO 溶液不反应的是( )
3
A.甲酸 B.乙二酸
C.安息香酸 D.苯酚
[答案] D
3.写出下列变化的化学方程式。并指明反应类型
3[答案] ①2CHCHCHO+O――→2CHCHCOOH,氧化反应
3 2 2 3 2
②CH===CH+HO――→CHCHOH,加成反应
2 2 3 2
③CHCHCOOH+CHOH CHCHCOOCH+HO,酯化反应(或取代反应)
3 2 2 5 3 2 2 5 2
④CHCHCOOCH+NaOH――→CHCHCOONa+CHOH,取代反应(或水解反应)
3 2 2 5 3 2 2 5
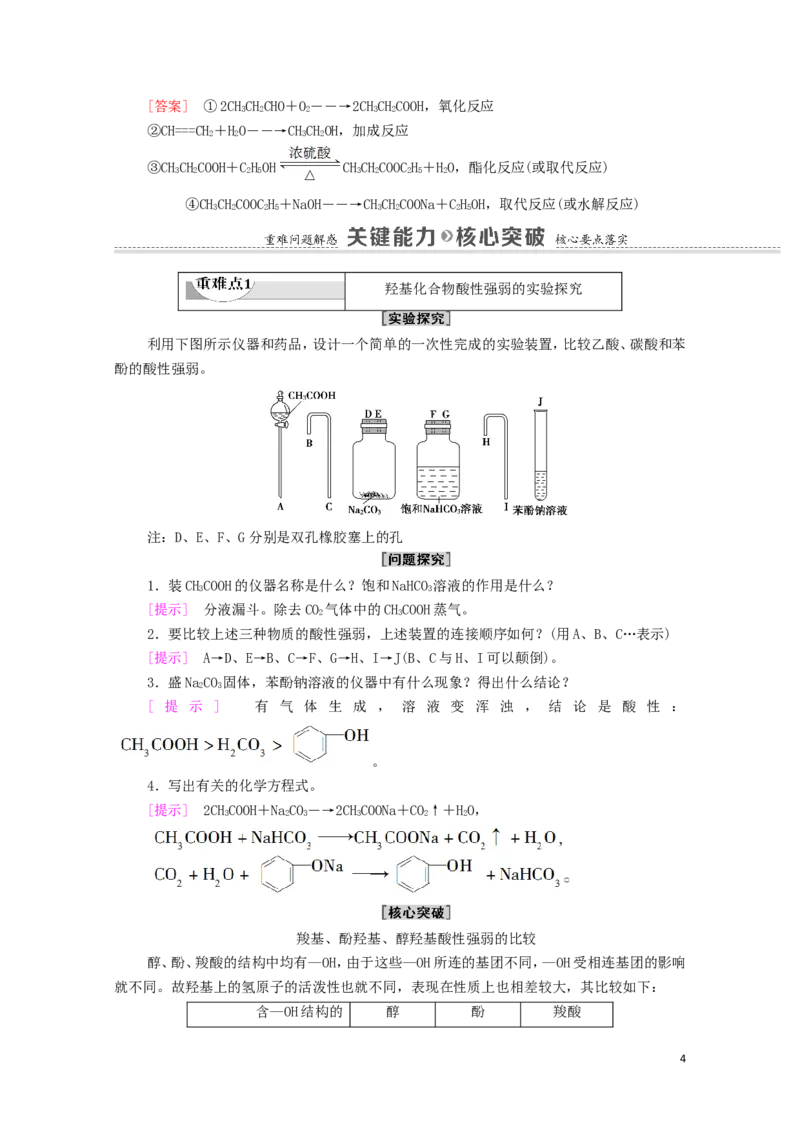
羟基化合物酸性强弱的实验探究
利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,比较乙酸、碳酸和苯
酚的酸性强弱。
注:D、E、F、G分别是双孔橡胶塞上的孔
1.装CHCOOH的仪器名称是什么?饱和NaHCO 溶液的作用是什么?
3 3
[提示] 分液漏斗。除去CO 气体中的CHCOOH蒸气。
2 3
2.要比较上述三种物质的酸性强弱,上述装置的连接顺序如何?(用A、B、C…表示)
[提示] A→D、E→B、C→F、G→H、I→J(B、C与H、I可以颠倒)。
3.盛NaCO 固体,苯酚钠溶液的仪器中有什么现象?得出什么结论?
2 3
[ 提 示 ] 有 气 体 生 成 , 溶 液 变 浑 浊 , 结 论 是 酸 性 :
。
4.写出有关的化学方程式。
[提示] 2CHCOOH+NaCO―→2CHCOONa+CO↑+HO,
3 2 3 3 2 2
羧基、酚羟基、醇羟基酸性强弱的比较
醇、酚、羧酸的结构中均有—OH,由于这些—OH所连的基团不同,—OH受相连基团的影响
就不同。故羟基上的氢原子的活泼性也就不同,表现在性质上也相差较大,其比较如下:
含—OH结构的 醇 酚 羧酸
4物质
比较项目
氢原子(—OH) 的活泼性 ――――→
在水溶液中电离 极难电离 微弱电离 部分电离
酸碱性 中性 很弱的酸性 弱酸性
与Na反应 反应放出H 反应放出H 反应放出H
2 2 2
与NaOH反应 不反应 反应 反应
与NaHCO 反应 不反应 不反应 反应放出CO
3 2
微点拨:①羧酸均为弱酸,低级羧酸,酸性一般比HCO 强,但高级脂肪酸酸性很弱。
2 3
②低级羧酸能使紫色石蕊溶液变红,醇、酚、高级脂肪酸不能使紫色石蕊溶液变红。
③含有n个羟基或羧基的物质与Na反应:1 mol物质中含有n mol羟基或羧基,分别对应
mol H 的生成。
2
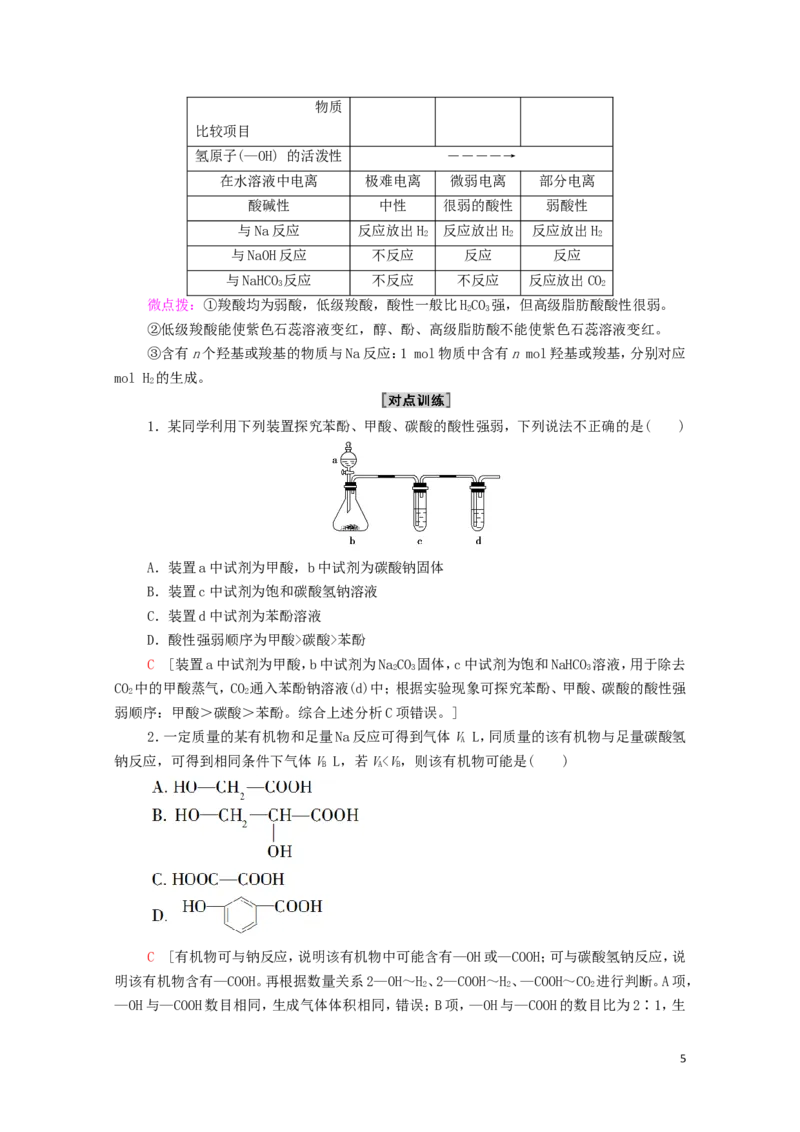
1.某同学利用下列装置探究苯酚、甲酸、碳酸的酸性强弱,下列说法不正确的是( )
A.装置a中试剂为甲酸,b中试剂为碳酸钠固体
B.装置c中试剂为饱和碳酸氢钠溶液
C.装置d中试剂为苯酚溶液
D.酸性强弱顺序为甲酸>碳酸>苯酚
C [装置a中试剂为甲酸,b中试剂为NaCO 固体,c中试剂为饱和NaHCO 溶液,用于除去
2 3 3
CO 中的甲酸蒸气,CO 通入苯酚钠溶液(d)中;根据实验现象可探究苯酚、甲酸、碳酸的酸性强
2 2
弱顺序:甲酸>碳酸>苯酚。综合上述分析C项错误。]
2.一定质量的某有机物和足量Na反应可得到气体V L,同质量的该有机物与足量碳酸氢
A
钠反应,可得到相同条件下气体V L,若VV,错误;C项,含2个—COOH,生成气体V