文档内容
第一节 糖类
发 展 目 标 体 系 构 建
1.认识糖类的组成和性质特点,能列举
典型糖类物质,能说明单糖、二糖和多糖
的区别与联系,培养“宏观辨识与微观
探析”的核心素养。
2.了解淀粉和纤维素及其与葡萄糖的关
系,了解葡萄糖的结构特点、主要性质与
应用,培养“科学探究与社会责任”的
核心素养。
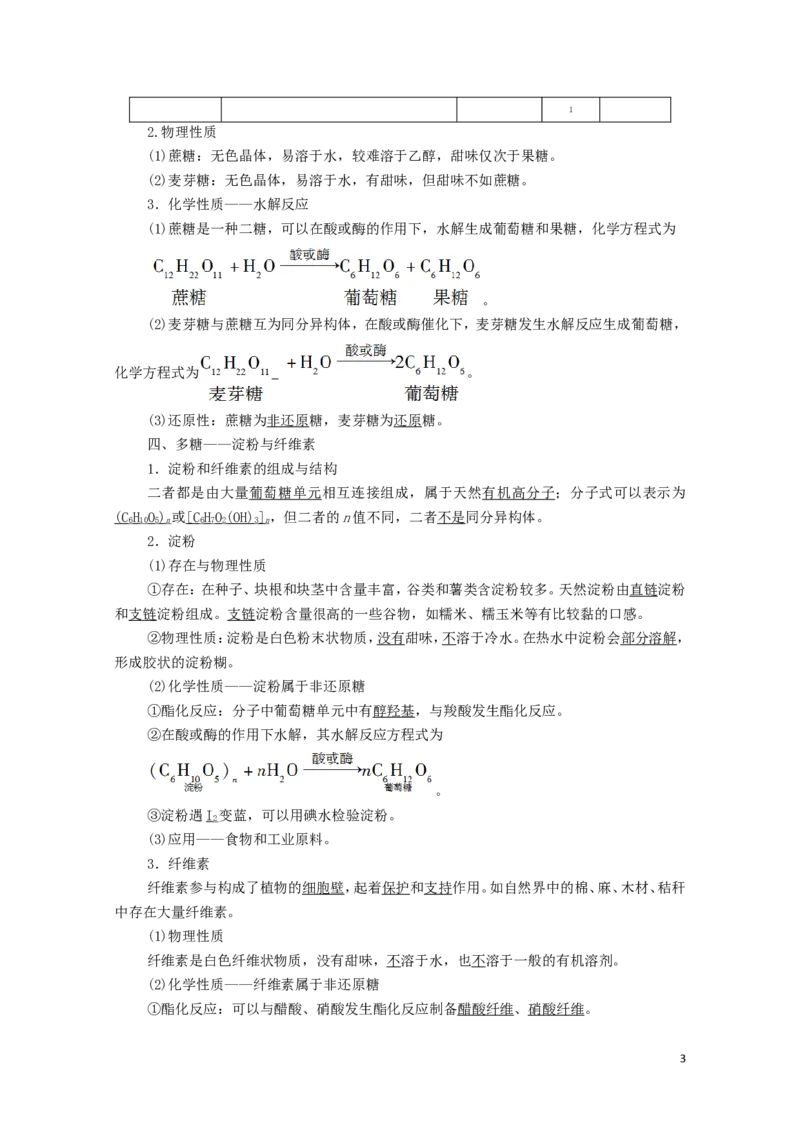
一、糖类的组成和分类
1.组成:一般含碳、氢、氧三种元素,通式一般为C(HO),称为碳水化合物。
m 2 n
但要注意:(1)糖类不一定均符合C(HO) 组成,如脱氧核糖的分子式为CH O。
m 2 n 5 10 4
(2)符合C(HO) 组成的物质不一定是糖类,如乙酸的分子式为CHO [ 或 C(HO)]。故碳
m 2 n 2 4 2 2 2 2
水化合物表示糖类并不准确。
2.定义:糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
3.分类
单糖 寡糖(低聚糖) 多糖
不能水解 1 mol糖水解后能产生 2 ~ 1 0 1 mol糖水解后能产生10 mol
概念
的糖 mol单糖的糖 以上单糖的糖
葡萄糖、果
代表物及 蔗糖、麦芽糖 淀粉、纤维素
糖
分子式
CH O C H O (CH O)
6 12 6 12 22 11 6 10 5 n
二、单糖
1.葡萄糖
(1)存在与物理性质
葡萄糖存在于水果、蜂蜜,以及植物的种子、叶、根、花中。动物的血液和淋巴液中也含有
葡萄糖。葡萄糖是易溶于水的无色晶体,熔点为146 ℃,有甜味,但甜度不如蔗糖。
(2)分子式与结构特点
分子式为CH O,分子中含有醛基和羟基,属于醛糖。结构简式为CHOH(CHOH)CHO。
6 12 6 2 4
(3)化学性质
葡萄糖具有醛和醇的特征反应
1①还原性:与新制Cu(OH) 悬浊液反应、银镜反应、使溴水和酸性高锰酸钾溶液褪色。
2
②不饱和性:与H 发生加成反应。
2
③与羧酸等发生取代反应。1 mol葡萄糖可以与5_mol 乙酸发生酯化反应。
④体内氧化反应提供能量,是一种重要的营养物质。
CH O+6O――→6CO+6HO
6 12 6 2 2 2
葡萄糖
微点拨:葡萄糖的环状结构
αD吡喃葡萄糖 链状葡萄糖 βD吡喃葡萄糖
2.果糖
(1)存在与物理性质
果糖在水果和蜂蜜中含量较高,它比蔗糖的甜度高。纯净的果糖为无色晶体,易溶于水,
吸湿性强。
(2)分子式与结构特点
果糖的分子式为CH O,是葡萄糖的同分异构体。果糖是一种多羟基酮,属于酮糖。结构简
6 12 6
式为 。
3.核糖与脱氧核糖
核糖与脱氧核糖分别是生物体的遗传物质 核糖核酸 (RNA )与 脱氧核糖核酸 (DNA )的重要组
成部分。它们都是含有5个碳原子的单糖——戊糖。均为醛糖,具有还原性。
二者的结构简式分别为CHOH(CHOH)CHO和CHOH(CHOH)CHCHO。
2 3 2 2 2
4.糖类分子与手性
(1)手性碳原子:在分子中连有4 个不同的原子或原子团的碳原子叫做不对称碳原子,也
叫手性碳原子。
(2)手性分子:含有手性碳原子存在不能重叠、互为镜像的对映异构体的分子称手性分子:
如 为手性分子。
三、二糖——蔗糖与麦芽糖
1.来源及用途
名称 存在 常见物质 分子式 用途
大多数植物体中(甜菜、甘蔗中含量 C H O
12 22 1
蔗糖 红糖、白糖 甜味食品
最高)
1
麦芽糖 发芽的谷粒和麦芽中 饴糖 C H O 甜味食品
12 22 1
21
2.物理性质
(1)蔗糖:无色晶体,易溶于水,较难溶于乙醇,甜味仅次于果糖。
(2)麦芽糖:无色晶体,易溶于水,有甜味,但甜味不如蔗糖。
3.化学性质——水解反应
(1)蔗糖是一种二糖,可以在酸或酶的作用下,水解生成葡萄糖和果糖,化学方程式为
。
(2)麦芽糖与蔗糖互为同分异构体,在酸或酶催化下,麦芽糖发生水解反应生成葡萄糖,
化学方程式为 。
(3)还原性:蔗糖为非还原糖,麦芽糖为还原糖。
四、多糖——淀粉与纤维素
1.淀粉和纤维素的组成与结构
二者都是由大量葡萄糖单元相互连接组成,属于天然有机高分子;分子式可以表示为
(CH O) 或[CHO(OH)],但二者的n值不同,二者不是同分异构体。
6 10 5 n 6 7 2 3 n
2.淀粉
(1)存在与物理性质
①存在:在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。天然淀粉由直链淀粉
和支链淀粉组成。支链淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感。
②物理性质:淀粉是白色粉末状物质,没有甜味,不溶于冷水。在热水中淀粉会部分溶解,
形成胶状的淀粉糊。
(2)化学性质——淀粉属于非还原糖
①酯化反应:分子中葡萄糖单元中有醇羟基,与羧酸发生酯化反应。
②在酸或酶的作用下水解,其水解反应方程式为
。
③淀粉遇I 变蓝,可以用碘水检验淀粉。
2
(3)应用——食物和工业原料。
3.纤维素
纤维素参与构成了植物的细胞壁,起着保护和支持作用。如自然界中的棉、麻、木材、秸秆
中存在大量纤维素。
(1)物理性质
纤维素是白色纤维状物质,没有甜味,不溶于水,也不溶于一般的有机溶剂。
(2)化学性质——纤维素属于非还原糖
①酯化反应:可以与醋酸、硝酸发生酯化反应制备醋酸纤维、硝酸纤维。
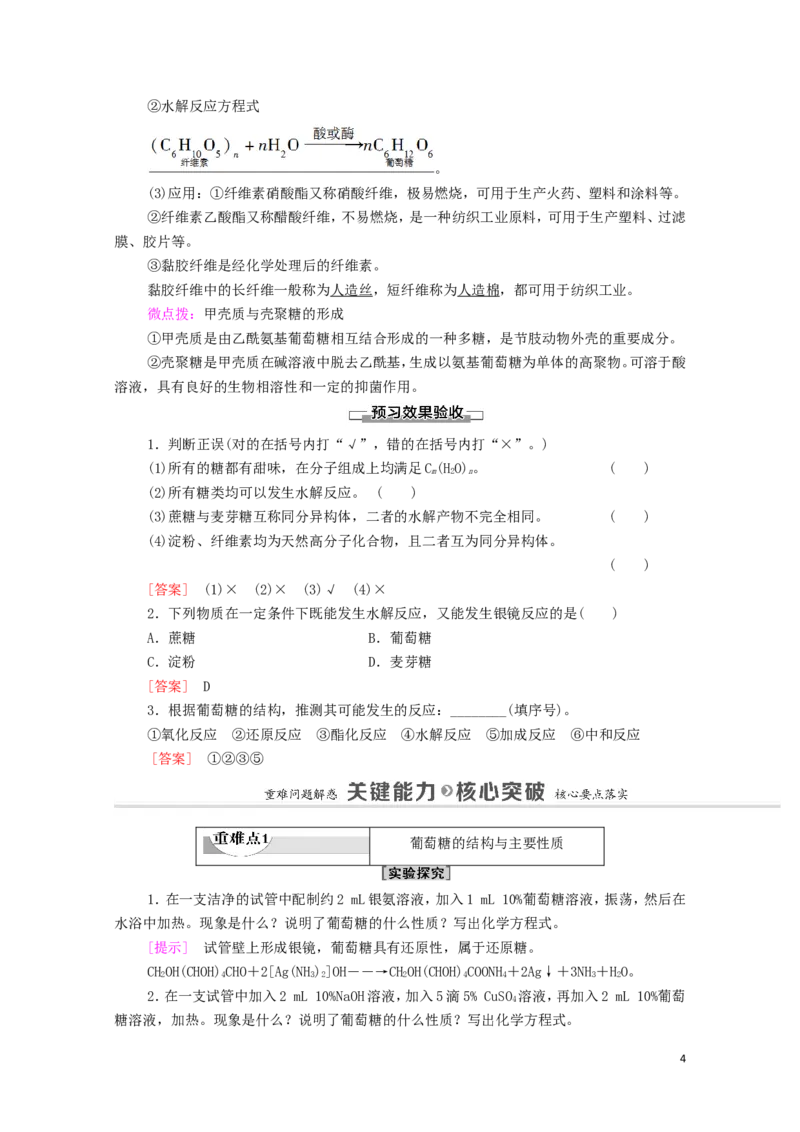
3②水解反应方程式
。
(3)应用:①纤维素硝酸酯又称硝酸纤维,极易燃烧,可用于生产火药、塑料和涂料等。
②纤维素乙酸酯又称醋酸纤维,不易燃烧,是一种纺织工业原料,可用于生产塑料、过滤
膜、胶片等。
③黏胶纤维是经化学处理后的纤维素。
黏胶纤维中的长纤维一般称为人造丝,短纤维称为人造棉,都可用于纺织工业。
微点拨:甲壳质与壳聚糖的形成
①甲壳质是由乙酰氨基葡萄糖相互结合形成的一种多糖,是节肢动物外壳的重要成分。
②壳聚糖是甲壳质在碱溶液中脱去乙酰基,生成以氨基葡萄糖为单体的高聚物。可溶于酸
溶液,具有良好的生物相溶性和一定的抑菌作用。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)所有的糖都有甜味,在分子组成上均满足C(HO)。 ( )
m 2 n
(2)所有糖类均可以发生水解反应。 ( )
(3)蔗糖与麦芽糖互称同分异构体,二者的水解产物不完全相同。 ( )
(4)淀粉、纤维素均为天然高分子化合物,且二者互为同分异构体。
( )
[答案] (1)× (2)× (3)√ (4)×
2.下列物质在一定条件下既能发生水解反应,又能发生银镜反应的是( )
A.蔗糖 B.葡萄糖
C.淀粉 D.麦芽糖
[答案] D
3.根据葡萄糖的结构,推测其可能发生的反应:________(填序号)。
①氧化反应 ②还原反应 ③酯化反应 ④水解反应 ⑤加成反应 ⑥中和反应
[答案] ①②③⑤
葡萄糖的结构与主要性质
1.在一支洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡,然后在
水浴中加热。现象是什么?说明了葡萄糖的什么性质?写出化学方程式。
[提示] 试管壁上形成银镜,葡萄糖具有还原性,属于还原糖。
CHOH(CHOH)CHO+2[Ag(NH)]OH――→CHOH(CHOH)COONH+2Ag↓+3NH+HO。
2 4 3 2 2 4 4 3 2
2.在一支试管中加入2 mL 10%NaOH溶液,加入5滴5% CuSO 溶液,再加入2 mL 10%葡萄
4
糖溶液,加热。现象是什么?说明了葡萄糖的什么性质?写出化学方程式。
4[提示] 溶液有砖红色沉淀产生,葡萄糖具有还原性,属于还原糖。
CHOH(CHOH)CHO+2Cu(OH)+NaOH――→CHOH(CHOH)COONa+CuO↓+3HO。
2 4 2 2 4 2 2
1.葡萄糖的性质
反应类型 试剂或条件 表现性质的官能团
加成反应 H/Ni
2
银氨溶液
醛基
新制Cu(OH) 悬浊液
2
氧化反应
使溴水褪色
生理氧化 —
酯化反应 与乙酸等 羟基
微点拨:1 mol葡萄糖完全酯化需乙酸5 mol。
2.工业制备葡萄糖和酒精
(1)工业制葡萄糖
(2)葡萄糖发酵生成酒精
CH O――→2CHOH+2CO↑。
6 12 6 2 5 2
(3)对应转化关系
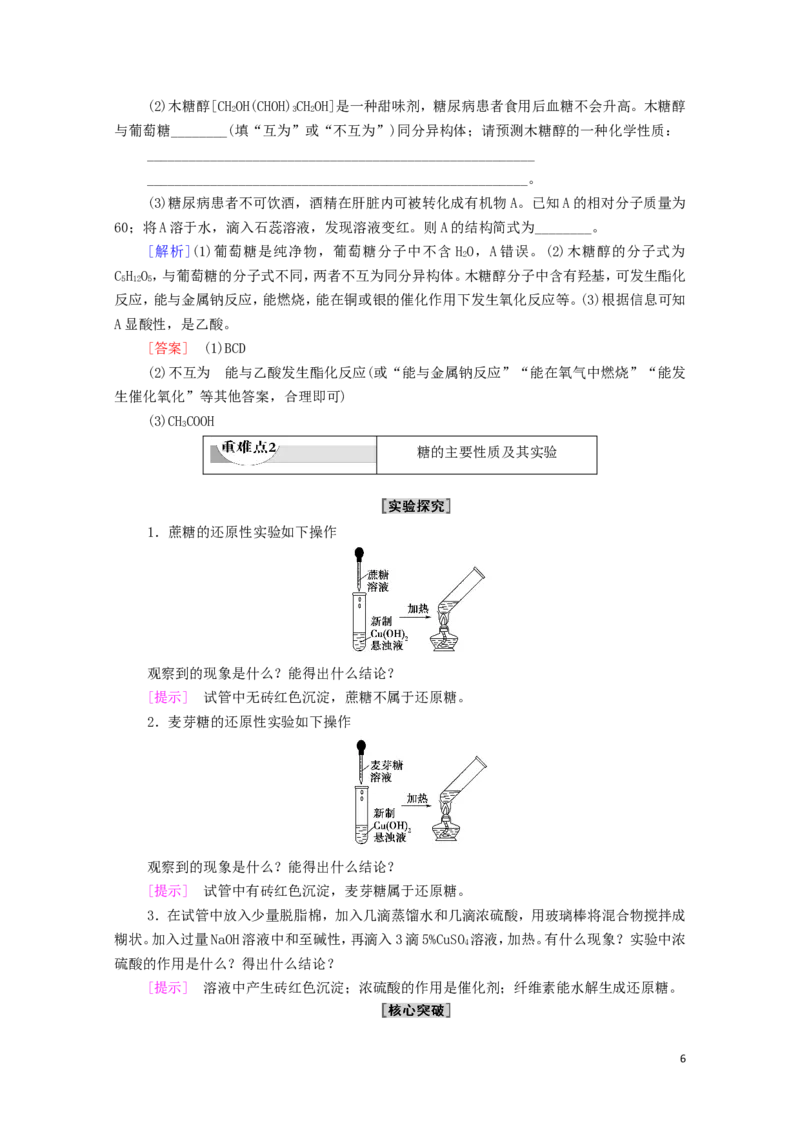
1. 关于葡萄糖和果糖的说法错误的是 ( )
A.葡萄糖和果糖都是单糖,互为同分异构体
B.葡萄糖和果糖都不能发生银镜反应
C.二者都易溶于水,且果糖比葡萄糖甜
D.葡萄糖与乙酸作用生成葡萄糖五乙酸酯
B [葡萄糖和果糖的分子式相同,而结构不同,二者互为同分异构体;葡萄糖中含有醛基,
能发生银镜反应,而果糖虽然不是醛糖,但它能发生银镜反应;每个葡萄糖分子中含有5个羟
基,与足量乙酸发生酯化反应生成葡萄糖五乙酸酯。]
2.糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合征,以高血糖为主要标志。长期摄
入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖。下列说法正确的是________(填字母)。
A.葡萄糖的分子式可表示为C(HO),则每个葡萄糖分子中含6个HO
6 2 6 2
B.可用新制氢氧化铜悬浊液来检验糖尿病患者尿液中的葡萄糖
C.葡萄糖是一种重要的工业原料,可用于食品加工、医疗、合成维生素C等
D.淀粉水解的最终产物是葡萄糖
5(2)木糖醇[CHOH(CHOH)CHOH]是一种甜味剂,糖尿病患者食用后血糖不会升高。木糖醇
2 3 2
与葡萄糖________(填“互为”或“不互为”)同分异构体;请预测木糖醇的一种化学性质:
_______________________________________________________
______________________________________________________。
(3)糖尿病患者不可饮酒,酒精在肝脏内可被转化成有机物A。已知A的相对分子质量为
60;将A溶于水,滴入石蕊溶液,发现溶液变红。则A的结构简式为________。
[解析](1)葡萄糖是纯净物,葡萄糖分子中不含 HO,A错误。(2)木糖醇的分子式为
2
CH O,与葡萄糖的分子式不同,两者不互为同分异构体。木糖醇分子中含有羟基,可发生酯化
5 12 5
反应,能与金属钠反应,能燃烧,能在铜或银的催化作用下发生氧化反应等。(3)根据信息可知
A显酸性,是乙酸。
[答案] (1)BCD
(2)不互为 能与乙酸发生酯化反应(或“能与金属钠反应”“能在氧气中燃烧”“能发
生催化氧化”等其他答案,合理即可)
(3)CHCOOH
3
糖的主要性质及其实验
1.蔗糖的还原性实验如下操作
观察到的现象是什么?能得出什么结论?
[提示] 试管中无砖红色沉淀,蔗糖不属于还原糖。
2.麦芽糖的还原性实验如下操作
观察到的现象是什么?能得出什么结论?
[提示] 试管中有砖红色沉淀,麦芽糖属于还原糖。
3.在试管中放入少量脱脂棉,加入几滴蒸馏水和几滴浓硫酸,用玻璃棒将混合物搅拌成
糊状。加入过量NaOH溶液中和至碱性,再滴入3滴5%CuSO 溶液,加热。有什么现象?实验中浓
4
硫酸的作用是什么?得出什么结论?
[提示] 溶液中产生砖红色沉淀;浓硫酸的作用是催化剂;纤维素能水解生成还原糖。
61.蔗糖与麦芽糖比较
二糖 蔗糖 麦芽糖
C H O
12 22 1
分子式 C H O
12 22 11
1
关系 同分异构体
属类 非还原糖 还原糖
水解产物 葡萄糖与果糖 葡萄糖
微点拨:检验水解产物为葡萄糖时,一定要先加NaOH溶液中和作催化剂的稀硫酸,至溶液
呈碱性后再加银氨溶液或新制的Cu(OH) 悬浊液,否则实验会失败。
2
2.淀粉与纤维素比较
多糖 淀粉 纤维素
分子通式 (CH O) (CH O)
6 10 5 n 6 10 5 n
关系 n值不同,分子式不同,不是同分异构体
属类 天然有机高分子,非还原糖
水解产物 葡萄糖 葡萄糖
微点拨:淀粉遇I 变蓝色。
2
3.淀粉水解程度的实验设计
(1)实验原理
判断淀粉水解的程度时,要注意检验产物中是否生成葡萄糖,同时还要确认淀粉是否水解
完全。用银氨溶液或新制的Cu(OH) 悬浊液和碘水来检验淀粉是否发生了水解及水解是否完全。
2
(2)实验步骤
(3)实验现象及结论
现象A 现象B 结论
① 未出现银镜 溶液变蓝色 淀粉尚未水解
② 出现银镜 溶液变蓝色 淀粉部分水解
③ 出现银镜 溶液不变蓝色 淀粉完全水解
1.下列关于二糖的说法中不正确的是( )
A.蔗糖与麦芽糖互为同分异构体
B.蔗糖与麦芽糖的分子式都是C H O
12 22 11
C.蔗糖与麦芽糖的水解产物完全相同
D.麦芽糖能发生银镜反应,蔗糖不能发生银镜反应
C [蔗糖与麦芽糖的分子式都是C H O ,二者互为同分异构体;麦芽糖是还原性二糖,而
12 22 11
7蔗糖无还原性;蔗糖的水解产物是果糖和葡萄糖,而麦芽糖的水解产物只有葡萄糖。]
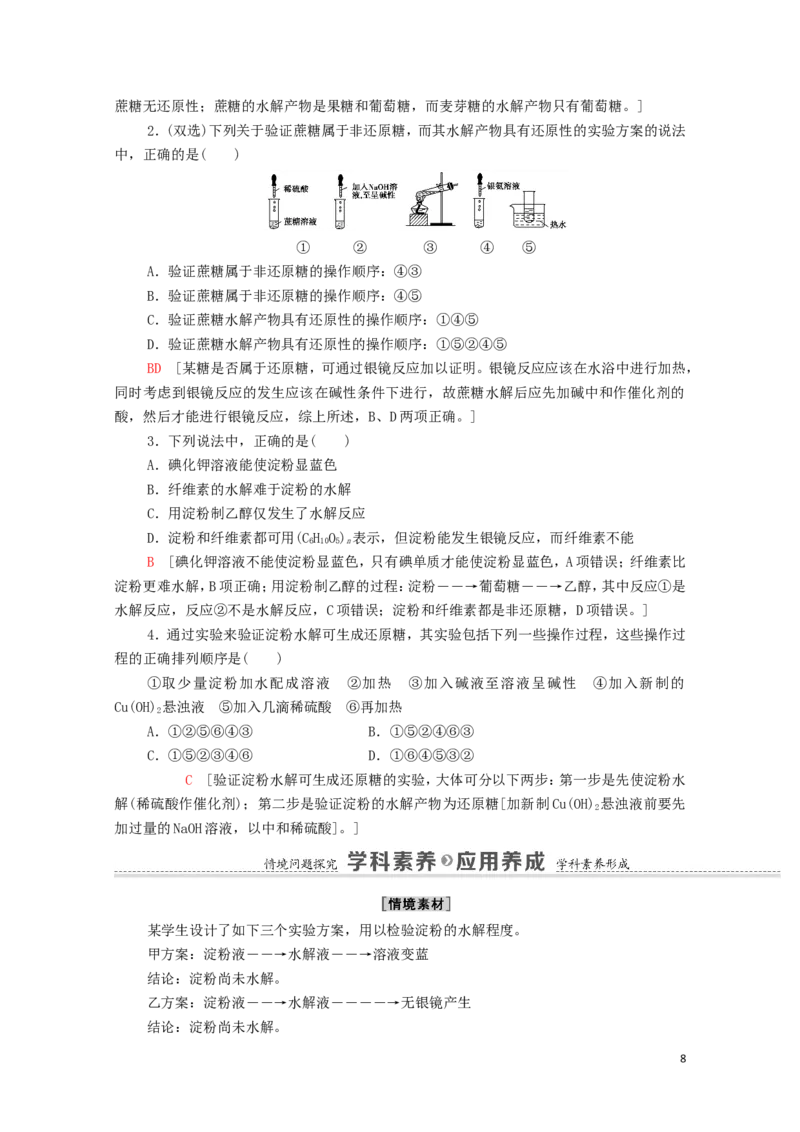
2.(双选)下列关于验证蔗糖属于非还原糖,而其水解产物具有还原性的实验方案的说法
中,正确的是( )
① ② ③ ④ ⑤
A.验证蔗糖属于非还原糖的操作顺序:④③
B.验证蔗糖属于非还原糖的操作顺序:④⑤
C.验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D.验证蔗糖水解产物具有还原性的操作顺序:①⑤②④⑤
BD [某糖是否属于还原糖,可通过银镜反应加以证明。银镜反应应该在水浴中进行加热,
同时考虑到银镜反应的发生应该在碱性条件下进行,故蔗糖水解后应先加碱中和作催化剂的
酸,然后才能进行银镜反应,综上所述,B、D两项正确。]
3.下列说法中,正确的是( )
A.碘化钾溶液能使淀粉显蓝色
B.纤维素的水解难于淀粉的水解
C.用淀粉制乙醇仅发生了水解反应
D.淀粉和纤维素都可用(CH O) 表示,但淀粉能发生银镜反应,而纤维素不能
6 10 5 n
B [碘化钾溶液不能使淀粉显蓝色,只有碘单质才能使淀粉显蓝色,A项错误;纤维素比
淀粉更难水解,B项正确;用淀粉制乙醇的过程:淀粉――→葡萄糖――→乙醇,其中反应①是
水解反应,反应②不是水解反应,C项错误;淀粉和纤维素都是非还原糖,D项错误。]
4.通过实验来验证淀粉水解可生成还原糖,其实验包括下列一些操作过程,这些操作过
程的正确排列顺序是( )
①取少量淀粉加水配成溶液 ②加热 ③加入碱液至溶液呈碱性 ④加入新制的
Cu(OH) 悬浊液 ⑤加入几滴稀硫酸 ⑥再加热
2
A.①②⑤⑥④③ B.①⑤②④⑥③
C.①⑤②③④⑥ D.①⑥④⑤③②
C [验证淀粉水解可生成还原糖的实验,大体可分以下两步:第一步是先使淀粉水
解(稀硫酸作催化剂);第二步是验证淀粉的水解产物为还原糖[加新制Cu(OH) 悬浊液前要先
2
加过量的NaOH溶液,以中和稀硫酸]。]
某学生设计了如下三个实验方案,用以检验淀粉的水解程度。
甲方案:淀粉液――→水解液――→溶液变蓝
结论:淀粉尚未水解。
乙方案:淀粉液――→水解液――――→无银镜产生
结论:淀粉尚未水解。
8丙方案:淀粉液――→水解液―――――→
结论:淀粉完全水解。
(1)根据上述现象,分析以上三个方案的操作及结论是否正确,并说明理由。
(2)如果淀粉已经完全水解,请你仿照上述格式设计一个方案证明。
(3)如果淀粉部分发生水解,请你仿照上述格式设计一个方案证明。
[提示](1)①操作正确,结论错误;淀粉有可能部分水解。
②操作错误,结论亦错误;在酸性条件下即使有淀粉发生水解生成葡萄糖,也不会发生银
镜反应。
③操作错误,结论亦错误;如果NaOH过量,可与碘发生反应,因此无法检验是否存在淀粉。
(2)淀粉液――→水解液――→无现象
可得结论:淀粉完全水解。
可得结论:淀粉部分水解。
通过淀粉水解程度的实验探究,培养学生“科学探究与证据推理”的核心素养。
1.下列关于糖类的叙述正确的是( )
①含有碳、氢、氧三种元素的有机化合物属于糖类 ②糖类是碳和水的化合物,又称碳水
化合物 ③凡是能溶于水且具有甜味的物质都属于糖类 ④糖类是多羟基醛或多羟基酮及能
水解生成它们的物质 ⑤符合C(HO) 的有机物都是糖类
m 2 n
A.①② B.③⑤
C.④ D.①④
C [糖类含有碳、氢、氧三种元素,但含有碳、氢、氧三种元素的化合物的种类很多,如醇、
醛、羧酸等,所以不能用“含有碳、氢、氧”来定义糖类,①错误。大多数糖类化合物可用通式
C(HO) 表示,最早被称为“碳水化合物”,这只是说明了其组成,并不表示这类物质的结构,
m 2 n
故绝对不是碳和水的化合物,且随着化学学科的发展,人们发现称糖类为“碳水化合物”并不
准确,②错误。有甜味的物质不一定是糖类,如甘油有甜味,但不是糖类,糖类也不一定有甜味,
9如淀粉和纤维素,③错误。HCHO、CHCOOH也符合C(HO),但不是糖,⑤错误。]
3 m 2 n
2.下列说法不正确的是( )
A.葡萄糖不可能由纤维素制取
B.葡萄糖在酒化酶作用下转化为乙醇和二氧化碳
C.葡萄糖是人体所需能量的重要来源
D.葡萄糖能与银氨溶液发生反应
A [纤维素在一定条件下水解可制取葡萄糖,A项错误;葡萄糖在酒化酶的作用下可分解
为乙醇和CO,B项正确;葡萄糖在人体内发生缓慢氧化,提供人体活动所需要的能量,C项正确;
2
葡萄糖分子中含有醛基,能与银氨溶液发生银镜反应,D项正确。]
3.(双选)下列说法不正确的是( )
A.向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入新制的Cu(OH),加热,没有砖红
2
色沉淀生成,说明淀粉没有水解成葡萄糖
B.蔗糖、麦芽糖的分子式都是C H O ,二者互为同分异构体
12 22 11
C.纤维素和淀粉遇碘水均显蓝色
D.麦芽糖及其水解产物均能发生银镜反应
AC [检验淀粉的水解产物,应在冷却后加入NaOH溶液中和作催化剂的稀硫酸,然后加入
新制的Cu(OH),A项错误;蔗糖、麦芽糖的分子式相同,但结构不同,二者互为同分异构体,B项
2
正确;遇碘显蓝色是淀粉的特性,C项错误;麦芽糖及其水解生成的葡萄糖中均含有醛基,二者
都属于还原糖,均能发生银镜反应,D项正确。]
4.下列物质中既能发生水解反应,也能发生银镜反应,其水解产物中还有能发生银镜反
应的是( )
①乙醛 ②葡萄糖 ③甲酸甲酯 ④蔗糖 ⑤麦芽糖 ⑥纤维素 ⑦淀粉
A.①②⑤ B.③④⑥
C.③⑤ D.④⑤
C [能发生水解反应的物质有③④⑤⑥⑦,能发生银镜反应的物质有①②③⑤,水解产物
中有能发生银镜反应的物质有③④⑤⑥⑦,故C正确。]
5.(素养题)根据图所示转化关系,回答下列问题:
(1)工业上制镜和热水瓶胆镀银,常利用上述反应中的________(填序号)。
(2)①②的反应类型为________(填字母)。
A.氧化反应 B.加成反应
C.水解反应 D.消去反应
(3)反应⑦可用于检验糖尿病患者尿液中的葡萄糖含量,该反应的化学方程式为
10____________________________________________
______________________________________________________。
(4)葡萄糖在人体内彻底氧化分解的化学方程式为
_______________________________________________________
______________________________________________________。
[解析](1)工业上制镜和热水瓶胆镀银都是利用了葡萄糖和银氨溶液反应还原出单质银
的性质,所以应为反应⑥。(2)反应①②是淀粉在不同条件下的水解反应。(3)反应⑦为葡萄糖
与新制Cu(OH) 的反应。
2
[答案] (1)⑥ (2)C (3)CHOH—(CHOH)—CHO+2Cu(OH) +NaOH――→CHOH—
2 4 2 2
(CHOH)—COONa+CuO↓+3HO (4)CH O+6O―→6CO+6HO
4 2 2 6 12 6 2 2 2
11