文档内容
第三章 铁 金属材料
第一节 铁及其化合物 课时作业
第一课时 铁的单质
基础达标
1.下列关于铁的叙述中错误的是( )
A.纯净的铁是光亮的银白色金属 B.铁能被磁体吸引
C.铁是地壳中含量最多的金属元素 D.铁具有延展性和导热性,可制作炊具
2.下列物质能由单质直接化合生成的是 ( )
A.Al S B.FeCl
2 3 2
C.SO D.CuI
3 2
3.下列关于铁的性质的描述中,不正确的是 ( )
A.具有还原性,易被氧化 B.高温下能与水蒸气反应产生氢气
C.能在氯气中燃烧产生棕黄色的烟 D.铁的氧化物均能溶于水且与水发生反应
4.关于实验室铁和稀盐酸反应的描述正确的是 ( )
A.这是一个置换反应
B.反应的化学方程式是2Fe+6HCl===2FeCl +3H↑
3 2
C.实验现象是出现气泡,溶液由无色变为棕黄色
D.如果把稀盐酸改为浓盐酸会出现钝化现象
5.已知钠、铁都能与水反应,下列叙述不正确的是 ( )
A.它们反应的难易程度不同 B.它们反应的产物不完全相同
C.都需在高温条件下进行 D.反应类型都是置换反应
6.下列物质中,在一定条件下与铁反应,且铁元素的化合价能变为+3价的是
( )
A.氯化铁溶液 B.硫酸铜溶液
C.氯气 D.稀盐酸
7.能使铁溶解,但不能生成沉淀的溶液是 ( )
A.AgNO 溶液 B.FeCl 溶液
3 3
C.CuSO 溶液 D.FeSO 溶液
4 4
8.如图所示装置,可用以制取和观察 在空气中被氧化时颜色的变化。下列说法错误的是( )
A.实验前,应事先煮沸溶液除去溶解氧
B.装置Ⅰ可制取FeSO 溶液并排尽装置内空气
4
C.关闭止水夹可观察到装置Ⅱ中溶液进入装置Ⅰ中
D.取下装置Ⅱ的橡皮塞可观察沉淀颜色变化
9.铁是日常生活中使用最广泛的金属,下列关于铁的一些说法正确的是( )
A.常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏、贮运浓硫酸
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe O
3 4
C.铁是较活泼的金属,它与卤素单质(X )反应的生成物均为FeX
2 3
D.铁的氧化物有FeO、Fe O 和Fe O,均为黑色固体
2 3 3 4
10.将过量的铁片投入热的浓硫酸中,下列判断正确的是( )
A.金属铁片表面因生成致密氧化膜而不反应 B.会立即生成H
2
C.会立即生成SO ,且只生成SO D.除了SO 外,还会有H 产生
2 2 2 2
能力提升
11.下列实验操作和现象、结论或目的均正确的是 ( )
已知:KSCN溶液可以使Fe3+显红色
选项 操作和现象 结论或目的
向红砖粉末中加入盐酸,充分反应后取上层清液
A 红砖中含有氧化铁
于试管中,滴加KSCN溶液2~3滴,溶液呈红色
CO还原Fe O 得到的黑色固体加入盐酸溶解后再
2 3
B 黑色固体中没有Fe O
3 4
加入KSCN溶液,溶液不显红色
取少量Fe(NO ) 试样加水溶解,加稀HSO 酸 该Fe(NO ) 试样已经变
3 2 2 4 3 2
C
化,滴加KSCN溶液,溶液变为红色 质
向某溶液中通入Cl,然后再加入KSCN溶液,变
2
D 原溶液中含有Fe2+
红色
12.“秦砖汉瓦”是我国传统建筑文化的一个缩影。同是由黏土烧制的砖瓦,有的是黑
色的,有的却是红色的,你猜测其中的原因可能是( )
A.土壤中含有铁粉、二氧化锰等B.黑砖瓦是煅烧过程中附着了炭黑,红砖瓦则是添加了红色耐高温染料
C.土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu
D.土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色 Fe O 或FeO和红色
3 4
Fe O
2 3
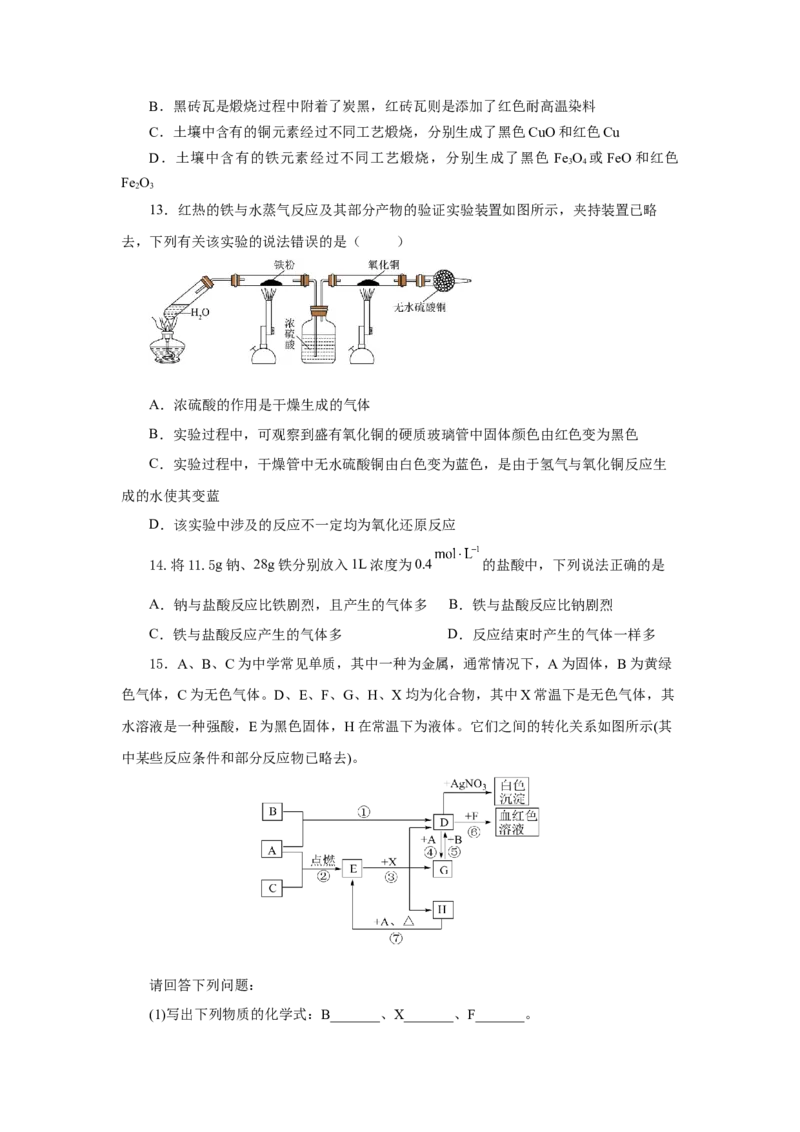
13.红热的铁与水蒸气反应及其部分产物的验证实验装置如图所示,夹持装置已略
去,下列有关该实验的说法错误的是( )
A.浓硫酸的作用是干燥生成的气体
B.实验过程中,可观察到盛有氧化铜的硬质玻璃管中固体颜色由红色变为黑色
C.实验过程中,干燥管中无水硫酸铜由白色变为蓝色,是由于氢气与氧化铜反应生
成的水使其变蓝
D.该实验中涉及的反应不一定均为氧化还原反应
14.将11.5g钠、28g铁分别放入1L浓度为0.4 的盐酸中,下列说法正确的是
A.钠与盐酸反应比铁剧烈,且产生的气体多 B.铁与盐酸反应比钠剧烈
C.铁与盐酸反应产生的气体多 D.反应结束时产生的气体一样多
15.A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿
色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其
水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其
中某些反应条件和部分反应物已略去)。
请回答下列问题:
(1)写出下列物质的化学式:B_______、X_______、F_______。(2)在反应①~⑦中,不属于氧化还原反应的是___________(填编号)。
(3)反应④的离子方程式是________________________________________________。
(4)反应⑦的化学方程式是________________________________________________。
直击高考
16.向一定量的Fe、FeO、Fe O 的混合物中加入100mL1mol/L的盐酸,恰好使混合物
2 3
完全溶解,放出224mL(标准状况下)的气体。所得溶液中加入KSCN溶液无红色出现,混
合物中铁元素的质量分数为
A.81.4% B.77.8%
C.68.6% D.无法计算
17.在一定条件下用普通铁粉和水蒸气反应可以得到铁的氧化物。该氧化物又可经过
此反应的逆反应生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击受
热时会燃烧,所以俗称“引火铁”。请分别用下图所示的两套仪器装置,制取上述铁的氧
化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1盐酸,其他试剂自选(装置中必
要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
填写下列空白:
(1)实验进行时,试管A中应加入的试剂是 ;烧瓶B的作用
是 ;烧瓶C的作用是 ;在试管D中收
集到的是 。
(2)实验时,U形管G中应加入的试剂是 ________ _ ;分液漏斗H中
应加入 。
(3)两套装置中,在实验时需要加热的仪器是 (填该仪器对应的字母)。
(4)试管E中发生反应的化学方程式是 。
(5)为了安全,在E管中的反应发生前,在F出口处必须 ;
E管中的反应开始后,在F出口处应 。