文档内容
2024-2025 连云港市新海高级中学 4 月质检
化学试题
(时间75分钟 满分100分)
一、单选题(共13小题 满分39分)
1.化学已渗透人类生活的各个方面。下列说法不正确的是
A.高纯度的硅单质广泛用于制作光导纤维
B.“光化学烟雾”的形成与氮氧化合物有关
C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
D.二氧化硫可作为食品添加剂
2.下列化学用语错误的是
A. 的形成过程:
B.乙烯的结构简式:
C. 的结构式:
D.钾的原子结构示意图:
3.下列有机物中,属于同系物的一组是
A. B.
C. D.
4.下列化学反应前后,体系的能量变化与下图不符的是
A.2Na + 2H O=2NaOH + H ↑ B.2Al + Fe O 2Fe + Al O
2 2 2 3 2 3
C.C H + 5O 3CO + 2H O D.C + H O(g) CO + H
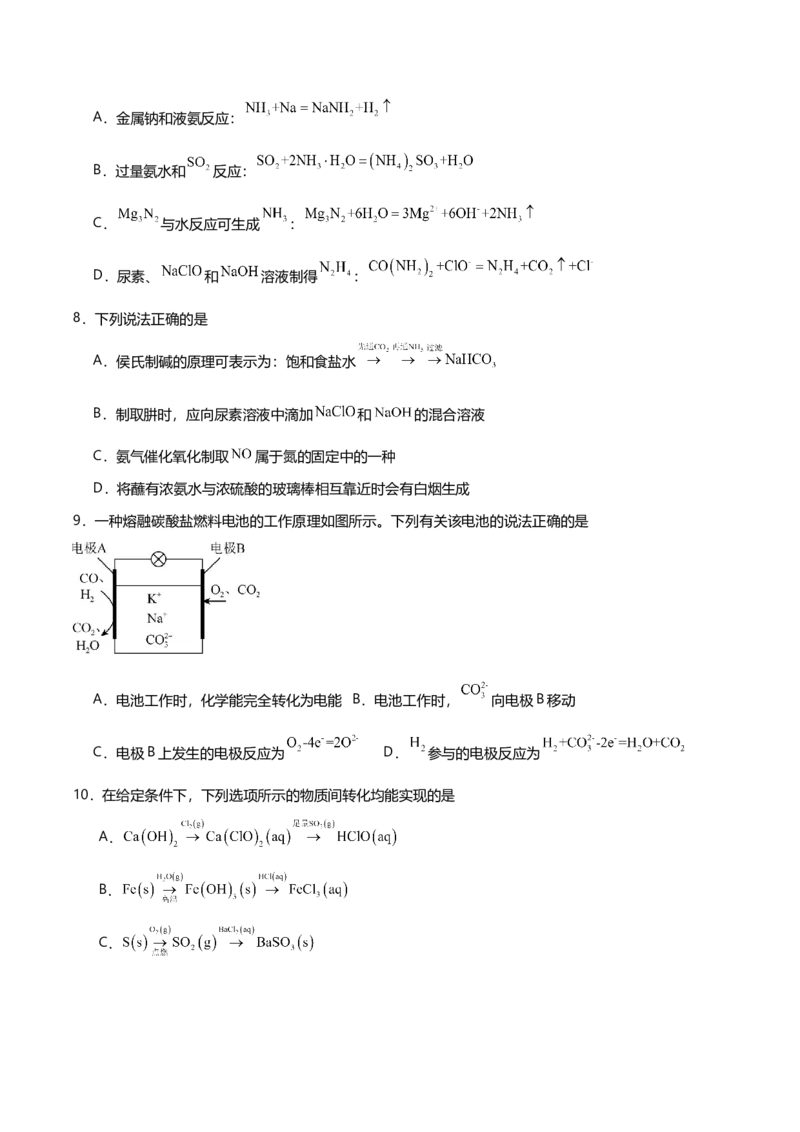
3 8 2 2 2 2 25.一定温度下,向容积为 的密闭容器中通入两种气体发生化学反应生成另外两种气体,反应中各物质
的物质的量变化如图所示,对该反应的推断合理的是
A.该反应的化学方程式为
B.反应进行了 的平均反应速率为
C.反应进行到 时,
D.反应进行到 时,各物质的反应速率相等
氮的常见氢化物有氨 和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种
常用的还原剂。 与水反应可生成 ,液氨发生微弱电离产生 ,液氨能与碱金属(如 、K)
反应产生氢气。 中一个H被 取代,可得 。尿素 、 和 溶液一起
反应可制得 。
阅读以上材料,完成下列问题:
6.实验室利用下列装置制取收集氨气,能够达到实验目的的是
A B C D
制取氨气 干燥氨气 收集氨气 尾气吸收
7.下列化学反应表示正确的是A.金属钠和液氨反应:
B.过量氨水和 反应:
C. 与水反应可生成 :
D.尿素、 和 溶液制得 :
8.下列说法正确的是
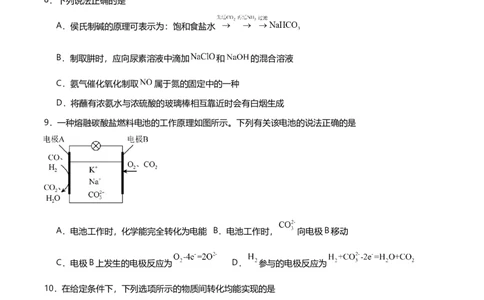
A.侯氏制碱的原理可表示为:饱和食盐水
B.制取肼时,应向尿素溶液中滴加 和 的混合溶液
C.氨气催化氧化制取 属于氮的固定中的一种
D.将蘸有浓氨水与浓硫酸的玻璃棒相互靠近时会有白烟生成
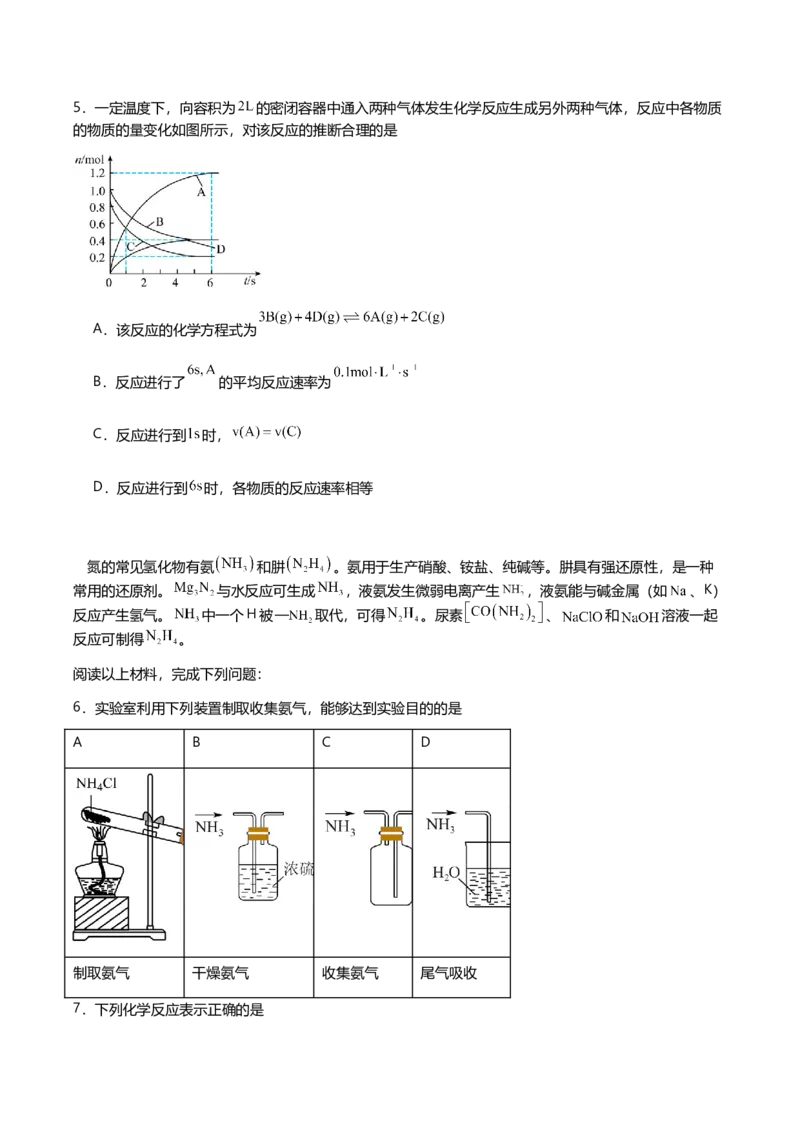
9.一种熔融碳酸盐燃料电池的工作原理如图所示。下列有关该电池的说法正确的是
A.电池工作时,化学能完全转化为电能 B.电池工作时, 向电极B移动
C.电极B上发生的电极反应为 D. 参与的电极反应为
10.在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.D.
11.常温下,下列实验探究方案能够达到探究目的的是
选
实验操作和现象 结论
项
向溶液X中加入少量稀NaOH溶液,将湿润的红色石蕊试纸置
A 溶液X不含NH
于试管,试纸未变蓝色
向Na CO 溶液中加入硝酸,将产生的气体直接通入硅酸钠溶液 酸性:硝酸>碳酸
B 2 3
中,产生白色胶状沉淀硅酸 >硅酸
C 向含有酚酞的NaOH溶液中通入SO ,溶液红色褪去 SO 有漂白性
2 2
D
向1mL0.1mol/LFeCl
3
溶液中滴加5mL0.1mol/LKI溶液,再滴加 FeCl
3
和KI反应为
几滴KSCN溶液,观察溶液颜色变红 可逆反应
A.A B.B C.C D.D
12.利用 氧化尿素制备 水合肼 ,同时可制备 ,制备流程如图所示:
已知: 有强还原性, 能与 反应生成 亚硫酸钠溶液的 约为
下列说法错误的是
A.步骤 反应时,若产物中 ,则
B.步骤Ⅱ反应的离子方程式为
C.步骤Ⅱ中须将尿素缓慢加入 碱性溶液中
D.步骤Ⅳ中反应过程中控制溶液为碱性,有利于吸收
13.一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同价态含 粒子的浓度随时间变化如图所示。下列说法正确的是
A. (Ⅲ)能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下, (Ⅱ)和 (Ⅶ)能大量共存
D.总反应为:
二、解答题(共4小题 满分61分)
14.H 、CO、CH 等都是重要的能源,也是重要的化工原料。
2 4
(1)25℃,101kPa时,8.0gCH 完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化
4
学方程式: 。
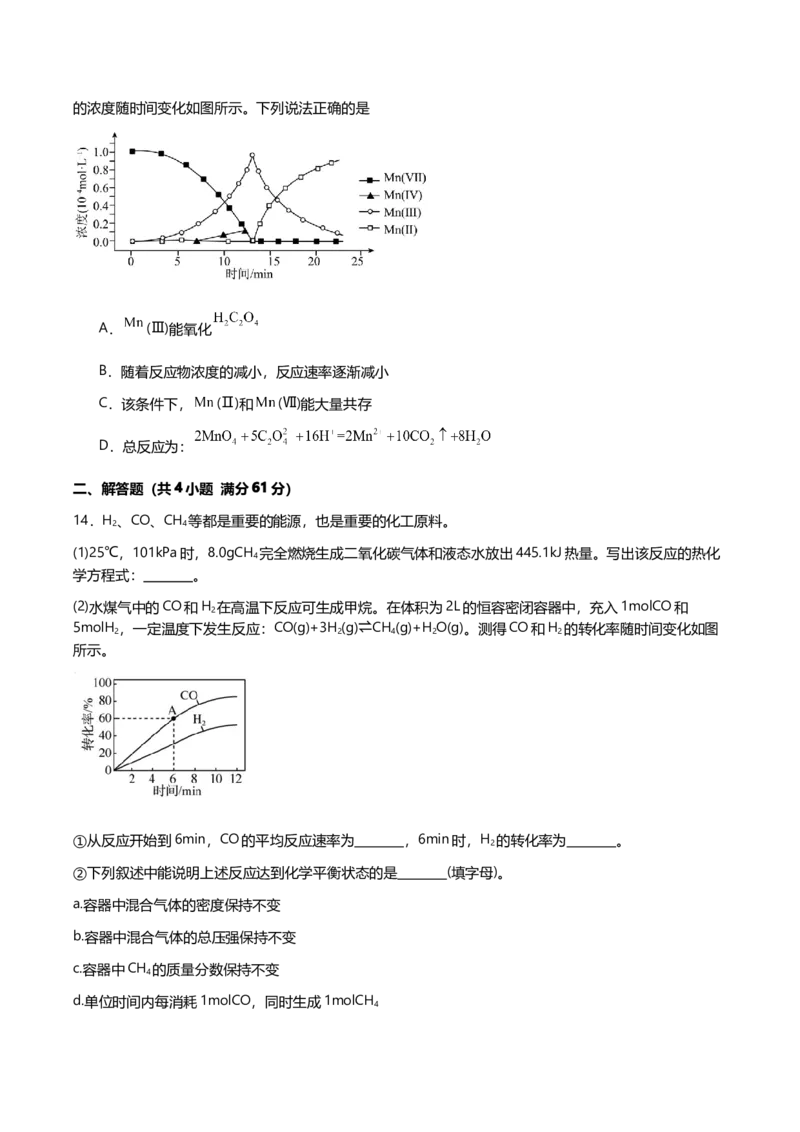
(2)水煤气中的CO和H 在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和
2
5molH ,一定温度下发生反应:CO(g)+3H (g)⇌CH (g)+H O(g)。测得CO和H 的转化率随时间变化如图
2 2 4 2 2
所示。
①从反应开始到6min,CO的平均反应速率为 ,6min时,H 的转化率为 。
2
②下列叙述中能说明上述反应达到化学平衡状态的是 (填字母)。
a.容器中混合气体的密度保持不变
b.容器中混合气体的总压强保持不变
c.容器中CH 的质量分数保持不变
4
d.单位时间内每消耗1molCO,同时生成1molCH
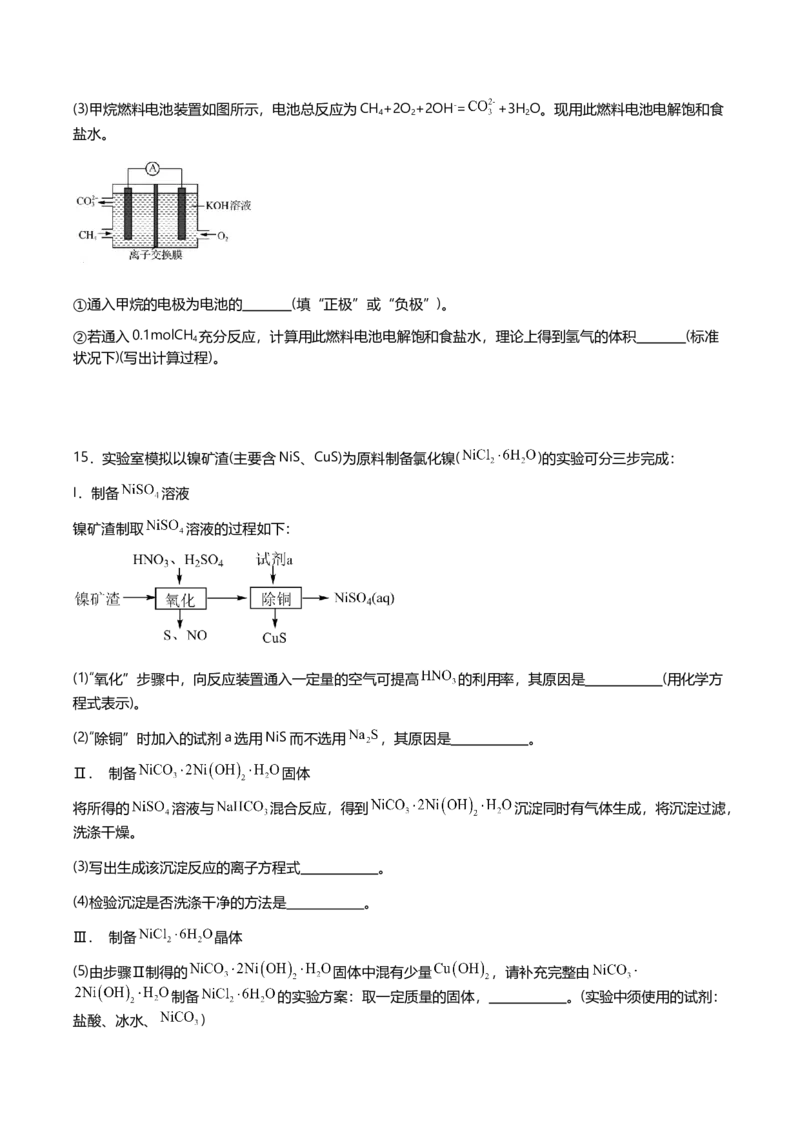
4(3)甲烷燃料电池装置如图所示,电池总反应为CH +2O +2OH-= +3H O。现用此燃料电池电解饱和食
4 2 2
盐水。
①通入甲烷的电极为电池的 (填“正极”或“负极”)。
②若通入0.1molCH 充分反应,计算用此燃料电池电解饱和食盐水,理论上得到氢气的体积 (标准
4
状况下)(写出计算过程)。
15.实验室模拟以镍矿渣(主要含NiS、CuS)为原料制备氯化镍( )的实验可分三步完成:
I.制备 溶液
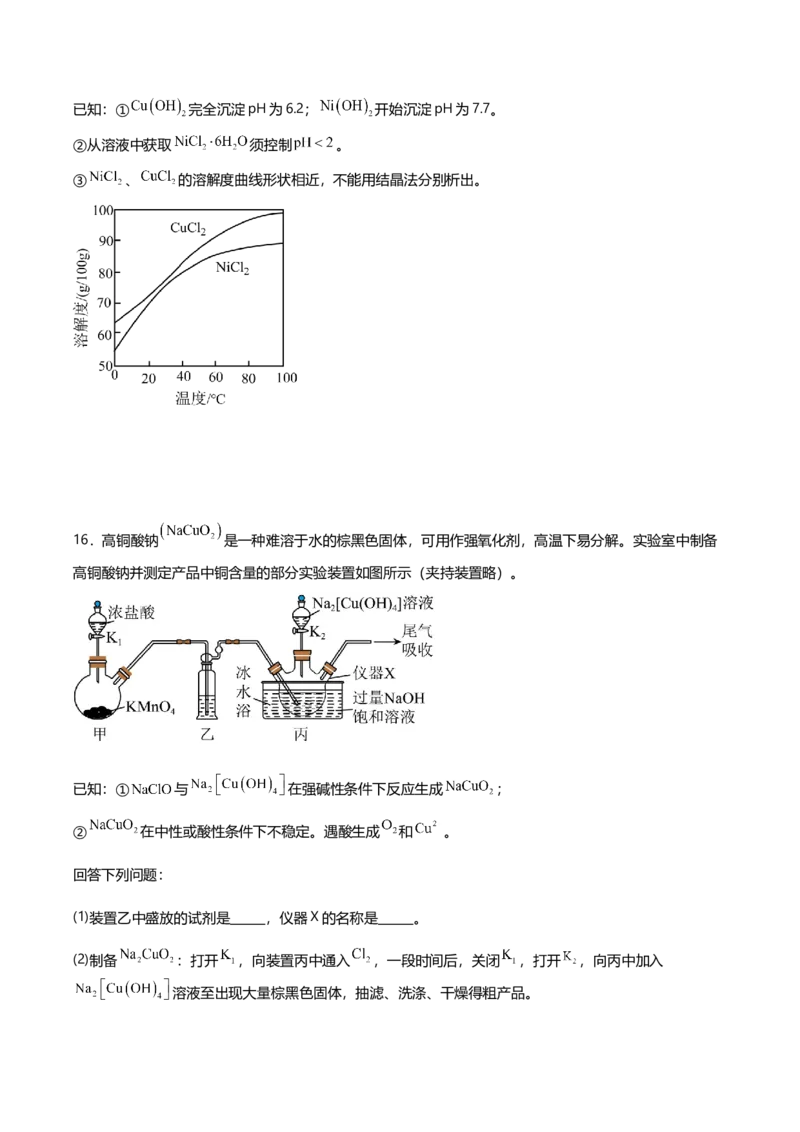
镍矿渣制取 溶液的过程如下:
(1)“氧化”步骤中,向反应装置通入一定量的空气可提高 的利用率,其原因是 (用化学方
程式表示)。
(2)“除铜”时加入的试剂a选用NiS而不选用 ,其原因是 。
Ⅱ. 制备 固体
将所得的 溶液与 混合反应,得到 沉淀同时有气体生成,将沉淀过滤,
洗涤干燥。
(3)写出生成该沉淀反应的离子方程式 。
(4)检验沉淀是否洗涤干净的方法是 。
Ⅲ. 制备 晶体
(5)由步骤Ⅱ制得的 固体中混有少量 ,请补充完整由
制备 的实验方案:取一定质量的固体, 。(实验中须使用的试剂:
盐酸、冰水、 )已知:① 完全沉淀pH为6.2; 开始沉淀pH为7.7。
②从溶液中获取 须控制 。
③ 、 的溶解度曲线形状相近,不能用结晶法分别析出。
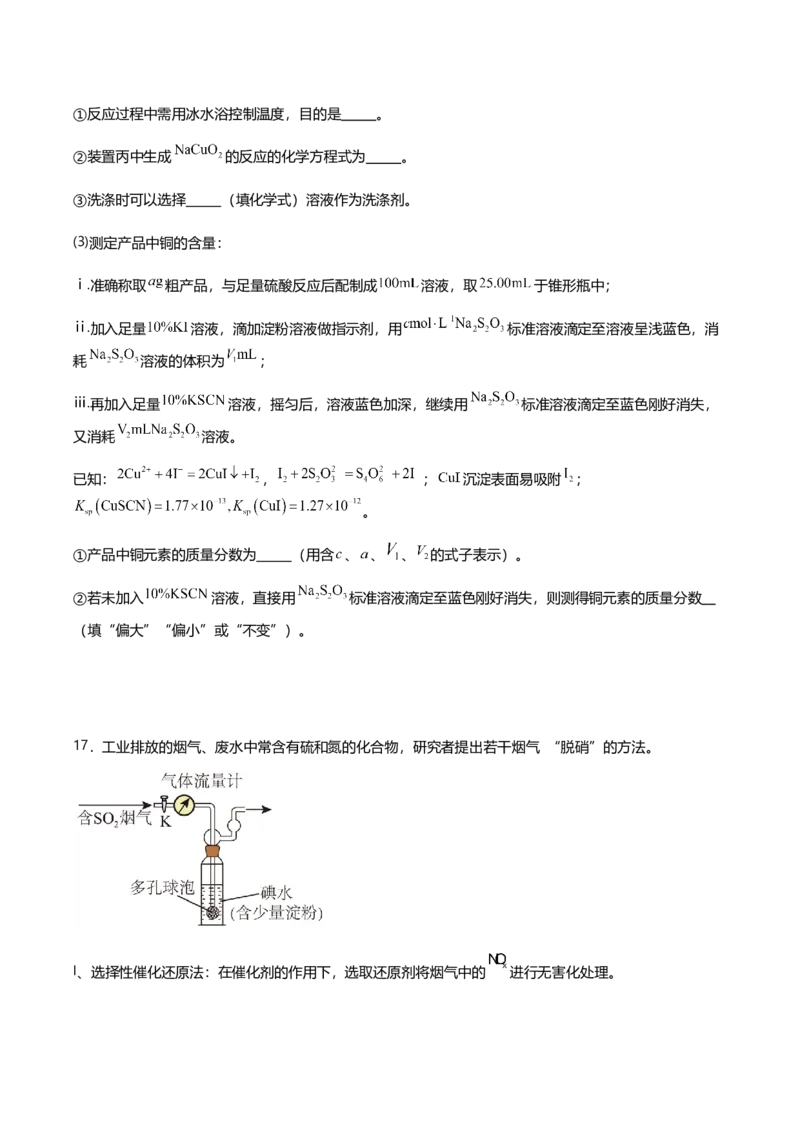
16.高铜酸钠 是一种难溶于水的棕黑色固体,可用作强氧化剂,高温下易分解。实验室中制备
高铜酸钠并测定产品中铜含量的部分实验装置如图所示(夹持装置略)。
已知:① 与 在强碱性条件下反应生成 ;
② 在中性或酸性条件下不稳定。遇酸生成 和 。
回答下列问题:
(1)装置乙中盛放的试剂是 ,仪器X的名称是 。
(2)制备 :打开 ,向装置丙中通入 ,一段时间后,关闭 ,打开 ,向丙中加入
溶液至出现大量棕黑色固体,抽滤、洗涤、干燥得粗产品。①反应过程中需用冰水浴控制温度,目的是 。
②装置丙中生成 的反应的化学方程式为 。
③洗涤时可以选择 (填化学式)溶液作为洗涤剂。
(3)测定产品中铜的含量:
ⅰ.准确称取 粗产品,与足量硫酸反应后配制成 溶液,取 于锥形瓶中;
ⅱ.加入足量 溶液,滴加淀粉溶液做指示剂,用 标准溶液滴定至溶液呈浅蓝色,消
耗 溶液的体积为 ;
ⅲ.再加入足量 溶液,摇匀后,溶液蓝色加深,继续用 标准溶液滴定至蓝色刚好消失,
又消耗 溶液。
已知: , ; 沉淀表面易吸附 ;
。
①产品中铜元素的质量分数为 (用含 、 、 、 的式子表示)。
②若未加入 溶液,直接用 标准溶液滴定至蓝色刚好消失,则测得铜元素的质量分数
(填“偏大”“偏小”或“不变”)。
17.工业排放的烟气、废水中常含有硫和氮的化合物,研究者提出若干烟气 “脱硝”的方法。
I、选择性催化还原法:在催化剂的作用下,选取还原剂将烟气中的 进行无害化处理。(1)写出选取 做还原剂时与烟气中的NO发生反应的化学方程式 。
II、氧化法:以NaClO溶液作为吸收剂进行 “脱硝”。控制过程中溶液的酸性,将烟气中的NO转化为
NO 向NaClO溶液中加入硫酸调节酸性后,可用于脱除NO。
(2)①不用盐酸调节NaClO溶液初始pH的原因是 。
②将 时NaClO溶液脱除NO的离子方程式补充完整: 。
III、在水处理领域,化学技术扮演着重要角色。
(3)用铝粉处理处理碱性废水中的 ,转化为无害气体和[Al(OH) ]-,该化学反应中,氧化剂还原剂物质的
4
量之比为 。
(4)催化还原法
①在W-Cu/Al O 的催化条件下,使用H 作为还原剂,可将水中的 转化为N 该反应机理分为三步,如
2 3 2 2.
图所示:第一步: 在Cu表面被还原为NO ,Cu被氧化为CuO;第二步:NO 从Cu表面迁移至W
的表面;第三步:H 在W表面吸附并解离为活性氢原子(W-H), 。(补充完整该步反应机理)
2
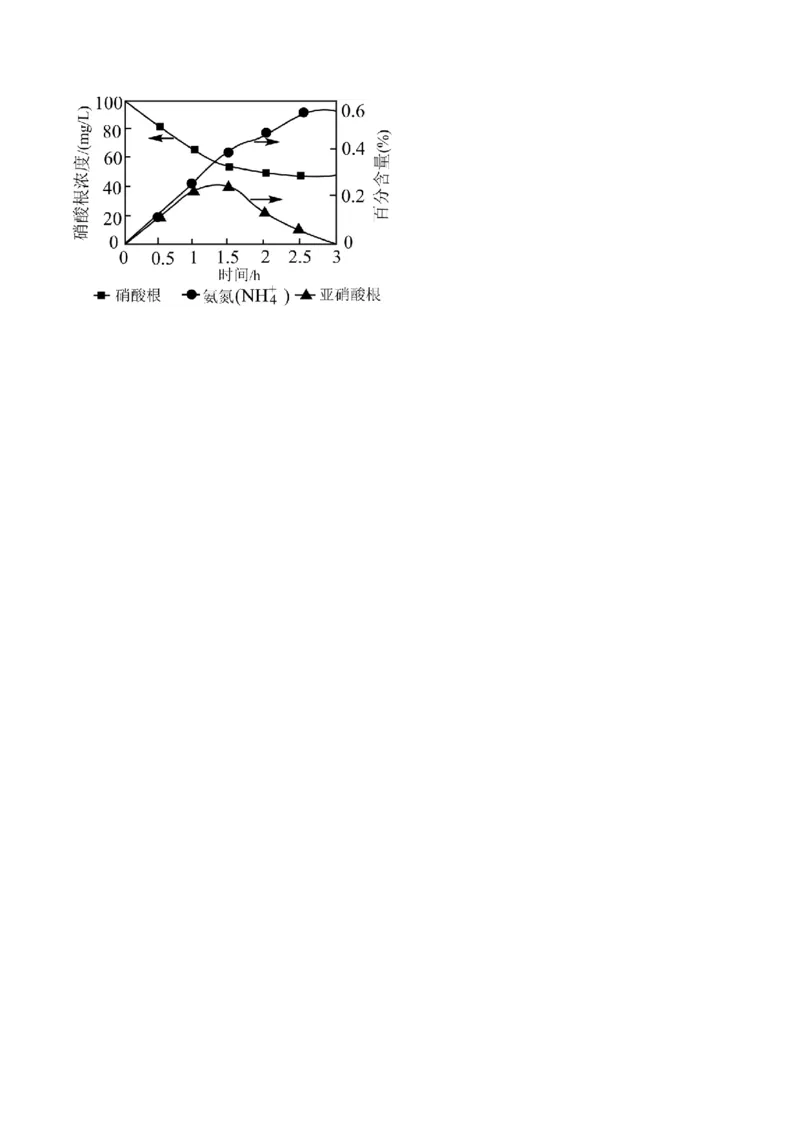
②若改用Pd-Cu/Al O 作为还原硝酸盐过程的催化剂,其催化机理与W-Cu/Al O 相似。但还原过程中检测
2 3 2 3
到三种含氮化合物微粒,其浓度变化如图所示,在1.5~2.5h过程中,硝酸根 部分转化为 的可能
原因是 。