文档内容
222000222444---222000222555连连连云云云港港港市市市新新新海海海高高高级级级中中中学学学 444月月月质质质检检检
化化化学学学试试试题题题
(((时时时间间间777555分分分钟钟钟 满满满分分分111000000分分分)))
一一一、、、单单单选选选题题题(((共共共111333小小小题题题 满满满分分分333999分分分)))
1.化学已渗透人类生活的各个方面。下列说法不正确的是
A.高纯度的硅单质广泛用于制作光导纤维
B.“光化学烟雾”的形成与氮氧化合物有关
C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
D.二氧化硫可作为食品添加剂
2.下列化学用语错误的是
A. 的形成过程:
B.乙烯的结构简式:
C. 的结构式:
D.钾的原子结构示意图:
3.下列有机物中,属于同系物的一组是
A. B.
C. D.
4.下列化学反应前后,体系的能量变化与下图不符的是
A.2Na+2H2O=2NaOH+H2↑ B.2Al+Fe2O3 2Fe+Al2O3
C.C3H8+5O2 3CO2+2H2O D.C+H2O(g) CO+H2
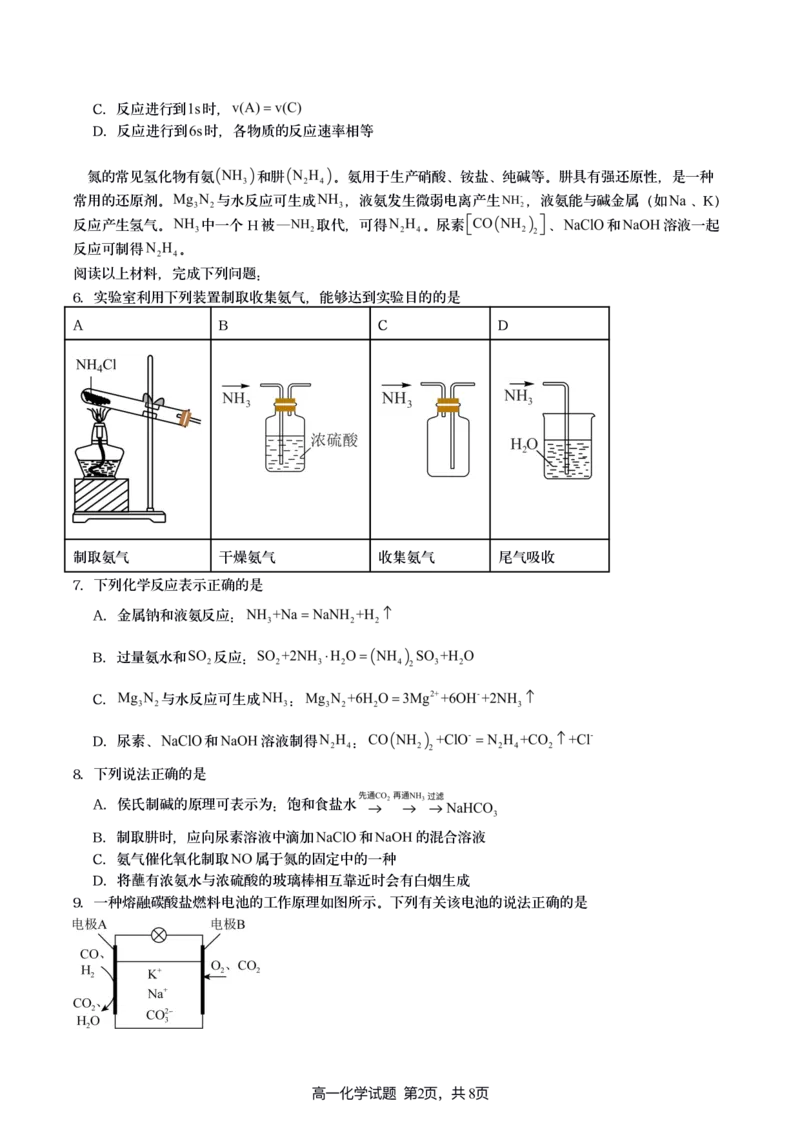
5.一定温度下,向容积为 的密闭容器中通入两种气体发生化学反应生成另外两种气体,反应中各物质
的物质的量变化如图所示,对该反应的推断合理的是
A.该反应的化学方程式为
B.反应进行了 的平均反应速率为
⾼⼀化学试题 第1⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}C.反应进行到 时,
D.反应进行到 时,各物质的反应速率相等
氮的常见氢化物有氨 和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种
常用的还原剂。 与水反应可生成 ,液氨发生微弱电离产生 ,液氨能与碱金属(如 、K)
反应产生氢气。 中一个H被 取代,可得 。尿素 、 和 溶液一起
反应可制得 。
阅读以上材料,完成下列问题:
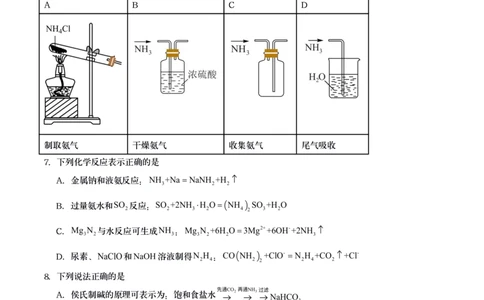
6.实验室利用下列装置制取收集氨气,能够达到实验目的的是
A B C D
制取氨气 干燥氨气 收集氨气 尾气吸收
7.下列化学反应表示正确的是
A.金属钠和液氨反应:
B.过量氨水和 反应:
C. 与水反应可生成 :
D.尿素、 和 溶液制得 :
8.下列说法正确的是
A.侯氏制碱的原理可表示为:饱和食盐水
B.制取肼时,应向尿素溶液中滴加 和 的混合溶液
C.氨气催化氧化制取 属于氮的固定中的一种
D.将蘸有浓氨水与浓硫酸的玻璃棒相互靠近时会有白烟生成
9.一种熔融碳酸盐燃料电池的工作原理如图所示。下列有关该电池的说法正确的是
⾼⼀化学试题 第2⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}A.电池工作时,化学能完全转化为电能 B.电池工作时, 向电极B移动
C.电极B上发生的电极反应为 D. 参与的电极反应为
10.在给定条件下,下列选项所示的物质间转化均能实现的是
A.
B.
C.
D.
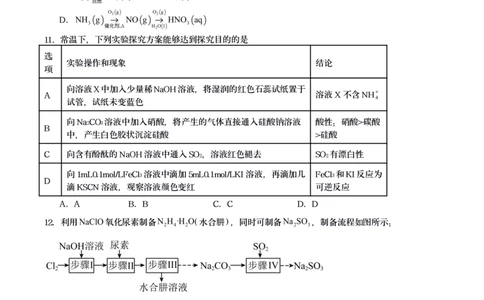
11.常温下,下列实验探究方案能够达到探究目的的是
选
实验操作和现象 结论
项
向溶液X中加入少量稀NaOH溶液,将湿润的红色石蕊试纸置于
A 溶液X不含NH
试管,试纸未变蓝色
向Na2CO3溶液中加入硝酸,将产生的气体直接通入硅酸钠溶液 酸性:硝酸>碳酸
B
中,产生白色胶状沉淀硅酸 >硅酸
C 向含有酚酞的NaOH溶液中通入SO2,溶液红色褪去 SO2有漂白性
向1mL0.1mol/LFeCl3溶液中滴加5mL0.1mol/LKI溶液,再滴加几 FeCl3和KI反应为
D
滴KSCN溶液,观察溶液颜色变红 可逆反应
A.A B.B C.C D.D
12.利用 氧化尿素制备 水合肼 ,同时可制备 ,制备流程如图所示:
已知: 有强还原性, 能与 反应生成 亚硫酸钠溶液的 约为
下列说法错误的是
A.步骤 反应时,若产物中 ,则
B.步骤Ⅱ反应的离子方程式为
C.步骤Ⅱ中须将尿素缓慢加入 碱性溶液中
D.步骤Ⅳ中反应过程中控制溶液为碱性,有利于吸收
⾼⼀化学试题 第3⻚,共8⻚
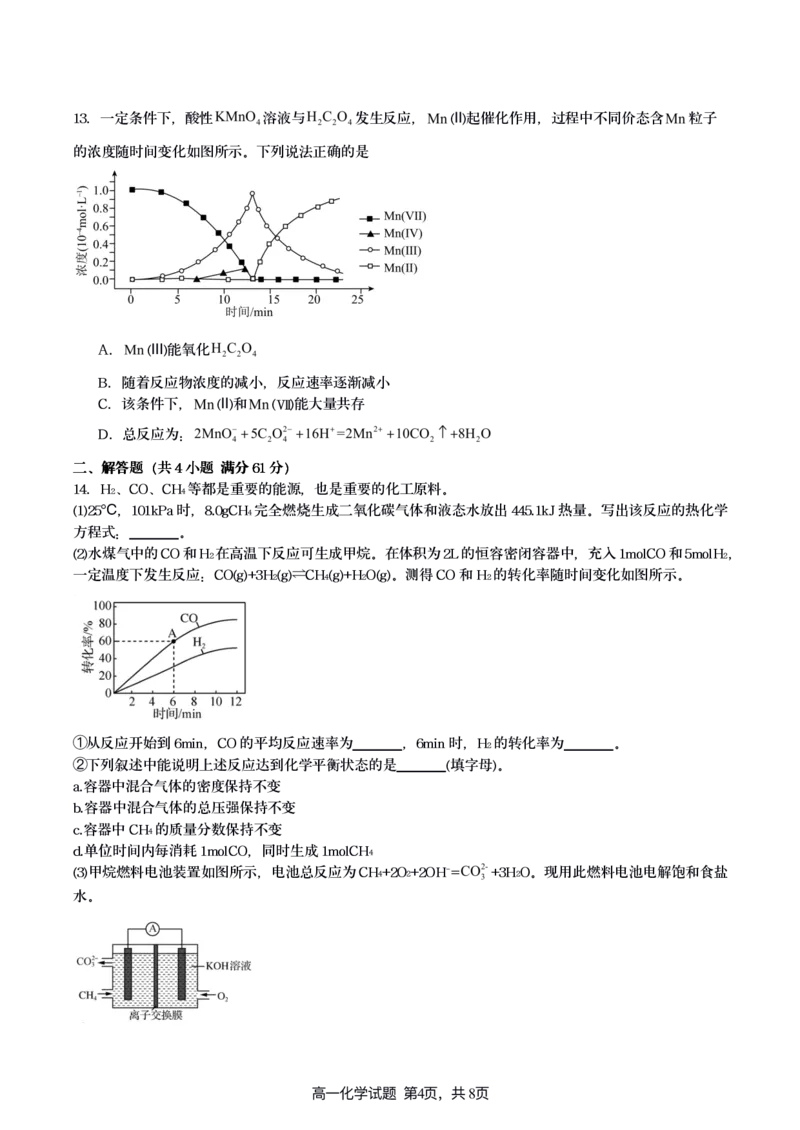
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}13.一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不同价态含 粒子
的浓度随时间变化如图所示。下列说法正确的是
A. (Ⅲ)能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下, (Ⅱ)和 (Ⅶ)能大量共存
D.总反应为:
二二二、、、解解解答答答题题题(((共共共444小小小题题题 满满满分分分666111分分分)))
14.H2、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)25℃,101kPa时,8.0gCH4完全燃烧生成二氧化碳气体和液态水放出445.1kJ热量。写出该反应的热化学
方程式: 。
(2)水煤气中的CO和H2在高温下反应可生成甲烷。在体积为2L的恒容密闭容器中,充入1molCO和5molH2,
一定温度下发生反应:CO(g)+3H2(g)⇌CH4(g)+H2O(g)。测得CO和H2的转化率随时间变化如图所示。
①从反应开始到6min,CO的平均反应速率为 ,6min时,H2的转化率为 。
②下列叙述中能说明上述反应达到化学平衡状态的是 (填字母)。
a.容器中混合气体的密度保持不变
b.容器中混合气体的总压强保持不变
c.容器中CH4的质量分数保持不变
d.单位时间内每消耗1molCO,同时生成1molCH4
(3)甲烷燃料电池装置如图所示,电池总反应为CH4+2O2+2OH-= +3H2O。现用此燃料电池电解饱和食盐
水。
⾼⼀化学试题 第4⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}①通入甲烷的电极为电池的 (填“正极”或“负极”)。
②若通入0.1molCH4充分反应,计算用此燃料电池电解饱和食盐水,理论上得到氢气的体积 (标准状
况下)(写出计算过程)。
15.实验室模拟以镍矿渣(主要含NiS、CuS)为原料制备氯化镍( )的实验可分三步完成:
I.制备 溶液
镍矿渣制取 溶液的过程如下:
(1)“氧化”步骤中,向反应装置通入一定量的空气可提高 的利用率,其原因是 (用化学
方程式表示)。
(2)“除铜”时加入的试剂a选用NiS而不选用 ,其原因是 。
Ⅱ. 制备 固体
将所得的 溶液与 混合反应,得到 沉淀同时有气体生成,将沉淀过滤,
洗涤干燥。
(3)写出生成该沉淀反应的离子方程式 。
(4)检验沉淀是否洗涤干净的方法是 。
Ⅲ. 制备 晶体
(5)由步骤Ⅱ制得的 固体中混有少量 ,请补充完整由
制备 的实验方案:取一定质量的固体, 。(实验中须使用
的试剂:盐酸、冰水、 )
已知:① 完全沉淀pH为6.2; 开始沉淀pH为7.7。
②从溶液中获取 须控制 。
③ 、 的溶解度曲线形状相近,不能用结晶法分别析出。
⾼⼀化学试题 第5⻚,共8⻚
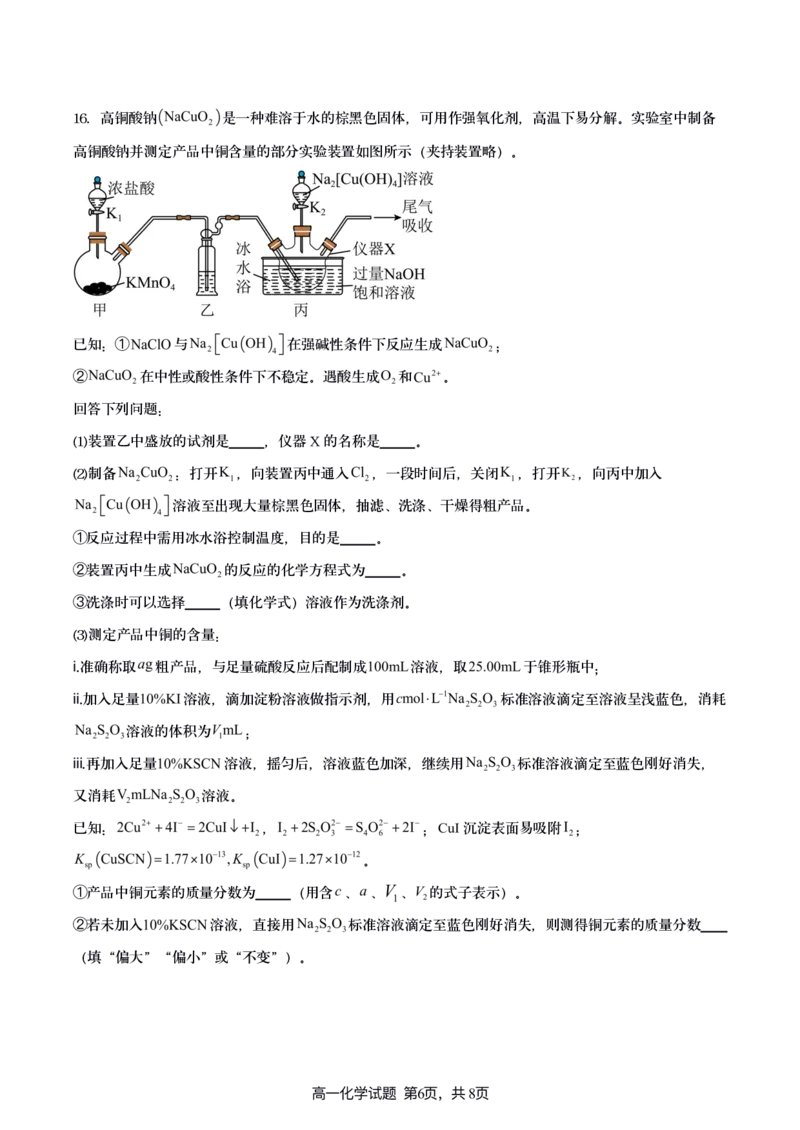
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}16.高铜酸钠 是一种难溶于水的棕黑色固体,可用作强氧化剂,高温下易分解。实验室中制备
高铜酸钠并测定产品中铜含量的部分实验装置如图所示(夹持装置略)。
已知:① 与 在强碱性条件下反应生成 ;
② 在中性或酸性条件下不稳定。遇酸生成 和 。
回答下列问题:
(1)装置乙中盛放的试剂是 ,仪器X的名称是 。
(2)制备 :打开 ,向装置丙中通入 ,一段时间后,关闭 ,打开 ,向丙中加入
溶液至出现大量棕黑色固体,抽滤、洗涤、干燥得粗产品。
①反应过程中需用冰水浴控制温度,目的是 。
②装置丙中生成 的反应的化学方程式为 。
③洗涤时可以选择 (填化学式)溶液作为洗涤剂。
(3)测定产品中铜的含量:
ⅰ.准确称取 粗产品,与足量硫酸反应后配制成 溶液,取 于锥形瓶中;
ⅱ.加入足量 溶液,滴加淀粉溶液做指示剂,用 标准溶液滴定至溶液呈浅蓝色,消耗
溶液的体积为 ;
ⅲ.再加入足量 溶液,摇匀后,溶液蓝色加深,继续用 标准溶液滴定至蓝色刚好消失,
又消耗 溶液。
已知: , ; 沉淀表面易吸附 ;
。
①产品中铜元素的质量分数为 (用含 、 、 、 的式子表示)。
②若未加入 溶液,直接用 标准溶液滴定至蓝色刚好消失,则测得铜元素的质量分数
(填“偏大”“偏小”或“不变”)。
⾼⼀化学试题 第6⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}17.工业排放的烟气、废水中常含有硫和氮的化合物,研究者提出若干烟气 “脱硝”的方法。
I、选择性催化还原法:在催化剂的作用下,选取还原剂将烟气中的 进行无害化处理。
(1)写出选取 做还原剂时与烟气中的NO发生反应的化学方程式 。
II、氧化法:以NaClO溶液作为吸收剂进行 “脱硝”。控制过程中溶液的酸性,将烟气中的NO转化为
NO 向NaClO溶液中加入硫酸调节酸性后,可用于脱除NO。
(2)①不用盐酸调节NaClO溶液初始pH的原因是 。
②将 时NaClO溶液脱除NO的离子方程式补充完整: 。
III、在水处理领域,化学技术扮演着重要角色。
(3)用铝粉处理处理碱性废水中的 ,转化为无害气体和[Al(OH)4]-,该化学反应中,氧化剂还原剂物质的
量之比为 。
(4)催化还原法
①在W-Cu/Al2O3的催化条件下,使用H2作为还原剂,可将水中的 转化为N2.该反应机理分为三步,如
图所示:第一步: 在Cu表面被还原为NO ,Cu被氧化为CuO;第二步:NO 从Cu表面迁移至W的
表面;第三步:H2在W表面吸附并解离为活性氢原子(W-H), 。(补充完整该步反应机理)
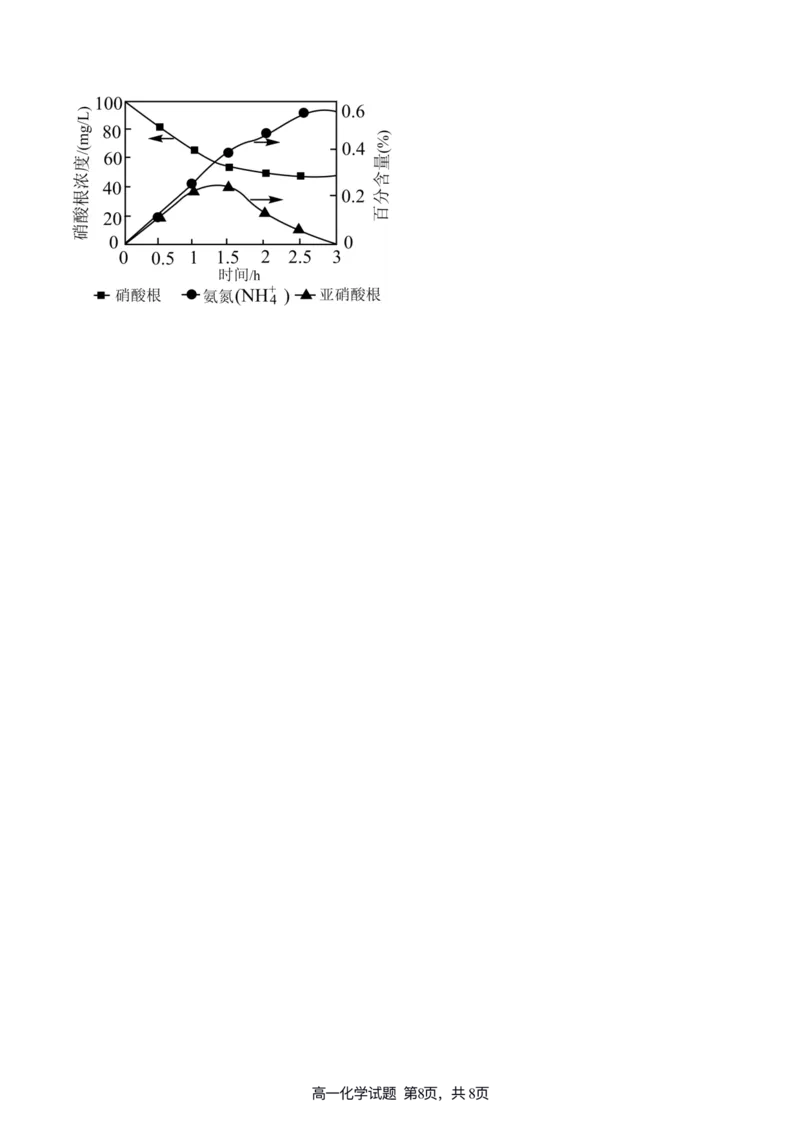
②若改用Pd-Cu/Al2O3作为还原硝酸盐过程的催化剂,其催化机理与W-Cu/Al2O3相似。但还原过程中检测
到三种含氮化合物微粒,其浓度变化如图所示,在1.5~2.5h过程中,硝酸根 部分转化为 的可能
原因是 。
⾼⼀化学试题 第7⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}⾼⼀化学试题 第8⻚,共8⻚
{#{QQABbYSsxgiwkBYACY7rEwHgCAgQkJATLSoGBVAaKAxLQAFIFAA=}#}