文档内容
第三章 铁 金属材料
第一节 铁及其化合物 课时作业
第二课时 铁的重要化合物—铁的氧化物和氢氧化物
基础达标
1.火星被称为“红色的星球”,这是因为它的岩石和土壤中含有丰富的( )
A.FeO B.Fe O
3 4
C.Fe O D.Fe
2 3
【答案】C
【解析】A.氧化亚铁为黑色,与火星被称为“红色的星球”无关,A错误;B.四氧
化三铁为黑色,与火星被称为“红色的星球”无关,B错误;C.Fe O 是一种红棕色粉
2 3
末,俗称“铁红”,是赤铁矿的主要成分,所以火星岩石和土壤中含有丰富的Fe O,C正
2 3
确;D.铁单质为银白色,与火星被称为“红色的星球”无关,D错误;故答案选C。
2.下列关于铁及其化合物的叙述正确的是( )
A.氢氧化铁受热分解可制得Fe O
3 4
B.Fe O、Fe O 都有磁性
2 3 3 4
C.FeO不稳定,在空气里受热,能迅速被氧化
D.高温下,铁能与水蒸气反应生成Fe O
2 3
【答案】C
【解析】A.氢氧化铁受热分解可制得Fe O,A错误;B.Fe O 具有磁性,Fe O 无
2 3 3 4 2 3
磁性,B错误;C.FeO不稳定,在空气里受热,能迅速被氧化为Fe O,C正确;D.高温
3 4
下,铁能与水蒸气反应生成Fe O 和氢气,D错误; 故选C。
3 4
3.铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发生钝化时,可生成一
3
种化学式为Fe O 的化合物,它可以看作由FeO和Fe O 组成的复杂氧化物。该化合物可
8 11 2 3
以表示为( )
A.FeO·3Fe O B.2FeO·3Fe O
2 3 2 3
C.FeO·2Fe O D.2FeO·Fe O
2 3 2 3
【答案】B
【解析】化合物 Fe O 可以看作由 FeO 和 Fe O 组成的复杂氧化物,设化学式为
8 11 2 3
nFeO·mFe O,则。解得n=2,m=3,该化合物可以表示为2FeO·3Fe O。
2 3 2 34.下列说法正确的是( )
A.Fe O 与HCl反应生成FeCl 、FeCl ,所以Fe O 是碱性氧化物
3 4 2 3 3 4
B.NaO 与盐酸反应生成盐和水,所以NaO 是碱性氧化物
2 2 2 2
C.FeO、Fe O 与硫酸反应只生成盐和水,所以都是碱性氧化物
2 3
D.NaHSO 在水中能电离出氢离子溶液显酸性,所以NaHSO 是酸
4 4
【答案】C
【解析】A.Fe O 与HCl反应生成FeCl 、FeCl 和水,生成两种盐,所以Fe O 不是
3 4 2 3 3 4
碱性氧化物,A错误;B.NaO 与盐酸反应生成盐和水、O,所以NaO 不是碱性氧化
2 2 2 2 2
物,B错误;C.FeO、Fe O 与硫酸反应生成盐和水,所以都是碱性氧化物,C正确;D.
2 3
NaHSO 能电离出H+,同时产生金属阳离子Na+及酸根离子SO 2-,所以NaHSO 是盐,D错
4 4 4
误;选C。
5.用如图所示实验装置进行相关实验探究,其中装置合理的是( )
选项 A B C D
证明Na能和水
加热分解固体
实验目的 制备Fe(OH) 稀释浓硫酸 反应,且Na的
2
NaHCO
3
密度比煤油大
实验装置
A.A B.B C.C D.D
【答案】D
【解析】A.碳酸氢钠受热分解产生水,试管口应向下倾斜,A不合理;B.Fe(OH)
2
容易被氧气氧化为Fe(OH) ,应尽量避免NaOH溶液与空气接触,具体操作为使用长滴管
3
且将长滴管插入硫酸亚铁溶液中,再将NaOH溶液挤出,B不合理;C.稀释浓硫酸应在烧
杯中进行,不能在容量瓶中进行,C不合理;D.煤油不溶于水,分层,通过观察钠在水
层和煤油层之间上下跳动,证明Na能和水反应,且Na的密度比煤油大,D合理;答案选
D。
6.下列有关物质用途的说法中,不正确的是( )
A.Cl 用于自来水消毒 B.Fe O 用作红色油漆和涂料
2 3 4C.NaHCO 用于蒸馒头 D.NaO 用作供氧剂
3 2 2
【答案】B
【解析】A.氯气能与水反应生成具有强氧化性的次氯酸,次氯酸具有杀菌消毒作
用,A正确;B.氧化铁为红棕色,用作红色油漆和涂料,B错误;C.NaHCO 水溶液显
3
碱性,当发面发过,有较多的酸性物质时,加入NaHCO 能够与酸反应产生二氧化碳气
3
体,减少了酸性物质,使蒸的馒头蓬松,口感好,C正确; D.过氧化钠与水、二氧化碳
反应都生成氧气,故可用作供氧剂,D正确;故合理选项是B。
7.下列离子方程式中,不正确的是( )
A.氯化铁溶液与氨水反应:Fe3++3OH-=Fe(OH) ↓
3
B.铁与稀盐酸反应:Fe+2H+=Fe2++H ↑
2
C.FeCl 溶液与氯水反应:2Fe2++Cl=2Fe3++2Cl-
2 2
D.Fe(OH) 与盐酸反应:Fe(OH) +3H+=Fe3++3H O
3 3 2
【答案】A
【解析】A.氯化铁与氨水中的一水合氨反应生成氢氧化铁和氯化铵,一水合氨是弱
碱,应保留化学式,反应的离子方程式为3NH ·H O+Fe3+=Fe(OH) ↓+3NH +,A错误;B.
3 2 3 4
铁与稀盐酸反应生成氯化亚铁和氢气,反应的离子方程式为Fe+2H+=Fe2++H ↑,B正确;
2
C.FeCl 溶液与氯水中的氯气反应生成氯化铁,反应的离子方程式为2Fe2++Cl=2Fe3+
2 2
+2Cl-,C正确;D.Fe(OH) 与盐酸反应生成氯化铁和水,反应的离子方程式为
3
Fe(OH) +3H+=Fe3++3H O,D正确;答案选A。
3 2
8.用如图装置可以制备 沉淀,下列说法不正确的是( )
A.该实验应该先打开C,一段时间后再关闭C
B.实验完成时,在A容器中得到白色沉淀
C.如果将NaOH溶液直接滴入 溶液中,最终得到红褐色沉淀
D.本实验制备的氢氧化亚铁可以相对较长时间保持白色状态
【答案】B【解析】A.该实验应该先打开C,利用生成的氢气排出装置内的空气,氢气纯净
后,再关闭C,故A正确;B.实验完成时,A容器中没有白色沉淀,白色沉淀在B容器
中得到,故B错误;C.如果将NaOH溶液直接滴入FeSO 溶液中,有氧气带入,开始生
4
成的白色沉淀迅速变为灰绿色,最终得到红褐色沉淀,故C正确;D.本实验利用氢气排
出装置内的空气,因此本实验制备的氢氧化亚铁可以相对较长时间保持白色状态,故D正
确。综上所述,答案为B。
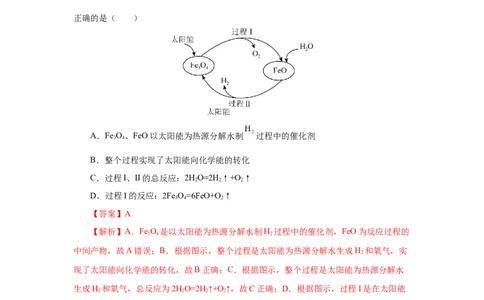
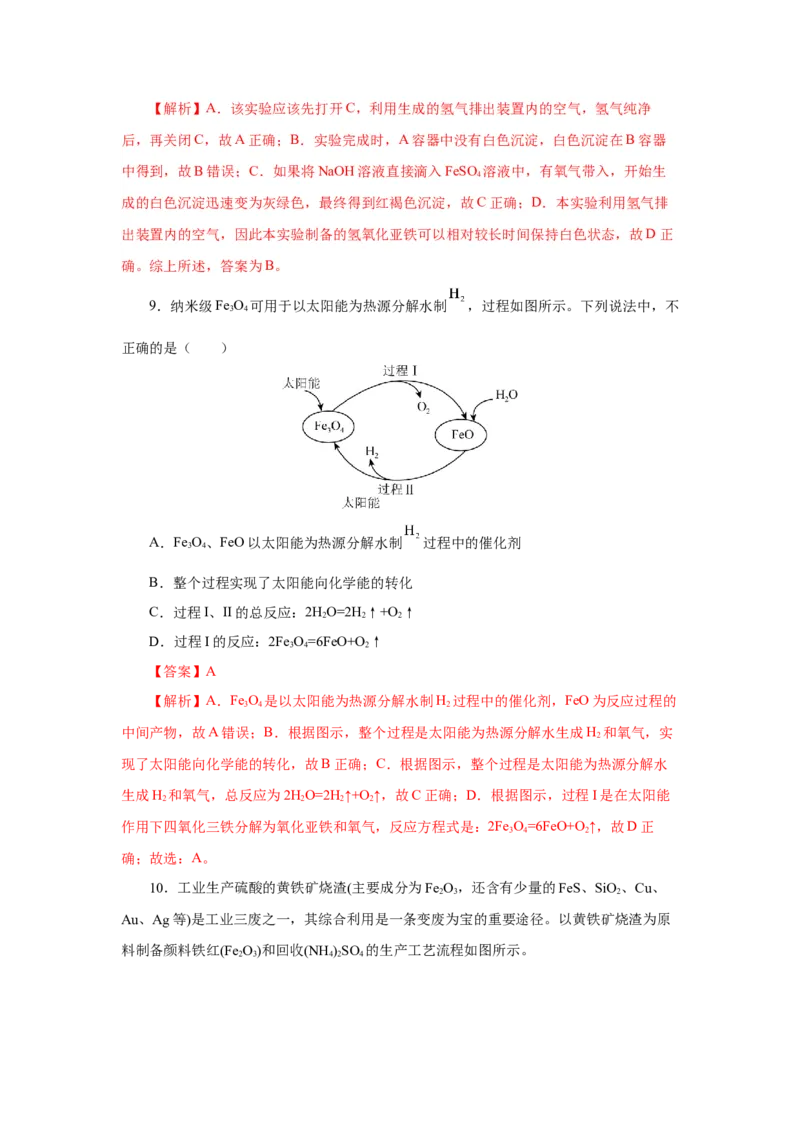
9.纳米级Fe O 可用于以太阳能为热源分解水制 ,过程如图所示。下列说法中,不
3 4
正确的是( )
A.Fe O、FeO以太阳能为热源分解水制 过程中的催化剂
3 4
B.整个过程实现了太阳能向化学能的转化
C.过程I、II的总反应:2HO=2H↑+O ↑
2 2 2
D.过程I的反应:2Fe O=6FeO+O ↑
3 4 2
【答案】A
【解析】A.Fe O 是以太阳能为热源分解水制H 过程中的催化剂,FeO为反应过程的
3 4 2
中间产物,故A错误;B.根据图示,整个过程是太阳能为热源分解水生成H 和氧气,实
2
现了太阳能向化学能的转化,故B正确;C.根据图示,整个过程是太阳能为热源分解水
生成H 和氧气,总反应为2HO=2H↑+O ↑,故C正确;D.根据图示,过程I是在太阳能
2 2 2 2
作用下四氧化三铁分解为氧化亚铁和氧气,反应方程式是:2Fe O=6FeO+O ↑,故D正
3 4 2
确;故选:A。
10.工业生产硫酸的黄铁矿烧渣(主要成分为Fe O,还含有少量的FeS、SiO、Cu、
2 3 2
Au、Ag等)是工业三废之一,其综合利用是一条变废为宝的重要途径。以黄铁矿烧渣为原
料制备颜料铁红(Fe O)和回收(NH )SO 的生产工艺流程如图所示。
2 3 4 2 4下列说法不正确的是 ( )
A.将矿渣粉碎和提高溶解温度能提高“废渣溶解”速率
B.“氧化”的目的是将+2价铁氧化为+3价铁
C.(NH )Fe (SO )(OH) 中Fe的化合价为+3价
4 2 6 4 4 12
D.该工艺流程中,两次加入氨水都是为了把Fe3+转化为Fe(OH)
3
【答案】D
【解析】A.适当加热、将固体粉碎、不断搅拌等都可以提高“废渣溶解”速率,故
A正确;B.“氧化”的目的是将亚铁离子氧化为铁离子,故B正确;C.
(NH )Fe (SO )(OH) 中N为−3价,H为+1价,O为−2价,S为+6价,根据物质不显电
4 2 6 4 4 12
性,得到Fe的化合价是+3价。故C正确;D.该工艺流程图中,第一次加入氨水得到
(NH )Fe (SO )(OH) 沉淀,第二次加入氨水前溶液为含铁离子的溶液,加氨水后发生的反
4 2 6 4 4 12
应是将铁离子沉淀,故D错误;故选D。
能力提升
11.中华传统文化与化学紧密相关,下列有关物质成分的叙述正确的是( )
A.柴窑烧制出的“明如镜,薄如纸,声如磬”的瓷器,其主要原料为硅的氧化物
B.古书中对“强水”有如下记录:“性最烈,能蚀五金,其水甚强……”,“强
水”是由浓硝酸和浓盐酸按体积比为3:1混合而成
C.《新修本草》中有关于“青矾”的描述为:“本来绿色,新出窟未见风者,正如
琉璃,烧之赤色”。这里的赤色物质是Fe O
3 4
D.东汉魏伯阳在《周易参同契》中对的描述:“……得火则飞,不见埃尘,将欲制
之,黄芽为根。”这里的黄芽是指硫
【答案】D
【解析】A.烧制瓷器原料为黏土,主要成分为硅酸盐,A错误;B.浓HNO 与浓
3
HCl按1:3体积比所得的混合物叫王水,能溶解金和铂,B错误;C.四氧化三铁为黑色
固体,不是赤色,C错误;D.液态的金属汞,受热易变成汞蒸气,汞属于重金属,能使
蛋白质变性,属于有毒物质,但常温下能和硫反应生成硫化汞,从而防止其变成汞气体,黄芽指呈淡黄色的硫单质,D正确;故答案为:D。
12.用铁泥(主要成分为Fe O、FeO和Fe)制备纳米Fe O(平均直径25nm)的流程示意
2 3 3 4
图如图:
下列叙述错误的是( )
A.铁红可用于油漆、油墨、建筑物着色剂
B.步骤②中,发生反应的离子方程式是2Fe3++Fe=3Fe2+、Fe+2H+=Fe2++H ↑
2
C.步骤④中使用过量的HO 有利于提高纳米Fe O 产率
2 2 3 4
D.为验证纳米态的Fe O,可将其形成分散系,做丁达尔效应实验
3 4
【答案】C
【解析】铁泥(主要成分为Fe O、FeO和Fe)与稀盐酸反应得到的滤液A的溶质为氯化
2 3
铁、氯化亚铁、过量的盐酸,加入铁粉还原铁离子:2Fe3++Fe=3Fe2+,过滤,分离出过量的
铁,滤液B的溶质为氯化亚铁,加入氢氧化钠溶液,生成Fe(OH) 浊液,向浊液中加入双
2
氧水氧化生成Fe(OH) ,再与氯化亚铁加热搅拌发生反应生成Fe O,过滤、洗涤、干燥得
3 3 4
产品Fe O,据此分析解答。A.铁红的主要成分是氧化铁,为红棕色,可用于油漆、油
3 4
墨、建筑物的着色剂,A项正确;B.滤液A中溶质为氯化铁、氯化亚铁、过量的稀盐
酸,加入铁粉还原铁离子和除去过量的盐酸:2Fe3++Fe=3Fe2+、Fe+2H+=Fe2++H ↑,B项正
2
确;C.步骤④中,过量的HO 在步骤⑤中会继续氧化+2价的铁,因此步骤④中HO 不
2 2 2 2
能过量,C项错误;D.纳米态Fe O 的平均直径25nm,形成的分散系属于胶体,可以通
3 4
过做丁达尔效应实验验证,D项正确;答案选C。
13.元素的“价-类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,
它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图。下图为
铁元素的“价-类”二维图,其中的箭头表示部分物质间的转化关系,下列说法正确的是(
)A.铁与高温水蒸气的反应可实现上述转化①
B.加热Fe(OH) 发生转化⑥,Fe O 加水溶解可转化为Fe(OH)
3 2 3 3
C.由图可预测:高铁酸盐(FeO2-)具有强氧化性,可用于饮用水的消毒
4
D.FeO是一种黑色粉末,只能用作还原剂
【答案】C
【解析】A.铁与高温水蒸气反应生成四氧化三铁和氢气,不能实现上述转化①,故
A错误;B.加热Fe(OH) 发生转化⑥分解生成氧化铁,Fe O 不溶于水,加水不溶解,不
3 2 3
可实现转化③,故B错误;C.高铁酸盐(FeO2-)具有强氧化性,与水反应生成Fe(OH) 胶
4 3
体,其中Fe元素化合价由+6价变为+3价,则O元素化合价由-2价变为0价,即有氧气生
成,可用于消毒,则反应的离子方程式为4FeO2-+10H O=4Fe(OH) (胶体)+3O ↑+8OH-,生
4 2 3 2
成的氢氧化铁胶体具有较大表面积,吸附悬浮杂质可以作净水剂,故C正确;D.FeO是
一种黑色粉末,其中Fe元素显+2价既可作氧化剂又可作还原剂,故D错误;故答案为C
14.回答下列问题
(1)下列各图示中,能较长时间观察到Fe(OH) 白色沉淀的是____________。
2
(2)用下列方法可制得白色的Fe(OH) 沉淀:用不含Fe3+的FeSO 溶液与用不含O 的蒸
2 4 2馏水配制的NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述FeSO 溶液时还需加入___________________。
4
②除去蒸馏水中溶解的O 常采用__________________的方法。
2
③生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶
2 2 4
液液面下,再挤出NaOH溶液。这样操作的理由是
____________________________________。
(3)除去FeCl 溶液中少量的FeCl ,可加入_______________________,反应的离子方
2 3
程式为_____________________________________________。
【答案】(1)①②③⑤
(2) 稀硫酸、铁屑 煮沸 避免生成的Fe(OH) 沉淀接触O
2 2
(3) 足量铁粉 Fe+2Fe3+=3Fe2+
【解析】若想制得Fe(OH) ,并在较长时间不被氧化成Fe(OH) ,需先排尽装置内的空
2 3
气,再将不含O 的NaOH与FeSO 溶液接触发生反应。
2 4
(1)装置①②③⑤中,除去保证药品自身不溶解O 外,还能有效防止空气中O 的溶
2 2
入,而装置④中,NaOH溶液在滴入过程中,较长时间与空气接触,会溶入少量氧气,从
而导致生成的Fe(OH) 被氧化为Fe(OH) ,很难看到生成白色沉淀,效果欠佳。故选
2 3
①②③⑤。答案为:①②③⑤;
(2)①用硫酸亚铁晶体配制上述FeSO 溶液时,为防止Fe2+被空气中氧气氧化为
4
Fe3+,需加入还原剂Fe,为防止Fe2+发生水解,需加入硫酸抑制水解,所以还需加入稀硫
酸、铁屑。②气体的溶解度随温度升高而减小,所以除去蒸馏水中溶解的O 常采用煮沸的
2
方法。③生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO
2 2 4
溶液液面下,再挤出NaOH溶液,从而使得NaOH溶液没有机会与空气接触。这样操作的
理由是:避免生成的Fe(OH) 沉淀接触O。答案为:稀硫酸、铁屑;煮沸;避免生成的
2 2
Fe(OH) 沉淀接触O;
2 2
(3)除去FeCl 溶液中少量的FeCl ,可加入还原剂且不引入新的杂质离子,所以应加
2 3
入足量铁粉,反应的离子方程式为Fe+2Fe3+=3Fe2+。答案为:足量铁粉;Fe+2Fe3+=3Fe2+。
直击高考
15.向一定量的Fe、FeO、Fe O 的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使
2 3
混合物完全溶解,放出1.344 L NO(标准状况),向所得溶液中加入KSCN溶液,无明显变化。若用足量的CO在加热条件下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24 mol B.0.21 mol
C.0.16 mol D.0.14 mol
【答案】B
【解析】n(HNO)=0.12 L×4 mol·L-1=0.48 mol,n(NO)==0.06 mol,向所得溶液中
3
加入KSCN溶液,无明显变化,说明全部生成Fe2+,溶液中溶质为Fe(NO ) ,根据原子守
3 2
恒,则原混合物中Fe的物质的量为=0.21 mol,故用足量的CO在加热条件下还原相同质
量的混合物,最终得到铁的物质的量为0.21 mol,故B项正确。
16.某化学学习小组设计了下列方法探究氢氧化亚铁的制备等相关问题。
(1)用NaOH溶液和FeSO 溶液直接反应,方法如图。该方法能观察到白色的Fe(OH)
4 2
沉淀,但沉淀颜色快速发生变化。请分析沉淀颜色变化的原因(用化学方程式表示):
__________________________________________________________________。
(2)该小组为探究反应物浓度对Fe(OH) 制备效果的影响,以Fe(OH) 沉淀白色持续时
2 2
间(t)为指标,t越大,实验效果越好。部分实验数据如表(w代表质量分数):
实验 序号 w(FeSO)/% w(NaOH)/% t/s
4
i 2.5 15 149
ii 5 15 138
iii 10 15 93
iv 5 25 142
v 5 35 180
①实验i、ii、iii的目的是______________________________________。
②该小组同学通过实验推断:其他条件不变时,所用NaOH溶液的浓度越大,实验效
果越好。推断的证据是______________________________________________。
③由绿矾晶体(FeSO •7H O)固体配制250mL0.10mol•L-1FeSO 溶液,需要用到的仪器有
4 2 4
药匙、玻璃棒、烧杯、托盘天平、250mL容量瓶、_________________。以下操作会导致所配溶液浓度偏低的是_________________。
A.容量瓶中原有 少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
(3)若向FeSO 溶液中加入足量NaO,观察到的现象是
4 2 2
____________________________。
【答案】4Fe(OH) +O +2H O=4Fe(OH) 探究其他条件相同时,FeSO 溶液浓度对
2 2 2 3 4
Fe(OH) 制备效果的影响 沉淀持续时间t:v>iv>ii 胶头滴管 BD 有红褐色沉
2
淀生成,有气体放出
【解析】(1)FeSO 和NaOH发生复分解反应生成Fe(OH) ,Fe(OH) 被空气中的氧气氧
4 2 2
化生成Fe(OH) ,化学方程式为4Fe(OH) +O +2H O=4Fe(OH) ;
3 2 2 2 3
(2) ①实验i、ii、iii的变量是FeSO 溶液浓度,目的是:探究其他条件相同时,FeSO
4 4
溶液浓度对Fe(OH) 制备效果的影响;②实验v、iv、ii的变量是NaOH溶液浓度,其他条
2
件不变时,所用NaOH溶液的浓度越大,沉淀持续时间越长,实验效果越好,则证据是:
沉淀持续时间t:v>iv>ii;③配制一定物质的量浓度溶液配制的步骤:计算、称量、溶解、
移液、洗涤、定容等,用到的仪器:药匙、玻璃棒、烧杯、托盘天平、250mL容量瓶、胶
头滴管;
A.定容时还需要加入蒸馏水,则容量瓶中原有少量蒸馏水对所配溶液浓度无影响,A不
选;
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中,则残留在杯壁上的溶质没有完全转移到容
量瓶,导致所配溶液浓度偏低,B选;C.定容时俯视刻度线导致溶液体积偏小,依据
c=n/V可知溶液浓度偏高,C不选;D.定容摇匀后发现溶液体积低于刻度线,再补加少量
蒸馏水至刻度线,导致加入水的体积增大,溶液浓度偏低,D选;故选:BD;
(3) Na O 和水反应生成NaOH和O,NaOH再和FeSO 溶液反应生成Fe(OH) 中,由
2 2 2 4 2
于NaO 过量,则Fe(OH) 被氧化为Fe(OH) ,观察到的现象是有红褐色沉淀生成,有气体
2 2 2 3
放出。