文档内容
第三章 铁 金属材料
第一节 铁及其化合物
第二课时 铁的重要化合物—铁的氧化物和氢氧化物
【学习目标】1.通过学习铁的氧化物和氢氧化物,学会从物质类别和元素价态的视角认识具有变价元
素物质间的转化关系,并建立认识模型,丰富研究物质的思路和方法。
2.通过实验探究铁的氢氧化物的化学性质,并能用化学方程式或离子方程式正确表示。体会实验对认
识和研究物质性质的重要作用,形成证据意识。
3.结合应用实例,将铁的氧化物和氢氧化物性质的知识运用于解决生产、生活中简单的化学问题,强
化性质决定用途的观念。
【学习重点】铁的氧化物性质、铁的氢氧化物性质及制备
【学习难点】制备氢氧化亚铁的实验设计
【课前预习】
旧知回顾:1.金属化合物的主要类型及转化是 金属氧化物 → 氢氧化物(碱)→盐;金属化合物类别
不同、 价态 不同, 性质 不同。
2.铁在氧气中燃烧的化学方程式为: 3Fe+2O ===== Fe O (填化学式),铁锈的主要成分为 F e O
2 3 4 2 3
。
新知预习:1.铁在化合物中主要有 + 2 、 + 3 两 种价态,铁的氧化物主要有氧化亚铁、氧化铁(又名
铁红 )、 四氧化三铁(又名 磁性氧化铁)三种。氧化铁 常用作红色油漆和涂料,赤铁矿的主要成分是
Fe O 。
2 3
2.FeSO 和NaOH溶液反应的现象:生成白色絮状沉淀迅速变成灰绿色,最后变成红褐色,化学方程
4
式:FeSO + 2NaOH=Fe(OH ) + N aSO 、 4Fe(OH ) + O + 2H O == =4Fe(OH)
4 2 2 4 2 2 2 3
【课中探究】
情景导入:红砖和青砖都是生活中用到的建筑材料(见PPT图片),两者都含的铁的氧化物。红砖的
成分是粘土(主要是硅酸盐),红色来自于三氧化二铁。其中的主要反应是焦炭和水在高温下反应生成一氧
化碳和氢气(又叫水煤气),两种气体都有还原性,在高温下降三价铁还原成二价得到氧化亚铁是黑色的—
是青砖。出窑前不加水则得到三价铁的氧化物是红棕色的—是红砖。。
一、铁的氧化物
活动一、探究铁的氧化物分类及物理性质
任务一、阅读教材P66-67页内容,思考铁的氧化物类型及物理性质是什么?并完成下表内容:
【答案要点】
名称 氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe O Fe O
2 3 3 4
俗名 — 铁红 磁性氧化铁铁的化合价 +2 +3 +2,+3
颜色、状态 黑色粉末 红棕色粉末 黑色晶体
溶解性 都不溶于水
任务二、问题探究:结合铁的氧化物的物理性质,思考烧制砖瓦时,向窑内添加大量的煤炭后封窑 1
天,从窑顶向下慢慢浇水7天的目的是什么?红砖和青砖两者颜色不同的原因是什么?
【答案要点】①烧制砖瓦时,从窑顶向下慢慢浇水的目的是水蒸气和窑内高温的炭发生化学反应产生
大量的还原气体(氢气和一氧化碳),它们把氧化铁又逐渐还原成为四氧化三铁,而制得青砖。
②两者颜色不同的原因是两者所含的铁的氧化物是不一样,红砖中含的是氧化铁,青砖中含的是四氧
化三铁。
【对应训练】1.下列说法正确的是( )
A.赤铁矿的主要成分是Fe O
3 4
B.Fe O 为碱性氧化物,可与水反应生成Fe(OH)
2 3 3
C.铁锈的主要成分是Fe O
2 3
D.Fe O 中铁元素有+2价和+3价,Fe O 是混合物
3 4 3 4
【答案】C
【解析】赤铁矿、铁锈的主要成分均是Fe O ,A错误,C正确;Fe O 为碱性氧化物,但不与水反
2 3 2 3
应,B错误;Fe O 为化合物,不是混合物,D错误。
3 4
2.“秦砖汉瓦”是我国传统建筑文化的一个缩影。同是由黏土烧制的砖瓦,有的是黑色的,有的却
是红色的,你猜测其中的原因可能是( )
A.土壤中含有铁粉、二氧化锰等
B.黑砖瓦是煅烧过程中附着了炭黑,红砖瓦则是添加了红色耐高温染料
C.土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu
D.土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色Fe O 或FeO和红色Fe O
3 4 2 3
【答案】D
【解析】黏土中含有铁元素,在烧制砖瓦时,与O 反应,生成氧化物,铁元素的氧化物有3种,FeO
2
与Fe O 为黑色,Fe O 为红棕色,故D项正确。
3 4 2 3
活动二、探究铁的氧化物的化学性质
任务一、铁元素可以形成三种氧化物,分别是氧化亚铁( FeO )、氧化铁(Fe O )和四氧化三铁
2 3
(Fe O)。分别从物质类别和元素价态两方面推测这三种氧化物的化学性质有什么异同?
3 4
【答案要点】①从分类的角度分析,三者都是金属氧化物,都能与酸反应。三者都难溶于水,不与水
反应。
②从价态的角度分析, FeO、 Fe O 既有氧化性又有还原性, Fe O 主要有氧化性。
3 4 2 3
任务二、阅读教材P57第三自然段,根据各类物质的通性和氧化还原反应规律,结合下表回答铁的氧
化物具有哪些主要化学性质?
, 【答案要点】FeO Fe O Fe O
2 3 3 4
铁的化合价 +2 +3 +2、+3
氧化物类别 碱性氧化物 碱性氧化物 不是碱性氧化物
与非氧化性酸反应 FeO+2H + =Fe2+ Fe O+6H + =2Fe3+ +3H O Fe O+8H + =2Fe3+ + Fe2+
2 3 2 3 4
+H O +4H O
2 2
与还原剂反应 FeO+CO\o(\s\up6(_ Fe O+3CO\o(\s\up6(____ 3Fe O+8Al=====9Fe+4Al O
2 3 3 4 2
____)Fe+CO _)2Fe+3CO
(H 、CO、Al等) 2 2 3
2
用途 用作红色油漆和涂料; 炼铁、电讯器材、烤蓝等
赤铁矿是炼铁原料
任务三、归纳总结铁的三种氧化物组成、性质各有何特点及主要用途有哪些?
【答案要点】①化合态铁的常见化合价只有+2价和+3价,Fe O 可以看成由FeO和Fe O 按物质的
3 4 2 3
量之比1∶1组合而成的复杂氧化物,通常也可写成FeO·Fe O 的形式。
2 3
②FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物。氧化铁常用作红色油漆和涂料,赤铁矿(主
2 3 3 4
要成分是Fe O)是炼铁原料。工业炼铁的反应原理:Fe O+3CO=====2Fe+3CO。
2 3 2 3 2
③Fe O 与盐酸反应可分别看作Fe O、FeO与盐酸反应,然后把两个反应式相加。
3 4 2 3
④FeO、Fe O 遇氧化性酸(如HNO)发生氧化还原反应,+2价的铁均被氧化成+3价。
3 4 3
【对应训练】1.下列关于铁的氧化物说法错误的是 ( )
A.铁的氧化物在通常状况下都是有色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.FeO在空气中加热生成Fe O
2 3
D.工业上常使用铁的氧化物作原料冶炼铁
【答案】C
【解析】铁的氧化物在通常状况下都是有色固体,如氧化铁是红棕色固体,氧化亚铁和四氧化三铁都
是黑色固体,故A正确;四氧化三铁是一种复杂的铁的氧化物,可看作是由 FeO、Fe O 组成的化合物,
2 3
它与盐酸反应后的溶液中同时存在Fe2+和Fe3+,B正确;FeO在空气中加热生成Fe O ,故C错误;工业
3 4
上常使用铁的氧化物作原料,用一氧化碳冶炼铁,故D正确。
2.关于铁的三种氧化物(FeO、Fe O、Fe O),下列叙述中正确的是( )
2 3 3 4
A.铁的三种氧化物中铁元素的化合价完全相同
B.都是碱性氧化物,都能与盐酸反应生成氯化铁和水
C.铁的三种氧化物在高温条件下都能被CO还原为Fe
D.四氧化三铁中铁元素有+2价和+3价,它是一种混合物
【答案】C
【解析】A.铁的三种氧化物(FeO、Fe O、Fe O)中Fe元素的化合价分别为+2,+2和+3,+3价,各
2 3 3 4
不相同,A错误;B.碱性氧化物与酸反应会生成相应的盐和水,FeO、Fe O、Fe O 分别与盐酸反应生成
2 3 3 4
的是亚铁盐、亚铁盐和铁盐、铁盐,Fe O 不属于碱性氧化物,B错误;C.CO具有还原性,可在高温条
3 4件下将铁的三种氧化物还原为Fe,C正确;D.四氧化三铁中铁元素有+2价和+3价,能写出化学式,所
以四氧化三铁为纯净物,不是混合物,D错误;故选C。
二、铁的氢氧化物
活动一、铁的氢氧化物性质、制备及转化
任务一、实验探究:完成教材P67【实验3-1】,补充实验:向FeCl 溶液中滴加NaOH溶液,描述实
3
验现象并分析可能的原因?
【答案要点】①氯化铁溶液中滴加氢氧化钠溶液有红褐色沉淀生成,该沉淀为氢氧化铁,方程式为:
Fe3+ + 3OH- = Fe(OH) ↓。
3
②向FeSO 溶液中滴加NaOH溶液,看到白色絮状沉淀迅速变灰绿色,最后变红褐色沉淀。(见PPT
4
图片)
③在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,因此现象是白色絮状沉淀迅速变成灰绿
2 3
色,最后变成红褐色,反应的化学方程式为:4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
任务二、归纳小结:铁的氢氧化物的制备方法、性质及转化有何规律?并完成下表内容。
【答案要点】
名称 氢氧化亚铁 氢氧化铁
化学式 Fe(OH) Fe(OH)
2 3
颜色、状态 白色固体 红褐色固体
水溶性 都不溶于水
与盐酸反应(离子
Fe(OH) +2H+===Fe2++2HO Fe(OH) +3H+===Fe3++3HO
2 2 3 2
方程式)
不稳定,受热易分解:
稳定性 在空气中不稳定,易被氧化
2Fe(OH) =====Fe O+3HO
3 2 3 2
制备方法
Fe2++2OH-===Fe(OH) ↓ Fe3++3OH-===Fe(OH) ↓
2 3
(离子方程式)
方程式:4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
转化 现象:Fe(OH) 转化成Fe(OH) 的特殊现象是白色沉淀迅速变成灰绿色,
2 3
最终变成红褐色。
【对应训练】1.下列说法中,不正确的是( )
A.FeCl 溶液和FeCl 溶液都是黄色的
3 2
B.Fe(OH) 是白色的,Fe(OH) 是红褐色的
2 3
C.FeO、 Fe O 都能与盐酸反应
2 3
D.FeCl 溶液、FeCl 溶液都能与NaOH溶液反应
3 2
【答案】A
【解析】A.FeCl 溶液是黄色的,FeCl 溶液是浅绿色的,A项错误;B.Fe(OH) 是白色的,Fe(OH)
3 2 2 3
是红褐色的,B项正确;C.FeO、 Fe O 都是金属氧化物,金属氧化物一般都能与盐酸反应,C项正确;
2 3D.FeCl 溶液、FeCl 溶液与NaOH溶液反应分别生成氢氧化铁沉淀和氢氧化亚铁沉淀,故FeCl 溶液、
3 2 3
FeCl 溶液都能与NaOH溶液反应,D项正确;答案选A。
2
2.将一定量铁粉溶解于足量稀硫酸中,然后向溶液中滴加足量NaOH溶液,充分反应后过滤将滤渣
在空气中加热至1000℃完全反应,最终得到的固体的成分为( )
A.FeO B.Fe(OH) C.Fe O D.Fe(OH)
2 2 3 3
【答案】C
【解析】将一定量铁粉溶解于足量稀硫酸中发生反应:Fe+H SO =FeSO+H ↑,然后向溶液中滴加足量
2 4 4 2
NaOH溶液,发生反应:FeSO +2NaOH=Fe(OH) ↓+Na SO ,4Fe(OH) +O +2H O=4Fe(OH) ,充分反应后过
4 2 2 4 2 2 2 3
滤将滤渣在空气中加热至1000℃完全反应,反应为:2Fe(OH) \o(\s\up6(_____)Fe O+3H O,最终得到的固体
3 2 3 2
成分为Fe O;
2 3
故选C。
活动二、探究Fe(OH) 的制备方法
2
任务一、结合教材P689页“思考与讨论”:由实验3-1可知,白色的Fe(OH) 会被溶解在溶液中的氧
2
气氧化。那么,在实验室里,如何得到Fe(OH) 呢?
2
【答案要点】 Fe(OH) 会被溶解在溶液中的氧气氧化,因此实验室中得到 Fe(OH) 的关键是防止氧气
2 2
的干扰。其中包括溶液中的氧气的干扰与空气中的氧气的干扰。制备Fe(OH) 时应注意:
2
①Fe2+必须是新制的,并放入铁粉,以防Fe2+被氧化成Fe3+;
②为了防止Fe2+被氧化,配制FeSO 溶液的蒸馏水和NaOH溶液要煮沸,尽可能除去O。
4 2
③为了防止滴加NaOH溶液时带入空气,可将吸有NaOH溶液的长滴管伸入FeSO 溶液的液面下,再
4
挤出NaOH溶液。
④为防止Fe2+被氧化,还可以向盛有FeSO 溶液的试管中加入少量的煤油或其他密度小于水而不溶于
4
水的有机物、排除装置中的空气等,以隔绝空气。
任务二、方法探究:下图为实验方案改进,请讨论图①的防氧化原理。图②的防氧化原理和图①类
似,如何操作才能达到目的?用图③装置能制备氢氧化亚铁吗?若能,该如何操作?【答案要点】①图①铁粉和硫酸反应得到H,装置充满了H,生成的Fe(OH) 没有与O 接触。
2 2 2 2
②图②打开止水夹a,检验试管B出口处排出的氢气的纯度。当排出的H 纯净时,夹紧止水夹a。
2
③ 能。具体操作:注射器A吸入NaOH溶液后用硅胶塞封口,再用注射器B将FeSO 溶液缓慢推入注射
4
器A中,使两溶液混合反应。
任务三、归纳小结:Fe(OH) 和Fe(OH) 性质的比较,填写下表内容:
2 3
化学式 Fe(OH) Fe(OH)
2 3
物质类别 二元弱碱 三元弱碱
色态 白色固体 红褐色固体
溶解性 难溶于水 难溶于水
与非氧化性
Fe(OH) +2H+=== Fe2++2HO Fe(OH) +3H+===Fe3++3HO
2 2 3 2
强酸反应
与氧化性酸 3Fe(OH) +10HNO(稀) ===
2 3
同上
反应 3Fe(NO )+NO↑+8HO
3 3 2
不稳定性 在空气中分解产物很复杂 2Fe(OH) =====Fe O+3HO
3 2 3 2
【对应训练】1.实验室可用图装置制备Fe(OH) 。下列说法不正确的是( )
2
A.配制NaOH溶液和FeSO 溶液的蒸馏水要提前煮沸
4
B.实验前可在FeSO 溶液上面加一层煤油
4
C.得到的Fe(OH) 为红褐色固体
2
D.实验结束后的胶头滴管,要先用盐酸浸泡,再用水洗
【答案】C
【解析】如图,利用NaOH溶液与FeSO 溶液反应得到Fe(OH) 和NaSO ,Fe(OH) 易被空气氧化。A
4 2 2 4 2
项,FeSO 和Fe(OH) 中铁元素呈+2,易被氧化,故配制NaOH溶液和FeSO 溶液的蒸馏水要提前煮沸,
4 2 4
除去水中溶解的氧气,正确;B项,实验前可在FeSO 溶液上面加一层煤油,浮在水面上,可隔绝空气,
4
正确;C项,得到的Fe(OH) 为白色固体,错误;D项,实验结束后的胶头滴管含碱性溶液,要先用盐酸
2
浸泡,再用水洗,正确。
2.关于甲、乙、丙、丁四套装置的说法正确的是( )A.用装置甲制取氯气
B.用装置乙除去氢气中的少量氯化氢
C.用丙装置可以较长时间看到白色Fe(OH) 白色沉淀
2
D.用丁装置证明碳酸氢钠受热易分解
【答案】C
【解析】A.MnO 与浓盐酸混合制取Cl 需要在加热条件下进行,装置中缺少加热装置,因此不能用
2 2
于制取Cl,A项错误;B.HCl溶于水产生盐酸,盐酸与NaHCO 发生产生CO 气体,导致Cl 中含有新杂
2 3 2 2
质CO 气体,不能达到目的,B项错误;C.试管中Fe与HSO 反应产生FeSO 和H,产生的H 将试管
2 2 4 4 2 2
A、B及导气管中空气排出,待其中没有空气后,关闭阀门a,反应产生的H 又将A中新制取的FeSO 压
2 4
入B试管中,发生反应:FeSO +2NaOH=Fe(OH) ↓+Na SO ,由于处于H 的惰性环境,产生的Fe(OH) 不会
4 2 2 4 2 2
被氧化,因此可以较长时间观察到Fe(OH) 白色沉淀,C项正确;D.固体加热时为防止产生的水蒸气冷凝
2
回流,试管口应该略向下倾斜,D项错误;答案选C。
【课后巩固】1.下列有关物质的性质与用途不具有对应关系的是( )
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.聚合硫酸铁能水解并形成胶体,可用于净水
C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
【答案】D
【解析】A.铁粉能与O 反应,因此铁粉可用作食品保存的吸氧剂,物质的性质与用途具有对应关
2
系,故A不符合题意;B.聚合硫酸铁能水解并形成胶体,胶体能吸附杂质,因此聚合硫酸铁可用于净
水,物质的性质与用途具有对应关系,故B不符合题意;C.FeCl 具有氧化性,氯化铁和铜反应生成氯化
3
铜和氯化亚铁,因此氯化铁可用于腐蚀印刷电路板上的Cu,物质的性质与用途具有对应关系,故C不符
合题意;D.纳米Fe O 能与酸反应生成氯化亚铁、氯化铁和水,纳米Fe O 可用作铁磁性材料,物质的性
3 4 3 4
质与用途不具有对应关系,故D符合题意。综上所述,答案为D。
2.《神农本草经》记载:“磁石,味辛寒,主周痹风湿,肢节中痛,不可持物,洗洗酸消,除大热
烦满及耳聋。”下列说法错误的是( )A.磁石的主要成分是碱性氧化物Fe O B.磁石呈黑色
3 4
C.磁石不溶于水 D.磁石可作药材使用
【答案】A
【解析】A.磁石的主要成分是Fe O,但不是碱性氧化物, 碱性氧化物是能和酸作用,只生成一种
3 4
盐和水的金属氧化物;而四氧化三铁虽可以和酸反应,但同时生成铁盐和亚铁盐两种盐,所以不是碱性氧
化物,A错误;B.磁石呈黑色,B正确;C.磁石的主要成分是Fe O,难溶于水,C正确;D.根据题意
3 4
可做药材,D正确;故选A。
3.下列有关铁及其化合物的说法中正确的是( )
A.Fe O 常用作油漆、涂料、油墨和橡胶的黑色颜料
2 3
B.铁与水蒸气在高温下的反应产物为Fe O 和H
2 3 2
C.铁的氧化物都难溶于水,且不与水反应
D.FeO不稳定,在空气中受热会迅速被氧化成Fe O
2 3
【答案】C
【解析】A.Fe O 俗称铁红,红棕色固体,常用作油漆、涂料、油墨和橡胶的红色颜料,故A错误;
2 3
B.铁与高温水蒸气反应产物为四氧化三铁,故B错误;C.铁有三种氧化物氧化亚铁、氧化铁、四氧化三
铁,均不溶于水,且不能与水反应,故C正确;D.FeO不稳定,在空气中受热转化成四氧化三铁,故D
错误;故选:C。
4.氧化还原反应广泛存在,下列变化中没有发生氧化还原反应的是( )
A.用焦炭将Fe O 冶炼成生铁
2 3
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化
C.用石灰浆粉刷墙壁
D.Fe(OH) 白色沉淀在空气中放置变成红褐色
2
【答案】C
【解析】A.用焦炭将Fe O,冶炼成生铁,反应为置换反应,C、Fe的化合价发生改变,为氧化还原
2 3
反应,A与题意不符;B.FeO是一种黑色粉末,不稳定,在空气中受热,变为四氧化三铁,为氧化还原
反应,B与题意不符;C.用石灰浆粉刷墙壁,为氢氧化钙与二氧化碳反应生成碳酸钙和水,各元素的化
合价未变,为非氧化还原反应, C符合题意;D.Fe(OH) 白色沉淀在空气中放置最终变成红褐色,原理
2
为:4Fe(OH) +O +2H O=4Fe(OH) ,涉及氧化还原反应,D与题意不符;故选C。
2 2 2 3
5.下列各图示中能较长时间观察到Fe(OH) 的是( )
2A.①②③ B.①②④ C.①②③④ D.②③④
【答案】B
【解析】①稀硫酸和铁粉生成H,氢气排除了装置中的空气,在滴加氢氧化钠溶液,可以观察到白色
2
沉淀;②稀硫酸和铁粉生成H,打开a止水夹,氢气排除了装置中的空气,过一段时间关闭a止水夹,A
2
中生成硫酸亚铁的试管压强增大,将硫酸亚铁压如B试管,可以观察到白色沉淀;③与空气直接接触,
Fe(OH) 迅速被空气氧化成灰绿色最终变成红褐色的Fe(OH) ,不能较长时间观察到Fe(OH) 白色沉淀;④
2 3 2
在硫酸亚铁溶液上面加苯液封,隔绝空气,能较长时间观察到Fe(OH) 白色沉淀;综上所述,①②④符合
2
题意;故选B。
6.某实验兴趣小组同学采用如图所示装置制备Fe(OH) ,下列说法错误的是( )
2
A.实验开始前,应检查装置气密性
B.气体a的主要成分为氢气
C.为了制备较纯的Fe(OH) ,应打开K,关闭K,将装置内的气体尽可能赶出去
2 1 2
D.盛装稀盐酸的仪器使用前要检查是否漏液
【答案】C
【解析】铁和稀盐酸反应生成氯化亚铁和氢气,开始实验时打开K ,产生的氢气将装置内空气排尽,
2
再关闭K ,利用压强差将氯化亚铁溶液压至氢氧化钠溶液中生成 Fe(OH) 沉淀;A项,由于Fe(OH) 易被
2 2 2
氧化,该实验关键是隔绝氧气,且铁和稀盐酸反应生成氢气,则实验开始前,应检查装置气密性,正确;
B项,铁和稀盐酸反应生成氯化亚铁和氢气,产生的氢气将装置内空气排尽,气体a的主要成分为氢气,
正确;C项,开始实验时打开K ,产生的氢气将装置内空气排尽,错误;D项,为方便控制反应进度,盛
2
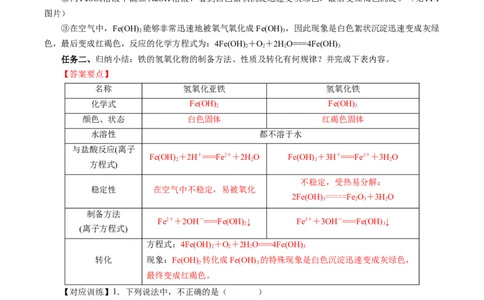
装稀盐酸的仪器分液漏斗使用前要检查是否漏液,正确。7.用废铁屑[主要成分为Fe和铁锈(Fe O),还含有C等难溶于酸的杂质]为原料制备Fe O 的一种实验
2 3 2 3
流程如下:
下列与流程相关的装置或操作正确且能达到实验目的的是( )
A.可在装置甲中进行“酸浸”操作
B.按图乙所示操作配制“酸浸”所需的3 mol·L-1 HSO 溶液
2 4
C.用装置丙过滤“酸浸”后所得悬浊液
D.用装置丁灼烧Fe(OH) 固体制Fe O
3 2 3
【答案】A
【解析】由题给流程可知,向废铁屑中加入稀硫酸酸浸、过滤得到含有Fe2+、Fe3+的滤液和含有碳的
滤渣;向滤液中加入氢氧化钠溶液,在空气中静置、过滤得到氢氧化铁;灼烧氢氧化铁得到氧化铁。A
项,由图可知,甲装置为固液不加热装置,可进行“酸浸”操作,正确;B项,配制“酸浸”所需的稀硫
酸溶液时,胶头滴管应在容量瓶的正上方,不能插入容量瓶中,错误;C项,过滤时,应用玻璃棒引流,
防止溶液溅出,错误;D项,灼烧氢氧化铁固体时,应在坩埚中进行,不能在烧杯中直接灼烧固体,错
误。
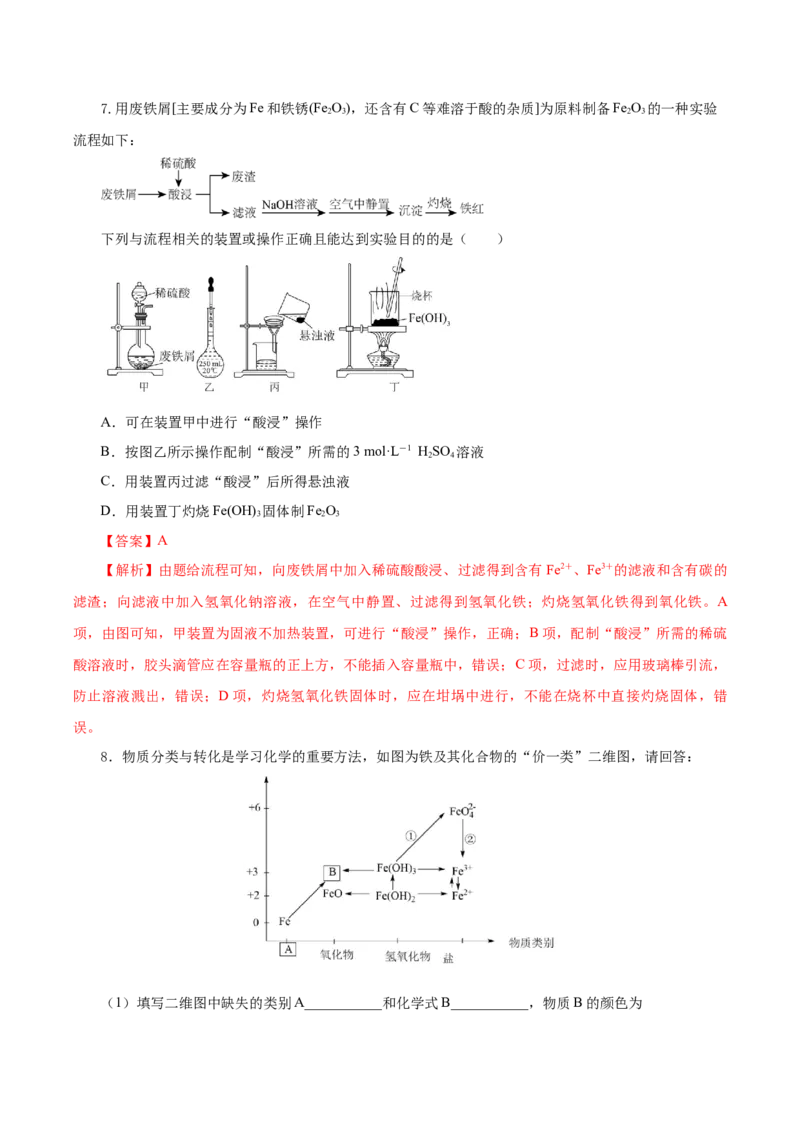
8.物质分类与转化是学习化学的重要方法,如图为铁及其化合物的“价一类”二维图,请回答:
(1)填写二维图中缺失的类别A___________和化学式B___________,物质B的颜色为___________。
(2)利用下述反应可实现转化①:2Fe(OH) +3ClO-+4OH-=2FeO2-+3Cl-+5HO,用单线桥法
3 4 2
标注电子转移情况______________________________________________________________,并指明氧化
剂:___________(填化学式)。
(3)结合二维图中信息推测在转化②中FeO2-表现的性质为_________(填“还原性”或“氧化
4
性”)。
(4)向FeCl 溶液试管底部加入NaOH溶液,放置一段时间后。观察到的实验现象为
2
___________________________________________________________________________________。
【答案】(1)单质 Fe O 红棕色
2 3
(2) ClO-
(3)氧化性
(4)有白色絮状沉淀生成,迅速变为灰绿色,最终变为红褐色沉淀
【解析】(1)根据二维图,Fe为单质,即A为单质,B为氧化物,且Fe元素为价态为+3价,即B
的化学式为Fe O;Fe O 为红棕色固体;(2)Fe(OH) 中Fe的化合价由+3价升高为+6价,ClO-中Cl的
2 3 2 3 3
价态由+1降低为-1价,用单线桥表示形式为 ;氧化
剂为ClO-;(3)转化②中Fe的化合价由+6价降低为+3价,高铁酸根离子表现氧化性;故答案为氧化
性;(4)FeCl 与NaOH溶液反应生成白色絮状沉淀Fe(OH) ,Fe(OH) 容易被氧化成Fe(OH) ,现象为:
2 2 2 3
有白色絮状沉淀生成,迅速变为灰绿色,最终变为红褐色沉淀。