文档内容
第三章 烃的衍生物
第二节 醇 酚
3.2.1 醇
1.了解醇的典型代表物——乙醇的结构及性质。
2.了解乙醇消去反应制乙烯实验和醇催化氧化和消去反应的条件。
教学重点:乙醇的结构特点和化学性质
教学难点:醇的结构和性质
任务一:认识醇
1.书写乙醇的分子式、结构式、结构简式、结构特点及官能团。
2.对下列物质进行分类,并总结醇、酚的定义
3. 饱和一元醇定义、通式
4. 醇的分类
5. 甲醇的物理性质、危害及应用
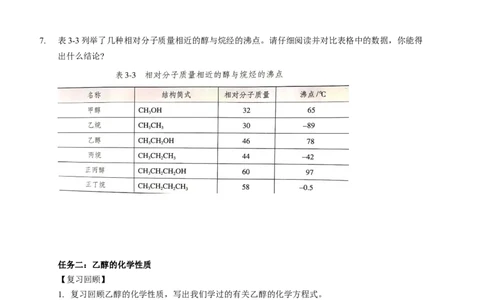
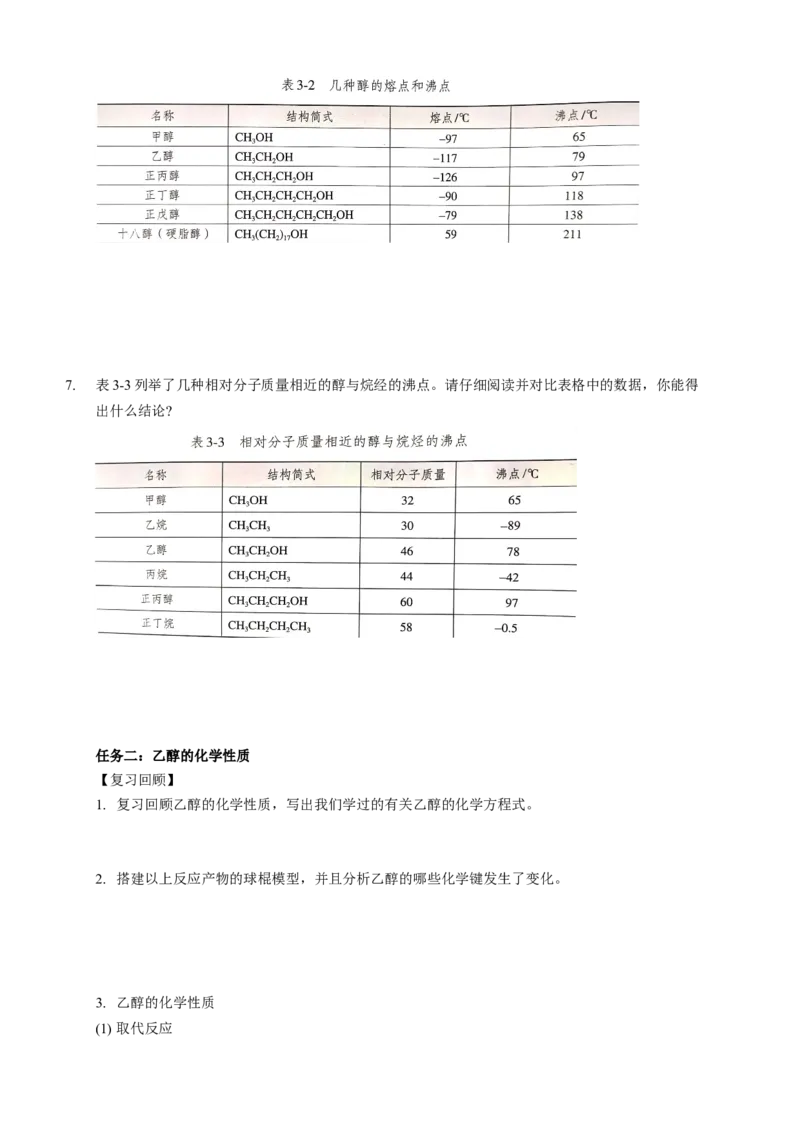
6. 以几种醇的熔点和沸点为例,同时结合烷烃的物理性质的变化规律,总结醇的物理性质。7. 表3-3列举了几种相对分子质量相近的醇与烷经的沸点。请仔细阅读并对比表格中的数据,你能得
出什么结论?
任务二:乙醇的化学性质
【复习回顾】
1. 复习回顾乙醇的化学性质,写出我们学过的有关乙醇的化学方程式。
2. 搭建以上反应产物的球棍模型,并且分析乙醇的哪些化学键发生了变化。
3. 乙醇的化学性质
(1) 取代反应①乙醇与浓氢溴酸混合加热后发生取代反应,生成溴乙烷,这是制备溴乙烷的方法之一。
化学方程式为:
②如果把乙醇和浓硫酸的混合物的温度控制在140℃左右,乙醇将以另一种方式脱水,即每两个乙
醇分子间会脱去一个水分子而生成乙醚。
化学方程式为:
乙醚是一种 、 的液体,沸点34.5℃,有 ,具有麻醉作用。乙
醚
溶于水, 溶于有机溶剂,它本身是一种优良溶剂,能溶解多种有机物。
③酯化反应
化学方程式为:
[知识拓展]
1. 醚的定义
2. 醚的官能团
3. 醚的表示
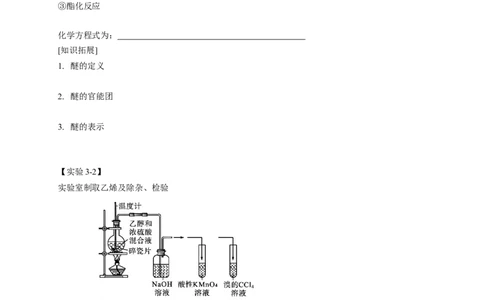
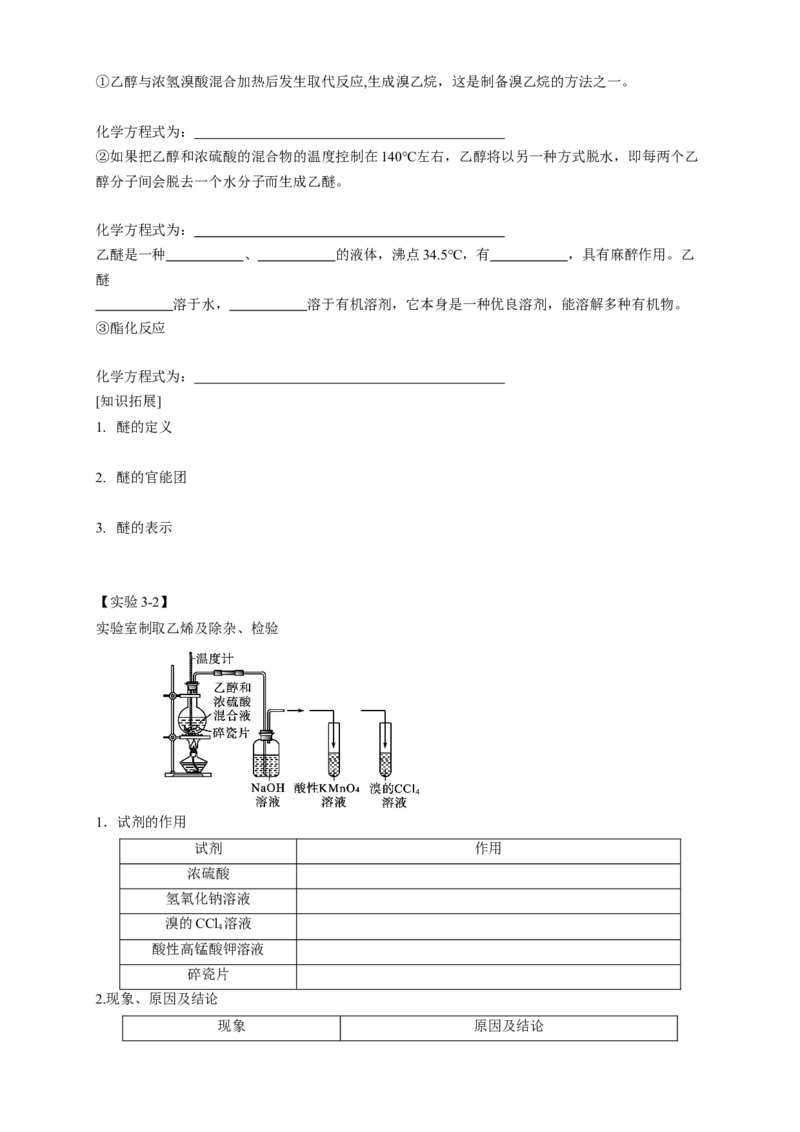
【实验3-2】
实验室制取乙烯及除杂、检验
1.试剂的作用
试剂 作用
浓硫酸
氢氧化钠溶液
溴的CCl 溶液
4
酸性高锰酸钾溶液
碎瓷片
2.现象、原因及结论
现象 原因及结论烧瓶中液体逐渐变黑
溴的CCl 溶液褪色
4
酸性高锰酸钾溶液褪色
[小结]
(2) 消去反应
乙醇在浓硫酸的作用下,加热到170 ℃时生成乙烯。
化学方程式为:
[思考与讨论]
(1)溴乙烷与乙醇都能发生消去反应,二者的反应有什么异同?
(2)请写出分子式为C HO的有机化合物的同分异构体的结构简式。
3 8
【实验3-3】
实验方案:
在试管中加入酸性重铬酸钾溶液,然后滴加乙醇,充分振荡,观察实验现象。
实验现象:
实验结论:
其氧化过程:
[小结]
(3) 氧化反应
氧化反应:有机化合物分子中 或 的反应
还原反应:有机化合物分子中 或 的反应
①乙醇的燃烧
化学方程式为:
②乙醇的催化氧化
化学方程式为:
③乙醇与酸性重铬酸钾溶液
氧化过程:
任务三:知识建构
乙醇知识建构【答案】
任务一:认识醇
1. 略
2. 醇:羟基与饱和碳原子相连的化合物称
酚:羟基与苯环直接相连而形成的化合物
3.饱和一元醇:由烷烃所衍生的一元醇,如甲醇、乙醇;
饱和一元醇的通式为C H OH。,
n 2n+1
4.分类
5.甲醇(CHOH)是无色、具有挥发性的液体,易溶于水,沸点为65℃。甲醇有毒,误服会损伤视
3
神经,甚至致人死亡。甲醇广泛应用于化工生产,也可作为车用燃料。乙二醇和丙三醇都是无色、
黏稠的液体,都易溶于水和乙醇,是重要的化工原料。
6.物理性质
(1)沸点
①饱和一元醇,随分子中碳原子个数的增加,醇的沸点升高。
②碳原子数相同时,羟基个数越多,醇的沸点越高。
(2)溶解性:甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例混溶。
(3)密度:醇的密度比水的密度小。
7.相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃的沸点。这是由于醇分子中羟基的氧
原子与另一醇分子羟基的氢原子间存在着氢键。甲醇、乙醇和丙醇均可与水互溶,这也是因为醇分
子与水分子之间形成了氢键。
任务二:乙醇的化学性质
【复习回顾】
1.(1)与活泼金属(如Na)发生反应,其反应方程式为2CHCHOH+2Na→2CH CHONa+H↑,
3 2 3 2 2
(2)(3)氧化反应
2.
3.(1)CHCHOH+HBr――→CHCHBr+HO。
3 2 3 2 2
C HOH+C HOH――→C HOC H+HO。
2 5 2 5 2 5 2 5 2
无色 易挥发 特殊气味 微 易
C HOH+C HOH――→C HOC H+HO。
2 5 2 5 2 5 2 5 2
[知识拓展]
1. 醚:由两个烃基通过一个氧原子连接起来的化合物
2. 醚的官能团:
3. 醚的结构可用R—O—R'来表示,R和R'都是烃基,可以相同,也可以不同。
【实验3-2】
实验室制取乙烯及除杂、检验
1.试剂的作用
试剂 作用
浓硫酸 催化剂和脱水剂
吸收二氧化硫和乙醇(都与酸性高锰酸钾溶液反应,SO 能与
2
氢氧化钠溶液
溴的CCl 溶液反应)
4
溴的CCl 溶液 验证乙烯的不饱和性
4
酸性高锰酸钾溶液 验证乙烯的还原性
碎瓷片 防止暴沸
2.现象、原因及结论
现象 原因及结论
烧瓶中液体逐渐变黑 浓硫酸与乙醇作用生成碳单质
溴的CCl 溶液褪色 乙烯与溴单质发生加成反应
4
酸性高锰酸钾溶液褪色 乙烯被酸性高锰酸钾氧化
[小结]
(2)CHCHOH CH CH↑+H O
3 2 2 2 2
[思考与讨论]
1.
CHCHCHBr CHCHCHOH
3 2 2 3 2 2
反应条件 NaOH乙醇溶液 加热 浓硫酸,加热至170 ℃1. 化学键断裂 C—Br C—H C—O C—H
2. 化学键生成 碳碳双键 碳碳双键
C 反应产物 CH CH NaBr HO CH CH HO
2 2 2 2 2 2
H
CHCHOH CHCH(CH)OH`
3 2 2 3 3
【实验3-3】
溶液由橙红色变为绿色
乙醇能被酸性重铬酸钾溶液氧化,
[小结]
(3) 失去氢原子 加入氧原子 加入氢原子 失去氧原子
任务三:乙醇知识建构
1. 新修改的 机动车驾驶证申领和使用规定 于2010年4月1日起实施,新规规定酒驾一次扣
12分,出此拳治理酒驾是因酒后驾车是引发交通事故的重要原因。如图所示为交警在对驾驶
员是否饮酒进行检测。其原理是:橙色的酸性 水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的 。下列对乙醇的描述与此测定原理有关的是
乙醇沸点低 乙醇密度比水小 乙醇具有还原性 乙醇是烃的含氧衍生物 乙醇可与羧
酸在浓硫酸的作用下发生取代反应
A. B. C. D.
【答案】C
【解析】
乙醇沸点低,易挥发,易被检测,与测定原理有关;
乙醇密度比水小,可与水以任意比混溶,与测定原理无关;
乙醇分子中含有羟基,具有还原性, 具有强氧化性,可以把乙醇迅速氧化自身生成蓝
绿色的 ,与测定原理有关;
乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关;
乙醇可与羧酸在浓硫酸的作用下发生取代反应,与测定原理无关;
对乙醇的描述与此测定原理有关的是 。
故选C。
2. 关于卤代烃与醇的说法不正确的是
A. 卤代烃与醇发生消去反应的条件不同
B. 既可以发生消去反应,又可以被氧气催化氧化
C. 不同的卤代烃通过消去反应可能会生成相同的烯烃
D. 可以发生消去反应,那么 也可以发生消去反应
【答案】B
【解析】
A.卤代烃在氢氧化钠的醇溶液中发生消去反应,醇发生消去反应是在浓硫酸作催化剂条件下,条件
不同,故A正确;B.发生消去反应生成烯烃,羟基所在碳上无氢原子,不能被氧气催化氧化,故B错误;
C.不同的卤代烃通过消去反应可能会生成相同的烯烃,故C正确;
D. ,与Br相连的C的邻位上有H原子,能发生消去反应,故D正确,
故选B。
3. 以下四种有机物:
其中既能发生消去反应又能发生催化氧化生成醛的是
A. 和 B. 只有 C. 和 D. 和
【答案】C
【解析】
醇类物质中能发生消去反应, 所连C的邻位C上应含有H原子;能发生催化氧化反应生成醛
类,应含有 的结构,以此解答该题。
可发生消去反应,可被氧化生成酮,故错误;
既能发生催化氧化生成丁醛,又能发生消去反应生成 丁烯,故正确;
既能发生催化氧化生成 甲基丙醛,又能发生消去反应生成 甲基丙烯,故正确;
,可发生消去反应,但不能发生催化氧化,故错误。
故选:C。4. 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
A. 和金属钠反应时断裂 键
B. 在加热和有铜催化下与 反应时断裂 和 键
C. 和乙酸反应制备乙酸乙酯时断裂 键
D. 在空气中完全燃烧时断裂 键
【答案】C
【解析】
A.乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,即 断裂,故A正确;
B.乙醇在铜催化下与 反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的碳氢键,
即 断裂,故B正确;
C.酯化反应时“酸脱羟基醇脱氢”,所以乙醇和乙酸反应制备乙酸乙酯时断裂 键,故C错误;
D.在空气中完全燃烧时生成二氧化碳和水,断裂 ,故D正确。
故选C。
5. 某二元醇的结构简式为 ,关于该有机物的说法错误的是
A. 用系统命名法命名: 甲基 , 庚二醇
B. 该有机物通过消去反应能得到6种不同结构的二烯烃
C. 该有机物可通过催化氧化得到醛类物质
D. 该有机物能与足量金属Na反应产生
【答案】C
【解析】
A.有机物的最长碳链有7个碳原子,2个羟基分别位于2号和5号碳原子上,甲基位于5号碳原子
上,系统命名法命名为: 甲基 , 庚二醇,故A正确;B. 左边羟基消去,形成3种不同位置的双键,右边羟基消去可形成2种不同位置
双键,故可得 种不同结构的二烯烃,故B正确;
C.只含 结构,该有机物中可通过催化氧化得到的是酮,而不是醛类物质,故C错误;
D. 该有机物含有2mol羟基,能与足量金属Na反应产生1mol氢气,标准状况下的体积为
,故D正确。
故选C。