文档内容
第五章 化学生产中的重要非金属元素
第一节 硫及其化合物
第一课时 硫和二氧化硫
【学习目标】1.从硫元素在周期表中的位置出发,通过分析硫原子的结构特点及问题探究,了解硫单
质在自然界的存在及物理性质和化学性质,培养宏观辨识与微观探析的化学核心素养。
2.通过实验探究、思考交流,从硫、二氧化硫的属类及硫元素化合价角度,了解二氧化硫的性质及主
要用途,,初步建立可逆反应的概念,体会性质决定用途的核心理念。
3.通过对比分析,结合真实情境中的应用实例和实验探究,理解SO 的酸性、漂白性及强还原性。知
2
道三氧化硫的物理性质及化学性质,并能正确书写相关化学方程式。
【学习重点】硫及二氧化硫的化学性质
【学习难点】二氧化硫性质的实验设计及原理探究
【课前预习】
旧知回顾:1.元素价态与物质氧化性、还原性有和关系?
【答案要点】同种元素不同价态的物质,处于最高价态时只具有氧化性;处于最低价态时只具有还原
性;处于中间价态时既有氧化性又有还原性。如:S2-具有还原性,S具有既有氧化性又有还原性,SO 具
2
有既有氧化性又有还原性,NaSO 具有既有氧化性又有还原性,SO 具有氧化性(填〝氧化性〞、〝还原
2 3 3
性〞)。
2.什么是酸性氧化物,请举例说明。
【答案要点】酸性氧化物是指能与碱反应,并且只生成盐和水的氧化物。酸性氧化物具有一些的通
性,如:CO+2NaOH+=H O+Na CO;CO+Ca(ClO) +HO= CaCO ↓+2HClO等。
2 2 2 3 2 2 2 3
新知预习:1.从化合价的角度看硫单质具有哪些化学性质?并举例说明。
【答案要点】①氧化性:如 S 与 Fe、Cu、H 反应的化学方程式依次为 Fe+S=====FeS、2Cu+
2
S=====Cu S、H+S=====HS等。
2 2 2
②还原性:如S与O 反应的化学方程式为S+O=====SO ,在空气中燃烧火焰为淡蓝色;与强氧化剂
2 2 2
反应(如浓硫酸)的化学方程式为S+2HSO (浓)=====3SO ↑+2HO。
2 4 2 2
③既体现S的氧化性又体现S的还原性:S与NaOH溶液反应的化学方程式为3S+6NaOH=====2NaS
2
+NaSO +3HO等。
2 3 2
2.硫的氧化物及主要性质分别是什么?
【答案要点】硫的氧化物有二氧化硫和三氧化硫两种,均为酸性氧化物。二氧化硫中硫元素为 +4
价,因此二氧化硫既具有氧化性,又具有还原性。
【课中探究】
情景导入:硫是重要的非金属元素,也是人类最早认识的化学元素之一,在元素周期表中硫元素位于
第三周期第ⅥA族。硫原子核外电子排布最外层电子数是 6,易得到2个电子形成8电子相对稳定结构,化学性质比较活泼。而淡黄色的硫单质及含硫化合物常常被炼丹家所使用,硫单质也是黑火药的主要成
分。硫及其化合物在现代生产和生活中仍发挥着重要的作用。自然界中游离态的硫一般存在于火山口附近
或岩层里。
一、硫单质的性质
活动一、硫原子的结构及硫单质的物理性质
任务一、根据硫元素在周期表中位置,思考硫原子的结构及化合价有何特点?与氯、氧元素相比有何
不同?
【答案要点】①硫位于元素周期表中的第三周期第ⅥA族,其原子结构示意图为 ,硫原子
最外层有6个电子,在化学反应中容易得到电子,形成-2价硫的化合物。
②硫元素的原子半径比氯原子半径大,硫原子得电子能力比氯原子弱,硫化氢的稳定性比氯化氢弱。
③硫元素的非金属性比氧元素弱,在富含氧气的地表附近的含硫化合物中,硫常显+4或+6价,氧为
-2价。
任务二、阅读教材P2页内容,观察图5-1或硫粉样品,思考硫单质具有哪些重要的物理性质性质?并
填写下表内容。
【答案要点】
溶解性
俗称 颜色状态 硬度
水 酒精 CS
2
硫黄 黄色晶体 质脆、易研成粉末 难溶 微溶 易溶
【注意】因硫单质难溶于水,微溶于酒精,易溶于二硫化碳,因此若试管内壁附着有单质硫时,可以
用CS 洗涤除去。
2
【对应训练】1.下列说法不正确的是( )
A.由于地壳的岩层里含硫及其化合物,因此火山喷出物中含有HS、SO 等硫的化合物
2 2
B.化石燃料直接燃烧会产生对大气有严重污染的SO 气体
2
C.硫在空气中燃烧的产物是SO ,在氧气中燃烧的产物是SO
2 3
D.硫是一种淡黄色晶体,不溶于水,微溶于酒精
【答案】C【解析】SO 转化成SO 的条件是催化剂、加热,而S在氧气中燃烧只能生成SO ,不具备SO 转化成
2 3 2 2
SO 的条件。
3
2.《天工开物》中篇·燔石中记载:“凡烧硫黄石,与煤矿石同形。……石精感受火神,化出黄光飞
走,遇盂掩住不能上飞,则化成汁液靠着盂底,其液流入弦袋之中,其弦又透小眼流入冷道灰槽小池,则
凝结而成硫黄矣。”下列说法错误的是
A.硫磺的化学式为HSO
2 4
B.硫元素全部以化合态存在于自然界中
C.硫难溶于水,微溶于酒精,易溶于二硫化碳中
D.描述制取硫的过程中涉及氧化还原反应、气化、液化、凝固
【答案】B
【解析】硫磺的化学式为S,A选项错误;B.硫元素既有单质存在于火山喷发口附近及地壳的岩层
中,又有化合态存在于自然界,B选项错误;C.硫难溶于水,微溶于酒精,易溶于二硫化碳中,C选项正
确;D.A.通过以上描述,由硫黄石加热,发生氧化还原反应得硫蒸气,冷凝为液态流入“弦袋之
中”,再凝固为固态,A选项正确;答案选B。
活动二、硫单质的化学性质
任务一、阅读教材P2页内容,结合硫原子的结构特点,思考硫单质具有哪些化学性质,有何规律和
用途?并写出有关化学反应方程式。
【答案要点】①硫是较活泼的非金属元素,能与许多金属、非金属发生反应(体现氧化性或还原
性)。
②在一定条件下可与金属Fe、Cu及H、O 等非金属单质反应:
2 2
Fe+S=====FeS(硫化亚铁),S是氧化剂(体现氧化性),Fe是还原剂;
2Cu+S=====Cu S(硫化亚铜),S是氧化剂(体现氧化性),Cu是还原剂;
2
H+S=====HS(硫化氢),S是氧化剂(体现氧化性),H 是还原剂;
2 2 2
S+O=====SO ,S是还原剂(体现还原性),O 是氧化剂。
2 2 2
注意:氯气在一定条件下于Fe、Cu反应,生成高价态的FeCl 、CuCl。
3 2
③规律:硫与变价金属反应时生成低价态的金属硫化物,而不是高价态。如Fe与S反应生成FeS而不
是Fe S,硫与氧气反应,不论氧气是否足量、浓度如何,其一步反应都只能生成SO ,不能生成SO 。
2 3 2 3
④用途:硫常用于制造硫酸、化肥、农药、火药、硫磺皂等,还可用于制造硫化橡胶(见 PPT图
片)。
任务二、拓展探究:硫单质既具有氧化性,又具有还原性,请尝试写出硫单质分别与浓硫酸、浓硝酸
及强碱(氢氧化钠溶液)反应的化学方程式。据此,你对实验室除去试管内壁附着的硫有哪些新认识?
【答案要点】①硫与浓HSO 反应:S+2HSO (浓)=====3SO ↑+2HO
2 4 2 4 2 2
②硫与浓HNO 反应:S+6HNO(浓)=====HSO +6NO ↑+2HO
3 3 2 4 2 2
③与强碱的反应3S+6NaOH=====2NaS+NaSO +3HO (用热碱溶液清洗硫)
2 2 3 2
④常用两种方法除去试管内壁附着的硫:a.物理法:常用CS 将硫单质与其他物质分离,也可用CS 洗去试管内壁上的硫单质。
2 2
b.化学法:加氢氧化钠溶液溶解。3S+6NaOH=====2NaS+NaSO +3HO,硫既表现氧化性,又表现
2 2 3 2
还原性。
【注意】向NaS和NaSO 的混合溶液中加入稀HSO :2NaS+NaSO +3HSO ===3S↓+3NaSO +
2 2 3 2 4 2 2 3 2 4 2 4
3HO。既S2-和SO在酸性条件不可以大量共存。
2
【对应训练】1.关于硫的叙述正确的是( )
A.硫的非金属性较强,在自然界中只以化合态存在
B.可用水溶解过滤分离硝酸钾和硫黄的混合物
C.硫与金属或非金属反应时都作氧化剂
D.硫的氧化性比氯气强
【答案】B
【解析】硫在自然界中的存在形式既有化合态又有游离态;硝酸钾易溶于水,硫黄不溶于水,用水溶
解过滤可分离二者的混合物;硫与金属、氢气等反应时作氧化剂,硫与氧气等反应时作还原剂;硫的氧化
性比氯气弱(硫与铁反应生成硫化亚铁,氯气与铁反应生成氯化铁)。
2.下列说法错误的是( )
A.残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去
2
B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
【答案】D
【解析】A.硫易溶于CS ,且能与热NaOH溶液反应生成可溶性的NaS和NaSO ,故A正确;B.
2 2 2 3
硫单质具有弱氧化性,硫单质与变价金属反应时一般生成低价态的金属硫化物,故 A正确;C.汞蒸气有
毒,汞和硫反应生成硫化汞,实验室里不慎洒落一些汞,可撒上硫粉进行处理,故 C正确;D.硫在氧气
中燃烧只生成SO ,故D错误;选D。
2
二、二氧化硫的性质及应用
活动一、二氧化硫的性质
任务一、阅读教材P2-3页内容,观察二氧化硫样品,并闻气味,完成教材P3页【实验5-1】,思考二
氧化硫具有哪些物理性质?
【答案要点】①物理性质:二氧化硫是无色、有刺激性气味的有毒气体,是大气污染物之一;易溶于
水,通常状况下,1体积水溶解约40体积SO 。
2
②实验探究:
实验 二氧化硫溶于水(P3【实验5-1】)实验装置
图5-2 二氧化硫溶于水
实验原理 SO +HO HSO
2 2 2 3
实验用品 二氧化硫、水、试管、橡胶塞、水槽
如图5-2所示,把充满SO 、塞有橡胶塞的试管倒立在水中,在水面下打开橡胶
2
塞,观察试管内液面的上升待液面高度不再明显变化时,在水下用橡胶塞塞紧试管
实验步骤 口,取出试管,用pH试纸测定试管中溶液的酸碱度(保留该溶液供实验5-2使用)
实验现象 试管内液面上升,pH试纸变红色
实验结论 SO 易溶于水
2
实验说明 1体积水可溶解40体积SO
2
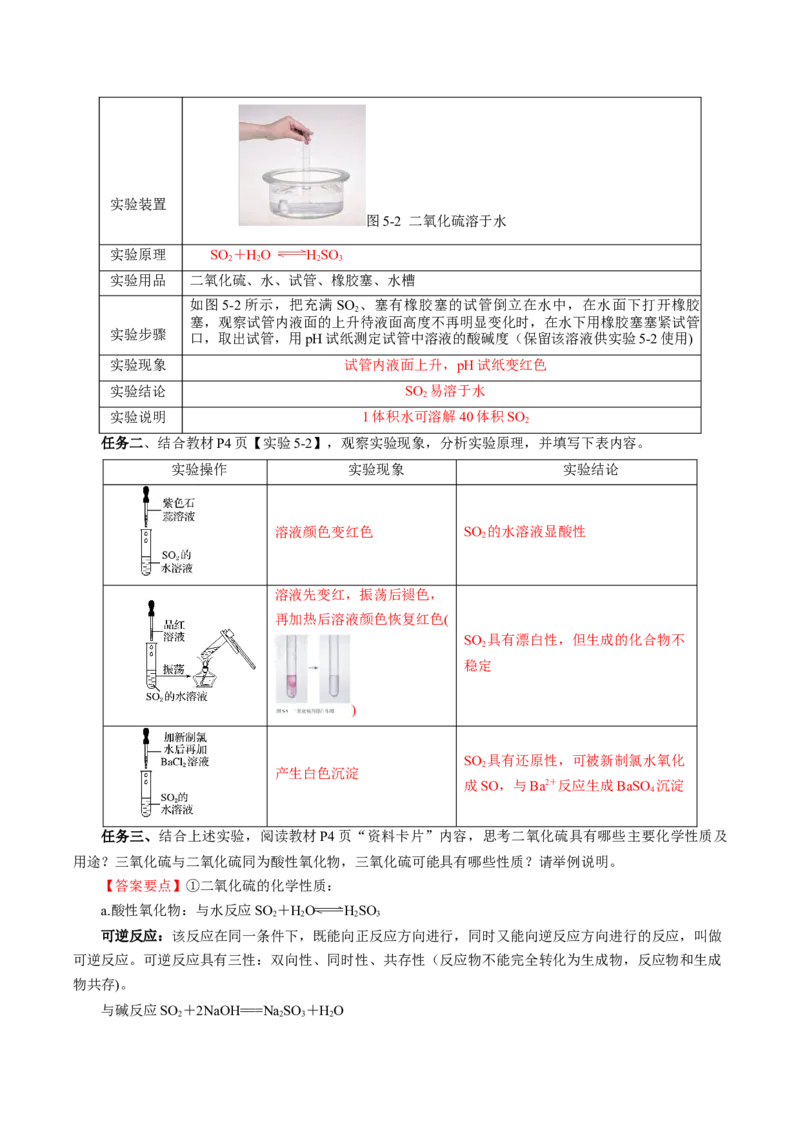
任务二、结合教材P4页【实验5-2】,观察实验现象,分析实验原理,并填写下表内容。
实验操作 实验现象 实验结论
溶液颜色变红色 SO 的水溶液显酸性
2
溶液先变红,振荡后褪色,
再加热后溶液颜色恢复红色(
SO 具有漂白性,但生成的化合物不
2
稳定
)
SO 具有还原性,可被新制氯水氧化
2
产生白色沉淀
成SO,与Ba2+反应生成BaSO 沉淀
4
任务三、结合上述实验,阅读教材P4页“资料卡片”内容,思考二氧化硫具有哪些主要化学性质及
用途?三氧化硫与二氧化硫同为酸性氧化物,三氧化硫可能具有哪些性质?请举例说明。
【答案要点】①二氧化硫的化学性质:
a.酸性氧化物:与水反应SO +HO HSO
2 2 2 3
可逆反应:该反应在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做
可逆反应。可逆反应具有三性:双向性、同时性、共存性(反应物不能完全转化为生成物,反应物和生成
物共存)。
与碱反应SO +2NaOH===Na SO +HO
2 2 3 2与碱性氧化物反应SO +CaO===CaSO
2 3
b.氧化性:SO 与HS发生归中反应。SO +2HS===3S+2HO
2 2 2 2 2
c.还原性:SO 在一定条件下与O 反应。2SO +O 2SO SO +HO===H SO
2 2 2 2 3 3 2 2 4
d.漂白性:二氧化硫具有漂白作用,工业上常用二氧化硫来漂白纸浆、毛、丝等。二氧化硫的漂白作
用是由于它能与某些有色物质结合而生成不稳定的无色物质。这些无色物质容易分解而使有色物质恢复原
来颜色。
此外,二氧化硫可用于杀菌消毒,还是一种食品添加剂。
②用途:漂白纸浆、毛、丝、草帽辫等;用于杀菌消毒。如在葡萄酒中添加适量(最大使用量
0.25g/L)的二氧化硫可以起到杀菌、抗氧化、保持葡萄酒的天然果香味等作用。
③三氧化硫的性质:
a.物理性质:标准状况下,SO 是一种无色固体,熔点(16.8℃)、沸点(44.8℃)较低,极易溶于水
3
生成硫酸。
b.化学性质:具有酸性氧化物的通性,与水剧烈反应生成硫酸:SO +HO===H SO ;三氧化硫通入氯
3 2 2 4
化钡溶液反应:SO +BaCl +HO===BaSO ↓+2HCl
3 2 2 4
【对应训练】1.下列说法中正确的是( )
A.三氧化硫极易溶于水,能与水反应生成硫酸
B.标准状况下,1 mol三氧化硫的体积为22.4 L
C.二氧化硫在空气中易被氧化为三氧化硫
D.三氧化硫具有漂白性,能使品红溶液褪色
【答案】A
【解析】标准状况下,三氧化硫为固态, 1 mol三氧化硫的体积不等于22.4 L;三氧化硫不具有漂白
性,不能使品红溶液褪色;在催化剂、加热的条件下,二氧化硫才能在空气中被氧化为三氧化硫。
2.下列各组两个反应互为可逆反应的是( )
①H+Cl=====2HCl与2HCl=====H↑+Cl↑
2 2 2 2
②H SO (浓)+2HBr===2H O+Br +SO ↑与Br +SO +2HO===2HBr+HSO
2 4 2 2 2 2 2 2 2 4
③2NO ===N O 与NO===2NO
2 2 4 2 4 2
催化剂 催化剂
④2SO
2
+O 2====△2SO
3
与2SO
3=====
△
==
2SO
2
+O
2
A.①② B.②③
C.③④ D.②④
【答案】C
【解析】可逆反应要求的是相同条件,①②呈现的反应条件不同,③④条件相同,故③④互为可逆反
应。
活动二、二氧化硫与氯气的漂白性比较及鉴别
任务一、讨论交流:根据表格内容,思考二氧化硫与氯气的漂白性有何不同?并完成表格内容。
【答案要点】
氯(气)水 SO
2HClO具有强氧化性,将有色物质氧化 SO 跟某些有色物质化合生成不稳定
漂白原理 2
成稳定的无色物质 的无色物质
反应类型 氧化还原反应 化合反应
特点 具有不可逆性,久置不恢复原色 具有可逆性,久置能恢复原色
仅适用于品红、有色的毛发、丝绸、
应用范围 适用于几乎所有的有机色质
纸浆、草帽辫等
①SO 的漂白原理与氯水不同,SO 漂白是SO 与某些有色物质生成不稳定的无
2 2 2
色物质。这些无色物质容易分解又使有色物质恢复原来的颜色。
②SO 虽具有漂白性,但不能漂白指示剂。因此将SO 通入紫色石蕊溶液中,溶
2 2
结论 液只会变红,不会褪色。
③氯气的漂白原理是氯气溶于水生成次氯酸具有强氧化性,将有色物质氧化成
无色物质而漂白,实质为氧化还原反应。加热时不能恢复到原来的颜色,这种
漂白效果是永久性的。
任务二、问题探究:结合下表信息,思考SO 和CO 的鉴别方法是什么?并完成表格内容。
2 2
【答案要点】①SO 和CO 都能使澄清石灰水变浑浊,若通入的气体过量,则沉淀都会消失,故不能
2 2
用澄清石灰水[或Ba(OH) ]鉴别SO 和CO。
2 2 2
②通常用以下方法鉴别SO 和CO。
2 2
试剂 操作 现象与结论
品红溶液褪色的是 SO ,不褪色的是
品红溶液 将气体分别通入品红溶液中 2
CO
2
酸性KMnO 将气体分别通入酸性KMnO 溶 KMnO 紫红色溶液褪色的是SO ,无变
4 4 4 2
溶液 液中 化的是CO
2
溴水(或氯水)褪色的是SO ,无变化的
溴水(或氯水) 将气体分别通入溴水(或氯水)中 2
是CO
2
产生黄色浑浊的是 SO ,无变化的是
氢硫酸 将气体分别通入氢硫酸溶液中 2
CO
2
③检验CO、SO 同时存在的实验设计流程
2 2
流程设计 检验SO ⇒除去SO ⇒ 检验SO 是否除尽⇒检验CO
2 2 2 2
选用试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清石灰水
4
实验现象 褪色 褪色 不褪色 变浑浊
【对应练习】1.为了除去CO 气体中的SO 气体,下列仪器和药品组合合理的是( )
2 2
仪器:①洗气瓶 ②干燥管
药品:③固态生石灰 ④苏打溶液 ⑤小苏打溶液
A.①⑤ B.②⑤
C.①③ D.①④
【答案】A
【解析】洗气瓶必须与液态试剂对应,干燥管必须与固态试剂对应。SO 既能与NaHCO 溶液反应,
2 3
又能与NaCO 溶液反应;CO 只能与NaCO 溶液反应,不能与NaHCO 溶液反应。
2 3 2 2 3 32.下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、KMnO (H+)、石蕊溶液褪色
2 4
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同
2 2 2
D.等物质的量的SO 和Cl 相遇在溶液中具有漂白能力
2 2
【答案】B
【解析】要正确解答本题,必须清楚常见漂白剂的漂白原理:Cl 、NaO 、HO 、O 等是因强氧化性
2 2 2 2 2 3
而具有漂白性;SO 是能和有机色质化合生成无色物质;活性炭是因吸附有机色质而漂白。SO 使溴水、酸
2 2
性KMnO 溶液褪色是因为SO 具有还原性,能使品红褪色是因其具有漂白性,SO 不能使指示剂褪色,A
4 2 2
选项错误;因为能使品红褪色的物质很多,不仅仅是 SO ,B选项正确;因为这些漂白剂的漂白原理不相
2
同,SO 漂白属于化合型,活性炭属于吸附型,漂白粉、NaO 属于氧化型,C选项错误;等物质的量的
2 2 2
SO 和Cl 相遇在溶液中反应生成HSO 和HCl,从而失去漂白能力,D选项错误。
2 2 2 4
【课后巩固】1.硫单质能与许多金属单质和非金属单质发生反应。下列说法正确的是( )
A.硫蒸气与红热的铁丝反应后,残留的硫可用二硫化碳洗涤
B.硫蒸气与红热的铜丝反应生成黑色的CuS固体
C.硫单质在化合反应中只体现氧化性
D.硫元素广泛存在于自然界中,火山口附近的环境中硫元素只以游离态形式存在
【答案】A
【解析】A.硫蒸气与红热的铁丝反应产生FeS,残留的硫易溶于CS,因此可用二硫化碳洗涤未反应
2
的硫单质,A正确;B.S单质氧化性比较弱,硫蒸气与红热的铜丝反应生成黑色的Cu S固体,B错误;
2
C.硫单质与氧气反应时,硫单质体现还原性;在与H 反应产生HS时表现氧化性,C错误;D.火山口
2 2
附近的环境中存在化合态的硫,D错误;故合理选项是A。
2.下列描述体现SO 酸性的是( )
2
A.SO 使品红溶液褪色 B.SO 使含有酚酞的氢氧化钠溶液褪色
2 2
C.SO 使酸性高锰酸钾溶液褪色 D.SO 与HS反应生成淡黄色沉淀
2 2 2
【答案】B
【解析】A.SO 有漂白性,使品红溶液褪色,A错误;B.SO 能与氢氧化钠溶液反应,使使含有酚
2 2
酞的氢氧化钠溶液褪色,体现SO 的酸性,B正确;C.酸性高锰酸钾有强氧化性,SO 使酸性高锰酸钾溶
2 2
液褪色,体现SO 的还原性,C错误;D.SO 与HS反应生成淡黄色沉淀,体现SO 的氧化性,D错误;
2 2 2 2
故选B。
3. 下列有关三氧化硫的说法中,正确的是( )
A.SO 极易溶于水,且与水反应生成HSO
3 2 4
B.SO 、SO 均具有漂白性,能使石蕊试液褪色
2 3C.SO 可与碱反应,但不与碱性氧化物反应
3
D.SO 与SO 一样是酸性氧化物,因此SO 可使品红溶液褪色
3 2 3
【答案】A
【解析】SO 不具有漂白性,SO 不能漂白指示剂,两者均可使石蕊试液变红色,故B、D错误;SO
3 2 3
既可与碱反应,也可与碱性氧化物反应。
4.依据下列实验,预测的实验现象正确的是( )
选项 实验内容 预测的实验现象或结论
A MgCl 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
2
B FeCl 溶液中滴加KSCN溶液 溶液变血红色
2
C 向某溶液中加入硝酸再滴加氯化钡溶液,有白色沉淀产生 则溶液中含有SO
D 酸性KMnO 溶液中通入SO 至过量 溶液紫红色褪去
4 2
【答案】D
【解析】A.向 MgCl2 溶液中滴加 NaOH 溶液至过量,二者反应产生白色难溶性碱 Mg(OH)2,
Mg(OH)2不溶于水,也不溶于过量NaOH,因此反应产生的白色沉淀不溶解,A错误;B.Fe2+与SCN-不
能反应产生红色物质,B错误;C.向某溶液中加入硝酸再滴加氯化钡溶液,有白色沉淀产生,由于HNO3
具有强氧化性,会将SO氧化产生SO,因此不能证明溶液中含有SO,C错误;D.酸性KMnO 溶液具有
4
强氧化性,会将具有还原性的SO2氧化产生硫酸,KMnO 被还原为无色Mn2+,因而溶液的紫红色会褪
4
去,D正确;故合理选项是D。
5.下列能说明硫的非金属性比氯弱的是( )
①氯气可溶于水,而硫难溶于水;
②硫最高价态+6,而氯最高价态为+7;
③铁与氯气化合生成FeCl ,铁与硫分化合生成FeS;
3
④H 与S化合需要加热至300℃以上,H 与氯气化合点燃即可反应。
2 2
A.①② B.①③ C.②④ D.③④
【答案】D
【解析】①元素的非金属性强弱与单质的溶解性无关,所以氯气可溶于水,而硫难溶于水不能说明硫
的非金属性比氯弱,故错误;②元素的非金属性与得失电子的难易有关,与得失电子数目的多少无关,所
以硫最高价态+6,而氯最高价态为+7不能说明硫的非金属性比氯弱,故错误;③铁与氯气化合生成氯化
铁,铁与硫分化合生成硫化亚铁说明氯气得到电子的能力强于硫,元素的非金属性强于硫元素,故正确;
④氢气与硫化合需要加热至300℃以上,氢气与氯气化合点燃即可反应说明氯气得到电子的能力强于硫,元素的非金属性强于硫元素,故正确;③④正确,故选D。
6.葡萄酒是以葡萄为原料酿造的一种果酒。此酒营养丰富,保健作用明显,它能调整新陈代谢的性能,
促进血液循环,防止胆固醇增加。如图是某品牌葡萄酒及说明书,我们可以看到“食品添加剂:二氧化
硫”。下列说法正确的是( )
A.SO 属于非法添加剂,不该添加到葡萄酒中
2
B.SO 具有还原性,少量的SO 可防止葡萄酒氧化变质
2 2
C.SO 具有还原性,不能用浓硫酸干燥
2
D.SO 可使溴水褪色,体现了它的漂白性
2
【答案】B
【解析】适量的SO 可防止葡萄酒被氧化,因此SO 可作为添加剂,A项错误,B项正确;SO 中S显
2 2 2
+4价,硫酸中的S为+6价,为相邻价态,不会发生氧化还原反应,C项错误;SO 能使溴水褪色,发生
2
的是氧化还原反应,体现了SO 的还原性,D项错误。
2
7.硫元素的几种化合物存在下列转化关系。下列说法正确的是( )
A.反应①中生成的 具有漂白性,可使溴水褪色
B.反应②中若 足量,就会生成
C.反应④中生成S既是氧化产物,也是还原产物
D.反应④中当转移 电子时,消耗 稀硫酸
【答案】B
【解析】A.Cu 与浓 HSO 加热反应生成 CuSO 、SO 和 HO,SO 使溴水褪色发生反应
2 4 4 2 2 2
SO +Br +2H O=HSO +2HBr,该反应中SO 被氧化,表现还原性,不是漂白性,A项错误;B.少量SO
2 2 2 2 4 2 2
与NaOH溶液反应生成NaSO ,足量SO 与NaOH溶液反应可生成NaHSO,B项正确;C.反应④中反应
2 3 2 3
为NaSO+H SO =Na SO +S↓+SO ↑+H O,S元素的化合价由NaSO 中+2价降至S中0价,生成的S是还
2 2 3 2 4 2 4 2 2 2 2 3
原产物,由NaSO 中+2价升至SO 中+4价,SO 是氧化产物,C项错误;D.反应④中消耗1molH SO 转
2 2 3 2 2 2 4
移2mol电子,D项错误;答案选B。
8.下图是实验室制取SO 并验证SO 的某些性质的装置,试回答:
2 2(1)在⑥中发生反应的化学方程式 : _______________________________。
(2)①中的实验现象为石蕊试液__________,此实验证明SO 是__________气体。
2
(3)②中的品红溶液________,证明SO 有________性。
2
(4)③中的实验现象是______________,证明SO 有________性。
2
(5)④中的实验现象是______________,证明SO 有________性。
2
(6)⑤的作用是__________,反应的化学方程式为__________________________。
【答案】 (1)Na SO +HSO (浓)===Na SO +HO+SO ↑
2 3 2 4 2 4 2 2
(2)变红 酸性 (3)褪色 漂白
(4)有淡黄色沉淀生成 氧化
(5)KMnO 溶液褪色 还原 (6)吸收SO ,防止SO 污染环境 SO +2NaOH===Na SO +HO
4 2 2 2 2 3 2
【解析】本题考查的是SO 制取和性质检验,SO 是酸性氧化物,具有酸性氧化物的通性,还具有漂
2 2
白性、氧化性和还原性。