文档内容
优秀领先 飞翔梦
想
2018年贵州省毕节市中考模拟卷(五)
化学
注意事项:
1.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置。
2.答题时,卷Ⅰ必须使用2B铅笔,卷Ⅱ必须使用0.5毫米黑色签字笔。将答案书写在答题卡
规定的位置,字体工整、笔迹清楚。
3.所有题目必须在答题卡上作答,在试卷上答题无效。
4.本试卷共4页,满分60分,考试时间50分钟。
5.考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量 H:1 C:12 O:16 Cl:35.5 Ca:40
卷Ⅰ
一、选择题(共8小题,每小题3分,
共24分。每小题只有一个选项
符合题意)
1.下列成语或典故中,涉及化学变化的是( C )
A.春风得意 B.掬水月在手 C.火上浇油 D.草木皆兵
2.化学实验操作直接影响实验结果和人身安全,下列关于实验操作的说法正确的是( D )
A.用10 mL量筒量取8.55 mL水
[来源:学科网ZXXK]
B.称量固体药品时,左盘放砝码,右盘放物体
C.稀释浓硫酸时,将水沿烧杯内壁注入盛有浓硫酸的烧杯中,并用玻璃棒搅拌
D.点燃可燃性气体前必须检验纯度
3.下列物质的分类中不正确的是( B )
A.单质:硅、水银、金刚石 B.碱:氢氧化钡、氢氧化钠、乙醇
C.盐:硝酸银、氯化铁、高锰酸钾 D.氧化物:氧化镁、三氧化硫、五氧化二磷
4.下列关于人体营养与健康的说法,不正确的是( D )
A.鱼类、豆类食物富含蛋白质 B.糖类是人体生命活动最主要的能量来源
C.人体内的脂肪是维持生命活动的备用能源 D.人体需要的维生素可在人体内合成
5.如图是五种粒子的结构示意图,下列说法错误的是( B )
A.图中粒子共能表示四种元素 B.图中表示阴离子的是c、e
C.图中b粒子的化学符号为Mg2+ D.图中d粒子在化学反应中易失去电子
6.下列设计的实验方案中(括号中为方法或试剂),你认为可行的是( B )
A.验证铁、铜、银的金属活动性顺序(硫酸亚铁溶液、硝酸铜溶液、银丝)
B.鉴别固体:氢氧化钠、氯化钠、硝酸铵(水)
C.除去二氧化碳中混有的少量一氧化碳(点燃)
D.分离氧化钙中混有的碳酸钙粉末(加水溶解,过滤)
www.youyi100.com
第 1 页 共 6 页优秀领先 飞翔梦
想
7.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列叙述错误的是( B )
A.t ℃时, 将等质量的甲、
1
乙分别配成饱和溶液,所得溶液质量:甲>乙
B.将t ℃时甲、丙的饱和溶液升温到t ℃,两种溶液中溶质的质量分数相等
1 2
C.将t ℃时甲的饱和溶液变为t ℃时甲的饱和溶液,可以采用蒸发溶剂的方法
2 3
D.将t ℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙
3
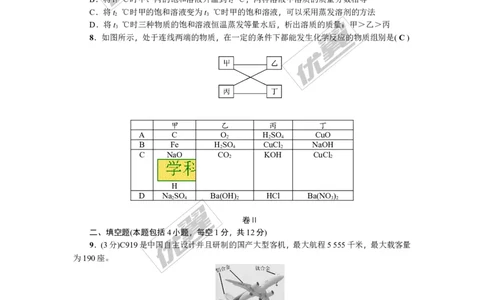
8.如图所示,处于连线两端的物质,在一定的条件下都能发生化学反应的物质组别是( C )
甲 乙 丙 丁
A C O HSO CuO
2 2 4
B Fe HSO CuCl NaOH
2 4 2
C NaO CO KOH CuCl
2 2
H
D NaSO Ba(OH) HCl Ba(NO)
2 4 2 3 2
卷Ⅱ
二、填空题(本题包括4小题,每空1分,共12分)
9.(3分)C919是中国自主设计并且研制的国产大型客机,最大航程5 555千米,最大载客量
为190座。
(1)图中标示的材料中,属于有机合成材料的是__合成橡胶__。
(2)飞机机身大量使用铝合金。铝合金具有的优点有:密度小、抗腐蚀性强,硬度比纯铝__大__。
(3)钛(Ti)和钛合金被认为是21世纪重要的金属材料。以金红石(主要成分是TiO)为原料生产
2
钛的步 骤有:①在高温下,向
金红石与焦炭的混合物中通入Cl,得到TiCl 和一种可燃性气体;②在稀有气体环境和加热条件
2 4
www.youyi100.com
第 2 页 共 6 页优秀领先 飞翔梦
想
下,用Mg和TiCl 反应得到Ti和MgCl。其中步骤①中的化学方程式为__TiO + 2C +
4 2 2
2Cl ===== TiCl + 2CO __。
2 4
10.(2分)化学源于生活,
生活中蕴含着许多化学知识。
(1)大枣含有蛋白质、糖类及维生素等营养素,其中起到调节人体新陈代谢、预防疾病作用的
是__维生素__。
(2)青少年处于生长发育期,为预防患佝偻病,可以多吃奶制品、虾皮等食物,补充人体需要的
__钙__元素。
11.(4分)水是生命之源,也是工农业生产不可缺少的物质。合理利用和保护水资源是我们义
不容辞的责任。
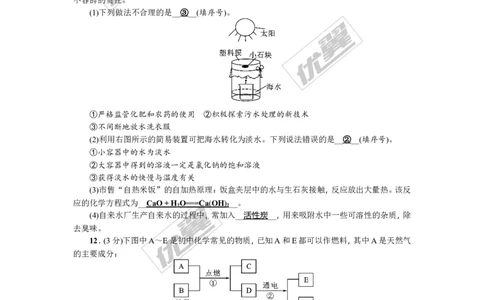
(1)下列做法不合理的是__③__(填序号)。
①严格监管化肥和农药的使用 ②积极探索污水处理的新技术
③不间断地放水洗衣服
(2)利用右图所示的简易装置可把海水转化为淡水。下列说法错误的是__②__(填序号)。
①小容器中的水为淡水
②大容器中得到的溶液一定是氯化钠的饱和溶液
③获得淡水的快慢与温度有关
(3)市售“自热米饭”的自加热原理:饭盒夹层中的水与生石灰接触,反应放出大量热。该反
应的化学方程式为__ CaO + H O == =Ca ( OH ) __。
2 2
(4)自来水厂生产自来水的过程中,常加入__活性炭__,用来吸附水中一些可溶性的杂质,除
去臭味。
12.(3分)下图中A~E是初中化学常见的物质,已知A和E都可以作燃料,其中A是天然气
的主要成分:
[来源:学科网ZXXK]
(1)反应①的化学方程式为__CH + 2O ===== CO + 2H O__。
4 2 2 2
(2)反应②中的产物B通常用__带火星的木条__检验。
(3)E物质作燃料的优点是__ 产物是水 , 无污染 ( 或 热值高 ) __(答一条即可)。
三、实验题(本题包括2小题,每空1分,共16分)
13.(8分)下图是实验室制取常见气体及检验相关性质的装置图,据图回答问题。
www.youyi100.com
第 3 页 共 6 页优秀领先 飞翔梦
想
(1)指出②、④装置中标号仪器的名称:X__分液漏斗__,Y__集气瓶__。
(2)用过氧化氢溶液与二氧化锰混合制取氧气时,需要选用的发生装置是__②__(填装置序号,
下同),收集装置是__ ④ 或 ⑤ __,反应的化学方程
式为__2HO ===== 2H O +
2 2 2
O↑__。
2
(3)二氧化碳的收集装置可选用__⑤__,二氧化碳的检验装置可选用__⑥__。
(4)实验室常用加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体。要制取并收集甲烷(密
度比空气小,难溶于水),可选用的发生、收集装置依次是__ ①③ ( 或 ①④ )__。
14.(8分)已知将CO 通入澄清石灰水中,溶液变浑浊;继续通CO 气体,溶液由浑浊又变澄
2 2
清,反应的化学方程式为CaCO+HO+CO===Ca(HCO)。某化学兴趣小组由此欲探究CO 与
3 2 2 3 2 2
NaOH溶液反应后的溶质组成。
【提出问题】CO 与NaOH溶液反应后的溶质由哪些物质组成?
2
【查阅资料】
①NaHCO+NaO
3
H===NaCO+HO
2 3 2
②盐酸滴入碳酸钠溶液中,实际反应分两步进行:
第一步反应:NaCO+HCl===NaCl+NaHCO
2 3 3
第二步反应:NaHCO+HCl===NaCl+HO+CO↑
3 2 2
【提出猜想】
猜想1:溶质为NaCO
2 3
猜想2:溶 质为NaHCO
3
猜想3:溶质为__NaCO 、 NaHCO __(填化学式,下同)
2 3 3
猜想4:溶质为__ NaOH 、 Na CO____
2 3 [来源:学#科#网Z#X#X#K]
【实验方案】
Ⅰ.甲组同学为确定CO 与NaOH溶液反应后所得溶液中溶质组成,设计如下实验方案。
2
(1)向所得溶液中加入足量的CaCl 溶液,若有白色沉淀生成,过滤后向滤液中加入足量的稀
2
盐酸,无气泡产生,则溶质为__NaCO 或
2 3
NaOH 和 Na C
2
O__。
3
www.youyi100.com
第 4 页 共 6 页优秀领先 飞翔梦
想
(2)向所得溶液中加入足量的CaCl 溶液,若无白色沉淀生成,向溶液中加入足量的稀盐酸,
2
有气泡产生,则溶质为__NaHC
O__。
3
(3)向所得溶液中加入足量的CaCl 溶液,若有白色沉淀生成,过滤后向滤液中加入足量的稀
2
盐酸,有气泡产生,则溶质为__NaCO 和 NaHCO __。
2 3 3
Ⅱ.乙组同学根据甲组同学的猜想,通过定量分析绘制出向所得溶液中逐滴加入稀盐酸的质
量与生成二氧化碳的质量关系示意图,请根据图象确定溶质成分。
A.NaCO B.__NaHCO__ C.__ NaOH 、 Na CO__ D.__NaCO、
2 3 3 2 3 2 3
NaHCO__
3
四、计算题(本题包括2小题,共8分)
15.(2分)农业生产上通常用溶质质量分数为10%~20%的食盐溶液来选种。
(1)现要配制200 kg溶质质量分数为20%
的食盐溶液,需要取用固体食
盐__40__kg。
(2)用60 kg溶质质量分数为
20%的食盐溶液,可稀释成
12%的食盐溶 液__100__kg。
解:(1)配制200 kg溶质质量分数为20%的食盐溶液,需要NaCl的质量为200 kg×20%=40
kg;
(2)设可稀释成12%的食盐溶液的质量为x。
60 kg×20%=x×12% x=100 kg
可稀释成12%的食盐溶液100 kg。
[来源:学科网]
16.(6分)某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石
样品20 g,把80 g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧
化硅等杂质不溶于水,不与稀盐酸反应)。根据实验数据计算:
实验次数 加入稀盐酸的质量/g 剩余固体的质
量/g
1 20 15
2 20 10
[来源:学&科&网Z&X&X&K]
3 20 6.8
4 20 n
(1)表中n的数值为__6.8__。
(2)样品中碳酸钙的质量分数是__66%__。
www.youyi100.com
第 5 页 共 6 页优秀领先 飞翔梦
想
(3)求盐酸中溶质的质量分数。
解:(1)由试题分析可知,20 g稀盐酸恰好能与石灰石中的5 g碳酸钙完全反应。第3次加入盐
酸后,固体质量减少不足5 g,说明碳酸钙已耗尽,故第4次实验中,不再反应,剩余固体质量仍为
6.8 g。
(2)样品中碳酸钙的质量分数:(20 g-6.8 g)÷20 g×100%=66%。
(3)设盐酸溶液中溶质的质量分数为x。
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 73
5 g 20 g×x
=
x=18.25%
答:盐酸溶液中溶质的质量分数为18.25%。
www.youyi100.com
第 6 页 共 6 页