文档内容
优秀领先 飞翔梦
想
2018年贵州省毕节市中考模拟卷(四)
化学
注意事项:
1.答题前,务 必将自己的
姓名、准考证号填写在答题卡规定的位置。
2.答题时,卷Ⅰ必须使用2B铅笔,卷Ⅱ必须使用0.5毫米黑色签字笔。将答案书写在答题卡
规定的位置,字体工整、笔迹清楚。
3.所有题目必须在答题卡上作答,在试卷上答题无效。
4.本试卷共4页,满分60分,考试时间50分钟。
5.考试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量 H:1 C:12 N:14 O:16 Na:23
卷Ⅰ
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.下列诗句中,只涉及物理变化的是( A )
A.只要功夫深,铁杵磨成针 B.爆竹声中一岁除,春风送暖入屠苏
C.千锤万凿出深山,烈火焚烧若等闲 D.春蚕到死丝方尽,蜡炬成灰泪始干
2.实验室的药品 和仪器
需要分类摆放,以下是四个药品橱柜存放的药品。实验室购进一瓶硫酸铜,应存放于( C )
3.下表是 几种作物适宜
生长的pH范围:
作物 马铃薯 茶树 水稻 莲
pH 4.8~5.5 5.0~5.5 6.0~7.0 8.0~9.0
某地土壤呈碱性,则该地适宜种植的作物是( D )
A.马铃薯 B.茶树 C.水稻 D.莲
4.有关粗盐提纯的实验操作合理的是( B )
A.溶解前用玻璃棒研磨大颗粒粗盐 B.过滤时液体的液面要低于滤纸边缘
C.加热蒸发时要不断搅拌直至水分全部蒸干 D.实验结束随即用手将蒸发皿从三脚架上取
下
[来源:Z|xx|k.Com]
5.国家卫计委发布 《中国
居民膳食指南(2016)》,倡导健康安全的生活理念,下列说法不合理的是( C )
www.youyi100.com
第 1 页 共 5 页优秀领先 飞翔梦
想
A.奶制品中含钙丰富,是日常饮食中钙的来源之一
B.食物合理搭配,以保证各种营养素的均衡摄入
C.硒、碘等微量元素在人体中的含量很少,对维持正常生命活动作用不大
D.糖类和油脂在人体内经氧化释放能量,提供机体活动和维持恒定体温的需
要
6.下列对现象解释合理的是( B )
A.铝具有良好的抗腐蚀性能,是因为它的化学性质很活泼
B.水墨画可长时间保存不变色是因为碳的化学性质在常温下不活泼
C.氢氧化钠需要密封保存是因为它会与空气中的氧气反应
D.“酒香不怕巷子深”是因为分子间有间隔
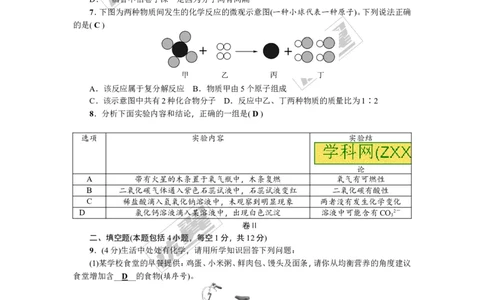
7.下图为两种物质间发生的化学反应的微观示意图(一种小球代表一种原子)。下列说法正确
的是( C )
A.该反应属于复分解反应 B.物质甲由5个原子组成
C.该示意图中共有2种化合物分子 D.反应中乙、丁两种物质的质量比为1∶2
8.分析下面实验内容和结论,正确的一组是( D )
选项 实验内容 实验结
论
A 带有火星的木条置于氧气瓶中,木条复燃 氧气有可燃性
B 二氧化碳气体通入紫色石蕊试液中,石蕊试液变红 二氧化碳有酸性
C 稀盐酸滴入氢氧化钠溶液中,未观察到明显现象 两者没有发生化学变化
D 氯化钙溶液滴入某溶液中,出现白色沉淀 溶液中可能含有CO2-
[来源:学科网ZXXK] 3
卷Ⅱ
二、填空题(本题包括4小题,每空1分,共12分)
9.(4分)生活中处处有化学,请用所学知识回答下列问题:
(1)某学校食堂的早餐提供:鸡蛋、小米粥、鲜肉包、馒头及面条,请你从均衡营养的角度建议
食堂增加含__D__的食物(填序号)。
A.蛋白质 B.油脂
C.糖类 D.维生素
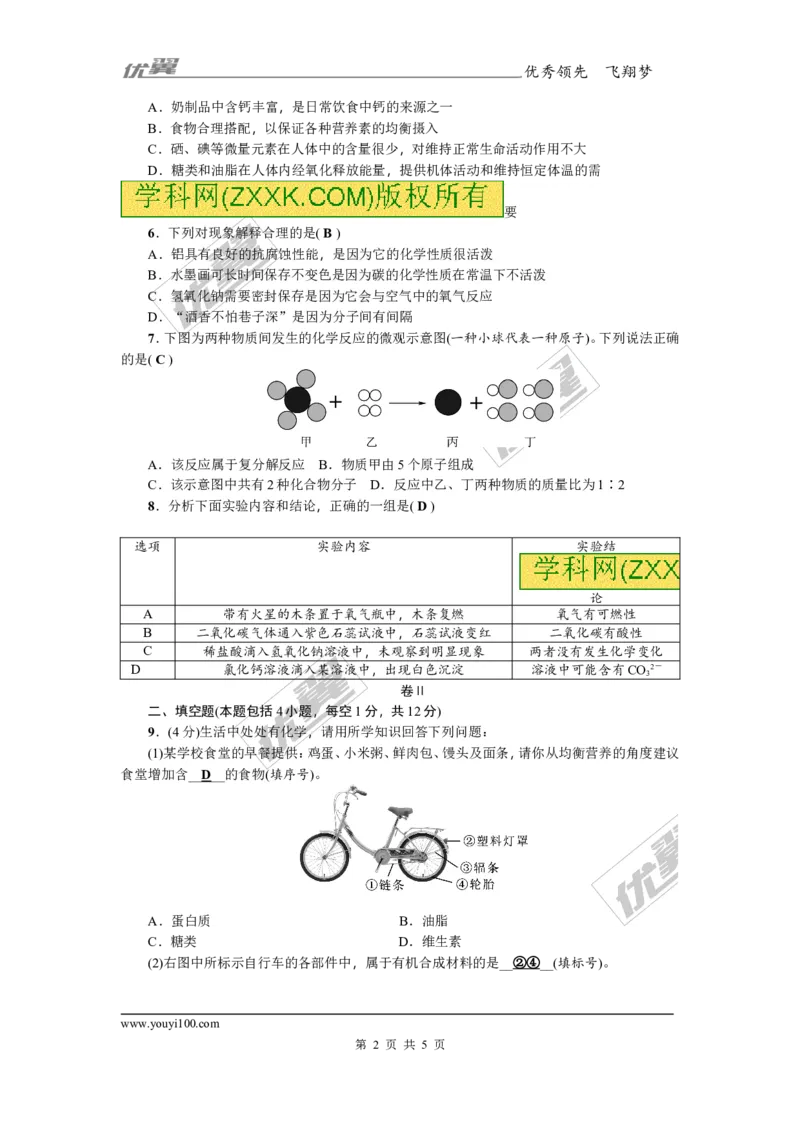
(2)右图中所标示自行车的各部件中,属于有机合成材料的是__②④__(填标号)。
www.youyi100.com
第 2 页 共 5 页优秀领先 飞翔梦
想
(3)甲醛(CHOH)有毒,误饮可使眼睛失明,甚至令人死亡,最新研究证明,用氨气(NH)处理
3 3
含有甲醛的工业废水,可使其转变成无毒的物质,有关反应的化学方程式为5CHOH+12O+
3 2
6NH=====3X+5CO+19HO,则X的化学式为__N__。
3 2 2 2
(4)丙烷(CH)是家用液化石油气的主要成分之一,它和甲烷在空气中燃烧的生成物相同,请
3 8
写出丙烷燃烧的化学方程式:__CH + 5O ===== 3CO + 4H O__。
3 8 2 2 2
10.(3分) 有一包白
色粉末,可能含有Ba(NO)、
3 2
NaSO、NaCO、NaNO 中的一种或几种,为了确定其组成,实验小组设计并进行如表实验:
2 4 2 3 3
实验步骤 实验操作 实验现象
步骤1 取样品加入足 有白色沉淀产生
量水,充分振荡,静置
步骤2 过滤后,往滤渣中加入过量的稀盐酸 沉淀全部溶解,并有气体产生
(1)实验中产生的气体是__二氧化碳
__。
(2)通过探究,该白色粉末中一定含有__ Ba ( NO ) 、 Na CO__,一定不含__NaSO__。
3 2 2 3 2 4
11.(3分)根据右图中a、b、c三种固体的溶解度曲线,回答问题。
(1)M点的意义是__ 温度为 t _ ℃ 时 , a 和 c 的溶解度相等 __。
2
(2)温度为t ℃时,a、b、c三种物质的溶解度从大到小的顺序是__a>b>c__。
1
(3)将t ℃时a、b、c三种物质的饱和溶液降温到t1℃时,三种溶液中溶质的质量分数由大到
3
小的顺序为__b>c>a__。
12.(2分)1774年,英国科学家普里斯特利进行了如图实验,取一根一端封闭的玻璃管,在玻
璃管的底部装入红色固体氧化汞,再装满汞(水银),将其倒扣在盛有汞的烧杯中,通过凸透镜将阳
光汇聚到氧化汞上,对其加热,使其发生化学反应,化学方程式为2HgO=====2Hg+O↑。
2
(1)氧化汞(HgO)中汞元素的化合价为__ + 2 __。
www.youyi100.com
第 3 页 共 5 页优秀领先 飞翔梦
想
(2)写出该实验的现象:__ 红色固体消失 ( 减少 ) 、管内液面下降 __(列举一点)。
三、实验题(本题包括2小题,每空1分,共16分)
13.(7分)结合有关性质探究的实验图,回答有关化学反应现象和实质的问题。
图一 图二 图三
(1)如图一,王亮同学将集气瓶中的二氧化碳缓缓倒入烧杯中,可观察到的现象是__两支蜡烛
自下而上依次熄灭__,该现象说明二氧化碳的性质有:①__ 不能燃烧 , 不支持燃烧 __;②__密度比
空气大__。
(2)如图二,将收集到的二氧化碳通过澄清石灰水中的现象为__澄清石灰水变浑浊__,该反应
发生的化学方程式为:__CO + Ca ( OH ) == =CaCO ↓ + H O__。
2 2 3 2
(3)如图三,对比两支试管内液面高低的不同,__能__(填“能
”或“不能”)说明二氧化碳
可溶于水,写出氢氧化钠与二氧化碳反应的化学方程式:__CO + 2NaOH == =Na CO + H O__。
2 2 3 2
14.(9分)实验室有失去标签的四瓶无色溶液,分别为Ca(OH)、NaCO、稀盐酸、NaCl溶液中
2 2 3
的一种,为鉴别它们,现将这四瓶无色溶液分别标号为A、B、C、D,某校化学兴趣小组的同学邀你
一同参与:
【提出问题】A、B、C、D分别是什么溶液?
【实验药品】失去标签的四瓶溶液和无色酚酞试液。
【实验仪器】试管、胶头滴管、烧杯等。
【收集证据】
实验操作 实验现象 实验结论
(1)分别取A、B、C、D溶液少量 A、B混合产生大量气泡,C、D A、B分别是__盐酸和碳酸钠__
于试管中,两两混合 混合无明显现象 溶液中的一种,A与B反应的
化学方程式为__NaCO+
2 3
2HCl == =2NaCl + H O +
2
CO↑__,C、D分别是__氢氧
2
化钙和氯化钠__溶液中的一种
[来
源:学|科|网]
(2)各取A、B、C、D溶液于四支 A、D变红,B、C无明显现象 A为__碳酸钠__溶液;C为__
试管中,分别滴加两滴无色酚 氯化钠__溶液;D为__氢氧化
酞试液,振荡 钙__溶液
【反思与体会】鉴别物质的关键是利用物质的特征性质。
【继续探究】将实验操作(2)实验后的四支试管中的溶液,倒入一洁净的烧杯中,充分反应静置
后发现,烧杯底部有白色沉淀,上层清液为无色。则上层清液中一定含有的溶质是__氯化钠__(指
示剂除外),可能含有的溶质是__氯化钙__。为验证可能含有的溶质是否存在,应补充实验的化学
方程式为__CaCl + Na CO == =CaCO ↓ + 2NaC l__。
2 2 3 3
四、计算题(本题包括2小题,共8分)
15.(2分)尿素[CO(NH)]是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物
2 2
质,长期施用没有不良影响。计算:
www.youyi100.com
第 4 页 共 5 页优秀领先 飞翔梦
想
(1)CO(NH) 中共含有__4__种元素。
2 2
(2)若CO(NH) 中含有6 g氮元素,则该CO(NH) 的质量为__12.9_g__(精确到0.1 g)。
2 2 2 2
解:(1)CO(NH) 中共含有C、O、N、H等4种元素。
2 2 [来源:学§科§网Z§X§X§K]
(2)尿素中N的质量分数为=,含6 g氮元素,则该尿素的质量为6 g÷≈12.9 g。
16.(6分)如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO 含量的过程如下:
3
取10粒该药剂研碎后放入烧杯中,加入50 g水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=
7时(已知药品中的其他成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗
稀盐酸11.5 g。称得反应后烧杯内物质的总质量为64.3 g。请计算:
[来源:Z#xx#k.Com]
(1)反应完成后生成气体的质量为__2.2__ g。
(2)反应后烧杯中溶液的质量和胃药中NaHCO 的质量分数。
3
解:(1)每粒0.5 g,10粒该药剂的质量为
0.5 g×10=5 g。由质量守恒定
律,生成二氧化碳气体的质量为5 g+50 g+11.5 g-64.3 g=2.2 g。
(2)设参加反应的碳酸氢钠的质量为x。
NaHCO+HCl===NaCl+HO+CO↑
3 2 2
84 44
x 2.2 g
= x=4.2 g
反应后烧杯中溶液的质量为4.2 g+50 g+11.5 g-2.2 g=63.5 g。
胃药中NaHCO 的质量分数为×100%=84%。
3
答:(1)生成气体2.2 g;(2)反应后烧杯中溶液的质量为63.5 g;胃药中NaHCO 的质量分数为
3
84%。
www.youyi100.com
第 5 页 共 5 页