文档内容
课题:二氧化碳和一氧化碳(第二课时)
一、学习目标:
1.记住CO的性质和重要用途.
2.知道CO使人中毒的原因及防护措施。
【课前预习】
1.CO有什么样的颜色和气味?
2.根据生活经验和已学知识你知道CO有哪些性质和用途?
【情境导入】
2010年12月15日新华社消息:“赣州一家六口煤气中毒身亡,最小死者仅两个月”,煤气的主要成分是什
么,为什么使人中毒呢?
二、自主探究:
知识点二:一氧化碳
【阅读】自学课本P 和P ,思考并回答以下问题:
121 122
1.CO有什么样的颜色和气味?有人用炉火取暖,为了防止煤气中毒,在炉火上放一盆水行吗?
2.CO燃烧放出热量并产生 色火焰,说明CO具有 _性,它是煤气的主要成份。
反应的化学方程式
3.CO为什么能使人毒?怎样防止煤气中毒?
【讨论】
1.为什么家用煤气中掺入具有难闻气味的气体?如果发生煤气泄漏应当怎么办?
2.煤炉中常发生哪些化学反应?请写出反应的化学方程式(参见书P 图6-22)。在燃烧很旺的煤炉中
118
最不可能发生哪个反应?
⑴ ;⑵ ;
⑶ ;⑷ 。
3.向一盆燃烧旺盛的炭火中洒少量的水,火焰更旺且为蓝色;但洒入较多的水,炭火熄灭,为什么?
■实验发现碳在高温下可以跟水反应生成一氧化碳和氢气,此反应吸收热量。化学方程式
。
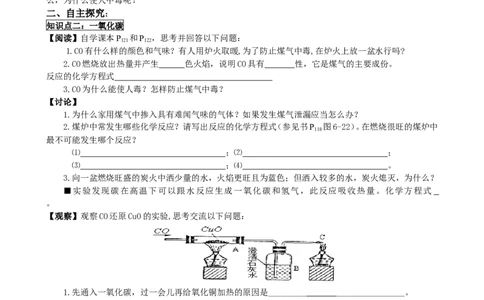
【观察】观察CO还原CuO的实验,思考交流以下问题:
1.先通入一氧化碳,过一会儿再给氧化铜加热的原因是_________ ________________。
2.根据实验事实填写下表:
观察到的现象 所发生现象的化学方程式
A处(CuO处)
B处(石灰水中)
C处
3.C处为什么要放一个点燃的酒精灯?
【归纳小结】
二,一氧化碳
1.碳的氧化物有 种,分别是 ,因CO 分子比CO分子多一个 ,所以二者性质有很大的
2
__________。
12.CO的性质:
⑴物性: 色 气味的气体, 溶于水,密度比空气略小,一般用 法收集。
⑵化性:
①可燃性:纯净的 CO 在空气在中点燃时,能产生 火焰,放出大量的热,化学方程式为:
。
②还原性:CO还原CuO反应的化学方程式为: 。
(_____的氧化铜逐渐变成光亮_____色,石灰水__ __)
③剧毒性:CO极易与血液中的 结合,从而使 ,造成生物体缺氧,甚至危及生命。
3.CO的用途:因CO具有可燃性,可以用作 ;CO具有还原性,可用于 。
【课堂小结】通过本节课的学习,你收获了什么?
【我的收获】
三、自我测评(1-5为必做, 6为选做,7为思考)
1.将充满下列气体的试管,分别倒立于槽中,试管内水位上升最高的是( )
A. H B. CH C. CO D. CO
2 4 2
2.下列做法存在安全隐患的是 ( )
A.在煤炉上放一壶水防止煤气中毒 B.在应用泡沫灭火器时,应先检查出气孔是否被堵塞
C.进入久未开启的菜窖前应先做灯火实验 D.点燃CO气体前,应先检验其纯度
3.要除去一氧化碳中的少量二氧化碳,可采用的最好措施为( )
A.点火燃烧 B.通过灼热的氧化铜粉末 C.通入石灰水中 D.通入石蕊试液中
4.区别CO、CO、O 三种气体,最简便的方法是( )
2 2
A.用带火星的木条 B.用燃着的木条 C.用澄清石灰水 D.用灼热的氧化铜
5.香烟燃烧产生的烟气中含有许多强致癌物和有害物质,其中对人体危害最大的物质除尼古丁和煤焦油外,
还有一种易与血红蛋白结合的有毒气体,该气体是( )
A.二氧化硫 B.一氧化碳 C.二氧化碳 D.氮气
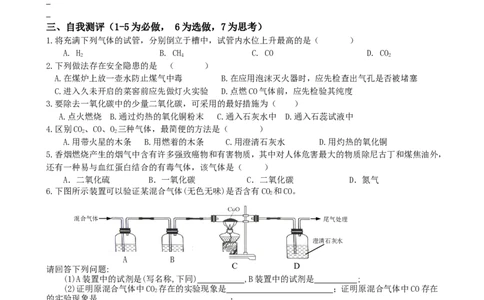
6.下图所示装置可以验证某混合气体(无色无味)是否含有CO 和CO。
2
混合气体 尾气处理
澄清石灰水
A B
A B C D
请回答下列问题:
(1)A装置中的试剂是(写名称,下同) ,B装置中的试剂是 ;
(2)证明原混合气体中CO 存在的实验现象是 ;证明原混合气体中CO存在
2
的实验现象是 ;
(3)如果没有B装置,对实验结果有何影响?
。
7.碳和部分碳的化合物间转化关系如图5所示。
(1)物质X的化学式为 。(2)在物质的分类中,
CO属于 物。
(3)从图中任选一种物质,它的一种用途
。
(4)写出图中转化关系中属于化合反应的一个化学方程式 。
【作业布置】P123练习与运用
2