文档内容
夯实双基
1.用一块废旧的铁丝石棉网,将铁丝望剪成几小片,用稀盐酸除去铁锈,放入锥形瓶中。如图,再向锥形瓶中
加入3~4mL饱和食盐水润湿铁丝,塞紧带导管的单孔塞,导管的一端伸入红色的水中,一段时间后,可
观察到的现象是( )
A.铁丝片生锈 B.红水上升到玻璃管中
[来源:学&科&网]
C.铁丝片生锈且红水上升到玻璃管中 D.铁丝片消失且红水上升到玻璃管中
【答案】C
2.“捕捉”空气有很多方法,某同学模仿教材中的“捕捉”实验。你认为他的哪个实验“捕捉”的空气与地
表附近所存在的空气成分相差较大( )
[来源:学&科&网][来源:学科网ZXXK]
A.用打气筒向气球充气,气球膨胀
B.将一个空量筒倒立于装满水的水缸中,用力往下压,量筒中留有气体
C.用口对气球呼气,气球膨胀 D.将一空玻璃瓶置于室内,盖上瓶盖
【答案】C
【解析】打气筒压缩的空气、量筒中存在的气体和空玻璃瓶中存放的气体,都是地表附近的空气。而口中呼出
的气体中,含有较多的水蒸气和二氧化碳气体,与空气的成分差别很大。学科*网
3.将燃着的木条分别放入如下图所示的两个集气瓶中,出现的现象是( )。
A.a熄灭,b更旺 B.a更旺,b熄灭
C.a、b都变旺 D.a、b都熄灭
【答案】B
【解析】 氧气支持燃烧,会使木条燃烧更旺;二氧化碳不支持燃烧,会使木条熄灭。学&科*网
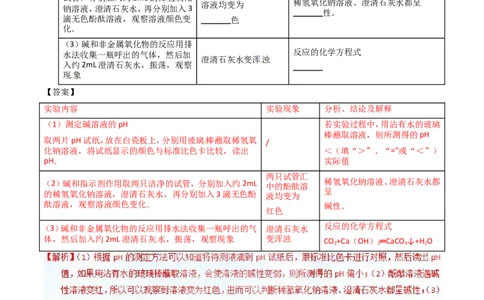
14.【2016年广东省南宁市】填写实验报告.
实验内容 实验现象 分析、结论及解释
(1)测定碱溶液的pH
若实验过程中,用沾有水的玻璃棒蘸取
取两片pH试纸,放在白瓷板上,分 溶液,则所测得的pH
别用玻璃棒蘸取稀氢氧化钠溶液, /
将试纸显示的颜色与
_______(填“>”、“=”或“<”)实
际值
_______比较,读出pH.
(2)碱和指示剂作用取两只洁净的
两只试管汇中的酚酞
试管,分别加入约2mL的稀氢氧化
溶液均变为 稀氢氧化钠溶液、澄清石灰水都呈
钠溶液,澄清石灰水,再分别加入3
_______性.
滴无色酚酞溶液,观察溶液颜色变 _______色
化.
(3)碱和非金属氧化物的反应用排
反应的化学方程式
水法收集一瓶呼出的气体,然后加
澄清石灰水变浑浊
入约2mL澄清石灰水,振荡,观察
_______
现象
【答案】
实验内容 实验现象 分析、结论及解释
(1)测定碱溶液的pH 若实验过程中,用沾有水的玻璃
棒蘸取溶液,则所测得的pH
取两片pH试纸,放在白瓷板上,分别用玻璃棒蘸取稀氢氧
/
化钠溶液,将试纸显示的颜色与标准比色卡比较,读出 <(填“>”、“=”或“<”)
pH. 实际值
两只试管汇
(2)碱和指示剂作用取两只洁净的试管,分别加入约2mL 稀氢氧化钠溶液、澄清石灰水都
中的酚酞溶
呈
的稀氢氧化钠溶液,澄清石灰水,再分别加入3滴无色酚 液均变为
酞溶液,观察溶液颜色变化. 碱性.
红色
(3)碱和非金属氧化物的反应用排水法收集一瓶呼出的气 澄清石灰水 反应的化学方程式
体,然后加入约2mL澄清石灰水,振荡,观察现象 变浑浊 CO +Ca(OH)═CaCO ↓+H O
2 2 3 2
5.【2016年海南省】 实验室有一瓶敞口放置的过氧化钠(Na O )固体,同学们想利用这瓶过氧化钠是否变质,
2 2
进行如下实验探究:
【查阅资料】2Na O +2CO ═2Na CO +O ,2Na O +2H O═4NaOH+O ↑
2 2 2 2 3 2 2 2 2 2
【提出猜想】①没有变质 ②部分变质 ③全部变质
【实验过程及结论】
2(1)取少量样品于试管中,加入足量水,无明显现象,证明猜想________正确(填序号);
(2)取少量(1)中所得溶液于试管中,滴加适量稀盐酸,有无色气体产生,证明原样品中一定含有
________;
(3)请在原有实验的基础上,进一步设计实验证明原样品中还可能含有什么物质.(简写实验步骤、现象
和结论)
【答案】(1)③;(2)碳酸钠; (3)取少量(1)中所得溶液于试管中,滴加过量的氯化钙溶液,然后想上层清液中加
入酚酞试液,溶液变红则含有氢氧化钠。学&科*网
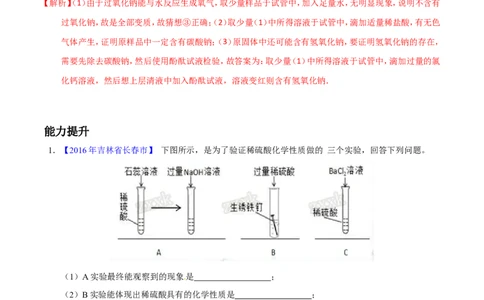
【解析】(1)由于过氧化钠能与水反应生成氧气,取少量样品于试管中,加入足量水,无明显现象,说明不含有
过氧化钠,故是全部变质,故猜想③正确;(2)取少量(1)中所得溶液于试管中,滴加适量稀盐酸,有无色
气体产生,证明原样品中一定含有碳酸钠;(3)原固体中还可能含有氢氧化钠,要证明氢氧化钠的存在,
需要先除去碳酸钠,然后使用酚酞试液检验,故答案为:取少量(1)中所得溶液于试管中,滴加过量的氯
化钙溶液,然后想上层清液中加入酚酞试液,溶液变红则含有氢氧化钠.
能力提升
1.【2016年吉林省长春市】 下图所示,是为了验证稀硫酸化学性质做的 三个实验,回答下列问题。
(1)A实验最终能观察到的现象是 ;
(2)B实验能体现出稀硫酸具有的化学性质是 ;
(3)C实验中发生反应的化学方程式为 ;
(4)将上述实验后所得溶液在烧杯中混合,观察到底部有沉淀层无色溶液,此时利用烧杯中的沉淀再选
择 适 当 试 剂 即 可 证 明 C 实 验 中 所 加 BaCl 溶 液 过 量 , 实 验 的 操 作 及 现 象 是
2
。
【答案】(1)溶液呈蓝色;(2)能与活泼金属或金属氧化物反应;(3)HSO +BaCl ==BaSO ↓+2HCl;(4)向无色
2 4 2 4
溶液中加入足量稀硫酸,始终有白色固体剩余
32.【2016年湖北省襄阳市】 实验桌上现有包白色粉末,可能是氢氧化钠、硫酸钠、碳酸钠和氯化铜的两种或
两种以上组成.现将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加
几滴无色酚酞,溶液变为红色.为进一步确定白色粉末的成分,同学们进行了如下探究.
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性.
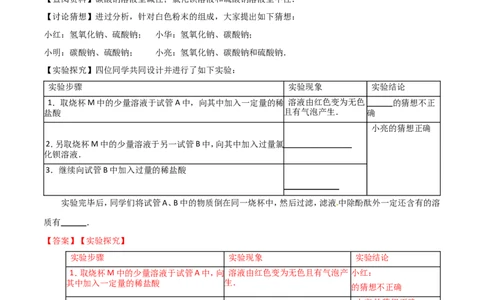
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠.
【实验探究】四位同学共同设计并进行了如下实验:
实验步骤 实验现象 实验结论
1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀 溶液由红色变为无色______的猜想不正
盐酸 且有气泡产生. 确
小亮的猜想正确
2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯________________
化钡溶液.
3.继续向试管B中加入过量的稀盐酸
_____________
实验完毕后,同学们将试管A、B中的物质倒在同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶
质有______.
【答案】【实验探究】
实验步骤 实验现象 实验结论
1.取烧杯M中的少量溶液于试管A中,向 溶液由红色变为无色且有气泡产 小红:
其中加入一定量的稀盐酸 生.
的猜想不正确
小亮的猜想正确
2.另取烧杯M中的少量溶液于另一试管B出现白色沉淀
中,向其中加入过量氯化钡溶液.
3.继续向试管B中加入过量的稀盐酸
沉淀一部分消失,并生成气泡
HCl、NaCl、BaCl ;
2
43.【2016年湖北省十堰市】 甲乙两同学在学习酸的化学性质时做了如图所示实验:
甲同学实验时没有观察到明显现象,乙同学实验时观察到有气泡发生:甲乙同学将反应完成后试管中的溶液
倒入,洁净的废液杯中,没有观察到明显现象.
【提出问题】废液杯中溶液的溶质是什么?
【猜想与假设】猜想1:废液中含有的溶质为NaCl、CaCl
2
猜想2:废液中含有的溶质为NaCl、CaCl 、HCl
2
猜想3:废液中含有的溶质为________(写化学式)
【验证与探究】甲同学取少量废液于试管中,加入紫色石蕊试液,溶液变红,则猜想________正确;乙同学取
少量的废液于试管中,加入适量氧化铁粉末,发现溶液变黄色,发生反应的化学方程式为________.
【表达与交流】甲乙同学都认为将该溶液直接排放会对环境造成危害,你认为处理该废液的最佳方法是
________.
【归纳与总结】确定反应后溶液中溶质的成分,除了要考虑生成物外,还要考虑________.
5【拓展与延伸】乙同学在实验完毕后查阅资料得知:少量盐酸与碳酸钠溶液反应能产生碳酸氢钠(反应的化学
方程式为Na CO +HCl═NaCl+NaHCO ),那么在【猜想与假设】中存在第4种猜想的可能,则猜想4:废液中
2 3 3
含有的溶质为 (写化学式)
【答案】【猜想与假设】NaCl、CaCl 、Ca(OH) ;【验证与探究】2;Fe O +3HCl=2FeCl +3H O;
2 2 2 3 3 2
【表达与交流】加熟石灰中和至中性(合理即可);【归纳与总结】生成物是否有剩余;
【拓展与延伸】NaCl、CaCl 、NaHCO 。
2 3
定反应后溶液中溶质的成分,除了要考虑生成物外,还要考虑生成物是否有剩余;【拓展与延伸】少量盐
酸与碳酸钠溶液反应能产生碳酸氢钠(反应的化学方程式为NaCO+HCl═NaCl+NaHCO ),那么在【猜
2 3 3
想与假设】中存在第4种猜想的可能,如果稀盐酸不足,废液中含有碳酸氢钠、氯化钙和氯化钠,则猜想
4:废液中含有的溶质为NaCl、CaCl 、NaHCO 。学科*网
2 3
4.【2016年湖北省鄂州市】 冬天饶老师配置了一瓶澄清石灰水,到了夏天石灰水变浑浊了,瓶壁和瓶底出
现了少量白色固体,同学们就此白色固体的成分探究如下:
[来源:Z。xx。k.Com]
(1)猜想:
①可能含有碳酸钙,生成碳酸钙的化学方程式为 。
②可能含有的另一种物质是 ,出现该物质的原因可能是温度升高,该物质的溶解度减小,
结晶析出。
(2)同学们通过实验证明了猜想②中物质的存在,请你也设计一个实验予以证明。
【答案】(1)①CO +Ca(OH) ==CaCO ↓+ H 0;②氢氧化钙;(2)取少量白色固体样品与试管中,加水振荡后,
2 2 3 2
再滴加几滴酚酞试液,如果溶液变红,说明固体样品中含有氢氧化钙
[来源:学*科*网Z*X*X*K]
67