文档内容
☆ 考点梳理 ☆
一、设计实验的一般思路:
1、明确实验目的;
2、知识整理;
3、 制定计划(选择实验用品、实验仪器并设计操作步骤);
4、进行实验;
5、得出结论;
6、反思交流。
二、实验方案评价的要点:
1、方案的可行性。在原理上是否可行。
2、安全性。实验是否安全、易于操作。
3、环保性。从环保角度来说,是否会给环境造成污染。
4、经济性。从经济的角度来说,是否达到节约资源或能源、成本低等要求。
☆ 考点典析 ☆
【题型一】实验方案的对比
如图所示,取三根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端绑上粗铜丝,
另一端系一火柴,点燃火柴,待快燃尽时,分别插入充满氧气的集气瓶中(预先放入一些水).观察到:I、
II中铁丝都剧烈燃烧,且II中铁丝燃烧比I中的更剧烈;III中铁丝没有燃烧。
[来源:学+科+网Z+X+X+K]
(1)为什么III中铁丝不能燃烧?
(2)分析II中铁丝燃烧比I中的更剧烈的原因。
1【解题方法】通过对比,找出方案的优缺点。
【答案】(1)实验III中火柴在铁丝上方,用其火焰内焰对铁丝加热,内焰温度低,没有对铁丝充分预热,因此
不能达到铁丝的着火点;
(2)实验II中铁丝绕成螺旋状,与氧气接触面积增大,反应更充分
【题型二】实验方案是否可行
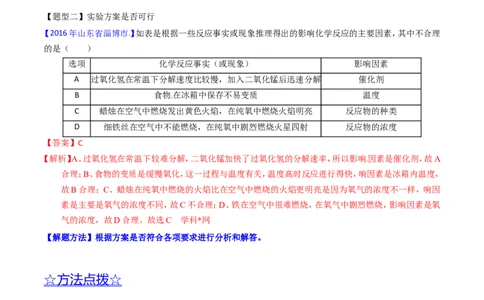
【2016年山东省淄博市】如表是根据一些反应事实或现象推理得出的影响化学反应的主要因素,其中不合理
的是( )
选项 化学反应事实(或现象) 影响因素
A 过氧化氢在常温下分解速度比较慢,加入二氧化锰后迅速分解 催化剂
B 食物在冰箱中保存不易变质 温度
C 蜡烛在空气中燃烧发出黄色火焰,在纯氧中燃烧火焰明亮 反应物的种类
D 细铁丝在空气中不能燃烧,在纯氧中剧烈燃烧火星四射 反应物的浓度
【答案】C
【解析】A、过氧化氢在常温下较难分解,二氧化锰加快了过氧化氢的分解速率,所以影响因素是催化剂,故A
合理;B、食物的变质是缓慢氧化,这一过程与温度有关,温度高时反应进行得快,响因素是冰箱内温度,
故B合理;C、蜡烛在纯氧中燃烧的火焰比在空气中燃烧的火焰更明亮是因为氧气的浓度不一样,响因
素是主要是氧气的浓度不同,故C不合理;D、铁在空气中很难燃烧,在氧气中剧烈燃烧,影响因素是氧
气的浓度,故D合理。故选C 学科*网
【解题方法】根据方案是否符合各项要求进行分析和解答。
☆ 方法点拨 ☆
1、设计实验时,应先确定实验的目的;然后根据实验中相关物质的性质预设实验步骤和可能出现的现象。
2、对于需要补充实验现象、实验操作步骤等形式的试题,要结合物质的性质进行细致的推理和论证。要
符合试题预设的步骤。
3、实验方案的评价可结合相应的角度进行了评价。
☆ 随堂小练 ☆
1.【2016年江苏省无锡市】根据实践经验,下列课外实验不能成功的是( )
A.用冷碟子收集蜡烛火焰上方的炭黑 B.用洁净的蛋壳和食醋制得二氧化碳
2C.用两杯等体积的水比较报纸与保鲜膜的透气性 D.用自制简易净水器制得纯净水
【答案】D
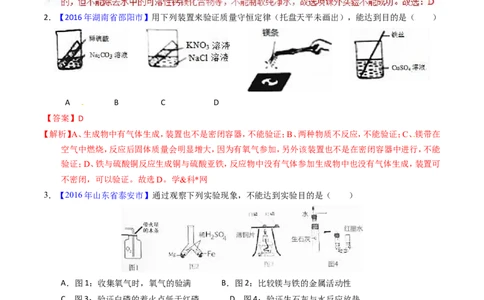
2.【2016年湖南省邵阳市】用下列装置来验证质量守恒定律(托盘天平未画出),能达到目的是( )
A B C D
【答案】D
【解析】A、生成物中有气体生成,装置也不是密闭容器,不能验证;B、两种物质不反应,不能验证;C、镁带在
空气中燃烧,反应后固体质量会明显增大,因为有氧气参加,另外该装置也不是在密闭容器中进行,不能
验证;D、铁与硫酸铜反应生成铜与硫酸亚铁,反应物中没有气体参加生成物中也没有气体生成,装置可
不密闭,可以验证。故选D。学&科*网
3.【2016年山东省泰安市】通过观察下列实验现象,不能达到实验目的是( )
A.图1:收集氧气时,氧气的验满 B.图2:比较镁与铁的金属活动性
C.图3:验证白磷的着火点低于红磷 D.图4:验证生石灰与水反应放热
【答案】C
【解析】A、检验氧气是否收集满时,应将带火星的木条放在集气瓶口,不能伸入瓶中,图中所示操作能达到实
验目的。B、金属的活动性越强,与酸反应的速率越快,通过比较与稀硫酸反应速率的快慢,可以镁与铁
的金属活动性,图中所示操作能达到实验目的。C、铜片的白磷燃烧、红磷不燃烧,但白磷和红磷距离火
焰的远近不同,不符合控制变量法的要求,图中所示操作不能达到实验目的。D、生石灰与水反应放出大
量的热,大试管内压强增大,使得墨水的液面发生变化,出现左低右高的现象,图中所示操作能达到实验
目的。故选:C。学&科*网
34.【2016年山东省威海市】 探究影响化学反应速率的因素
(1)发现和提出问题
[来源:学科网ZXXK]
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反
应以及反应速率的内因是 。
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是 ;夏天,将食品放
在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率。温度如何影响反应速率呢?
(2)猜想与假设 :温度越高,反应速率越快。
(3)收集证据
[来源:学*科*网Z*X*X*K][来源:Z§xx§k.Com]
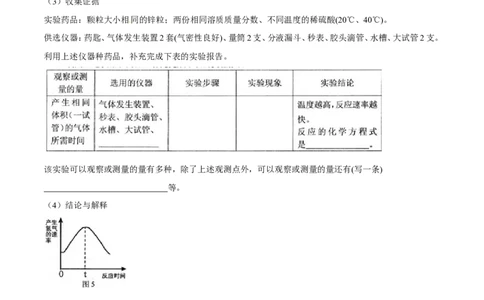
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数、不同温度的稀硫酸(20℃、40℃)。
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支。
利用上述仪器种药品,补充完成下表的实验报告。
该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有(写一条)
等。
(4)结论与解释
从微观的角度分析“温度越高,应速率越快”的原因是 。
(5)拓展分析
根据其他测定方法,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图5所
示。请据图分析:
时间0—t内,反应速率逐渐加快的主要原因是 ,
时间t以后,反应速率逐渐减慢的主要原因是 。
【答案】(l)反应物本身的性质(或反应物的组成/结构/组成和结构) 反应物的浓度(或氧气的浓度)
4(3)
选用仪器 实验步骤 实验现象 实验结论
1、分别取相同质量(或数量的锌粒于两套气体
发生装置中;
Zn + H SO
温度高的,收集一试 2 4
药匙、量筒 2、分别取相同体积、不同温度的稀硫酸加入两 === ZnSO +
管气体所需的时间短 4
套气体发生装置中; H↑
2 [来源:学#科#网]
3、记录收集一试管气体所需的时间
相同时间内收集气体的体积(或反应结束所需的时间或消耗等量锌粒所需的时间或消耗等量的稀硫酸
所需的时间)(4)温度越高,微粒运动速率加快,有效碰撞机会增多(5)反应放热,温度升高,反应速率
加快。 随着反应的进行,反应物的浓度减小,反应速率减慢。
56