文档内容
测试时间:45分钟 分值100分
姓名: 班级: 成绩:
基础过关检测(50分)
(1—10小题每小题4分,11小题10分,共50分)
1.(2016襄阳) 推理是学习化学的一种重要方法,下列推理正确的是( )
A.氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物
B.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
C.碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质ー定是碳酸盐
【答案】C
2.(2016衡阳)下列分析推理正确的是( )
A.有机物一定含有碳元素,所以含有碳元素的化合物一定是有机物
B.铝的化学性质比较活泼,所以在空气中铝比铁更容易被锈浊
C.酸溶液显酸性,所以显酸性的溶液一定是酸溶液
D.固体氢氧化钠具有吸水性,所以固体氢氧化钠可用作某些气体的干燥剂
【答案】D
【解析】A.有机物是指含碳元素的化合物,但含碳元素的化合物不一定是有机物,如一氧化碳、二氧化碳等;
B.铝的化学性质比铁活泼,在空气中更容易被氧化,但表面能生成一层致密的氧化铝薄膜,故铝制品比
铁制品更耐用;C.强酸弱碱盐的水溶液也显酸性,所以显酸性的溶液不一定是酸溶液,故错误;
3.【2016年山东省枣庄市】实验室中有两瓶失去标签的稀盐酸和氯化钠溶液,下列四种试剂中能将其鉴别出
来的是( )
A.AgNO 溶液 B.无色酚酞试液 C.K CO 溶液 D.Na SO 溶液
3 2 3 2 4
【答案】C
[来源:Z§xx§k.Com]
【解析】A、稀盐酸和氯化钠溶液均能与硝酸银溶液反应生成氯化银白色沉淀,不能出现两种明显不同的现象,
1不能鉴别,故选项错误。B、无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,稀盐酸和氯化钠溶液
分别显酸性、中性,使酚酞溶液分别显示无色、无色,不能出现两种明显不同的现象,不能鉴别,故选项
错误。C、KCO 溶液与盐酸反应产生二氧化碳气体,与氯化钠溶液不反应;分别滴加NaCO 溶液,产生
2 3 2 3
气泡的是盐酸,无明显变化的是氯化钠溶液;能出现两种明显不同的现象,可以鉴别,故选项正确。D、硫
酸钠溶液与稀盐酸和氯化钠溶液均不反应,不能出现两种明显不同的现象,不能鉴别,故选项错误。故选:
C。学*科*网
4.【2016年四川省达州市】将CO、CO 、H ,HCl,H O(气)和N 的混合气体依次通过足量的下列物质:①浓硫
2 2 2 2
酸 ②饱和氢氧化钠溶液 ③灼热的氧化铜粉末,充分反应后的剩余气体是( )
A.N 、CO 、H O B.N C.N 、HCl D.N 、CO
2 2 2 2 2 2 2
【答案】A
【解析】将CO、CO、H,HCl,HO(气)和N 的混合气体依次通过①浓硫酸,浓硫酸具有吸水性,原混合气体
2 2 2 2
中的水蒸气被除去;再通过②饱和氢氧化钠溶液,二氧化碳、HCl能与饱和氢氧化钠溶液反应,二氧化碳、
氯化氢被除去;氢气、一氧化碳具有还原性,能与灼热的氧化铜粉末反应,分别生成水蒸气、二氧化碳气
体,故充分反应后的剩余气体是N、CO、HO。故选:A。
2 2 2
5.【 2016年湖南省长沙市】判断金属Zn、Fe、Ag的金属活动性强弱有很多种方法,下列能作为判断依据的是(
)
A.根据金属导电性强弱判断 B.根据金属导热性快慢判断
C.根据锌能把铁从硫酸亚铁溶液中置换出来,铁能把银从硝酸银溶液中置换出来判断
D.根据金属的密度大小判断
【答案】C
6. 【2016年湖南省湘西州】下列物质鉴别的方法中,不能区分开来的是( )
A.用燃着的木条区分二氧化碳和氮气 B.用洁净的铁丝区分稀硫酸和氢氧化钠溶液
C.用观察法辨认氯酸钾和高锰酸钾固体 D.用盐酸区分氯化钠溶液和硝酸银溶液
【答案】A
【解析】A、氮气和二氧化碳都不能燃烧也不支持燃烧,不能用燃着的木条来鉴别它们,故错误;B、铁丝与稀
硫酸反应生成气体,而铁丝不与氢氧化钠溶液反应,故可以鉴别;C、氯酸钾固体为白色,高锰酸钾固体
为紫黑色,利用观察法可以鉴别,故正确;D、硝酸银和稀盐酸反应产生白色沉淀,而稀盐酸与氯化钠溶
液不能反应,故可以鉴别;故选:A。
7.【 2016年山东省菏泽市】某化学小组向一定量AgNO 和Cu(NO )混合溶液中加入一定量的Zn粉,充分反
3 3 2
应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是( )
2A.Zn(NO )、AgNO B.Zn(NO )、Cu(NO )、AgNO
3 2 3 3 2 3 2 3
C.Zn(NO )、Cu(NO ) D.Zn(NO )
3 2 3 2 3 2[来源:Zxxk.Com]
【答案】A
8、【2016年江苏省苏州市】下列各组离子在溶液中能大量共存的是( )
A.H+、SO 2﹣、OH﹣ B.H+、Cl﹣、CO 2﹣
4 3
C.Cu2+、Cl﹣、OH﹣ D.Na+、NO ﹣、SO 2﹣
3 4
【答案】D
【解析】A、H+、OH﹣两种离子能结合成水,不能大量共存,故选项错误。B、H+、CO2﹣两种离子能结合成水和二
3
氧化碳,不能大量共存,故选项错误。C、Cu2+、OH﹣两种离子能结合成氢氧化铜沉淀,不能大量共存,故
选项错误。D、三种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确。故选:D。
9、【2016年山东省泰安市】下列各组物质的溶液不用其他试剂无法鉴别的是( )
A.H SO NaCl Na CO CaCl B.HCl NaOH CuSO MgSO
2 4 2 3 2 4 4
C.Na CO K SO BaCl HCl D.NaNO HCl CaCl KOH
2 3 2 4 2 3 2
【答案】D
【解析】A、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一
次放出气体,该溶液为碳酸钠溶液;与碳酸钠溶液产生气体的溶液为HSO ,产生白色沉淀的为CaCl ;
2 4 2
与碳酸钠溶液混合无任何明显现象的为NaCl溶液;故不加其他试剂可以鉴别。B、uSO 溶液是蓝色的,
4
能与CuSO 溶液反应产生蓝色沉淀的是的是 NaOH溶液,能与NaOH溶液反应产生白色沉淀的是
4
MgSO 溶液,无明显变化的是HCl,故不加其他试剂可以鉴别。C、组内四种物质的溶液两两混合时,其
4
中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一次放出气体,该溶液为碳酸钠溶液;与碳酸
钠溶液产生气体的溶液为HCl,产生白色沉淀的为BaCl ;与碳酸钠溶液混合无任何明显现象的为KSO
2 2 4
3溶液;故不加其他试剂可以鉴别。D、组内四种物质的溶液两两混合时,盐酸能与氢氧化钾反应生成氯化
钾和水,但无明显变化,其余两两混合均没有明显象,故不加其他试剂无法鉴别。故选:D。
10、 【2016年山东省济宁市】某钠盐溶液中含有Cl﹣、OH﹣、CO 2﹣三种阴离子,仅用一份样品溶液,利用下面
3
的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是( )
①滴加Mg(NO ) 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加Ba(NO ) 溶液。
3 2 3 3 2
A.①②④②③ B.④②①②③ C.③②①②④ D.④②③②①
【答案】B
11、【2016年湖南省郴州市】 有一包白色的粉末,是(NH )SO、NaCl、BaCl 、NaCO、NaSO 中的一种或几
4 2 4 2 2 3 2 4
种,为确定白色粉末的成份,进行如下探究:
(1)取适量白色粉末与熟石灰混匀、共热,没有任何异味产生,说明原白色粉末一定不存在 ,其理
由是 ;
(2)另取适量白色粉末加入足量的水,搅拌,得到白色沉淀和无色溶液,可推测原白色粉末中一定含有
;
(3)取(2)中的白色沉淀,往其中加入过量的稀盐酸,产生大量的气泡,白色沉淀全部消失,说明原白色
粉末中一定还含有 ,一定不含有 ,写出产生白色沉淀的化学方程式
;
(4)取(2)中的无色溶液蒸干,得固体物质,此固体物质的成份可能有 种组成情况。
【答案】(1)硫酸铵 铵根离子和碱混合研磨会生成氨气(2)氯化钡(3)碳酸钠 硫酸钠
BaCl +Na CO =BaCO ↓+2NaCl(4)2 学&科*网
2 2 3 3
【解析】铵根离子和碱混合研磨会生成氨气,氯化钡和硫酸钠会生成不溶于酸的硫酸钡沉淀,氯化钡和碳酸钠
会生成溶于酸的碳酸钡沉淀,所以(1)取适量白色粉末与熟石灰混匀、共热,没有任何异味产生,说明原
白色粉末一定不存在硫酸铵,其理由是铵根离子和碱混合研磨会生成氨气;(2)另取适量白色粉末加入
足量的水,搅拌,得到白色沉淀和无色溶液,可推测原白色粉末中一定含有氯化钡;(3)取(2)中的白色
沉淀,往其中加入过量的稀盐酸,产生大量的气泡,白色沉淀全部消失,说明原白色粉末中一定还含有碳
酸钠,一定不含有硫酸钠,产生白色沉淀的化学方程式为:BaCl +Na CO =BaCO ↓+2NaCl;(4)取(2)中的
2 2 3 3
无色溶液蒸干,得固体物质,此固体物质的成份可能有氯化钠或氯化钠、氯化钡2种情况。学&科*网
[来源:Zxxk.Com]
4中考面对面
(1—10小题每小题4分11小题每步10分,共50分)
1.(2016苏州)分析和推理是化学学习中常用的思维方法。下列因果关系完全正确的一组是
A.洗洁精能够洗去餐具上的油污,是因为洗洁精能够溶解油污
[来源:学_科_网Z_X_X_K]
B.饱和澄清石灰水受热后变浑浊,是因为氢氧化钙的溶解度随温度升高而增大
C.碳酸钠溶液能使无色酚酞试液变红,是因为碳酸呐属于碱类物质
D.氯化銨与草术灰不能混合施用,是困为铵态氮肥与碱性物质混合产生氮气,降低肥效
【答案】D
2.(2016泰州)下列说法正确的是( )
A.分子可用直接构成物质,则溶质都以分子形式分散到溶剂中形成溶液
B.中和反应生成盐和水,则生成盐和水的反应都是中和反应
C.铵盐能与碱反应生成氨气,则硫酸铵不能与熟石灰混合施用
D.一氧化碳、二氧化碳组成元素相同,则一氧化碳、二氧化碳化学性质相同
【答案】C
【解析】A选项是错误的叙述,氯化钠溶液中溶质是离子形式存在;B选项是错误的叙述,非金属氧化物与碱
溶液的反应不属于中和反应;C选项是正确的叙述;D选项是错误的叙述二者的分子构成不同故化学性
质不同,故答案选择C
3.(2016菏泽)运用推理、类比等方法得出结论,是化学学习中常用的思维方式.以下类推结果正确的是(
)
A.铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B.水和过氧化氢的组成元素相同,则两者的化学性质相同
C.化合物是由不同种元素组成的纯净物,则只含有一种元素的物质一定不是化合物
D.碳酸盐遇酸有气体产生,则与酸反应产生气体的一定是碳酸盐
【答案】C
54.【2016年江苏省苏州市】鉴别下列各组物质,不能达到目的是( )
A.氧气与二氧化碳:带火星的木条 B.面粉与玉米粉:碘水
C.铜绿与二氧化锰:看颜色 D.酒精与白醋:闻气味
【答案】B
【解析】A、氧气有助燃性,二氧化碳无助燃性,故鉴别氧气与二氧化碳,可以用带火星的木条,故A正确;B、
面粉与玉米粉中都有淀粉,所以不能用碘水鉴别面粉和玉米粉,故B错误;C、铜绿为绿色,二氧化锰为
黑色,所以可用看颜色的方法鉴别,故C正确;D、酒精有特殊的香味,醋有特殊的酸味,所以可以通过气
味区别它们,故D正确。故选:B。
5. 【2016年广东省 】下表除去物质中所含少量杂质的方法错误的是( )
物质 杂质 除去杂质的方法
A. NaCl 泥沙 溶解、过滤、蒸发
B. N O 通过灼热的铜网
2 2
C. NaOH溶液 NaCO 加入稀盐酸至不再产生气泡
2 3
D. CO CO 先通过足量的氢氧化钠溶液,在通过浓硫酸
2
【答案】C
【解析】除杂质的要求是:要把杂质除去,但不能除去了需要的物质,更不能带入新的杂质。A中氯化钠易溶于
水,A正确;B中氧气能与铜反应生成氧化铜除去,B正确;C中加入的稀盐酸能与氢氧化钠反应,C错误;
D中二氧化碳与氢氧化钠反应生成碳酸钠除去,水蒸汽可通过浓硫酸除去,D正确。故选C。
6.【2016年湖南省长沙市】除去下列物质中含有的少量杂质,所选用的试剂不正确的是( )
选项 混合物 除杂试剂
A 一氧化碳中混有少量二氧化碳 足量的澄清石灰水
B 碳粉中混有少量氧化铜粉末 足量的稀盐酸
C 碳酸钙中混有少量氯化钠 足量的水
D 稀盐酸中混有少量稀硫酸 足量的硝酸钡溶液
【答案】D
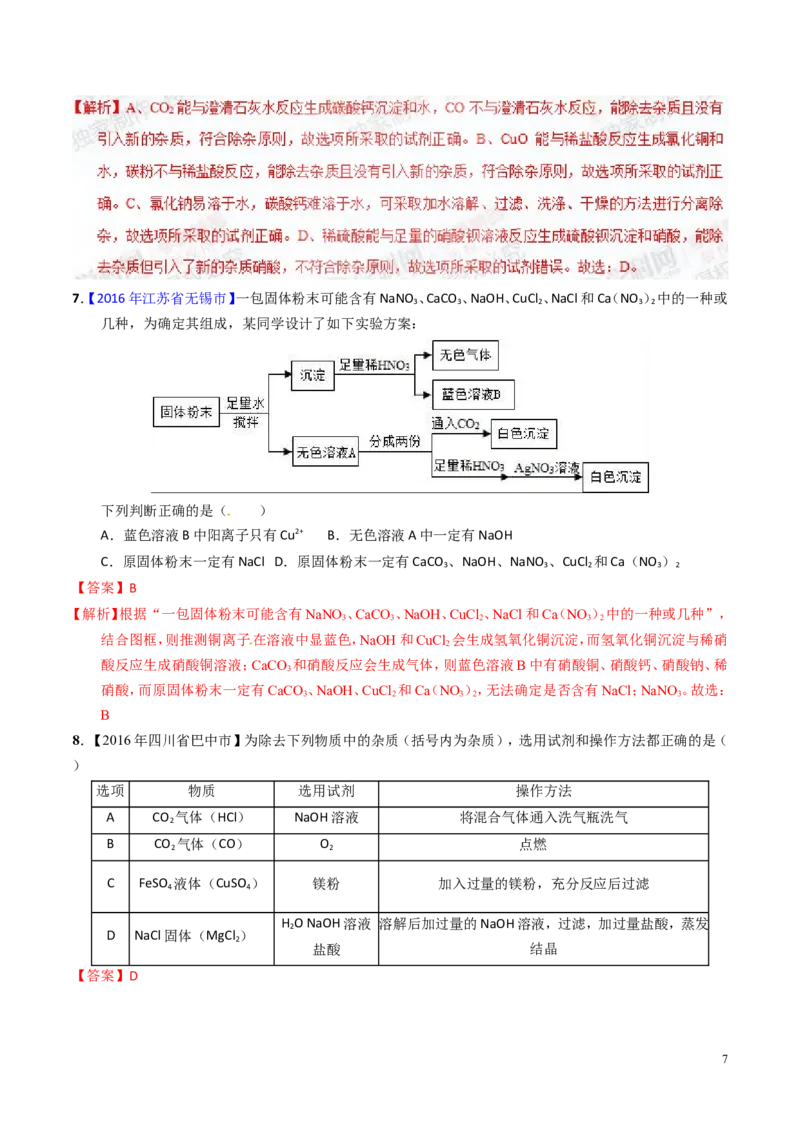
67.【2016年江苏省无锡市】一包固体粉末可能含有NaNO 、CaCO 、NaOH、CuCl 、NaCl和Ca(NO )中的一种或
3 3 2 3 2
几种,为确定其组成,某同学设计了如下实验方案:
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+ B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl D.原固体粉末一定有CaCO 、NaOH、NaNO 、CuCl 和Ca(NO )
3 3 2 3 2
【答案】B
【解析】根据“一包固体粉末可能含有NaNO 、CaCO 、NaOH、CuCl 、NaCl和Ca(NO )中的一种或几种”,
3 3 2 3 2
结合图框,则推测铜离子在溶液中显蓝色,NaOH和CuCl 会生成氢氧化铜沉淀,而氢氧化铜沉淀与稀硝
2
酸反应生成硝酸铜溶液;CaCO 和硝酸反应会生成气体,则蓝色溶液B中有硝酸铜、硝酸钙、硝酸钠、稀
3
硝酸,而原固体粉末一定有CaCO 、NaOH、CuCl 和Ca(NO ),无法确定是否含有NaCl;NaNO 。故选:
3 2 3 2 3
B
8.【2016年四川省巴中市】为除去下列物质中的杂质(括号内为杂质),选用试剂和操作方法都正确的是(
)
选项 物质 选用试剂 操作方法
A CO 气体(HCl) NaOH溶液 将混合气体通入洗气瓶洗气
2
B CO 气体(CO) O 点燃
2 2 [来源:学科网ZXXK]
C FeSO 液体(CuSO ) 镁粉 加入过量的镁粉,充分反应后过滤
4 4
H O NaOH溶液 溶解后加过量的NaOH溶液,过滤,加过量盐酸,蒸发
2
D NaCl固体(MgCl )
2 [来源:学科网]
盐酸 结晶
【答案】D
79.【2016年江苏省无锡市】只用下列鉴别方法不能把待鉴别物质区分开的是( )
选项 待鉴别物质 鉴别方法
A 软水、硬水 分别滴加肥皂水,搅拌,观察产生泡沫多少
B 棉纤维、羊毛纤维 分别点燃,闻燃烧产生的气味
C 氯化钠溶液、稀盐酸 分别滴加酚酞溶液,观察溶液颜色变化
D 氯化钾溶液、硫酸钠溶液 分别滴加氢氧化钡溶液,观察现象
【答案】C
【解析】A、肥皂水在软水中的泡沫较多,在硬水中的泡沫较少,现象不同,可以鉴别,故方法正确;B、羊毛纤维
由蛋白质组成,灼烧时产生烧焦的羽毛味;棉纤维,灼烧时没有;两种物质燃烧的现象不同,可以鉴别,
故方法正确;C、氯化钠和盐酸都不能使酚酞试液变色,不能鉴别,故方法错误;D、氢氧化钡能够和硫酸
钠反应产生白色沉淀,而和氯化钾没有明显现象,可以鉴别,故方法正确;故选项为:C。
10.【2016年山东省泰安市】除去下列各物质中混有的少量杂质,所用试剂和操作均正确的是( )
选项 物质 杂质 所用试剂和操作方法
A Na CO 溶液 Na SO 溶液 加入过量的Ba(NO ) 溶液,过滤
2 3 2 4 3 2
B H HCl 加过量的NaOH溶液,浓硫酸
2
C NaCl固体 细沙 加过量的足量的水溶解、过滤
D 铁粉 Fe O 加入适量的稀盐酸,过滤、洗涤、干燥
2 3
【答案】B
11.【2016年山东省烟台市】 如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表
8示转化关系,“﹣”表示相互能反应,部分反应物、生成物或反应条件已略去)。
甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良
酸性土壤,且C的溶液与D的溶液反应可得到B;C的溶液与乙的溶液反应生成蓝色沉淀;乙与丙两种
溶液反应生成两种不同颜色的沉淀。请回答:
(1)甲的化学式是 ;D的化学式是 。
(2)欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是 。
(3)E→C反应的化学方程式是 。
(4)乙与丙两种溶液反应的化学方程式是 。
【答案】(1)Fe Na CO (2)酚酞溶液 (3)CaO+H O=Ca(OH) (4)BaCl +CuSO ═CuCl +BaSO ↓
2 3 2 2 2 4 2 4
【解析】根据“图中的物质为初中化学常见物质”,“甲与A溶液反应得到浅绿色溶液”,说明生成亚铁离子;
根据“A、B发生中和反应,产物之一是厨房内常用的调味品”,说明生成氯化钠;根据“C常用于改良酸
性土壤,且C的溶液与D的溶液反应可得到B”,则说明C为氢氧化钙,D为碳酸钠溶液,B为氢氧化钠溶
液;根据“C的溶液与乙的溶液反应生成蓝色沉淀”,则蓝色溶液为氢氧化铜;根据“乙与丙两种溶液
反应生成两种不同颜色的沉淀”,则说明乙、丙分别可能为硫酸铜、氯化钡溶液;结合图框,推测甲可能
为铁,E可能为水,A可能为稀盐酸,代入检验,符合题意。(1)根据分析,甲的化学式是Fe;D的化学式是
Na CO 。(2)欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂酚酞
2 3
溶液。(3)E→C反应,即氧化钙与水反应生成氢氧化钙,故其反应的化学方程式是CaO+H O=Ca(OH)。
2 2
(4)乙与丙两种溶液反应的化学方程式是氯化钡溶液与硫酸铜溶液反应生成硫酸钡沉淀和氯化铜,反应
的化学方程式为:BaCl +CuSO ═CuCl +BaSO ↓。
2 4 2 4
9