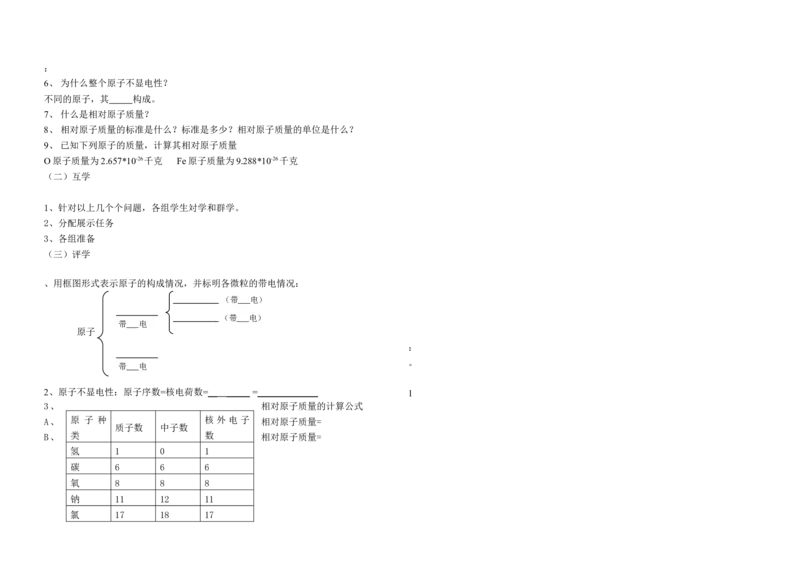文档内容
小粒子是 ;由原子构成的物质, 是保持物质化学性质的最小粒子,保持氧气
化学性质的最小粒子是 ;
四) 互学
课题1分子和原子
年级: 课型: 学科: 主备人: 审核人: 执教人:
一 、导学目标
认识物质是由分子、原子等微小粒子构成的。
培养抽象思维能力、想象力和分析、推理能力。
教学重点
认识分子、原子是客观存在的,是构成物质的两种微观粒子。认识微观粒子的特征。培养
对自然现象、试验现象的猜测、观察,分析、交流、总结等探究能力。
教学难点
从微观角度认识物质的变化。
二、导学过程:
(一)导入
生活中大家都有这样的经历,经过花园能闻到花香,经过厨房能闻到炒菜的香味,打开
酒瓶能闻到酒香这是为什么呢?湿衣服为什么晾在阳光下啊容易干?这些现象你能从
分子的角度来分析吗?
(二)问题、自学
1、构成物质的粒子有哪些?(48页)
2、分子的基本特征
a、分子和原子的体积都很 ;(48页末段)
b、分子在不断的 ,在受热的情况下,分子能量增加,运动速度 ;(49页首段)
c、分子间有 ,受热时间隔 ,遇冷时间隔 ;物质有固液气三种状态,
其中分子间间隔最大的是 态,分子间间隔最小的是 ;(49页末段)
d、同种分子性质 ,不同种分子性质 ;(50页首段)
e、分子是由 构成的。有些分子是由 原子构成,如O 、H 、N 、Cl ,大多数分
2 2 2 2
子是由 原子构成,如CO 、NO 、SO 、P O ;(50页3段)
2 2 2 2 5
3、由分子构成的物质在发生物理变化时,分子本身 ,变化的是 ,
由分子构成的物质在发生化学变化时,分子本身 ,变化的是 。(50页)
4、由分子构成的物质, 是保持物质化学性质的最小粒子,保持氧气化学性质的最1、一个水分子的质量约是3×10—26Kg,一滴水(以20滴水为1 mL计)中约有1.67×1021
个水分子说明分子具有的特点是 。
2、“酒香不怕巷子深”、花香在空气中的扩散、品红在空气中的扩散说明分子具有的特
点是___________________。生活中还有哪些现象能够说明分子在不断的运动?
请按照课本49页活动与探究实验步骤进行小组实验后,回答下列问题:
(1)酚酞溶液、浓氨水是什么颜色?浓氨水什么气味? 表明氨分子的运动比较___ _,
比酚酞更容易从烧杯中扩散到空气中。向盛有少量蒸馏水的烧杯中滴人2~3滴酚酞试
液,震荡,观察溶液为什么颜色,再向其中慢慢滴入浓氨水,观察溶液为什么颜色。因此
可以说明什么?
(2)参考课本49页图3-8,烧杯A与烧杯B哪些条件相同,什么条件不同?设计烧杯B与
A作为_______实验,是科学探究中经常使用的一种方法。
烧杯A 烧杯B
现象
解释
结论
【交流讨论】
请同学们观察演示实验后,小组讨论分子运动的快慢与温度有关吗?有什么关系呢?
【课堂探究2】1+1一定等于2吗?
请学生分别取25mL水与25 mL酒精,把它们相混合后,观察所得溶液体积是否等于
50mL?
这个实验说明物质的分子之间有 ,一种物质的分子穿插到另一种物
质分子空隙里去了。
(家庭小实验:将一体积黄豆与一体积绿豆混合,所得体积是否等于这两体积之和?)
请同学们利用这一观点来解释为什么物质存在固、液、气三种状态?为什么物质都有热
胀冷缩的现象?
( 五)评学
1、从分子的角度分子并解释为什么墙内开花在墙外能够闻到花香?香水汽油为什么要
密封保存?湿衣服晾在阳光下为什么比阴凉处干得更快?
2、水蒸发变为水蒸气体积增大是物理还是化学变化?是分子体积增大的缘故吗?为什
么6000升的氧气在加压的情况下可以装入容积为40升的钢瓶中?100ml酒精和100ml
水混合后总体积比200ml大还是小?为什么?
3
3、分别从宏观和微观的角度分析纯净物混合物有什么不同?
4、用分子的知识解释空气是混合物,冰水混合物是纯净物宏观 微观
混合物
纯净物
物理变化
化学变化
水的蒸发
三、随堂检测
练习册56页1-11题
课后作业练习册57页12-15题
四、板书设计:
五、导学反思:
:加热
第三单元课题1分子和原子 汞——汞+氧气
HgO分。
年级: 课型: 学科: 主备人: 审核人: 执教人:
一、导学目标
1、认识分子是保持物质的化学性质的最小粒子;原子是化学变化中的最小粒子。
2、培养抽象思维能力、想象力和分析、推理、归纳、比较的能力。
二、导学过程:
(一)、导入
分子的基本特征有哪些?举例说明
(二)、自学
1、分子原子的概念分别是什么?
2、原子的基本特征有哪些?
a、分子和原子的体积都很 ;
b、原子在不断的 ,
c、原子间有 ,受热时间隔 ,遇冷时间隔
d、同种原子性质 ,不同种原子性质 ;
e、原子是构成分子的粒子,同时有些原子也可以直接构成 ,比如
就是由原子直接构成的。
3、化学反应的本质是什么?
4、分子和原子的本质区别是什么?
5、分子原子有什么联系?
(三)互学
1、针对以上五个问题,各组学生対学和群学。(5分钟)
2、分配展示任务(2分钟)
3、各组准备(5分钟)
( 四)、评学
各组学生展示,鼓励学生提出质疑,老师适时给予补充或提示。
重点难点突破之化学反应的本质是:分子分解成原子,原子重新组合成新的组合
例
氧
化子分解成汞原子和氧原子,无数个汞原子直接汇聚成汞单质(因为汞单质是由原子直接
构成的),每两个氧原子结合成一个氧分子,无数个氧分子汇聚成氧气。
三、检测训练、
1、 是保持物质化学性质的最小粒子
2、 是化学变化中的最小粒子, 可以相互结合形成
3、化学变化的本质是
反应物的分子 原子 新分子 新物质
、
直接汇聚为
练习册59页1-7题
课后作业练习册60页8-14题
四、板书设计
五、导学反思第三单元课题2原子的结构
年级: 课型: 学科: 主备人: 审核人: 执教人:
一、导学目标
1、了解原子的构成情况。
2、记住原子及原子中各微粒的带电情况。
3、记住在原子中,原子序数=核电荷数=质子数=核外电子数。
二、导学过程
(一)导入
1.分子在化学变化中可以化分为原子,那么原子在化学变化是否可以再分呢?
2.1911年,卢瑟福进行了著名的α粒子散射实验,如下图
α粒子是带正电荷的微观粒子,α粒子流打在金属箔上出现不同的散射情况,说明
金属原子内部结构的有以下信息?
1.大部分α粒子能畅通无阻地穿过金属箔。
2.少量带正电的α粒子也能穿过金属箔,但发生较大偏转。
3.极少量带正电的α粒子发生大角度偏转甚至被弹回。
由此看出,原子是不是在任何情况下都是不可分割的实心小球呢?如果不是,那你
想象中的原子是什么样的呢?
(二)自学 、 问题
.阅读第53页,回答下列问题:
1、科学实验证明,原子是由居于原子中心的 和核外的 构成。原子核由
3、
题
4、为什么整个原子不显电性?
不同的原子,其 构成。
5、构成原子的各种粒子是否带电?若带电,是带正电荷,还是带负电荷?
核内的质子数和中子数是否相同:
6、为什么整个原子不显电性?
不同的原子,其 构成。
7、什么是相对原子质量?
8、相对原子质量的标准是什么?标准是多少?相对原子质量的单位是什么?
9、已知下列原子的质量,计算其相对原子质量
O原子质量为2.657*10-26千克 Fe原子质量为9.288*10-26千克
(二)互学
1、针对以上几个个问题,各组学生対学和群学。
2、分配展示任务
3、各组准备
(三)评学
、用框图形式表示原子的构成情况,并标明各微粒的带电情况:
(带 电)
(带 电)
带 电
原子
:
。
带 电
2、原子不显电性:原子序数=核电荷数= __ _____ =_____________ 1
3、 相对原子质量的计算公式
A、 原 子 种 核 外 电 子 相对原子质量=
质子数 中子数
B、 类 数 相对原子质量=
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17(1) ;(2) ;
(3) ;
三、训练检测
1.下列有关原子结构的说法中正确的是( )
A.构成原子核必不可少的粒子是质子 B.原子核都是由质子和中子构成的
C.原子中不存在带电粒子,因而整个原子不显电性
D.原子的空间主要被原子核所占据
2.下列有关原子结构的说法中错误的是 ( )
A.构成原子核必不可少的粒子是质子
B.在原子中,核电荷数一定等于质子数或核外电子数
C.原子核都是由质子和中子构成的
D.同类原子核中的质子数一定相同
3.硫原子的相对原子质量为32,质子数是16,则中子数是______,核外电子数是______,
核电荷数是______。
4.原子中决定相对原子质量大小的是( )
A.质子数和中子数 B.质子数和电子数 ()
C.中子数和电子数 D.核电荷数和电子数
5.下列有关相对原子质量的说法中正确的是( )
A.相对原子质量就是一个原子的真实质量
B.相对原子质量决定了原子的种类
C.氧原子的相对原子质量是16g
D.相对原子质量是一个比值,单位不是g或kg
6.据中央电视台对云南抚仙湖湖底考古的现场报道,科学家通过测定古生遗骸中碳14的含量来推
断古城的年代。碳14原子的核电荷数为6,相对原子质量为14。下列关于碳14原子的说法中错误的
是( )
A.中子数为6 B.质子数为6 C.核外电子数为6 D.质子数和中子数之和为14
四、板书设计
五、导学反思5、电子层与元素性质的关系元素的化学性质与原子核外电子的排布,特别是 的
6、
第三单元课题2原子的结构
7、
8、
9、
年级: 课型: 学科: 主备人: 审核人: 执教人:
10、
11、
一、 导学目标 12、
13、
(1)认识什么是原子结构示意图,了解核外电子的排布规律,知道元素化学性质与最
14、
外层电子数的关系。
15、
(2)通过观察1~18号元素的原子结构示意图,归纳原子最外层电子数与元素性质的 16、
17、
关系,培养学生对信息的整理和归纳能力。
18、
二、导学过程
19、
1、构成原子的基本粒子有哪些?各自带电情况如何?
20、
2、什么是相对原子质量?计算公式? 21、
22、
(一)导入
23、
原子是由位于中心的原子核与核外电子构成的,虽然原子的质量几乎全部集中在原
24、
子核上,但是原子核的体积却非常小,只占整个原子体积的十万分之一,在原子核的外 25、
面有“很大”的空间,核外电子就在这空间里做 高速的分层运动 。电子的运动
26、
27、
没有 固定的轨道却经常出现的区域,科学家把这经常出现的区域称为 电子层 。
28、
可见电子在核外是 分层 运动的,电子的分层运动叫 做电子的分层排布 。
29、
(二)问题、自学 30、
1、在含有多个电子的原子中,核外电子有不同的运动状态,离核近的运动能量较 ,离核远的 31、
电子能量越 。(54页二段) 32、
2、电子经常出现的区域叫电子层,已知元素的原子核外最少的只有几层?最多的有几层?什么叫最 33、
外层?(54页二段) 34、
3、原子结构示意图中,小圈表示 ,圈内的数字表示 ,弧线表示 ,弧线 35、
上面的数字表示 。(54页) 36、
4、核外电子的排布规律:仔细观察教材54页下边1-18号元素的原子结构示意图,归纳出核外电子 37、
排布的一般规律 38、
A、第一层最多排多少个电子? 39、
B、第二层最多排多少个电子? 40、
C、最外层最多排多少个电子? 41、
D、第n层最多排多少个电子? 42、
电子层由内到外,电子层上电子的能量逐渐 , 内层排满后再排外层 。 43、三、 训练检测、
数目有着密切的关系。
什么是稳定结构?
B、氦、氖等稀有气体化学性质比较 ,最外层电子数为 ,属于 结构。 得失电子;
C、镁、铝等金属元素最外层电子一般都 ,在化学反应中易 ;
D、氧、氯等非金属元素最外层电子一般都 ,在化学反应中易 。
三)、互学
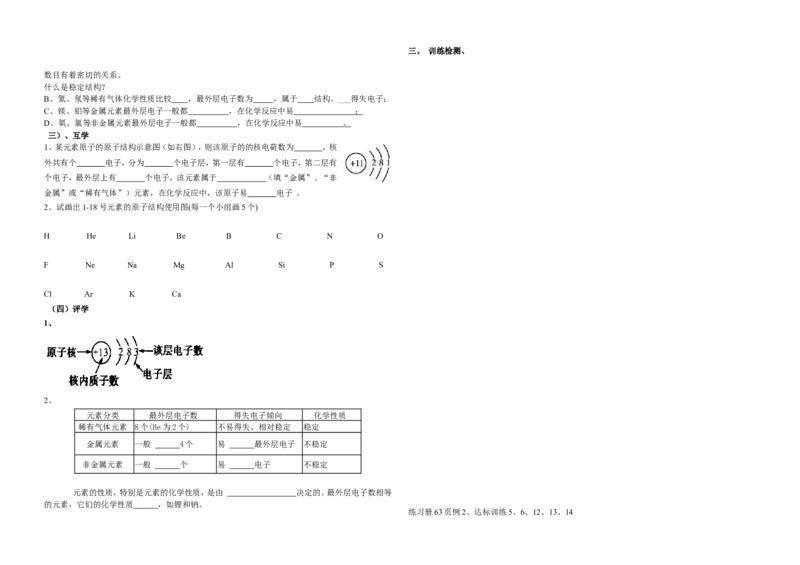
1、某元素原子的原子结构示意图(如右图),则该原子的的核电荷数为 ,核
外共有个 电子,分为 个电子层,第一层有 个电子,第二层有
个电子,最外层上有 个电子,该元素属于 (填“金属”、“非
金属”或“稀有气体”)元素,在化学反应中,该原子易 电子 。
2、试画出1-18号元素的原子结构使用图(每一个小组画5个)
H He Li Be B C N O
F Ne Na Mg Al Si P S
Cl Ar K Ca
(四)评学
1、
2、
元素分类 最外层电子数 得失电子倾向 化学性质
稀有气体元素 8个(He为2个) 不易得失、相对稳定 稳定
金属元素 一般 4个 易 最外层电子 不稳定
非金属元素 一般 个 易 电子 不稳定
元素的性质,特别是元素的化学性质,是由 决定的。最外层电子数相等
的元素,它们的化学性质 ,如锂和钠。
练习册63页例2、达标训练5、6、12、13、14课后作业63页15题
四、板书设计
五、导学反思第三单元课题2原子的结构
年级: 课型: 学科: 主备人: 审核人: 执教人:
一、导学目标
、
1、掌握离子的概念
2、离子的形成及离子的表示法(离子结构示意图和离子符号)
3、通过氯化钠NaCl的形成过程,了解离子的形成,认识离子是构成物质的一种粒子。
(一) 导入
朗读《漫游原子世界》,理解原子核外电子是如何运动的?它们能否挣脱原子核的吸引呢?
“我是一个小、小、小的电子,在原子内部很大的空间中围绕着原子核这个小老头不停地转动;我们在飞,却怎
么也飞不高。因为这老头长得很特别:虽然占据原子中央很小的地盘,却是由中子和质子构成,中子不带电,质子带
正电,因此,这小老头也带正电,很有能耐,正好把我们身上的负电深深吸引,所以我们很难脱离原子核的怀抱。”但
是总有一天我会长大,我要出去闯荡!
(二)问题
元素的性质,特别是元素的化学性质,是由 决定的。最外层电子数相等的元素,它们的化
学性质 ,如锂和钠,氯和溴等。
氦、氖等稀有气体化学性质比较 ,最外层电子数为 ,属于 结构。 得失电子;
镁、铝等金属元素最外层电子一般都 ,在化学反应中易 ;
氧、氯等非金属元素最外层电子一般都 ,在化学反应中易 。
过度:通过前面的学习我们已经知道原子核与核外电子所带电荷,电量相等电性相反,所以整个原
子不带电。金属元素原子和非金属元素原子在化学反应中都容易得失电子,那么得失电子后的原子
还是不带电吗?
(二)自学
1、什么是离子?
2、离子是如何形成的?
3、离子分为哪两种?
4、离子如何表示?
5、离子符号的含义?
6、数字的含义:
离子符号右上方数字的含义?
离子符号前面有数字时又是什么含义
(三)互学针对以上几个个问题,各组学生対学和群学。
离子化合物的形成过程,以氯化钠为例(见课本)
从图中,我们可以发现,离子是怎么样形成的?什么叫做离子?如何区别阳离子和阴离子?怎么
样书写离子符号?
(1)离子:因得失电子而带电荷的原子或原子团叫离子。如Na+、Cl-、OH-、SO2-等
4
(2)离子的分类:
阳离子:带正电的离子 质子数 电子数
离子
阴离子:带负电的离子 质子数 电子数
(3)离子符号
写法:在元素符号的右上角标明电量和电性(电量为1的可省略不写)
⑵表示意义:表示离子(或一个离子),如:Mg2+ ——表示一个镁离子
离子符号右上方数字的含义:一个镁离子带2个单位的正电荷
离子符号前面有数字的含义3Mg2+ :表示三个镁离子(离子符号前面的化学系数表示离子个数。)
(四)评学
三、训练检测
1. 元素的种类决定于( );元素的化学性质决定于( )
三、训练检测
A.最外层电子数 B. 中子数 C. 质子数 D.相对原子质量
1. 元素的种类决定于( );元素的化学性质决定于( )
A.最外层电子数 B. 中子数 C. 质子数 D.相对原子质量
2. 在下列示意图表示的粒子中① ② ③ ④ ⑤ ⑥
属于原子的有 ,属于阳离子的有 ,
属于同种元素的有 ,属于稳定结构的有
3. Ca2+右上角的数字表示的意义是( )
A.钙原子最外层上有两个电子 B.钙原子有两个电子层
C.钙离子带两个单位正电荷 D.两个钙离子
4. 下列不能直接构成物质的微粒是 ( )
A.电子 B.分子 C.原子 D.离子
5. 化学用语是学习化学的重要工具,下列化学用语书写错误的是( )
A. 2个氮原子2N B. 亚铁离子Fe2+ C. 镁离子 Mg+2 D. 3个铵根离子 3NH +
4
四、板书设计
五、导学反思