文档内容
第九单元测试卷
时间:90分钟 满分:100分
相对原子质量:Ca-40,C-12,O-16,H-1,Cl-35.5
一、单项选择题(每小题2分,共30分)
1. 把少量下列物质分别放到水中,充分搅拌,可以得到溶液是的( )
A.蔗糖 B.面粉 C.植物油 D.蒸馏水
2. 下列关于溶液的叙述,正确的是( )
A.无色透明的液体一定是溶液 B.溶液中各部分的性质均相同
C.植物油分散到水中可以形成溶液 D.溶液中只能有一种溶质
3. 市场上有一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动罐头使它们混合,
罐内饮料温度就会降低,这种固体物质可能是( )
A.硝酸铵 B.烧碱 C.食盐 D.熟石灰
4. 一杯10℃的硝酸钾溶液,能证明它是饱和溶液的方法是( )
A.蒸发5g水有固体溶质析出 B.加入少许硝酸钾晶体,晶体不减少
C.把溶液降温至0℃有固体溶质析出 D.上述三种方法都行
5. 要使一杯氯化铵不饱和溶液变为饱和溶液,可采取的方法是( )
A.加水 B.不断搅拌 C.升高温度 D.加氯化铵晶体
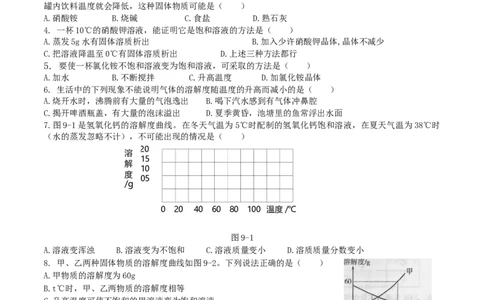
6. 生活中的下列现象不能说明气体的溶解度随温度的升高而减小的是( )
A.烧开水时,沸腾前有大量的气泡逸出 B.喝下汽水感到有气体冲鼻腔
C.揭开啤酒瓶盖,有大量的泡沫溢出 D.夏季黄昏,池塘里的鱼常浮出水面
7.图9-1是氢氧化钙的溶解度曲线。在冬天气温为5℃时配制的氢氧化钙饱和溶液,在夏天气温为38℃时
(水的蒸发忽略不计),不可能出现的情况是( )
0.20
溶
0.15
解
0.10
度
0.05
/g
0 20 40 60 80 100 温度/℃
图9-1
A.溶液变浑浊 B.溶液变为不饱和 C.溶液质量变小 D.溶质质量分数变小
8. 甲、乙两种固体物质的溶解度曲线如图9-2。下列说法正确的是( )
A.甲物质的溶解度为60g
B.t℃时,甲、乙两物质的溶解度相等
C.升高温度可使不饱和的甲溶液变为饱和溶液
D.t℃乙物质的饱和溶液降到20℃时,溶液中溶质质量分数增大
9. 炎热的夏天,小林打开冰箱,从4℃的冷藏室里拿出一杯底部还有少量蔗
糖晶体的溶液A,在室温下放置一段时间后,发现晶体消失了,得到溶液 B。
图9-2
下列说法中正确的是( )
A.4℃时,A溶液一定是饱和溶液
B.室温下,B溶液一定是饱和溶液
C.蔗糖晶体的溶解度随温度的升高而降低
D.A溶液中溶质的质量分数大于B溶液中溶质的质量分数
10. 将mg硫酸钾的不饱和溶液恒温蒸发水分至有晶体析出,在此变化过程中溶液里溶质质量分数 p%与时
1间t的关系正确的是( )
A B C D
图9-3
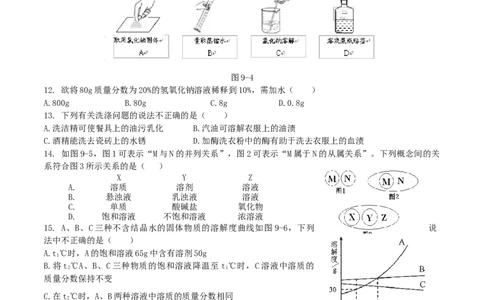
11. 现配制溶质质量分数为5%的NaCl溶液100g,下列操作错误的图示是( )
图9-4
12. 欲将80g质量分数为20%的氢氧化钠溶液稀释到10%,需加水( )
A.800g B.80g C.8g D.0.8g
13. 下列有关洗涤问题的说法不正确的是( )
A.洗洁精可使餐具上的油污乳化 B.汽油可溶解衣服上的油渍
C.酒精能洗去瓷砖上的水锈 D.加酶洗衣粉中的酶有助于洗去衣服上的血渍
14. 如图9-5,图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关
系符合图3所示关系的是( )
X Y Z
A. 溶质 溶剂 溶液
B. 悬浊液 乳浊液 溶液
C. 单质 酸碱盐 氧化物
D. 饱和溶液 不饱和溶液 浓溶液
15. A、B、C三种不含结晶水的固体物质的溶解度曲线如图 9-6,下列 说
法中不正确的是( )
A.t
1
℃时,A的饱和溶液65g中含有溶剂50g 图9-5
B.将t℃A、B、C三种物质的饱和溶液降温至 t℃时,C溶液中溶质的
2 1
质量分数保持不变
C.在t℃时,A、B两种溶液中溶质的质量分数相同
2
D.要从B溶液中得到B,通常可采用蒸发溶剂使其结晶的方法
图9-6
二、填空与简答题(共42分)
16.(5分)写出下列溶液中溶质的化学式:
溶液 溶质的化学式
(A)可用于金属表面除锈的稀硫酸溶液
(B)医疗消毒用的过氧化氢溶液(俗称双氧水)
(C)医疗消毒用的高锰酸钾溶液(俗称紫药水)
(D)医疗用的0.9﹪的氯化钠注射液(生理盐水)
(E)澄清的石灰水
17.(6分)用“>” “<” “=”填空:
2(1)50ml酒精与50ml水混合后体积 100ml;
(2)50℃时熟石灰的溶解度 20℃时熟石灰的溶解度;
(3)20℃时40g氯化钠加入100g水中,充分搅拌,形成溶液的质量 140g(20℃时氯化钠的溶解度
为36g);
(4)20℃时KNO 的溶解度为31.6g,则20℃时其饱和溶液的溶质质量分数 31.6%。
3
18.(8分)60℃时,将30克硝酸钾完全溶于270克水中,该溶液中溶质的质量分数为 ,若将该
溶液平均分成三等份:
①取第一份,温度升高到90℃,此时溶液溶质的质量分数为 。
②取第二份,要使溶液的质量分数变为原来的两倍,则需蒸发水 克。
③取第三份,要使溶液的质量分数变为原来的1/2,则需添加 克水。
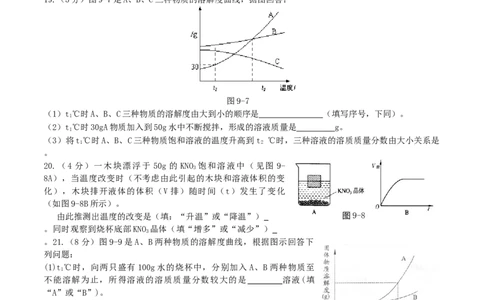
19.(5分)图9-7是A、B、C三种物质的溶解度曲线,据图回答:
图9-7
(1)t℃时A、B、C三种物质的溶解度由大到小的顺序是 (填写序号,下同)。
1
(2)t℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是 g。
1
(3)将t℃时A、B、C三种物质饱和溶液的温度升高到t ℃时,三种溶液的溶质质量分数由大小关系是
1 2
。
20.(4 分)一木块漂浮于 50g 的 KNO 饱和溶液中(见图 9-
3
8A),当温度改变时(不考虑由此引起的木块和溶液体积的变
化),木块排开液体的体积(V排)随时间(t)发生了变化
(如图9-8B所示)。
由此推测出温度的改变是(填:“升温”或“降温”) 图9-8
。同时观察到烧杯底部KNO 晶体(填“增多”或“减少”)
3
。21.(8分)图9-9是A、B两种物质的溶解度曲线,根据图示回答下
列问题:
(1)t℃时,向两只盛有100g水的烧杯中,分别加入A、B两种物质至
1
不能溶解为止,所得溶液的溶质质量分数较大的是 溶液(填
“A”或“B”)。
(2)t℃时,欲配制等质量的A.B两种物质的饱和溶液,所需水的质量
2
关系是A B。 (填写“>”、“<”或“=”,下同)
(3)将t℃的A.B两种物质的饱和溶液各200g,降温至t℃,析出晶体
2 1
的质量关系是A B。
(4)将t℃的A.B两种物质的饱和溶液各200g,升温至t℃,欲使它们
图9-9
2 1
仍为饱和溶液,若不改变溶剂质量,需加入固体溶质的质量关系是A
B。
22.(6分)下面的表格中列出了NHCl在不同温度下的溶解度:
4
温度/℃ 0 10 20 30 40 50 60 70 80
溶解度/g 29.4 33.3 37.2 41.4 45.8 50.4 55.2 60.2 65.6
3(1)由上表可推出溶解度曲线的变化规律是 。
(2)在20℃时,向100 g水中加入50 gNHCl,形成的 (填“饱和”或“不饱和”)溶液,将其
4
温度升高到60℃时,该溶液中溶质与溶剂的质量比为 。
三、实验探究题(共20分)
23.(9分)图9-10是配制50g质量分数为5% 的氯化钠溶液的操作过程示意图:
A B C D E
图9-10
试回答:
(1)B操作中应称量氯化钠的质量是 g。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分
度盘的左边,应进行的操作是 。
(2)D操作应选用 mL 的量筒(从10mL、50mL、100mL中选择);量水时,量筒必须平放,视线与
处保持水平。D处存在的错误是: 。
(3)E操作的作用是 。
(4)下列错误操作可能导致溶质质量分数偏低的是 (填序号)。
①B操作中砝码和氯化钠放错托盘;②用量筒量取水时,仰视凹液面最低处读数;③D操作时有少量
水溅出;④E操作中溶液洒落
24.(11分)小英在做饭时,发现很多因素都能影响食盐在水中溶解的速度。
(1)从你好能想到的可能影响食盐在水中溶解速率的因素中写出其中两项,并预测此因素对食盐溶解速
率的影响:因素① ,你的预测 。
因素② ,你的预测 。
(2)从你所列因素中选出一个,通过实验验证你的预测。写出你设计的实验方案
预测因素 探究方案 实验现象 结论
因素①(或因素②)
四、计算题(共8分)
25. 钙是维持人体正常功能所必需的元素.右图所示为某种补钙剂
“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸
的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反
应).烧杯内物质质量变为11.34g.试计算:
(1)每片钙尔奇中含碳酸钙的质量.
(2)所用稀盐酸中溶质的质量分数.
图9-11
4答案与点拨
一、单项选择题:
1.A
2.B
3.A
4.B
5.D
6.C 点拨:C项说明气体的溶解度随压强的减小而减小。
7.B
8.B 点拨:A项中缺失温度条件,应为45℃;由于甲的溶解度随温度的升高而增大,所以欲使甲的不饱
和溶液变为饱和溶液,应采取降温的方法,C错误;乙的溶解度随温度的降低而减小,所以降温时,在不
增加乙的情况下,乙的溶质质量分数不变,D错误。
9.A
10.C
11.C 点拨:溶液中溶质质量分数p%并不是从零开始的,故A错误;溶液中溶质质量分数p%,随着时间的
增加,其溶质质量分数会越来越大,而不是减少,故B错误;溶液中溶质质量分数p%,随着时间的增加,
其溶质质量分数会越来越大,溶液达到饱和时,溶质质量分数达到最大且不再发生改变,故 C正确;溶液
中溶质质量分数p%并不是从零开始的,故D错误。
12.A
13.B 点拨: 设需要加水的质量为xg。
则根据稀释前后溶质的质量不变,得:
80g×20%=(80g+x)×10%
解得x=80g。
14.A 点拨:溶质和溶剂并列,同属于溶液,所以 A正确;B、悬浊液和乳浊液不属于溶液.故选项B错
误;C、单质、酸碱盐、氧化物属于并列关系,故选项C错误;饱和溶液不一定是浓溶液,不饱和溶液不一
定是稀溶液.故选项D错误。
15.C 点拨:t℃时,A的溶解度是30g即100g水中溶30g,50g水中溶15g,所以溶液总质量为65g,故
1
A说法正确;由于C物质的溶解度随温度的升高而减小,所以t℃时C物质的饱和溶液降温至t℃,变为
2 1
不饱和溶液,溶质、溶剂都没变,溶质质量分数也不变,故B说法正确;由于在t℃,A、B两种物质的溶
2
解度相等,所以在t℃,A、B两种物质的饱和溶液中溶质的质量分数相等,A、B两种溶液并没有说是否饱
2
和,所以溶液的质量分数不一定相等,故C说法错误;由于B物质的溶解度随温度变化不大,所以从溶液
中结晶析出的方法是蒸发溶剂,故D说法正确。
二、填空与简答题:
16. HSO HO KmnO NaCl Ca(OH)
2 4 2 2 4 2
17. (1)< (2)< (3)< (4)<
18. 10% 10% 50 100
19. (1)B>C>A (2)65g (3)B>C>A
20. (1)降温 (2)增多
21. (1)B (2) = (3)> (4) >
22. (1)NHCl的溶解度随温度的升高而增大 (2)饱和 1︰2
4
三、实验探究题:
23. (1) 2.5g 减少氯化钠的质量 (2) 100 与凹液面最低处保持水平 量筒向里倒水时,没
有沿着烧杯内壁倾倒 (3)搅拌,加快氯化钠的溶解 (4)①②
524. (1)因素一:温度 预测温度越高,溶解越快
因素二:搅拌 预测搅拌可以加快溶解(或晶体颗粒大小,晶体颗粒越小,溶解越快)
(2)
四、计算题:
预测因 探究方案 实验现 结论
25. 解:(1)由题意可知,二氧化碳的质量为
素 象 2.0g+10g-11.34g=0.66g,
因素① 在两个烧杯中各放入 搅拌的 搅拌使 则设碳酸钙的质量为x,氯化氢的质量为y。
CaCO+2HCl═CaCl+HO+CO↑
(或因 50ml 的水,分别称取 烧杯中 食盐溶 3 2 2 2
100 73 44
素②搅 2g 颗粒大小相同的食 食盐先 解快
x y 0.66g
拌的影 盐,同时放进烧杯中, 溶解完 100/44=x/0.66g x=1.5g
响) 在一个烧杯中搅拌,观 73/44=y/0.66g y=1.095g
答:
察现象并记录两个烧杯
(2)所用稀盐酸中溶质的质量分数为:
中的食盐完全溶解所需
1.095g/10g=10.95%
的时间。
答:每片钙尔奇中含碳酸钙的质量为1.5g;所用
稀盐酸中溶质的质量分数为10.95%。
6