文档内容
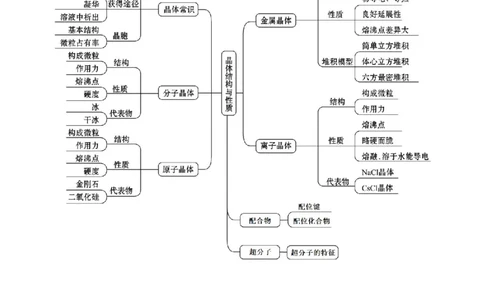
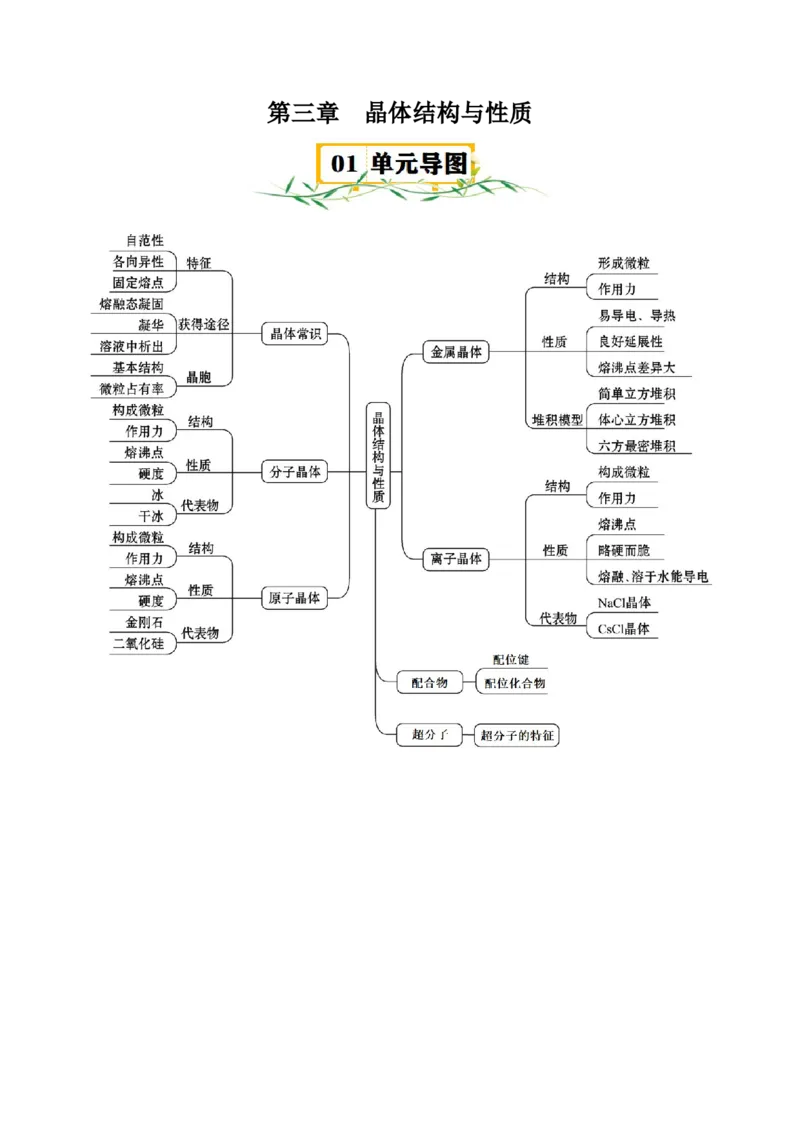
第三章 晶体结构与性质必背知识清单01 物质的聚集状态
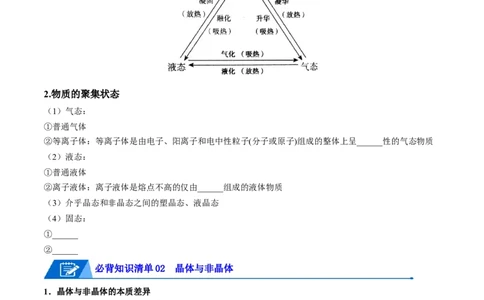
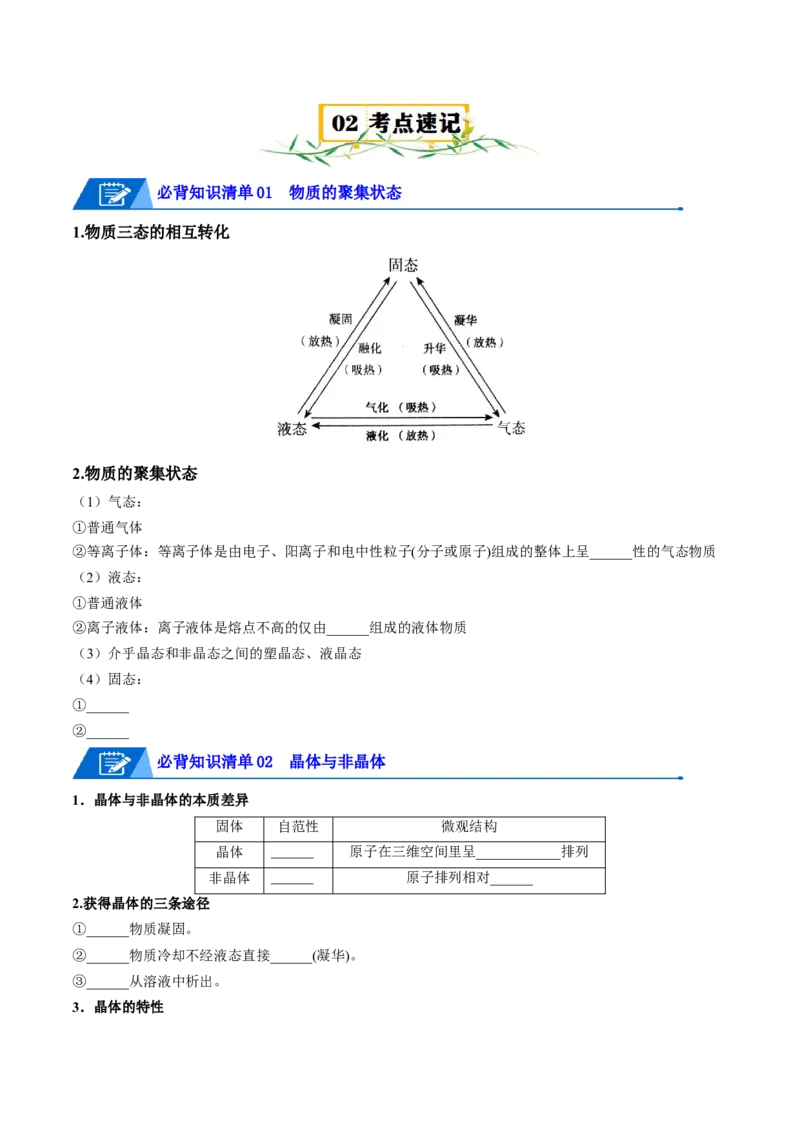
1.物质三态的相互转化
2.物质的聚集状态
(1)气态:
①普通气体
②等离子体:等离子体是由电子、阳离子和电中性粒子(分子或原子)组成的整体上呈______性的气态物质
(2)液态:
①普通液体
②离子液体:离子液体是熔点不高的仅由______组成的液体物质
(3)介乎晶态和非晶态之间的塑晶态、液晶态
(4)固态:
①______
②______
必背知识清单02 晶体与非晶体
1.晶体与非晶体的本质差异
固体 自范性 微观结构
晶体 ______ 原子在三维空间里呈____________排列
非晶体 ______ 原子排列相对______
2.获得晶体的三条途径
①______物质凝固。
②______物质冷却不经液态直接______(凝华)。
③______从溶液中析出。
3.晶体的特性(1)自范性:晶体能自发地呈现______外形的性质。
(2)各向异性:晶体在不同方向上表现出不同的____________。
(3)固定的熔点。
4.晶体与非晶体的测定方法
测熔点 晶体______固定的熔点,非晶体______固定的熔点
测定方法
可靠方法 对固体进行____________实验
必背知识清单03 晶胞
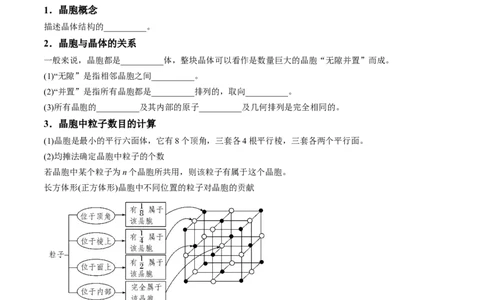
1.晶胞概念
描述晶体结构的__________。
2.晶胞与晶体的关系
一般来说,晶胞都是__________体,整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。
(1)“无隙”是指相邻晶胞之间__________。
(2)“并置”是指所有晶胞都是__________排列的,取向__________。
(3)所有晶胞的__________及其内部的原子__________及几何排列是完全相同的。
3.晶胞中粒子数目的计算
(1)晶胞是最小的平行六面体,它有8个顶角,三套各4根平行棱,三套各两个平行面。
(2)均摊法确定晶胞中粒子的个数
若晶胞中某个粒子为n个晶胞所共用,则该粒子有属于这个晶胞。
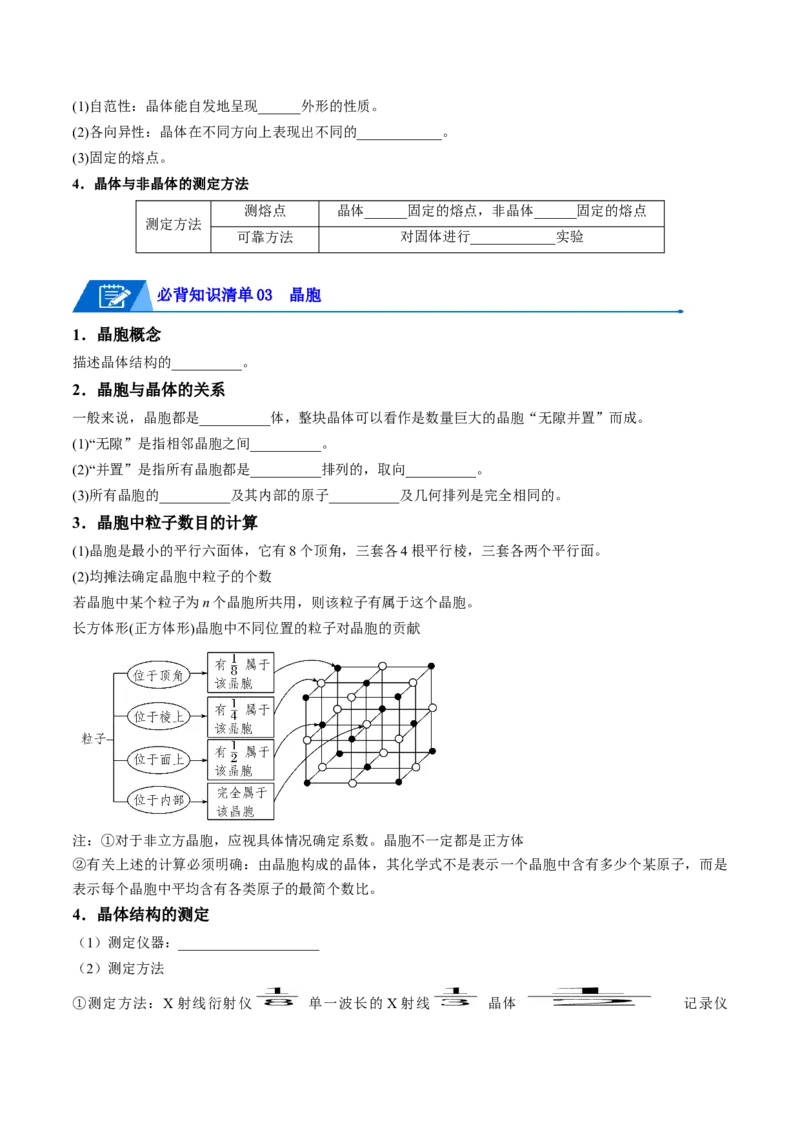
长方体形(正方体形)晶胞中不同位置的粒子对晶胞的贡献
注:①对于非立方晶胞,应视具体情况确定系数。晶胞不一定都是正方体
②有关上述的计算必须明确:由晶胞构成的晶体,其化学式不是表示一个晶胞中含有多少个某原子,而是
表示每个晶胞中平均含有各类原子的最简个数比。
4.晶体结构的测定
(1)测定仪器:____________________
(2)测定方法
1 1 1
①测定方法:X射线衍射仪 8 单一波长的 X射线 3 晶体 2 记录仪⃗产生
分立的斑点或明锐的衍射峰
②非晶体图谱中看不到分立的斑点或明锐的衍射峰
③X射线衍射图谱的应用
经过计算可以从衍射图形获得晶体结构的相关信息。
晶胞形状和大小
分子或原子在微观空间有序排列呈现的对称类型
衍射图通过计算获得
原子在晶胞里的数目和位置等
结合晶体化学组成的信息推出原子之间的相互关系
必背知识清单04 分子晶体
1.分子晶体的概念
只含__________的晶体,或者分子间以____________________结合形成的晶体叫分子晶体。
2.分子晶体中的粒子及粒子间的相互作用
3.常见的典型分子晶体
(1)所有______________:如HO、HS、NH 、CH、HX(卤化氢)等。
2 2 3 4
(2)部分______________:如X(卤素单质)、O、H、S、P、C 、稀有气体等。
2 2 2 8 4 60
(3)部分______________:如CO、SO 、NO 、PO、PO 等。
2 2 2 4 6 4 10
(4)几乎所有的____________:如HSO 、HNO、HPO 、HSiO 等。
2 4 3 3 4 2 3
(5)绝大多数有机物:如苯、四氯化碳、乙醇、冰醋酸、蔗糖等。
4.分子晶体的物理性质
(1)分子晶体熔、沸点______________,硬度______________。
(2)分子晶体______________导电。
(3)分子晶体的溶解性一般符合“______________”规律。
5.分子晶体的结构特征
分子非密堆积 分子密堆积
微粒间作用力 范德华力和氢键 范德华力
空间特点 每个分子周围紧邻的分子数小于12,空间利用 通常每个分子周围有12个紧邻的分子
率不高
举例 HF、NH 、冰 C 、干冰、I、O
3 60 2 2
6.常见分子晶体的结构分析
(1)冰晶体①结构:冰晶体中,水分子间主要通过______________形成晶体。由于氢键具有一定的______________,
一个水分子与周围四个水分子结合,这四个水分子也按照同样的规律再与其他的水分子结合。这样,每个
O原子周围都有______________个H原子,其中两个H原子与O原子以共价键结合,另外两个H原子与O
原子以氢键结合,使水分子间构成四面体骨架结构。其结构可用下图表示。
②性质:由于氢键具有方向性,冰晶体中水分子未采取密堆积方式,这种堆积方式使冰晶体中水分子的空
间利用率不高,留有相当大的空隙。当冰刚刚融化成液态水时,水分子间的空隙减小,密度反而增大,超
过4 ℃时,分子间距离加大,密度逐渐减小。
(2)干冰
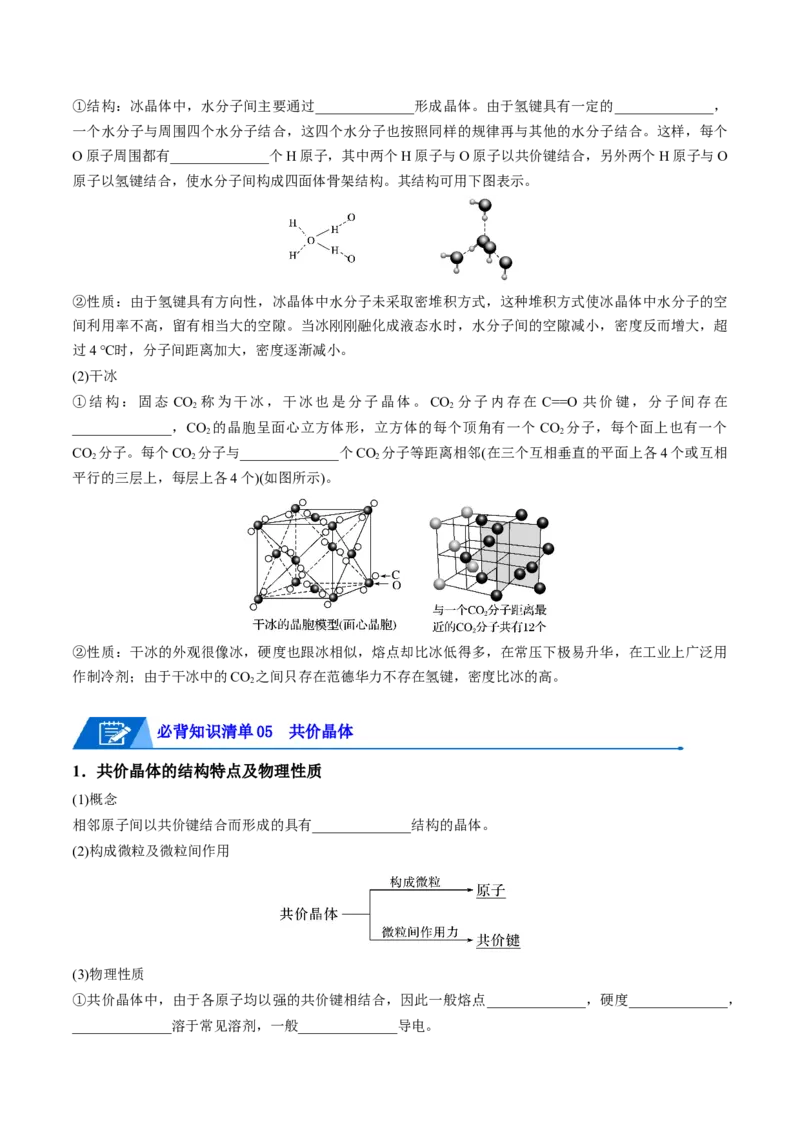
①结构:固态 CO 称为干冰,干冰也是分子晶体。CO 分子内存在 C==O 共价键,分子间存在
2 2
______________,CO 的晶胞呈面心立方体形,立方体的每个顶角有一个 CO 分子,每个面上也有一个
2 2
CO 分子。每个CO 分子与______________个CO 分子等距离相邻(在三个互相垂直的平面上各4个或互相
2 2 2
平行的三层上,每层上各4个)(如图所示)。
②性质:干冰的外观很像冰,硬度也跟冰相似,熔点却比冰低得多,在常压下极易升华,在工业上广泛用
作制冷剂;由于干冰中的CO 之间只存在范德华力不存在氢键,密度比冰的高。
2
必背知识清单05 共价晶体
1.共价晶体的结构特点及物理性质
(1)概念
相邻原子间以共价键结合而形成的具有______________结构的晶体。
(2)构成微粒及微粒间作用
(3)物理性质
①共价晶体中,由于各原子均以强的共价键相结合,因此一般熔点______________,硬度______________,
______________溶于常见溶剂,一般______________导电。②结构相似的共价晶体,原子半径越小,键长______________,键能越大,晶体的熔点越高。
2.常见共价晶体及物质类别
(1)某些单质:如 硼 (B )、 硅 (Si )、锗(Ge)、金刚石等。
(2)某些非金属化合物:如碳化硅(SiC)、二氧化硅(SiO)、氮化硼(BN)、氮化硅(Si N)等。
2 3 4
(3)极少数金属氧化物,如刚玉(α-Al O)等。
2 3
3.常见共价晶体结构分析
(1)金刚石晶体
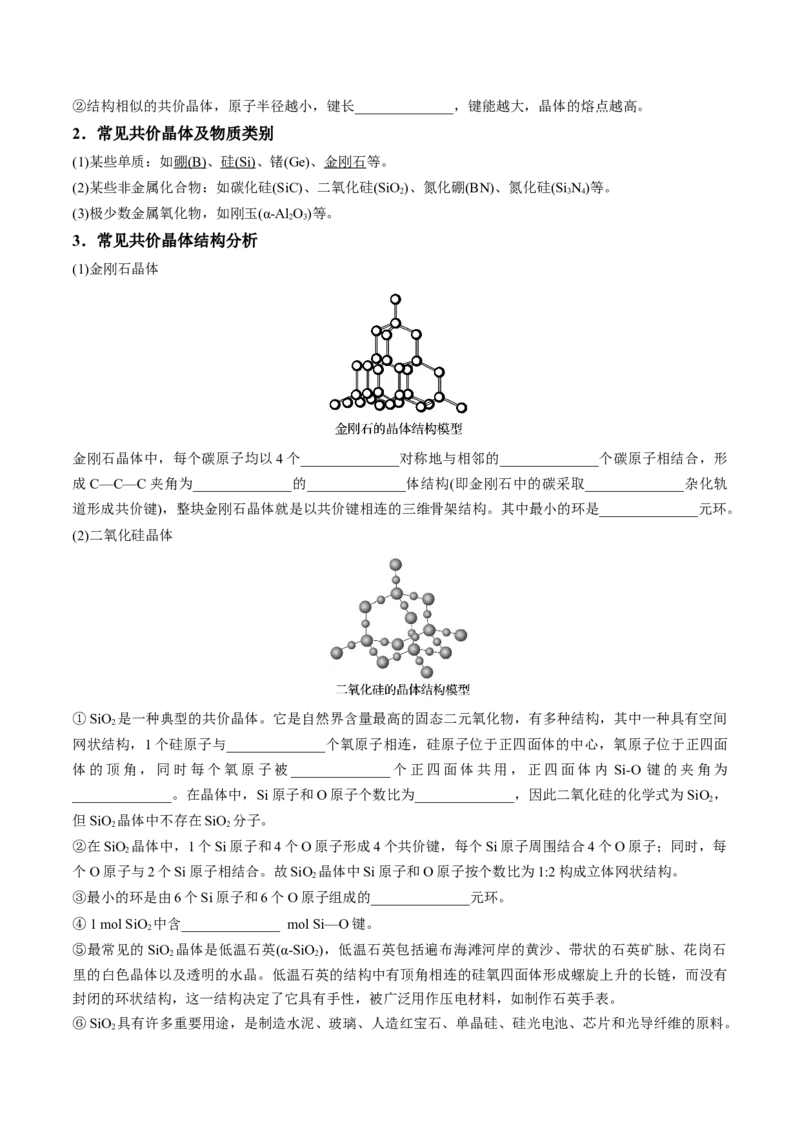
金刚石晶体中,每个碳原子均以4个______________对称地与相邻的______________个碳原子相结合,形
成C—C—C夹角为______________的______________体结构(即金刚石中的碳采取______________杂化轨
道形成共价键),整块金刚石晶体就是以共价键相连的三维骨架结构。其中最小的环是______________元环。
(2)二氧化硅晶体
①SiO 是一种典型的共价晶体。它是自然界含量最高的固态二元氧化物,有多种结构,其中一种具有空间
2
网状结构,1个硅原子与______________个氧原子相连,硅原子位于正四面体的中心,氧原子位于正四面
体的顶角,同时每个氧原子被______________个正四面体共用,正四面体内 Si-O 键的夹角为
______________。在晶体中,Si原子和O原子个数比为______________,因此二氧化硅的化学式为SiO ,
2
但SiO 晶体中不存在SiO 分子。
2 2
②在SiO 晶体中,1个Si原子和4个O原子形成4个共价键,每个Si原子周围结合4个O原子;同时,每
2
个O原子与2个Si原子相结合。故SiO 晶体中Si原子和O原子按个数比为1:2构成立体网状结构。
2
③最小的环是由6个Si原子和6个O原子组成的______________元环。
④1 mol SiO 中含______________ mol Si—O键。
2
⑤最常见的SiO 晶体是低温石英(α-SiO),低温石英包括遍布海滩河岸的黄沙、带状的石英矿脉、花岗石
2 2
里的白色晶体以及透明的水晶。低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,而没有
封闭的环状结构,这一结构决定了它具有手性,被广泛用作压电材料,如制作石英手表。
⑥SiO 具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维的原料。
2必背知识清单06 金属键与金属晶体
1.金属键
(1)概念:______________与“______________”之间存在的强烈的相互作用称为金属键。
(2)金属键的本质——“电子气理论”
金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用,从而把所有金属原子维
系在一起,这一理论称为“电子气理论”。由此可见,金属晶体跟共价晶体一样,是一种“巨分子”。
(3)金属键的特征
自由电子不是专属于某个特定的金属阳离子而是在整块固态金属中自由移动。金属键既没有
______________性,也没有______________性。
(4)影响金属键强弱的因素
一般来说,金属原子半径越小,价电子数______________,则金属键______________。
(5)金属键与金属熔、沸点的关系
金属晶体熔、沸点的高低与金属键的强弱有关。金属键越强,金属晶体的熔、沸点______________。
2.金属晶体
(1)概念:金属原子通过______________形成的晶体叫做金属晶体。
(2)金属晶体的特点
①构成金属晶体的微粒是______________和______________;
②在金属晶体中,不存在单个分子;
③金属晶体中金属阳离子被自由电子所包围
注:①含有阳离子的晶体中不一定含有阴离子,例如金属晶体中只有金属阳离子和自由电子,没有阴离子。
但晶体中有阴离子时,一定有阳离子。
②金属单质或合金的晶体属于金属晶体
(3)电子气理论解释金属材料的有关性质
①延展性:
当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但不会改变原来的排列方式,而且弥漫在
金属原子间的电子气可以起到类似轴承中滚珠之间润滑剂的作用,所以金属有良好的延展性。当向金属晶
体中掺入不同的金属或非金属原子时,就像在滚珠之间掺入了细小而坚硬的砂土或碎石一样,会使这种金
属的延展性甚至硬度发生改变,这也是对金属材料形成合金以后性能发生改变的一种比较粗浅的解释。
②导电性:
电子气理论还十分形象地用电子气在电场中定向移动解释金属良好的导电性
注:金属晶体有导电性,但能导电的物质不一定是金属。例如,石墨有导电性却属于非金属。还有一大类
能导电的有机高分子化合物,也不属于金属。
③电导率随温度的变化规律:
还可用电子气中的自由电子在热的作用下与金属原子频繁碰撞解释金属的电导率随温度升高而降低的现象。
(4)常见的合金①以铁为主要成分的碳钢、锰钢、不锈钢等
②以铜为主要成分的黄铜、青铜、白铜等
(5)电解质导电和金属导电的区别
必背知识清单07 离子晶体
物质类别 电解质 金属晶体
导电时的状态 ____________________________ ____________________________
导电粒子 ____________________________ ____________________________
导电时发生的变化 ____________________________ ____________________________
导电能力随温度的变化 ____________________________ ____________________________
1.离子键及其影响因素
(1)概念:阴、阳离子之间通过______________形成的化学键。
(2)影响因素:离子所带电荷数______________,离子半径______________,离子键越强。
特别提醒 离子键没有______________性和______________性。
2.离子晶体及其物理性质
(1)概念:由______________和______________相互作用而形成的晶体。
(2)离子晶体的性质
①熔、沸点较______________,硬度较______________。
②离子晶体不导电,但______________或______________后能导电。
③大多数离子晶体______________溶于水,______________溶于有机溶剂。
3.常见离子晶体的结构
(1)NaCl晶胞
NaCl晶胞如图所示,每个Na+周围距离最近的Cl-有_______个(上、下、左、右、前、后各1个),构成正
八面体,每个 Cl-周围距离最近的 Na+有_______个,构成正八面体,由此可推知晶体的化学式为
__________。
①每个Na+(Cl-)周围距离相等且最近的Na+(Cl-)是__________个。②每个晶胞中实际拥有的Na+数是_________个,Cl-数是_________个。
③若晶胞参数为a pm,则氯化钠晶体的密度为______________。
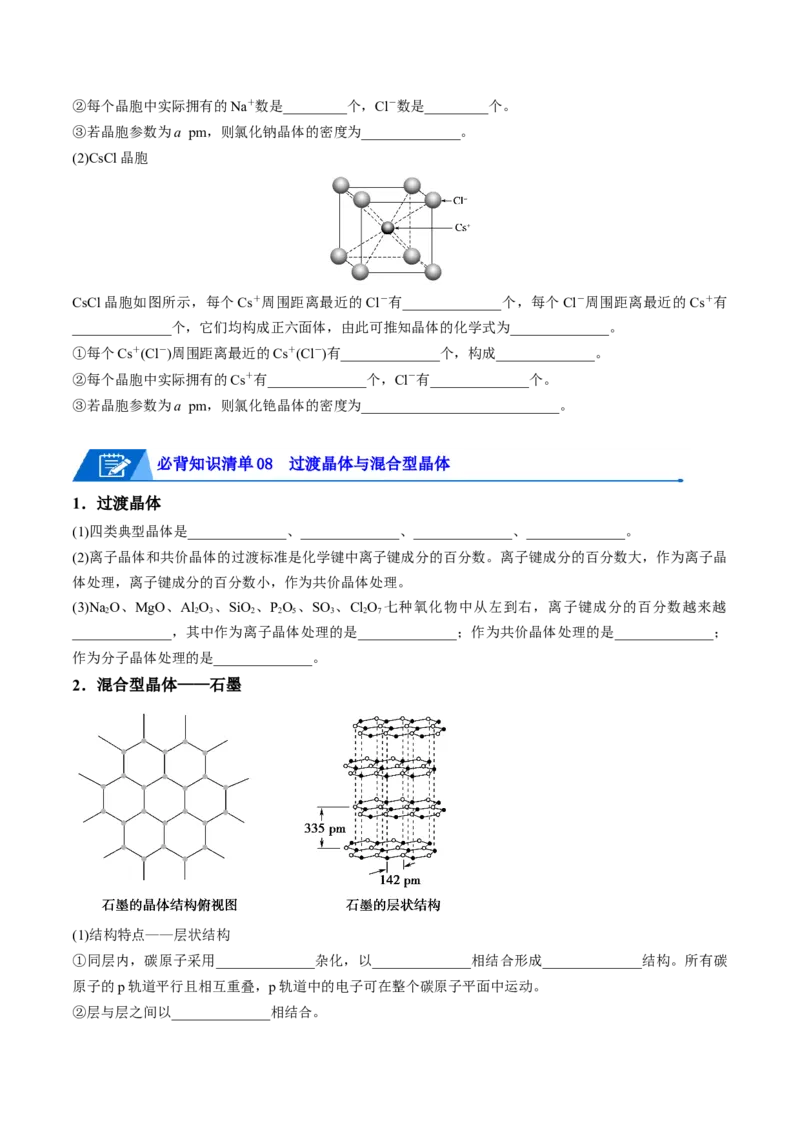
(2)CsCl晶胞
CsCl晶胞如图所示,每个Cs+周围距离最近的Cl-有______________个,每个Cl-周围距离最近的Cs+有
______________个,它们均构成正六面体,由此可推知晶体的化学式为______________。
①每个Cs+(Cl-)周围距离最近的Cs+(Cl-)有______________个,构成______________。
②每个晶胞中实际拥有的Cs+有______________个,Cl-有______________个。
③若晶胞参数为a pm,则氯化铯晶体的密度为____________________________。
必背知识清单08 过渡晶体与混合型晶体
1.过渡晶体
(1)四类典型晶体是______________、______________、______________、______________。
(2)离子晶体和共价晶体的过渡标准是化学键中离子键成分的百分数。离子键成分的百分数大,作为离子晶
体处理,离子键成分的百分数小,作为共价晶体处理。
(3)Na O、MgO、Al O 、SiO 、PO 、SO 、ClO 七种氧化物中从左到右,离子键成分的百分数越来越
2 2 3 2 2 5 3 2 7
______________,其中作为离子晶体处理的是______________;作为共价晶体处理的是______________;
作为分子晶体处理的是______________。
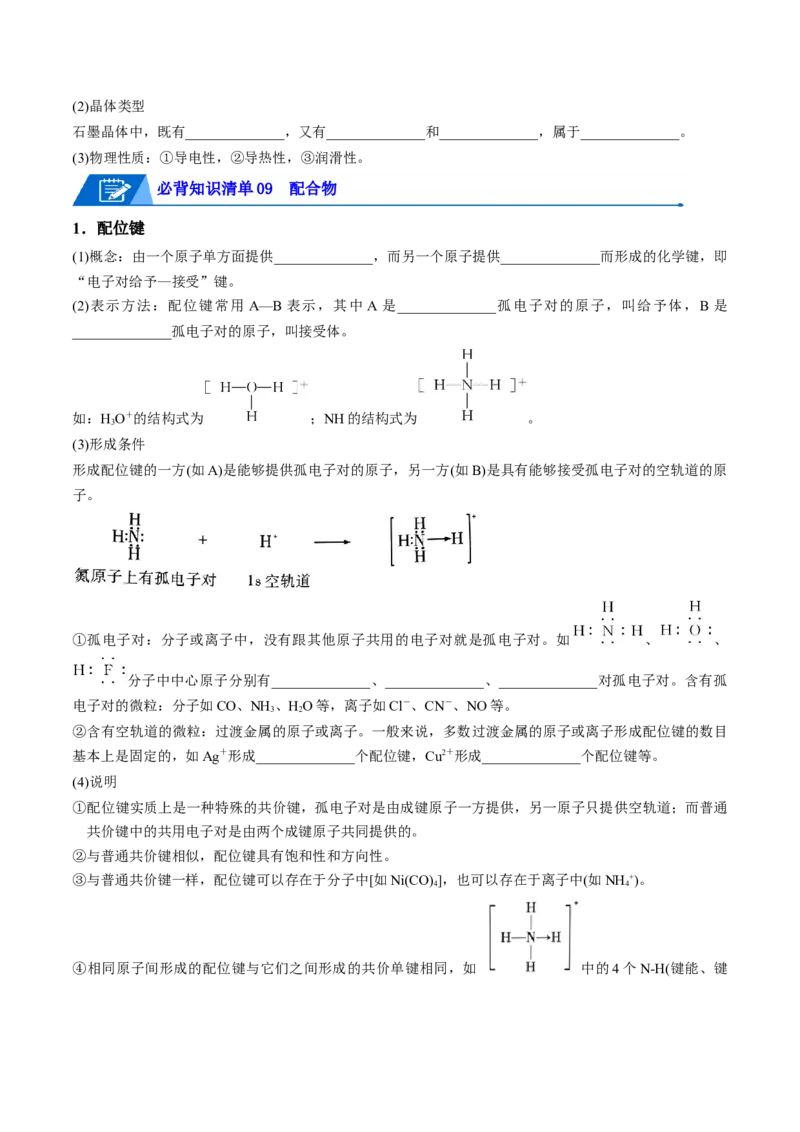
2.混合型晶体——石墨
(1)结构特点——层状结构
①同层内,碳原子采用______________杂化,以______________相结合形成______________结构。所有碳
原子的p轨道平行且相互重叠,p轨道中的电子可在整个碳原子平面中运动。
②层与层之间以______________相结合。(2)晶体类型
石墨晶体中,既有______________,又有______________和______________,属于______________。
(3)物理性质:①导电性,②导热性,③润滑性。
必背知识清单09 配合物
1.配位键
(1)概念:由一个原子单方面提供______________,而另一个原子提供______________而形成的化学键,即
“电子对给予—接受”键。
(2)表示方法:配位键常用 A—B 表示,其中 A 是______________孤电子对的原子,叫给予体,B 是
______________孤电子对的原子,叫接受体。
如:HO+的结构式为 ;NH的结构式为 。
3
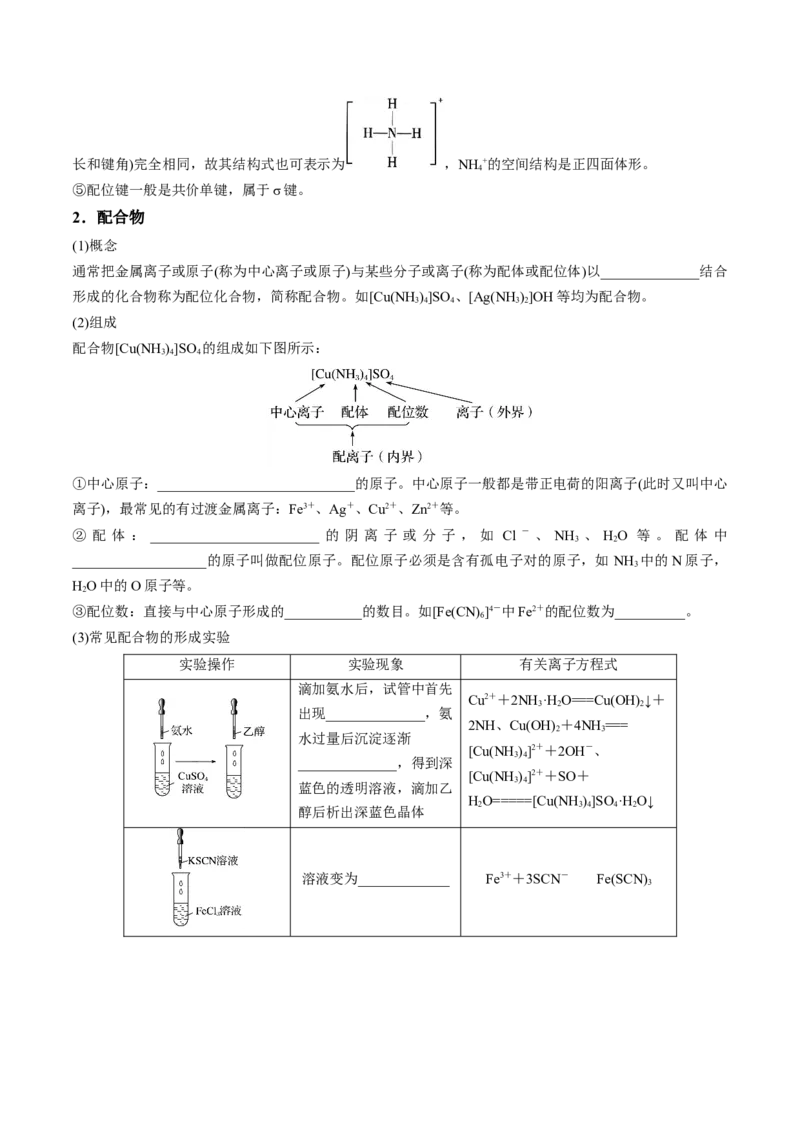
(3)形成条件
形成配位键的一方(如A)是能够提供孤电子对的原子,另一方(如B)是具有能够接受孤电子对的空轨道的原
子。
①孤电子对:分子或离子中,没有跟其他原子共用的电子对就是孤电子对。如 、 、
分子中中心原子分别有______________、______________、______________对孤电子对。含有孤
电子对的微粒:分子如CO、NH 、HO等,离子如Cl-、CN-、NO等。
3 2
②含有空轨道的微粒:过渡金属的原子或离子。一般来说,多数过渡金属的原子或离子形成配位键的数目
基本上是固定的,如Ag+形成______________个配位键,Cu2+形成______________个配位键等。
(4)说明
①配位键实质上是一种特殊的共价键,孤电子对是由成键原子一方提供,另一原子只提供空轨道;而普通
共价键中的共用电子对是由两个成键原子共同提供的。
②与普通共价键相似,配位键具有饱和性和方向性。
③与普通共价键一样,配位键可以存在于分子中[如Ni(CO) ],也可以存在于离子中(如NH +)。
4 4
④相同原子间形成的配位键与它们之间形成的共价单键相同,如 中的4个N-H(键能、键长和键角)完全相同,故其结构式也可表示为 ,NH +的空间结构是正四面体形。
4
⑤配位键一般是共价单键,属于σ键。
2.配合物
(1)概念
通常把金属离子或原子(称为中心离子或原子)与某些分子或离子(称为配体或配位体)以______________结合
形成的化合物称为配位化合物,简称配合物。如[Cu(NH )]SO 、[Ag(NH)]OH等均为配合物。
3 4 4 3 2
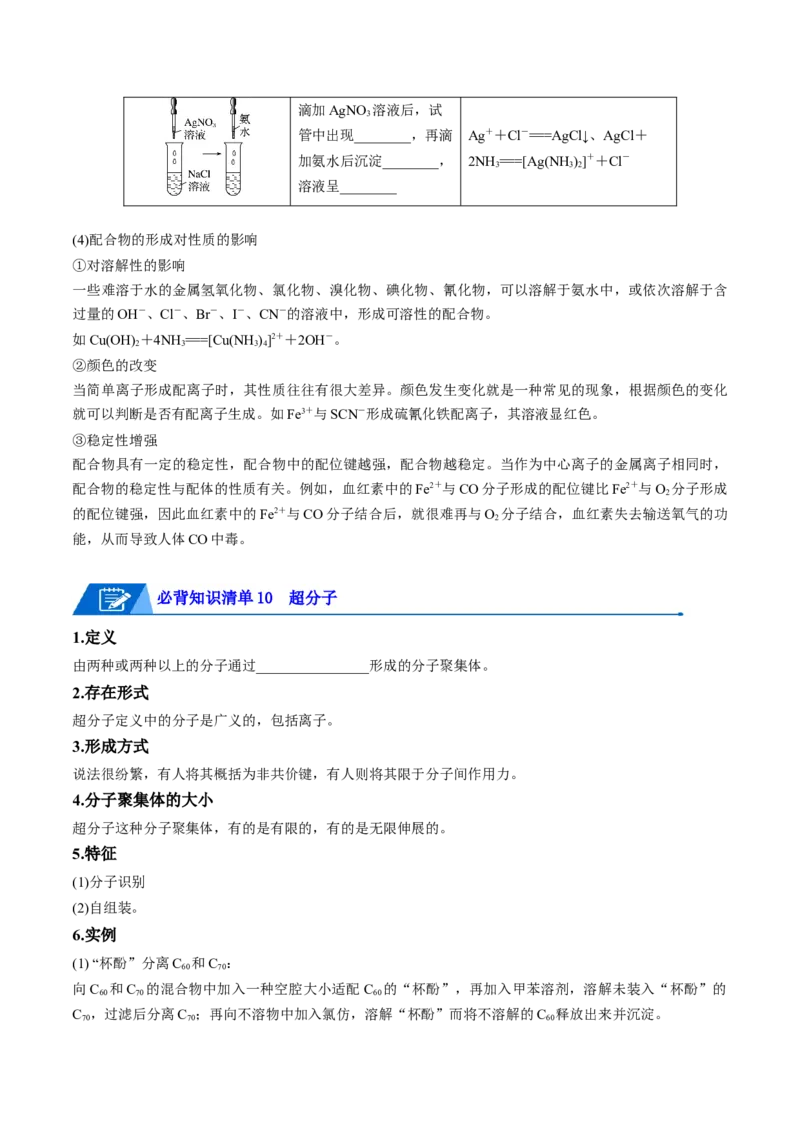
(2)组成
配合物[Cu(NH )]SO 的组成如下图所示:
3 4 4
①中心原子:____________________________的原子。中心原子一般都是带正电荷的阳离子(此时又叫中心
离子),最常见的有过渡金属离子:Fe3+、Ag+、Cu2+、Zn2+等。
② 配 体 : ________________________ 的 阴 离 子 或 分 子 , 如 Cl - 、 NH 、 HO 等 。 配 体 中
3 2
___________________的原子叫做配位原子。配位原子必须是含有孤电子对的原子,如 NH 中的N原子,
3
HO中的O原子等。
2
③配位数:直接与中心原子形成的___________的数目。如[Fe(CN) ]4-中Fe2+的配位数为__________。
6
(3)常见配合物的形成实验
实验操作 实验现象 有关离子方程式
滴加氨水后,试管中首先
Cu2++2NH ·H O===Cu(OH) ↓+
3 2 2
出现______________,氨
2NH、Cu(OH) +4NH ===
2 3
水过量后沉淀逐渐
[Cu(NH )]2++2OH-、
3 4
______________,得到深
[Cu(NH )]2++SO+
3 4
蓝色的透明溶液,滴加乙
HO=====[Cu(NH )]SO ·H O↓
2 3 4 4 2
醇后析出深蓝色晶体
溶液变为_____________ Fe3++3SCN-Fe(SCN)
3滴加AgNO 溶液后,试
3
管中出现________,再滴 Ag++Cl-===AgCl↓、AgCl+
加氨水后沉淀________, 2NH ===[Ag(NH )]++Cl-
3 3 2
溶液呈________
(4)配合物的形成对性质的影响
①对溶解性的影响
一些难溶于水的金属氢氧化物、氯化物、溴化物、碘化物、氰化物,可以溶解于氨水中,或依次溶解于含
过量的OH-、Cl-、Br-、I-、CN-的溶液中,形成可溶性的配合物。
如Cu(OH) +4NH ===[Cu(NH)]2++2OH-。
2 3 3 4
②颜色的改变
当简单离子形成配离子时,其性质往往有很大差异。颜色发生变化就是一种常见的现象,根据颜色的变化
就可以判断是否有配离子生成。如Fe3+与SCN-形成硫氰化铁配离子,其溶液显红色。
③稳定性增强
配合物具有一定的稳定性,配合物中的配位键越强,配合物越稳定。当作为中心离子的金属离子相同时,
配合物的稳定性与配体的性质有关。例如,血红素中的Fe2+与CO分子形成的配位键比Fe2+与O 分子形成
2
的配位键强,因此血红素中的Fe2+与CO分子结合后,就很难再与O 分子结合,血红素失去输送氧气的功
2
能,从而导致人体CO中毒。
必背知识清单10 超分子
1.定义
由两种或两种以上的分子通过________________形成的分子聚集体。
2.存在形式
超分子定义中的分子是广义的,包括离子。
3.形成方式
说法很纷繁,有人将其概括为非共价键,有人则将其限于分子间作用力。
4.分子聚集体的大小
超分子这种分子聚集体,有的是有限的,有的是无限伸展的。
5.特征
(1)分子识别
(2)自组装。
6.实例
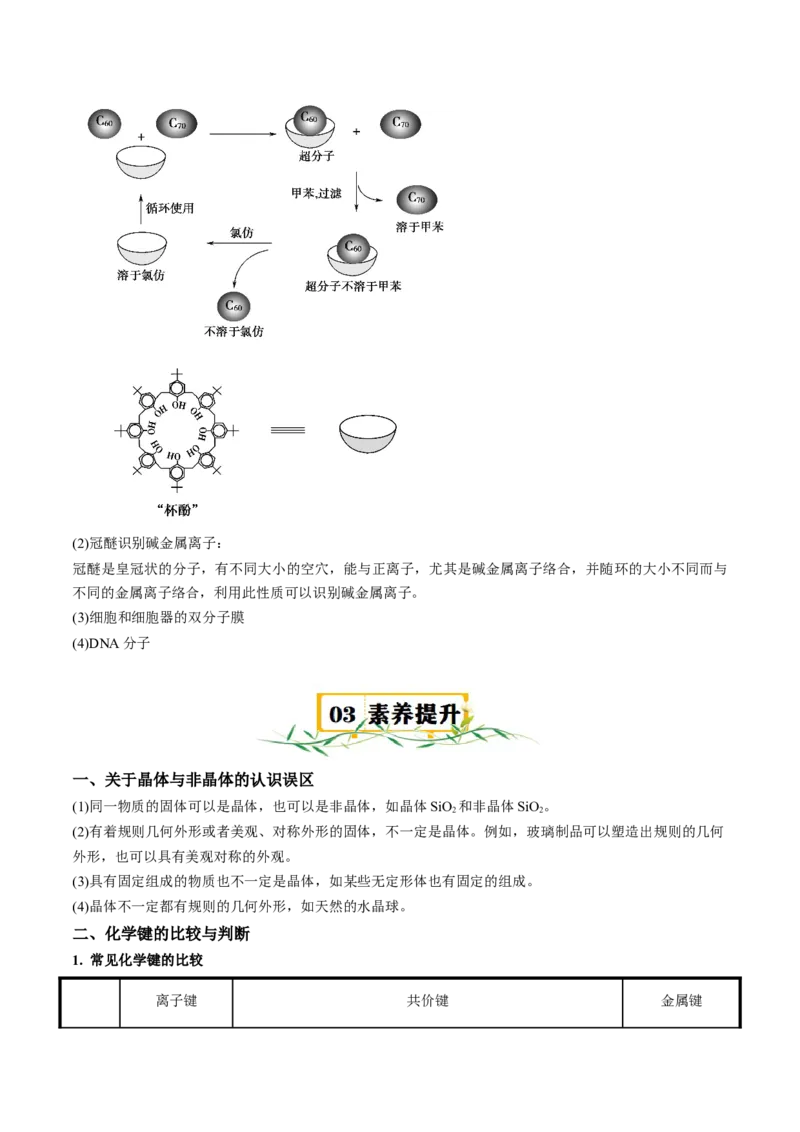
(1) “杯酚”分离C 和C :
60 70
向C 和C 的混合物中加入一种空腔大小适配C 的“杯酚”,再加入甲苯溶剂,溶解未装入“杯酚”的
60 70 60
C ,过滤后分离C ;再向不溶物中加入氯仿,溶解“杯酚”而将不溶解的C 释放出来并沉淀。
70 70 60(2)冠醚识别碱金属离子:
冠醚是皇冠状的分子,有不同大小的空穴,能与正离子,尤其是碱金属离子络合,并随环的大小不同而与
不同的金属离子络合,利用此性质可以识别碱金属离子。
(3)细胞和细胞器的双分子膜
(4)DNA分子
一、关于晶体与非晶体的认识误区
(1)同一物质的固体可以是晶体,也可以是非晶体,如晶体SiO 和非晶体SiO。
2 2
(2)有着规则几何外形或者美观、对称外形的固体,不一定是晶体。例如,玻璃制品可以塑造出规则的几何
外形,也可以具有美观对称的外观。
(3)具有固定组成的物质也不一定是晶体,如某些无定形体也有固定的组成。
(4)晶体不一定都有规则的几何外形,如天然的水晶球。
二、化学键的比较与判断
1. 常见化学键的比较
离子键 共价键 金属键非极性键 极性键 配位键
阴、阳离子间 金属阳离子与
相邻原子间通过共用电子对(电子云重叠)与原子核间的静电
本质 通过静电作用 自由电子间作
作用形成
形成 用
成键原子的
成键 得、失电子能 成键原子得、失 成键原子得、失 成键原子一方有
条件 力差别很大 电子能力相同 电子能力差别较 孤电子对(配位 同种金属或不
(元素 (金属元素与 (同种非金属元 小(不同种非金属 体)另一方有空轨 同金属(合金)
种类) 非金属元素之 素之间) 元素之间) 道(中心原子)
间)
无方向性、饱 无方向性、饱
特征 有方向性、饱和性
和性 和性
单质(如H),共
2
离子化合 共价化合物(如 离子化
价化合物(如 金属单质(金属
存在 物(离子 HCl),离子化合 合物(如
HO),离子化 晶体)
2 2
晶体) 物(如NaOH) NH Cl)
4
合物(如NaO)
2 2
成键原子电负性
一般阴、阳离
差值越大,键的 金属阳离子半
影响 子电荷越多,
极性越强;键 径越小,价电
强弱 半径越 —— ——
能越大,键长越 子越多,金属
因素 小,离子键越
短,共价键越牢 键越强
强
固
2.根据物质类别判断化学键类型
(1)离子化合物中一定有离子键,可能有共价键。由简单离子构成的离子化合物中只有离子键,如MgO、
NaCl等;由复杂离子(原子团)构成的离子化合物中既有离子键又有共价键,如(NH )SO 、KNO、NaOH、
4 2 4 3
NaO 等。
2 2
(2)共价化合物中只能有共价键,一定没有离子键。这是因为共价化合物中原子间都是通过共用电子形成化
学键,不存在带电荷的阴、阳离子,如HCl、CO、CH 等。
2 4
(3)金属单质中一般只存在金属键。(4)非金属单质(除稀有气体外)一般只存在非极性键。
3.中学常见物质中的化学键
①只有非极性键的物质:H、O、N、P、S、S、金刚石、晶体硅等。
2 2 2 4 2 8
②只有极性键的物质:HX(X为F、Cl、Br、I)、CO、SO 等。
2
③既有极性键、又有非极性键的物质:HO、C H、C H、C H、C HOH等。
2 2 2 2 2 4 6 6 2 5
④只有离子键的物质:如CaCl 、KO、KH等(固体)。
2 2
⑤既有离子键、又有非极性键的物质:NaO、NaS、CaC 等。
2 2 2 2 2
⑥既有离子键,又有极性键的物质:(NH )SO 、NH NO 等。
4 2 4 4 3
⑦稀有气体中不存在化学键。
⑧金属或合金中存在金属键。
三、配合物中配离子、中心原子、配体和配位数的确定方法
(1)配合物的内界是以配位键形成的,一般不电离,而内界和外界之间是通过离子键相结合的,可以完全电
离。因此可以根据配合物在溶液中的电离情况,通过实验及其数据可以确定内界和外界离子的个数,从而
可以确定其配离子、中心原子和配体。
如在1 mol [Cr(H O) Br ]Br·2H O形成的溶液中加入足量硝酸银,形成的淡黄色沉淀为1 mol,而不是3
2 4 2 2
mol,这是因为配合物[Cr(H O) Br ]Br·2H O由内界和外界组成,内界和外界通过离子键形成,在水溶液中
2 4 2 2
自由电离,而内界中通过配位键(特殊共价键)形成,在水溶液中不能完全电离形成游离的溴离子,所以沉
淀为1 mol,而不是3 mol。
(2)配位数:直接同中心离子(或原子)配位的原子数目叫中心离子(或原子)的配位数。要注意只含有一个配
位原子的配体称为单基配体,中心离子(或原子)同单基配体结合的数目就是该中心离子的配位数,如
[Fe(CN) ]4-中Fe2+的配位数为6。含有两个以上配位原子的配体叫多基配体,中心离子(或原子)同多基配体
6
配合时,配位数等于同中心离子(或原子)配位的原子数。例如,乙二胺分子中含有两个配位N原子,故在
[Pt(en) ]Cl (en代表乙二胺分子)中Pt2+的配位数为2×2=4,而配体只有两个,依次类推。
2 2
四、晶体类型的比较
1.四种晶体的比较
晶体 分子晶体 离子晶体 金属晶体 共价晶体
金属离子、自
构成微粒 分子 阴、阳离子 原子
由电子
范德华力(少数
微粒间作用力 离子键 金属键 共价键
有氢键)
熔、沸
较低 较高 一般较高 很高
点
硬度 小 略硬而脆 一般较大 很大
性质
不溶,有些与
溶解性 相似相溶 多数溶于水 不溶
水反应
机械加 不良 不良 良好 不良工性能
固态、液态均 固态时不导电,熔 大部分固
固态、熔融态
导电性 不导电,部分 融时导电,能溶于 态、熔融时
时导电
溶于水时导电 水的溶于水时导电 都不导电
金属原子的价 共价键键长
组成和结构相
离子所带电荷数 电子数多、半 短(电子云重
似的分子,相
作用力大小规律 多、半径小的离子 径小的金属离 叠多)、原子
对分子质量大
键强 子与自由电子 半径小的共
的范德华力大
间的作用力强 价键稳定
2.晶体类型的判断方法
(1)依据组成晶体的微观粒子和粒子间的作用判断
分子间通过分子间作用力形成的晶体属于分子晶体;由原子通过共价键形成的晶体属于共价晶体;由阴、
阳离子通过离子键形成的晶体属于离子晶体;由金属阳离子和自由电子通过金属键形成的晶体属于金属晶
体。
(2)依据物质的分类判断
①活泼金属的氧化物(如NaO、MgO等)、强碱[如KOH、Ba(OH) 等]和绝大多数的盐类是离子晶体。
2 2
②大多数非金属单质(除金刚石、石墨、晶体硼、晶体硅等外)、气态氢化物、非金属氧化物(除SiO 外)、
2
酸、绝大多数有机物(除有机盐外)是分子晶体。
③常见的共价晶体单质有金刚石、晶体硼、晶体硅等;常见的共价晶体化合物有碳化硅、SiO 等。
2
④金属单质(除汞外)与合金均属于金属晶体。
(3)依据晶体的熔点判断
离子晶体的熔点较高,常在数百至几千摄氏度;共价晶体的熔点高,常在一千至几千摄氏度;分子晶体的
熔点较低,常在数百摄氏度以下至很低温度;金属晶体多数熔点高,但也有熔点相当低的。
(4)依据导电性判断
离子晶体在水溶液中和熔融状态下都导电;共价晶体一般为非导体,但晶体硅能导电;分子晶体为非导体,
而分子晶体中的电解质(主要是酸和非金属氢化物)溶于水,使分子内的化学键断裂形成自由离子,也能导
电;金属晶体是电的良导体。
(5)依据硬度和机械性能判断
离子晶体硬度较大或略硬而脆;共价晶体硬度大;分子晶体硬度小且较脆;金属晶体多数硬度大,但也有
硬度较小的,且具有延展性。