文档内容
东明县2012——2013学年度第一学期期末考试
九年级化学试题
题号 一 二 三 四 总分
得分
可能用到的相对原子质量:H 1 C 12 O16 Fe 56
一、选择题(: 本大题共10小题,每小题2分,共20分)每小题给出的四个选项中,只有一个最
符合题意,请将正确答案的选项序号填在题后的答题栏里中。
1.下列物质的用途中,不是利用物理性质的是
A.用金刚石切割玻璃 B.用石墨制铅笔芯
C.用焦炭冶炼金属 D.用活性炭吸附气味和色素
2.一种新型的绿色电池——燃料电池,是把H、CO、CH 等燃料和空气不断输入,直接氧化,
2 4
使化学能转化为电能,被称为21世纪的“绿色发电站”。这三种气体可以作为燃料的原
因是
A.都是无毒无害的气体 B.都可燃烧并放出大量的热
C.燃料燃烧产物均为二氧化碳和水 D.均在自然界中大量存在
3.下列处理事故的方法错误的是
A.厨房油锅着火时用锅盖盖灭
B.电器着火应先切断电源,再用二氧化碳灭火器扑灭
C.扑灭森林火灾的有效方法之一,是将大火蔓延路线前的一片树木砍掉
D.发现燃气(天然气、煤气或液化石油气等)泄漏,点火检查泄漏处
4.如图所示的微观化学变化的反应类型是
A. 分解反应 B. 化合反应
C. 氧化反应 D. 置换反应
5.现代社会对能源的需求量越来越大。下列图示中,对环境有污染的发电方式是
1A.太阳能发电 B.风力发电 C.火力发电 D.潮汐发电
6.下列有关碳及其氧化物的说法错误的是
A.CO与CO 可用澄清石灰水鉴别 B.CO具有还原性,可用于铁的冶炼
2
C.金刚石和石墨结构中碳原子排列方式不同 D.CO 的过多排放可导致酸雨的产生
2
7.工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔,其燃烧的化学方
程式 ,则乙炔的化学式是
A. C H B. C H C. CH COOH D. C H
2 4 2 2 3 2 6
8.对于反应M+2N==3P,下列有关叙述正确的是
A.M、N相对分子质量之和一定等于P的相对分子质量
B.生成物P有可能是单质,也可能是化合物
C.M、N中若有一种物质为氧化物,则P一定也是氧化物
D.反应前M、N的质量之和一定不小于反应生成的P的质量
9.下列有关实验现象的描述中,正确的是
A.镁条中滴加稀盐酸后,迅速产生大量气泡,同时试管壁发热
B.高温加热氧化铜与木炭的混合粉,红色粉末变黑,同时产生使澄清石灰水变浑的气体
C.铜片可以在黄铜片表面刻画出清晰的划痕
D.铝丝插入少量硫酸铜溶液中,表面有红色物质出现,最终溶液由蓝色变成浅绿色
10.某气体由氢气、一氧化碳、甲烷中的一种或几种组成。点燃该气体后,在火焰上方罩
一干冷烧杯,烧杯内壁出现水雾。把烧杯迅速倒转过来,注入少量澄清石灰水并振荡,
石灰水变浑浊。下列对该气体组成的推断不正确的是
A. 可能只含有甲烷 B.可能只含有氢气
C.可能只含有氢气和一氧化碳 D.可能三种气体都存在
第一题答题栏:
题号 1 2 3 4 5 6 7 8 9 10
答案
2温馨提示:
请把第二、三、四题的答案答在第 6 页的答题纸上。
二、填空与简答题:(本题包括3小题,共13分)
11.(4分)燃料的发展促进了人类文明的不断进步。
(1)天然气、 ▲ 和煤被称为“化石燃料”。煤燃烧时产生的溶于水形成酸雨的气
体是 ▲ (填序号)。
A. SO B. CO C. CO D. NO
2 2 2
(2)在农村利用秸秆、杂草、人畜粪便等产生的沼气,沼气的主要成分是甲烷,甲烷燃烧的化
学方程式为 ▲ 。
(3)罐装液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等,因此液化
石油气属于 ▲ (“纯净物”或“混合物”) 。
12.(4分)随着人们生活水平的提高,私家车数量不断增加,给人们出行带来很多方便。
(1)目前多数汽车使用的燃料是 ▲ 。
(2)汽车表面喷漆主要是为了防锈,其原理是 ▲ 。
(3)与传统汽车相比,太阳能汽车低碳环保,真正实现了零排放。制造太阳能汽车所用的太
阳能电池需要大量的单质硅。单质硅是由石英固体(SiO)与碳在高温条件下反应制
2
得的,同时生成一种可燃性气体,该反应的化学方程式为 ▲ 。
(4)下列汽车配件及用品中,用合金制作的是(填字母) ▲ 。
a.钢铁外壳 b.玻璃车窗 c.橡胶轮胎 d.真皮座椅
13.(5分)已知A为黑色粉末,B为单质,D为红色单质。A、B、C、D、E五种物质之间的
转化关系下图所示。
A C +澄清石灰水 E↓
高温 ②
①
B D
请回答:
(1)写出下列物质的化学式:A: ▲ C: ▲
(2)写一种由B元素组成的单质的名称: ▲ ;
(3)写出下列反应的化学方程式:
反应①为 ▲ ;
反应②为 ▲ 。
三、实验与探究题:(本题包括2小题,共12分)
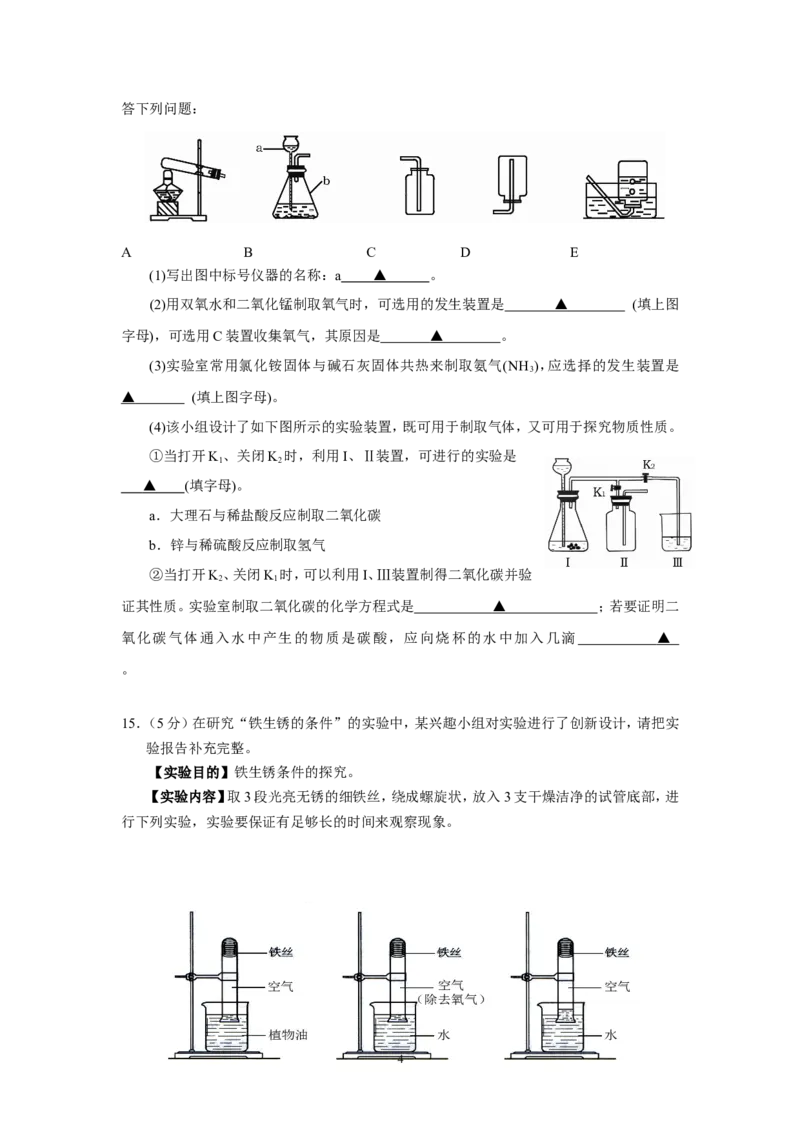
14.(7分)某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质。结合装置图,回
3答下列问题:
A B C D E
(1)写出图中标号仪器的名称:a ▲ 。
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是 ▲ (填上图
字母),可选用C装置收集氧气,其原因是 ▲ 。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH ),应选择的发生装置是
3
▲ (填上图字母)。
(4)该小组设计了如下图所示的实验装置,既可用于制取气体,又可用于探究物质性质。
①当打开K、关闭K 时,利用I、Ⅱ装置,可进行的实验是
1 2
▲ (填字母)。
a.大理石与稀盐酸反应制取二氧化碳
b.锌与稀硫酸反应制取氢气
②当打开K、关闭K 时,可以利用I、Ⅲ装置制得二氧化碳并验
2 1
证其性质。实验室制取二氧化碳的化学方程式是 ▲ ;若要证明二
氧化碳气体通入水中产生的物质是碳酸,应向烧杯的水中加入几滴 ▲
。
15.(5分)在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实
验报告补充完整。
【实验目的】铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进
行下列实验,实验要保证有足够长的时间来观察现象。
空空气气 空空气气 空空气气
((除除去去氧氧气气))
植植物物油油 水水 水水
4实验① 实验② 实验③
【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
【实验结论】铁生锈实际上是铁与空气中的 ▲ (填名称)发生反应的
结果。
【实验思考】
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 ▲ 。
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 ▲ 两种
现象来判断铁丝反应进行的情况。
(3)铝比铁活泼,但铝难腐蚀,原因是 ▲ 。
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什
么合理的建议 ▲ 。(答一点即可)
四、计算题:(本题包括1小题,共5分)
16. (5分)某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g
钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对
烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
(1)反应中产生氢气________▲ _____克。
(2)这种钢样品中铁的含量是多少?(精确到0.1%)
(3)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;
0.6%~2%为高碳钢。假设残留在烧杯中的黑色固体全部是炭,则这种钢属于
________▲ _____。
第二、三、四答题纸:
二、填空与简答题:(本题包括3小题,共13分)
11.(1)__________ _________
二
(2)_______________________________ (3)____________
填
空
与 12.(1)__________ (2)_____________________________
简 (3)___________________________________ (4)________
答
题
13.(1)A______ C_______ (2)_____________
5
(3)①_______________________________ ②______________________________三、实验与探究题:(本题包括2小题,共12分。)
14.(1)__________ (2)________ _________________________
三
(3)_______ (4)①_______
实 ②__________________________________ ______________
验
与
探
究 15.【实验结论】______________
题 【实验思考】(1)________ (2)____________________________
(3)________________________________________________________
(4)_________________________________________
四、计算题:(本题包括1小题,共5分)
16.解:(1)
(2)
(3)
九年级化学试题参考答案与评分建议
一、选择题(本大题共10小题,每小题2分,共20分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C B D A C D B D A B
二、填空与简答题:(本题包括3小题,各小题每空1分,共13分)
11.(1)石油 AD (2)CH+2O CO+2HO (3)混合物
4 2 2 2
12.(1)汽油 (2)隔离金属与氧气和水的接触
6(3)SiO+2C Si+2CO↑ (4)a
2
13.(1)A:CuO ;C:CO (2)金刚石或石墨或C
2 60
(3)①2CuO+C
高温
2 Cu+CO ↑ ;②Ca(OH) +CO ==CaCO ↓+H O
2 2 2 3 2
三、实验与探究题:(本题包括2小题,各小题每空1分,共12分)
14.(1)长颈漏斗 (2)B 氧气的密度比空气大
(3)A (4)①b ②CaCO +2HCl=CaCl +H O+CO↑ 紫色石蕊溶液
3 2 2 2
15. 【实验结论】氧气和水蒸气
【实验思考】(1)1/5(21%)(2)试管内空气体积减小(或试管内液面上升)
(3)易生成一层致密的氧化物保护膜,阻止铝不再被氧化
(4)回收利用(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案
均可)
四、计算题:(本题包括1小题,共5分)
16.(1)0.2 (1分)
(2)设5.7g钢样品中含铁质量为X,则:
Fe + 2HCl ===== FeCl + H↑ (1分)
2 2
56 2
X 0.2g
56︰2== X︰0.2g
X==5.6 g (1分)
则这种钢样品含铁:(5.6 g ÷5.7g)×100%=98.2% (1分)
(3)高碳钢 (1分)
7