文档内容
优秀领先 飞翔梦
想
实验活动 6 酸、碱的化学性质
知识要点 课标要求
1.酸、碱的化学性质(重点) 加深对酸和碱的化学性质的认识
2.体验实验探究的过程(重点) 初步学会实验操作的方法,通过实验解释生活中的一些
现象
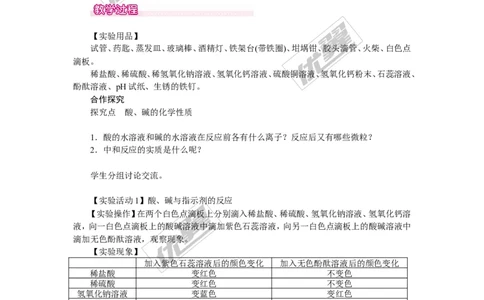
【实验用品】
试管、药匙、蒸发皿、玻璃棒、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管、火柴、白色点
滴板。
稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、
酚酞溶液、pH试纸、生锈的铁钉。
合作探究
探究点 酸、碱的化学性质
1.酸的水溶液和碱的水溶液在反应前各有什么离子?反应后又有哪些微粒?
2.中和反应的实质是什么呢?
学生分组讨论交流。
【实验活动1】酸、碱与指示剂的反应
【实验操作】在两个白色点滴板上分别滴入稀盐酸、稀硫酸、氢氧化钠溶液、氢氧化钙溶
液,向一白色点滴板上的酸碱溶液中滴加紫色石蕊溶液,向另一白色点滴板上的酸碱溶液中
滴加无色酚酞溶液,观察现象。
【实验现象】
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
稀盐酸 变红色 不变色
稀硫酸 变红色 不变色
氢氧化钠溶液 变蓝色 变红色
氢氧化钙溶液 变蓝色 变红色
【实验结论】酸能使紫色的石蕊溶液变成红色,使无色的酚酞溶液不变色;碱能使紫色的
石蕊溶液变成蓝色,使无色的酚酞溶液变成红色。
【实验活动2】酸与金属氧化物的反应
【实验操作】取两个生锈的铁钉放入两支试管中,然后加入约2mL稀盐酸,观察现象。当
观察到铁钉表面的锈去掉变得光亮时,将其中一支试管中的铁钉取出,洗净。继续观察另一
支试管中的现象,过一段时间将铁钉取出,洗净。比较两支铁钉。
【实验现象】①铁锈慢慢消失,溶液由无色慢慢变成黄色;②铁钉表面产生气泡;③后取
出的铁钉变小。
www.youyi100.com
第 1 页 共 2 页优秀领先 飞翔梦
想
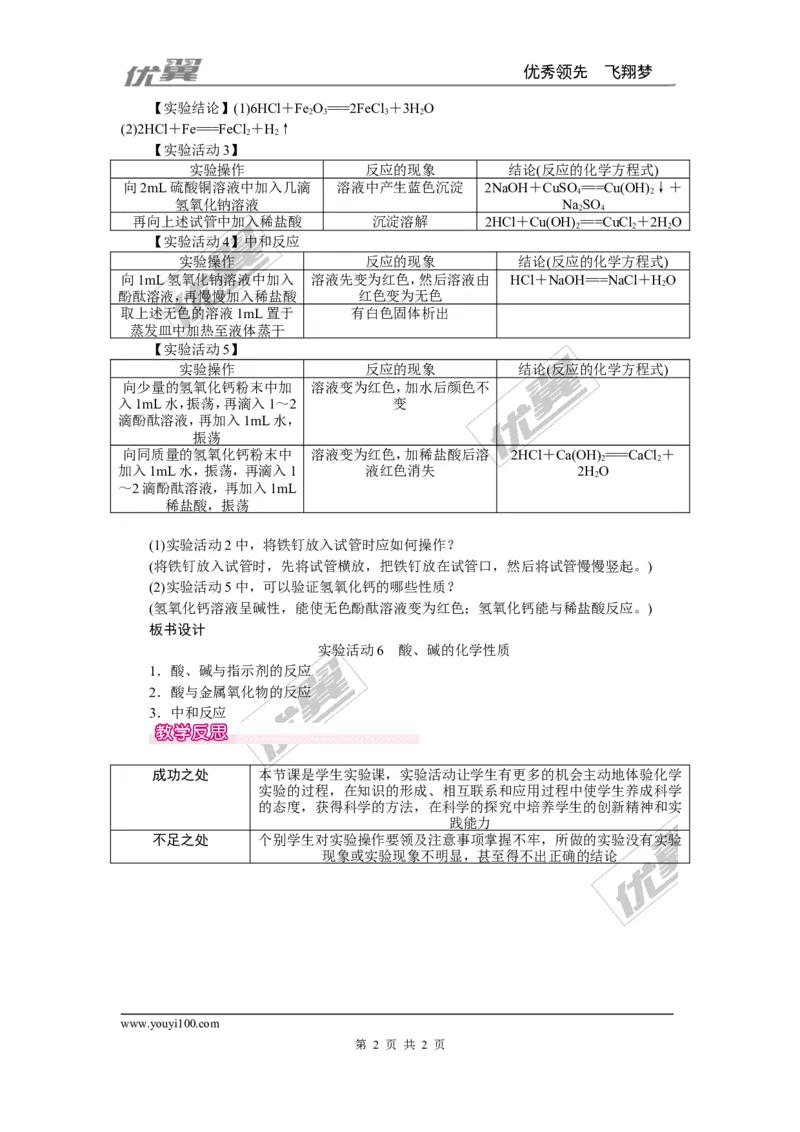
【实验结论】(1)6HCl+Fe O===2FeCl +3HO
2 3 3 2
(2)2HCl+Fe===FeCl +H↑
2 2
【实验活动3】
实验操作 反应的现象 结论(反应的化学方程式)
向2mL硫酸铜溶液中加入几滴 溶液中产生蓝色沉淀 2NaOH+CuSO ===Cu(OH) ↓+
4 2
氢氧化钠溶液 NaSO
2 4
再向上述试管中加入稀盐酸 沉淀溶解 2HCl+Cu(OH) ===CuCl +2HO
2 2 2
【实验活动4】中和反应
实验操作 反应的现象 结论(反应的化学方程式)
向1mL氢氧化钠溶液中加入 溶液先变为红色,然后溶液由 HCl+NaOH===NaCl+HO
2
酚酞溶液,再慢慢加入稀盐酸 红色变为无色
取上述无色的溶液1mL置于 有白色固体析出
蒸发皿中加热至液体蒸干
【实验活动5】
实验操作 反应的现象 结论(反应的化学方程式)
向少量的氢氧化钙粉末中加 溶液变为红色,加水后颜色不
入1mL水,振荡,再滴入1~2 变
滴酚酞溶液,再加入1mL水,
振荡
向同质量的氢氧化钙粉末中 溶液变为红色,加稀盐酸后溶 2HCl+Ca(OH) ===CaCl +
2 2
加入1mL水,振荡,再滴入1 液红色消失 2HO
2
~2滴酚酞溶液,再加入1mL
稀盐酸,振荡
(1)实验活动2中,将铁钉放入试管时应如何操作?
(将铁钉放入试管时,先将试管横放,把铁钉放在试管口,然后将试管慢慢竖起。)
(2)实验活动5中,可以验证氢氧化钙的哪些性质?
(氢氧化钙溶液呈碱性,能使无色酚酞溶液变为红色;氢氧化钙能与稀盐酸反应。)
板书设计
实验活动6 酸、碱的化学性质
1.酸、碱与指示剂的反应
2.酸与金属氧化物的反应
3.中和反应
成功之处 本节课是学生实验课,实验活动让学生有更多的机会主动地体验化学
实验的过程,在知识的形成、相互联系和应用过程中使学生养成科学
的态度,获得科学的方法,在科学的探究中培养学生的创新精神和实
践能力
不足之处 个别学生对实验操作要领及注意事项掌握不牢,所做的实验没有实验
现象或实验现象不明显,甚至得不出正确的结论
www.youyi100.com
第 2 页 共 2 页