文档内容
蚌埠铁路中学 2011----2012 学年第二学期初三期中试卷
化 学
时间:90分钟 满分: 100分
可能用到的相对原子质量 H:1, P:31,C:12, O:16 , Na:23 , S:32
一、选择题(每小题只有一个选项符合题意,本题包括16小题,每小题3分,共48分)
1.以下对氧气性质的叙述,错误的是( )
A.氧气在常温时是一种无色无气味的气体 B.氧气极易溶于水
C.氧气在低温高压时能变为液体或固体 D.氧气是一种化学性质比较活泼的气体
2.某化合物由两种元素组成,它在空气中完全燃烧时,只生成水和二氧化碳。根据质量守恒
定律,该化合物( )
A.由氮元素和氢元素组成 B.由碳元素和氧元素组成
C.由氢元素和氧元素组成 D.由碳元素和氢元素组成
3.第29届奥林匹克运动会将于2008年8月8日在北京举行。下列措施不符合绿色奥运理念
的是:( )
A.奥运场馆周围的路灯采用太阳能光伏发电技术
B.在奥运场地使用电动汽车和新型清洁燃料汽车
C.场馆附近的绿化采用微灌或滴灌智能控制技术
D.将奥运村的生活垃圾全部集中深埋
4. 下列实验操作的方法中正确的是
A. B. C. D.
5.人体吸入的O 有2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝
2
试用NaSeO 清除人体内的活性氧,NaSeO 中Se的化合价为( )
2 3 2 3
A.+2 B.+6 C.+4 D.-2
6. 小红在餐厅看到服务员用盖子熄灭酒精火锅,该灭火方法的主要原理是( )
A.清除可燃物 B.隔绝空气
C.降低可燃物着火点 D.使可燃物的温度降到着火点以下
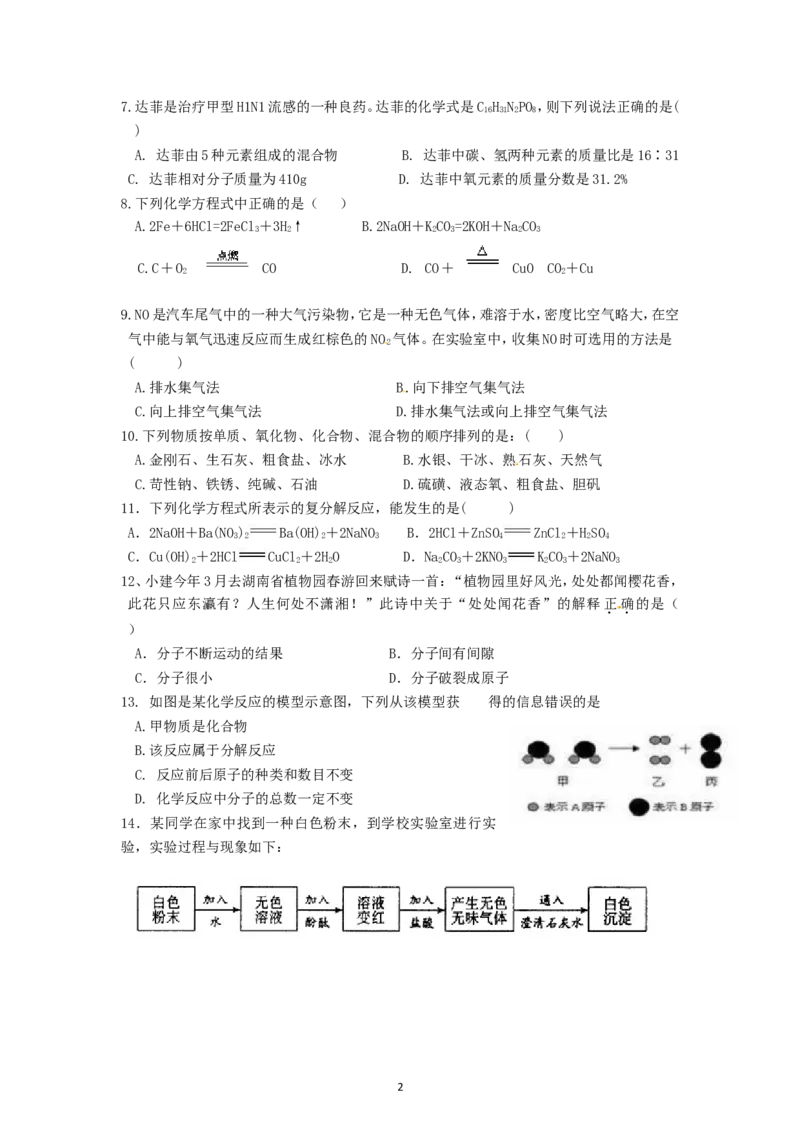
17.达菲是治疗甲型H1N1流感的一种良药。达菲的化学式是C H NPO,则下列说法正确的是(
16 31 2 8
)
A. 达菲由5种元素组成的混合物 B. 达菲中碳、氢两种元素的质量比是16∶31
C. 达菲相对分子质量为410g D. 达菲中氧元素的质量分数是31.2%
8.下列化学方程式中正确的是( )
A.2Fe+6HCl=2FeCl+3H↑ B.2NaOH+KCO=2KOH+NaCO
3 2 2 3 2 3
C.C+O CO D. CO+ CuO CO+Cu
2 2
9.NO是汽车尾气中的一种大气污染物,它是一种无色气体,难溶于水,密度比空气略大,在空
气中能与氧气迅速反应而生成红棕色的NO 气体。在实验室中,收集NO时可选用的方法是
2
( )
A.排水集气法 B.向下排空气集气法
C.向上排空气集气法 D.排水集气法或向上排空气集气法
10.下列物质按单质、氧化物、化合物、混合物的顺序排列的是:( )
A.金刚石、生石灰、粗食盐、冰水 B.水银、干冰、熟石灰、天然气
C.苛性钠、铁锈、纯碱、石油 D.硫磺、液态氧、粗食盐、胆矾
11.下列化学方程式所表示的复分解反应,能发生的是( )
A.2NaOH+Ba(NO) Ba(OH)+2NaNO B.2HCl+ZnSO ZnCl+HSO
3 2 2 3 4 2 2 4
C.Cu(OH)+2HCl CuCl+2HO D.NaCO+2KNO KCO+2NaNO
2 2 2 2 3 3 2 3 3
12、小建今年3月去湖南省植物园春游回来赋诗一首:“植物园里好风光,处处都闻樱花香,
此花只应东瀛有?人生何处不潇湘!”此诗中关于“处处闻花香”的解释正确的是(
)
A.分子不断运动的结果 B.分子间有间隙
C.分子很小 D.分子破裂成原子
13. 如图是某化学反应的模型示意图,下列从该模型获 得的信息错误的是
A.甲物质是化合物
B.该反应属于分解反应
C. 反应前后原子的种类和数目不变
D. 化学反应中分子的总数一定不变
14.某同学在家中找到一种白色粉末,到学校实验室进行实
验,实验过程与现象如下:
2对此粉末成分判断正确的是( )
A.该粉末可能是碳酸钙 B.该粉末可能是碳酸钠或碳酸氢钠
C.该粉末一定是一种碱 D.该粉末中含有熟石灰
15.实验兴趣小组的同学测定一些食物的pH如下表:
食物 牛奶 葡萄 鸡蛋清 苹果 玉米
pH 6 4 8 3 8
根据表中数据判断下列说法正确的是 ( )
A.牛奶和鸡蛋清都显碱性 B.胃酸过多的病人适宜多吃苹果
C.葡萄汁比苹果汁酸性强 D.葡萄汁能使紫色石蕊试液变红
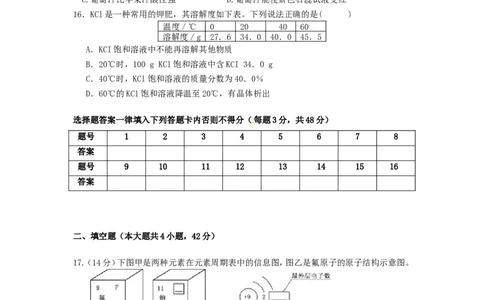
16.KCl是一种常用的钾肥,其溶解度如下表。下列说法正确的是( )
温度/℃ 0 20 40 60
溶解度/g 27.6 34.0 40.0 45.5
A.KCI饱和溶液中不能再溶解其他物质
B.20℃时,100 g KCl饱和溶液中含KCI 34.0 g
C.40℃时,KCl饱和溶液的质量分数为40.0%
D.60℃的KCl饱和溶液降温至20℃,有晶体析出
选择题答案一律填入下列答题卡内否则不得分(每题3分,共48分)
题号 1 2 3 4 5 6 7 8
答案
题号 9 10 11 12 13 14 15 16
答案
二、填空题(本大题共4小题,42分)
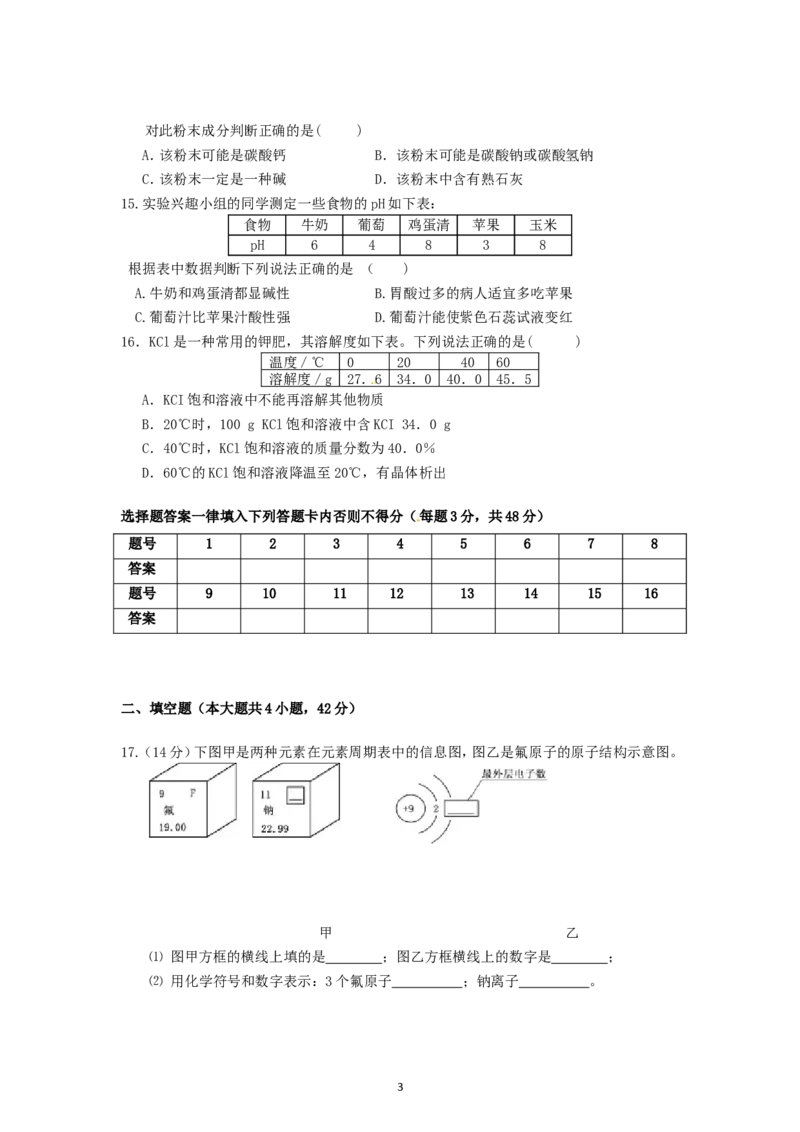
17.(14分)下图甲是两种元素在元素周期表中的信息图,图乙是氟原子的原子结构示意图。
甲 乙
⑴ 图甲方框的横线上填的是 ;图乙方框横线上的数字是 ;
⑵ 用化学符号和数字表示:3个氟原子 ;钠离子 。
3⑶ 钠元素属于 (填“金属”或“非金属”)元素;图甲所示两种元素形成化
物的化学式为 ,其中Na元素的质量分数为 。(精确到0.1%)
18.(8分)人体缺乏维生素C(简写“VC”)就会患坏血病,哥伦布探险时的许多船员就因此
而死亡。右图所示为某种“维生素C”说明书的一部分。请你回答:
⑴ 若正常成人每天对“VC”的最低需要量为60mg。
①当“VC”完全来自右图的“维生素 C”,则每天至少服用 __
次;
②当“VC”完全来自某种新鲜蔬菜(每1000g这种蔬菜含“VC”
120mg),则每天至少应食用这种蔬菜 g。
⑵ 取2片“维生素C”溶于水,滴入紫色石蕊溶液变红色,说
明“VC”的溶液显 性;加热该溶液至沸腾,红色消失,
表明“VC”受热时易被破坏,那么在烹调新鲜蔬菜时要减少“VC”的损失,应采取
的措施之一是 。
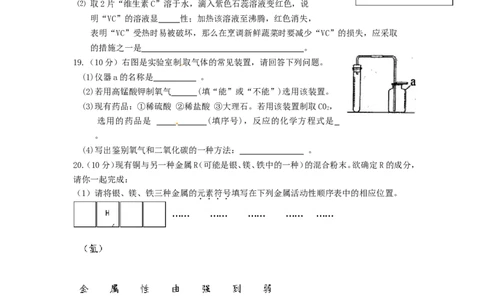
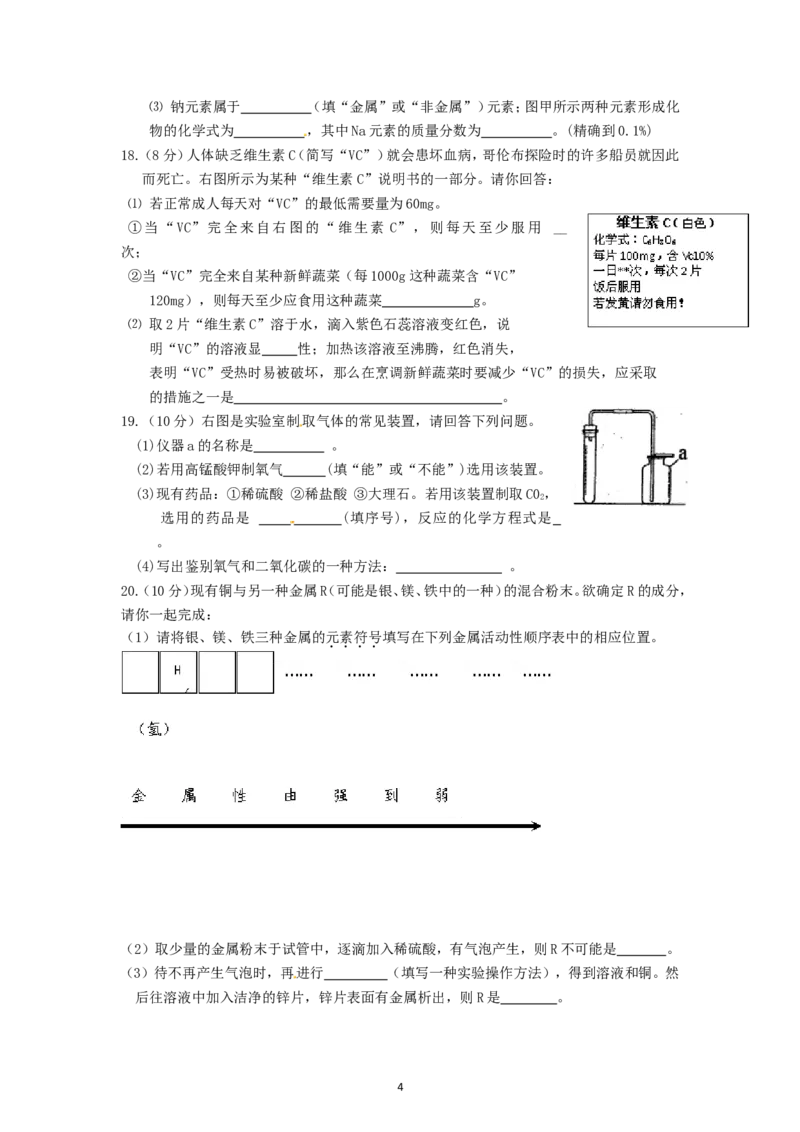
19.(10分)右图是实验室制取气体的常见装置,请回答下列问题。
(1)仪器a的名称是 。
(2)若用高锰酸钾制氧气 (填“能”或“不能”)选用该装置。
(3)现有药品:①稀硫酸 ②稀盐酸 ③大理石。若用该装置制取C0,
2
选用的药品是 (填序号),反应的化学方程式是
。
(4)写出鉴别氧气和二氧化碳的一种方法: 。
20.(10分)现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末。欲确定R的成分,
请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置。
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是 。
(3)待不再产生气泡时,再进行 (填写一种实验操作方法),得到溶液和铜。然
后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 。
4(4)写出金属R与稀硫酸反应的化学方程式 。该反
应的基本类型属于 (选填“化合”、“分解”、“置换”或“复分解”)反应。
三、计数题(本大题共2题共10分)。
21、20℃时,将50g NaCl放入100g水中,充分搅拌后所得NaCl溶液的溶质质量分数是多少?
(4分) (20℃时NaCl的溶解度为36g)
22.(6分)向50.0g 8.O%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液
pH=7.
(1)求反应前氢氧化钠溶液中溶质的质量 (2)求反应后生成硫酸钠的质量
5蚌埠铁路中学2011----2012学年第二学期期中考试
初三化学答案
选择题答案一律填入下列答题卡内否则不得分(每题3分,共48分)
题号 1 2 3 4 5 6 7 8
答案 B D D A C B C D
题号 9 10 11 12 13 14 15 16
答案 A B C A D B D D
17. ①Na 7 ②3F Na+ ③金属 NaF 54.8%
18. ⑴① 3 ②500 ⑵ 酸 凉拌生食、或少加食醋、或不要高温爆炒、或不要煮过
长时间(凡合理答案均给分)。
19. (1)集气瓶 (2)不能 (3)②③
(4)CaCO + 2HCl = CaCl+CO↑ +HO
3 2 2 2
20、(1)(每小格各1分,共3分)
(2)银(或Ag)
(3)过滤;铁(或Fe)
(4)Fe + HSO = FeSO + H↑;置换
2 4 4 2
21解析:由溶解度概念知,20℃时100g水中最多能溶解36g NaCl,而题目却给出了50g,很
显 然 NaCl 未 完 全 溶 解 , 溶 液 已 达 到 饱 和 。 故 该 溶 液 中 NaCl 的 质 量 分 数
22. (1)4克 (2)7.1克
6