文档内容
第八章 化学与可持续发展
单元知识清单
【知识导引】
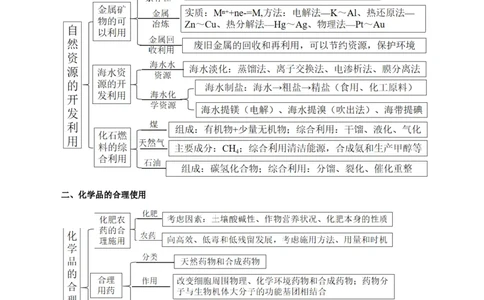
一、自然资源的开发利用
二、化学品的合理使用
三、环境保护与绿色化学
、【知识清单】
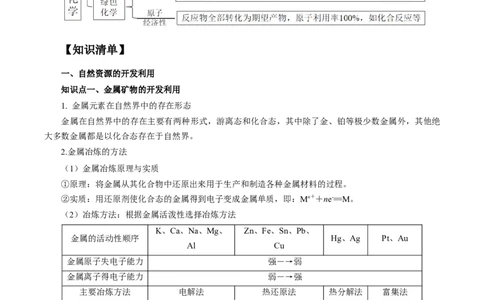
一、自然资源的开发利用
知识点一、金属矿物的开发利用
1. 金属元素在自然界中的存在形态
金属在自然界中的存在主要有两种形式,游离态和化合态,其中除了金、铂等极少数金属外,其他绝
大多数金属都是以化合态存在于自然界。
2.金属冶炼的方法
(1)金属冶炼原理与实质
①原理:将金属从其化合物中还原出来用于生产和制造各种金属材料的过程。
②实质:用还原剂使化合态的金属得到电子变成金属单质,即:Mn++ne-==M。
(2)冶炼方法:根据金属活泼性选择冶炼方法
K、Ca、Na、Mg、 Zn、Fe、Sn、Pb、
金属的活动性顺序 Hg、Ag Pt、Au
Al Cu
金属原子失电子能力 强―→弱
金属离子得电子能力 弱―→强
主要冶炼方法 电解法 热还原法 热分解法 富集法
还原剂或 强大电流 H、CO、C、 物理方法或
2
加热
特殊措施 提供电子 Al等加热 化学方法
①电解法:冶炼活泼金属(K→Al)
2NaCl(熔融) =====2Na+Cl↑
2
MgCl (熔融) =====Mg+Cl↑
2 2
2Al O(熔融) =====4Al+3O↑(冰晶石的作用为助溶剂,降低Al O 的熔点)
2 3 2 2 3
注意:①用电解法冶炼较活泼金属时,电解的是熔融的金属化合物,而不是金属化合物的水溶液。因
为在其水溶液中,阴极放电的是H+,而不是金属阳离子,故得不到金属单质。②工业上采用电解法冶炼铝和镁的原料分别为Al O 和MgCl ,而不是AlCl 和MgO。
2 3 2 3
原因:AlCl 是共价化合物,熔融时不导电;而MgO虽然是离子化合物,但其熔点太高,熔化时会消
3
耗大量的电能,成本较高。
③钾在实际生产中不用电解法,因为实际生产中用石墨电极,熔融的金属钾能渗透到石墨中,侵蚀电
极。还有钾太容易溶解在熔融的氯化钾中,以致钾不能浮在电解槽的上部加以分离收集;同时,还因为钾
在操作温度下迅速气化,增加了不安全因素。所以现在金属钾的生产方法都采用金属钠与氯化钾的反应。
②热还原法:冶炼中等活泼金属(Zn→Cu),常用的还原剂有焦炭、CO、H、一些活泼金属等
2
高炉炼铁:Fe O+3CO\o(\s\up6(_____)2Fe + 3CO ↑
2 3 2
铝热反应:2Al+Fe O ===== Al O+2Fe
2 3 2 3
注意:①铝热反应是利用铝的强还原性,在高温下将相对不活泼且熔点高的金属从其氧化物中还原出
来。故只有Al和比Al不活泼的金属形成的氧化物所组成的混合物才能称之为铝热剂。如 Al和MgO组成
的混合物不能称之为铝热剂。
②铝热反应实验注意问题:
A.镁带要打磨净表面的氧化膜,否则难以点燃。
B.氧化铁粉末要干燥,铝粉没有被氧化,否则难以反应。
C.要保证纸漏斗重叠时四周均为四层,且内层纸漏斗一定要用水润湿,以防高温物质从四周溅出。
D.因为铝热反应是一个典型的放热反应,反应中放出的大量热量能够使铁熔化,所以要垫细沙,这样
做的目的一是防止蒸发皿炸裂,二是防止熔融的金属溅出伤人。
E.实验装置应远离人群和易燃物。
③热分解法:冶炼不活泼金属(Hg、Ag)
2HgO ===== 2Hg+O↑
2
2Ag O ===== 4Ag+O↑
2 2
④其他方法:湿法炼铜——Fe+CuSO === FeSO +Cu
4 4
火法炼铜——Cu S+O ===== 2Cu+SO
2 2 2
注意:①最不活泼的金属(如Pt、Au)用物理方法获得。
②工业上金属冶炼一般分三个步骤:矿石富集(除杂、提高矿石中有效成分含量)→金属冶炼(适当
还原剂将金属化合物还原成金属单质)→金属精炼(加如试剂除杂或电解精炼,得纯金属)。
3.金属的回收和资源保护
(1)提高金属矿物的利用率;
(2)开发环保高效的金属冶炼方法;
(3)防止金属的腐蚀;
(4)使用其他材料代替金属材料,减少金属的使用量;
(5)加强废旧金属的回收和再利用。知识点二、海水资源的开发利用
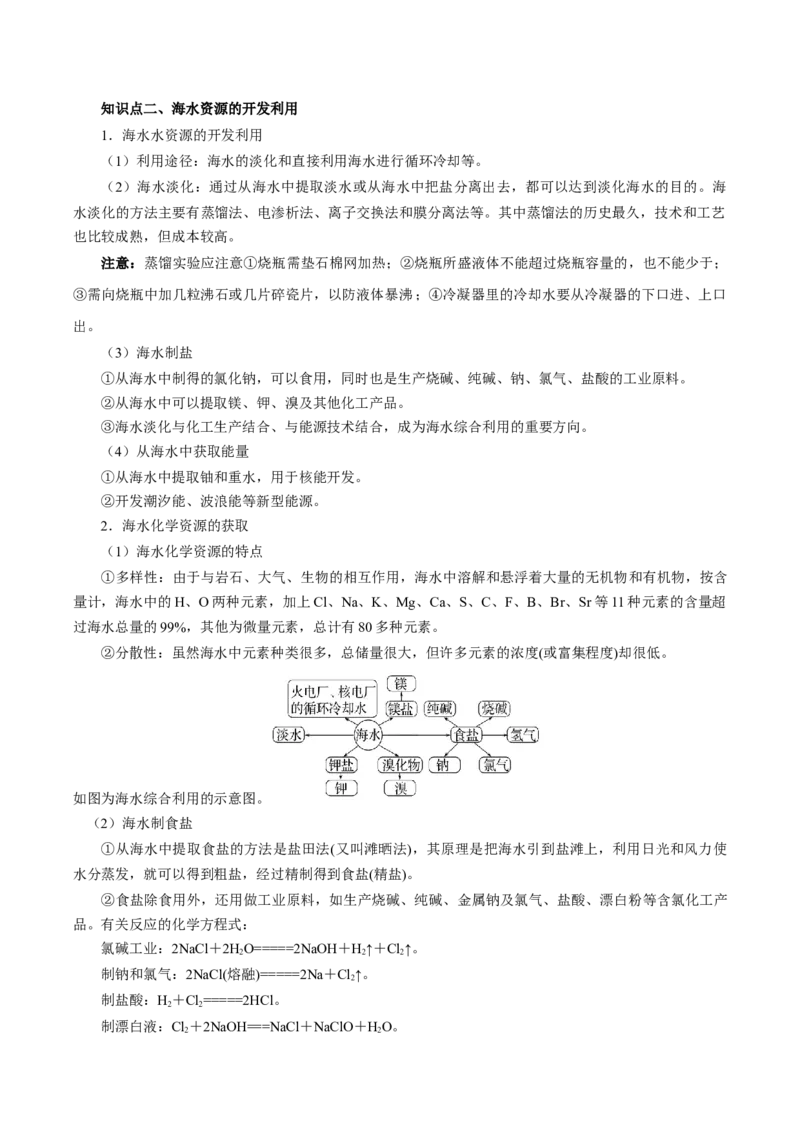
1.海水水资源的开发利用
(1)利用途径:海水的淡化和直接利用海水进行循环冷却等。
(2)海水淡化:通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。海
水淡化的方法主要有蒸馏法、电渗析法、离子交换法和膜分离法等。其中蒸馏法的历史最久,技术和工艺
也比较成熟,但成本较高。
注意:蒸馏实验应注意①烧瓶需垫石棉网加热;②烧瓶所盛液体不能超过烧瓶容量的,也不能少于;
③需向烧瓶中加几粒沸石或几片碎瓷片,以防液体暴沸;④冷凝器里的冷却水要从冷凝器的下口进、上口
出。
(3)海水制盐
①从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸的工业原料。
②从海水中可以提取镁、钾、溴及其他化工产品。
③海水淡化与化工生产结合、与能源技术结合,成为海水综合利用的重要方向。
(4)从海水中获取能量
①从海水中提取铀和重水,用于核能开发。
②开发潮汐能、波浪能等新型能源。
2.海水化学资源的获取
(1)海水化学资源的特点
①多样性:由于与岩石、大气、生物的相互作用,海水中溶解和悬浮着大量的无机物和有机物,按含
量计,海水中的H、O两种元素,加上Cl、Na、K、Mg、Ca、S、C、F、B、Br、Sr等11种元素的含量超
过海水总量的99%,其他为微量元素,总计有80多种元素。
②分散性:虽然海水中元素种类很多,总储量很大,但许多元素的浓度(或富集程度)却很低。
如图为海水综合利用的示意图。
(2)海水制食盐
①从海水中提取食盐的方法是盐田法(又叫滩晒法),其原理是把海水引到盐滩上,利用日光和风力使
水分蒸发,就可以得到粗盐,经过精制得到食盐(精盐)。
②食盐除食用外,还用做工业原料,如生产烧碱、纯碱、金属钠及氯气、盐酸、漂白粉等含氯化工产
品。有关反应的化学方程式:
氯碱工业:2NaCl+2HO=====2NaOH+H↑+Cl↑。
2 2 2
制钠和氯气:2NaCl(熔融)=====2Na+Cl↑。
2
制盐酸:H+Cl=====2HCl。
2 2
制漂白液:Cl+2NaOH===NaCl+NaClO+HO。
2 2制漂白粉:2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO。
2 2 2 2 2
侯氏制碱法:NaCl+NH +HO+CO===NaHCO↓+NH Cl
3 2 2 3 4
NaHCO 分解:NaHCO === Na CO + H O + CO
3 3 2 3 2 2
(3)从海水中制取镁、溴及其化工产品。
①海水中镁的提取流程:
主要化学反应: CaCO =====CaO+CO↑、CaO+HO===Ca(OH) ;
3 2 2 2
Ca(OH) +MgCl ===Mg(OH) ↓+CaCl
2 2 2 2
Mg(OH) +2HCl===MgCl +2HO、MgCl ·6H O MgCl +6H O;
2 2 2 2 2 2 2
MgCl (熔融)=====Mg+Cl↑。
2 2
注意:氯化镁溶液中结晶得到的晶体是MgCl ·6HO而不是无水MgCl ,MgCl ·6HO加热脱水通常在
2 2 2 2 2
氯化氢气流中进行。
②海水中溴的提取流程:
主要化学反应: Cl+2Br-===2Cl-+Br ;
2 2
Br +SO +2HO===H SO +2HBr。
2 2 2 2 4
注意:海水中溴的含量很小,需加热浓缩,富集Br-;再者海水呈碱性,会与Cl 反应,因此在通Cl
2 2
前,需将海水进行酸化处理。
知识点三、煤、石油和天然气的综合利用
1.煤的组成及其综合利用
(1)煤的组成:煤是由 有机物 和少量 无机物 组成的复杂混合物,其组成以 碳元素 为
主,还含有少量氢、氧、氮、硫 等元素。
(2)煤的综合利用:煤的综合利用的主要途径是煤的干馏、煤的气化和液化,目的是获得洁净的燃
料和多种化工原料。
①煤的干馏:将煤隔绝空气加强热使之分解的过程,也叫煤的焦化。煤的干馏产品 主要成分及名称 主要用途
气态 焦炉气、粗氨水、粗苯 燃料、化肥、炸药、医药、农药、合成材料
液态 煤焦油:苯、甲苯、二 炸药、医药、农药、合成材料、染料、筑路材
甲苯、酚类、萘、沥青 料、制碳素电极
固态 碳 冶金、合成氨造气、电石、燃料
②煤的气化:将其转化为可燃性气体的过程C + H O(g)\o(\s\up6(_____) CO + H 。
2 2
③煤的液化:通过直接液化或间接液化转化为液体燃料的过程CO + 2H =====CHOH。
2 3
注意:①煤的干馏发生复杂的物理和化学变化,煤的气化、液化都是化学变化。
②煤中不含苯、甲苯等芳香烃,这些芳香烃可通过煤干馏后得到的煤焦油进行分馏得到。
2.天然气的组成及其综合利用
(1)天然气的主要成分是CH,是一种清洁的化石燃料。
4
(2)综合利用:重要的化工原料,主要用于合成氨及生产甲醇等。
催化剂 催化剂
CH+HO CO +3H、CO +2H CHOH。
4 2 2 2 3
(3)可燃冰:天然气水合物是天然气与水在高压、低温条件下形成的类冰状结晶物质,其组成可表示
为CH·nH O,甲烷分子处于由多个水分子形成的笼中。外观像冰,具有可燃性,故又被称为“可燃冰”,
4 2
它被认为是21世纪的高效清洁能源。
3.石油的组成及其综合利用
(1)石油的组成:石油主要是由多种碳氢化合物化合物组成的混合物。
(2)石油的综合利用:分馏、裂化、裂解和催化重整等。
加工方法 定义 主要原料 主要产品或原理
常压分馏 通过加热和冷凝方法,把石油 石油 汽油、煤油、柴油、重油
分离成不同沸点范围内的产物
减压分馏 的过程。 重油 柴油、润滑油、燃料油、沥青、石蜡
在一定条件下,把相对分子质 碳原子数较多的烷烃、烯烃。
量大、沸点高的烃断裂为相对
裂化 烷烃
分子质量小、沸点低的烃的过 催化剂
程。 C 16 H 34 加 热 、 加 压 C 8 H 18 +C 8 H 16
乙烯、丙烯、甲烷
催化剂
采用比裂化更高的温度,使石 C H C H +C H
8 18 4 10 4 8
加热、加压
油分馏产品中长链的烃分裂成
裂解 烷烃
乙烯、丙烯等小分子的过程。
催化剂
即深度裂化。 C H CH+C H
4 10 加 热 、 加 压 4 3 6
催化剂
C H C H+C H
4 10 加 热 、 加 压 2 6 2 4
链状烃 环状烃(苯、甲苯等芳香烃)
在加热和催化剂的作用下,使
催化重整
链状烃发生结构的重新调整而转化为环状烃的过程。
注意:①石油分馏为物理变化,石油裂化、裂解都是化学变化。
②直馏汽油和裂化汽油的成分不同,性质有明显的区别——直馏汽油的成分为饱和烃,裂化汽油为饱
和烃和不饱和烃的混合物,故裂化汽油可以发生加成反应,可使酸性高锰酸钾溶液和溴水褪色。
③石油裂化的目的是提高轻质油的产量,石油裂解的目的是获得气态短链不饱和烃作化工原料。
4.以煤、石油和天然气为原料生产合成材料
(1)三大合成高分子材料:塑料、合成橡胶、合成纤维,这三大合成高分子材料主要是以煤、石
油、天然气为原料生产的。高分子化合物有天然的,如蛋白质、纤维素、淀粉等;也有人工合成的,如聚
乙烯等。
(2)合成高分子化合物的常见反应类型
①加聚反应:由许多小分子经过加成反应合成 高分子化合物的反应称为加成聚合反应,简称加聚反
应。
丙烯制聚丙烯:
②缩聚反应:由许多小分子经过缩合反应合成高分子化合物的同时生成许多小分子的反应称为缩合聚
合反应,简称缩聚反应。例如获得聚对苯二甲酸乙二酯:
二、化学品的合理使用
知识点一、化肥、农药的合理施用
1.化学品分类:化学品可分为大宗化学品和精细化学品两大类。如乙烯、硫酸、纯碱和化肥等属于
大宗化学品,医药、农药、日用化学品、食品添加剂等属于精细化学品。
2.化肥的合理施用
(1)考虑因素:土壤酸碱性、作物营养状况、化肥本身性质。
(2)应用实例:硝酸铵是一种高效氮肥,但受热或经撞击易发生爆炸,必须作改性处理后才能施
用;如将草木灰与铵态氮肥混合施用,肥效降低。
(3)过量施用化肥的危害
①很多化肥易溶于水,过量施用造成浪费。
②部分化肥随着雨水流入河流和湖泊,造成水体富营养化,产生水华等污染。
③不合理施用化肥会影响土壤的酸碱性和土壤结构。
(4)各类化肥的作用
①氮肥:能促使作物的茎、叶生长茂盛,叶色浓绿。②磷肥:能促进作物根系发达,增强抗寒抗旱能力,还能促进作物提早成熟,穗粒增多,籽粒饱满。
③钾肥:能促进作物生长健壮,茎秆粗硬,增强对病虫害和倒伏的抵抗能力,并能促进糖分和淀粉的
生成。
注意:①硝酸钾、硝酸铵受撞击时易发生爆炸,在使用时千万不能进行敲、砸等猛力撞击。
②铵态氮肥使用时要低温保存,深施盖土,避免受热;铵态氮肥不可以跟碱性物质(如草木灰等)混合
使用。
3.农药的安全使用
(1)农药的发展过程:早期农药有除虫菊、烟草等植物和波尔多液、石灰硫黄合剂等无机物。现在
人们研制出了有机氯农药、有机磷农药、氨基甲酸酯和拟除虫菊酯类农药等有机合成农药。
(2)发展方向:高效、低毒和低残留。
(3)安全使用措施:做好农药的保管工作;喷洒农药时注意个人安全的防护;不要采摘和食用刚喷
洒过农药的果实和蔬菜;洗涤瓜果时可将其放在水中浸泡几分钟除去残留的农药;若发生农药中毒,应立
即清除毒物并送医院治疗。
注意:①使用气雾型农药时,勿接近火源,不可存放在冰箱里,不可朝电器喷射。
②使用农药时应避免误食,防止与皮肤接触,减少对呼吸道的刺激。
③不要采摘和食用刚喷洒过农药水果、蔬菜,水果、蔬菜在洗涤时应先放入水中浸泡几分钟,以除去
残留农药。
④敌敌畏或甲胺磷农药都是酯类物质,若在使用过程中不慎接触了敌敌畏或甲胺磷农药,立即用肥皂
反复擦洗可避免中毒。
知识点二、合理用药
1.药物的分类:药物按来源分为天然药物与合成药物。
2.药物的作用机理
(1)有的药物通过改变机体细胞周围的物理、化学环境而发挥药效,如抗酸药。
(2)更多药物通过药物分子与机体生物大分子的功能基团结合而发挥药效,其分子结构与生物活性
密切相关。
(3)阿司匹林
①阿司匹林化学名称是乙酰水杨酸,具有解热镇痛作用。
②以水杨酸为原料制取阿司匹林的化学方程式为:
注意:长期服用阿司匹林会导致胃痛、头痛、眩晕、恶心等不适症状。
3.合理使用药物:
(1)在医生、药师指导下,遵循安全、有效、经济、适当的原则合理用药。滥用药物危害巨大,如无处方长期服用安眠药或镇静剂;滥用抗生素;服用兴奋剂等。
(2)不能滥用药物:大部分药物都有毒副作用,应在医生指导下使用,不可滥用,滥用药物主要是
指非法获得及使用受管制药物、无医生处方长期服用安眠药或镇静剂、运动员服用兴奋剂、服用毒品等。
(3)处方药和非处方药
①标识:处方药符号:Rx,非处方药其包装上有“OTC”。
②使用:处方药是需要凭医生处方才能从药房或药店获得,并要在医生的指导下使用的药物。非处方
药是不需要凭医生处方,消费者可自行购买和使用的药物。
(4)避免药物依赖、远离毒品
①毒品的概念:毒品是指由于非医疗目的而反复连续使用,能够产生依赖性即成瘾性的药品。
②远离毒品:吸毒危害巨大,人们一定要远离毒品。
注意:不是所有能与盐酸反应的物质都可以作为抗酸药,理论上能与盐酸反应的物质可降低胃酸的浓
度,但具体选择物质时要考虑物质对胃的刺激性、灼伤性及与胃酸反应后产物的毒性。如 NaCO 碱性太
2 3
强;BaCO 与盐酸反应生成的重金属离子Ba2+会使人中毒等。
3
知识点三、安全使用食品添加剂
1.功能及使用
(1)功能:食品添加剂可以改善食品品质和色、香、味,以及防腐、保鲜等,食品添加剂的使用满
足了人们对食品多样化的需求。
(2)使用:在规定范围内合理使用食品添加剂,对人体健康不会产生不良影响,但违规使用或者超
量使用食品添加剂都会损害人体健康。
2.作用及分类
类别 作用 品种
天然色素如红曲红、胡萝卜素、姜黄、叶绿素铜钠
着色剂 改善食品色泽
盐、焦糖色等;合成色素如柠檬黄、苋菜红、靛蓝等
增味剂 增加食品鲜味 味精等
膨松剂 使食品松软或酥脆 碳酸氢铵、碳酸氢钠等
凝固剂 改善食品形态 盐卤、葡萄糖酸-δ-内酯等
防腐剂 防止食品腐败变质 苯甲酸及其钠盐、山梨酸及其钾盐、亚硝酸钠
抗氧化剂 防止食品因氧化而变质 抗坏血酸(即维生素C)等
营养强化剂 补充必要的营养成分 碘酸钾、维生素、碳酸钙、硫酸亚铁、硫酸锌
注意:①使用食品添加剂时,要严格按照国家规定的标准,任何违背国家标准的行为,都是违法的,
更不准把国家列为违禁物的物质当作食品添加剂在食品中使用。
②“食品添加剂”与“绿色食品”的关系:食品添加剂的使用和“绿色食品”不相违背。只要在合理
的限量范围内使用,就不会对人体构成伤害。“绿色食品”是指无公害的食品,要求生产食品的环境好,食品的生产过程遵守国家有关规定,产品经过专门检测,包装、储存、运输等过程也要严格按照有关标准
进行。
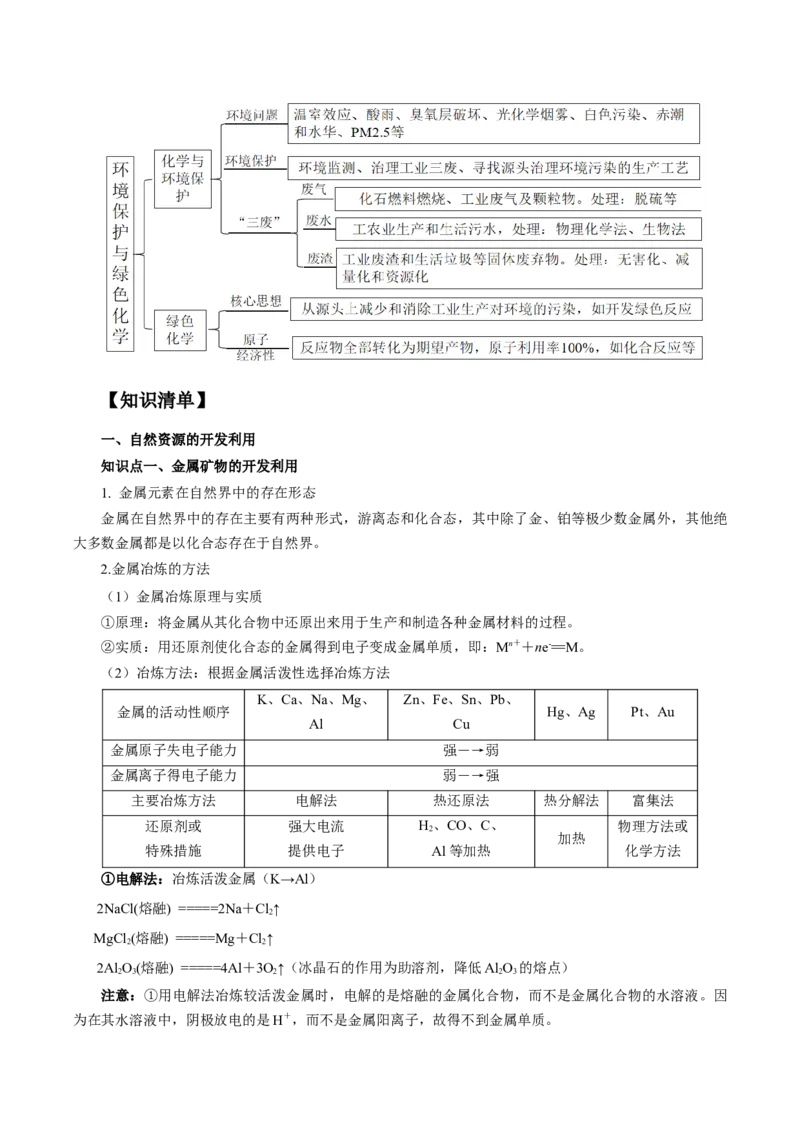
三、环境保护与绿色化学
知识点一、化学与环境保护
1.环境保护
(1)环境问题:主要是指由于人类不合理地开发和利用自然资源而造成的生态环境破坏,以及工农
业生产和人类生活所造成的环境污染。
环境问题 主要污染物 主要危害
温室效应 CO 造成全球气候变暖,水位上升,陆地面积减小等
2
酸雨 SO 、NO 土壤酸化、水源污染、建筑物被腐蚀等
2 x
到达地球表面的紫外线明显增多,给人类健康及生态环境
臭氧层破坏 氟氯代烷、NO
x
带来多方面危害
光化学烟雾 碳氢化合物、NO 刺激人体器官,特别是人的呼吸系统,使人生病甚至死亡
x
①在土壤中影响农作物吸收水分和养分,导致农作物减
产。
白色污染 废弃塑料制品
②混入生活垃圾中难处理、难回收。
③易被动物当作食物吞入,导致动物死亡
废水中含氮、磷元 使水体富营养化,导致水中藻类疯长,消耗水中溶解的
赤潮和水华
素的营养物质 氧,使水体变得浑浊、水质恶化
PM2.5 颗粒物 污染空气,形成雾霾天气,增加交通事故,危害人体健康
(2)环境保护的任务
①环境监测:对污染物的存在形态、含量等进行分析和鉴定,提供可靠的分析数据。
②治理工业三废:废水、废气、废渣。
③寻找源头治理环境污染的生产工艺:杜绝污染物的排放,能从根本上解决环境问题。
2.“三废”污染及防治
(1)大气污染及防治
①污染物主要来源:除了自然因素外,大气污染物主要来自化石燃料的燃烧和工业生产过程产生的废
气及其携带的颗粒物。
②次生污染物的形成: 。
③防治措施:用CaCO 、CaO、Ca(OH) 、NH 等吸收脱硫生成CaSO 及(NH )SO 等、用CH 、H 等
3 2 3 4 4 2 3 4 2
在Pt、Pd等的催化作用下将氮氧化物还原为N 和HO等。
2 2(2)废水的处理方法
①常用的污水处理方法有物理法、化学法和生物法等。
②污水处理的常用化学方法中和法、氧化还原法、沉淀法等。
③污水处理的流程
一级处理:通常采用物理方法,即用格栅间、沉淀池等除去污水中不溶性的污染物。经一级处理后的
水一般达不到排放标准,一级处理作为预处理。
二级处理:采用生物方法(又称微生物法)及某些化学方法,除去水中的可降解有机物等污染物。经二
级处理后的水一般可以达到国家规定的排放标准。
三级处理:主要采用化学沉淀法、氧化还原法、离子交换法和反渗透法等,对污水进行深度处理和净
化。经三级处理后水可用于绿化和景观用水等。
(3)固体废弃物的处理
工业废渣和生活垃圾等固体废物的处理应遵循无害化、减量化和资源化的原则,达到减少环境污染和
资源回收利用这两个重要目的。
知识点二、绿色化学
1.绿色化学
(1)概念:“绿色化学”也称环境友好化学,其核心思想就是改变“先污染后治理”的观念和做
法,利用化学原理和技术手段,减少或消除产品在生产和应用中涉及的有害化学物质,实现 从源头上
减少和消除环境污染。
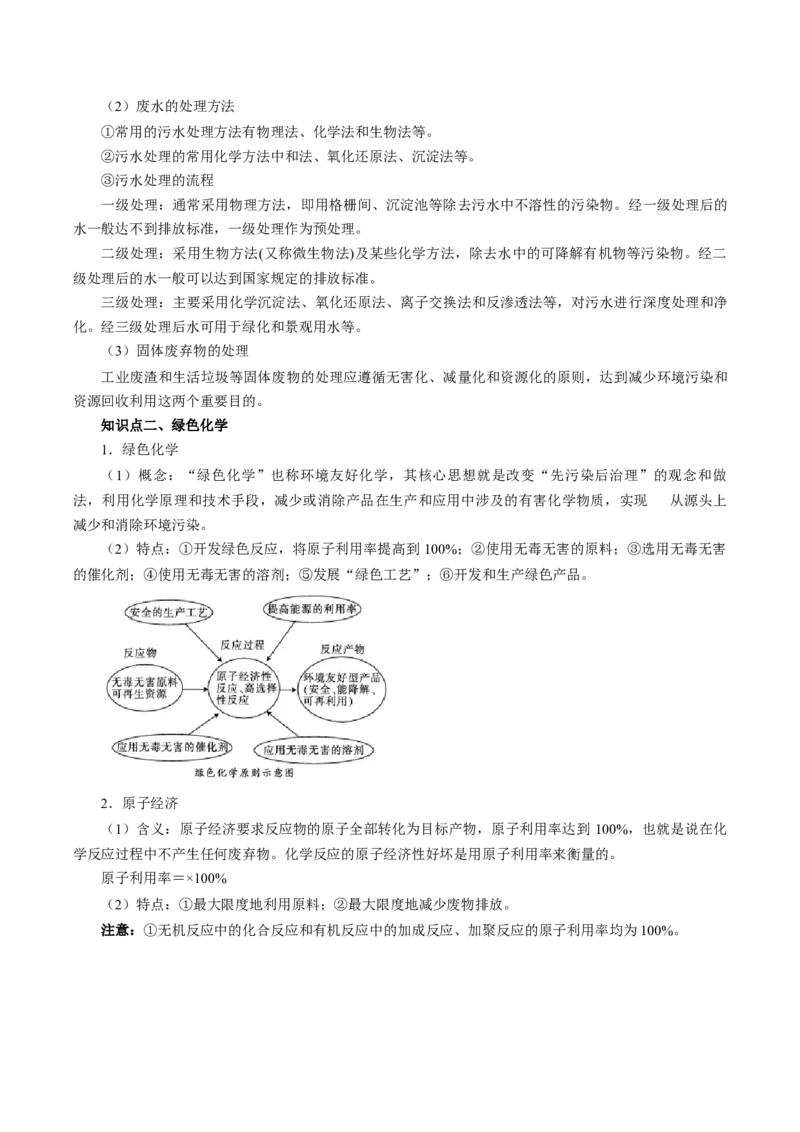
(2)特点:①开发绿色反应,将原子利用率提高到 100%;②使用无毒无害的原料;③选用无毒无害
的催化剂;④使用无毒无害的溶剂;⑤发展“绿色工艺”;⑥开发和生产绿色产品。
2.原子经济
(1)含义:原子经济要求反应物的原子全部转化为目标产物,原子利用率达到 100%,也就是说在化
学反应过程中不产生任何废弃物。化学反应的原子经济性好坏是用原子利用率来衡量的。
原子利用率=×100%
(2)特点:①最大限度地利用原料;②最大限度地减少废物排放。
注意:①无机反应中的化合反应和有机反应中的加成反应、加聚反应的原子利用率均为100%。