文档内容
湖南省邵阳市邵阳县2017-2018学年九年级上学期化学期末考试试卷
一、单选题
1.下列变化属于物理变化的是( )
A. 纸张燃烧 B. 食物腐烂
C. 粮食酿酒 D. 湿衣服晾干
2.空气成分中,体积分数最大的是 ( )
A. 氧气 B. 氮
气 C. 二氧化
碳 D. 稀有气体
3.地壳中含量最多的元素是( )
A. 氧 B.
硅 C.
铝 D. 铁
4.下列物质在氧气中燃烧,产生大量白烟的是( )
A. 红磷 B. 木炭
C. 甲烷
D. 铁丝
5.1991年,我国化学家张青莲与另一位科学家合作,测定了铟(In)元素的相对原子质量新值.铟元素的
核电荷数为49,相对原子质量为115.铟原子的核外电子数为( )
A. 115 B. 49 C. 66 D. 164
6.决定元素种类的是( )
A. 质子数 B. 电子数
C. 中子数
D. 最外层电子数
7.意大利科学家率先合成了一种新型的氧分子﹣﹣O 分子,对其说法正确的是( )
4
A. 它是一种化合物 B. 它是一种单质 C. 它是由O 组成的混合
2
物 D. 它的氧化性比O 差
2
8.已知反应3A+2B=2C+D,B,A 两物质完全反应时质量比为4:3.若生成C和D共140克,则反应消耗B
的质量为( )
A. 120 克 B. 100
克 C. 80
克 D. 60克
9.维生素C的化学式是C H O 。下列关于维生素C的说法正确的是( )
6 8 6
A. 属于氧化物
B. 相对分子质量为176gC. 由三种元素组成
D. 碳、氢、氧元素的质量比为3:4:3
10.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH) 、碳粉、氧化铁等涂覆在铝箔上制成。Ni
2
(OH) 中Ni的化合价为( )
2
A. +1 B. +2 C. +3 D. +4
11.下列说法有科学错误的是( )
A. 生铁不含铁 B. 铅笔不是
铅 C. 纯碱不是
碱 D. 白开水不是白色
12.下列物质属于纯净物的是( )
A. 粗盐 B. 生铁
C. 石灰石
D. 液氧
13.下列叙述中,错误的是( )
A. 分子是保持物质化学性质的最小粒子,在化学变化中可以再分 B. 铁在氧气中
燃烧生成了三氧化二铁
C. 有腐蚀性的药品应该放在玻璃器皿里称量 D. 点燃可燃性气体之前,必须检
验气体的纯度
14.2003年3月20日开始的伊战争中,伊拉克人在首都巴格达城外点燃早已准备好的石油,让浓浓的黑烟
笼罩着天空,以干扰美军战机的轰炸,浓浓的黑烟说明石油中含有( )
A. 碳元素 B. 氧元
素 C. 氢元
素 D. 硫元素
15.紫衫醇是一种新型抗癌药,其化学式为C H NO , 下列对紫衫醇叙述正确的是( )
47 51 14
①该物质由碳、氢、氮、氧四种元素组成
②该物质是由多种原子构成的纯净物
③该物质中碳、氢、氮、氧元素的质量比为47:51:1:14
④该物质的一个分子中含有113个原子
A. ①④ B. ②③
C. ①③
D. ③④
16.下列排放到空气中的物质不使空气受到污染的是( )
A. 煤燃烧产生的烟
B. 燃烧烟花爆竹的产物
C. 汽车排放的尾气
D. 氢气在空气中燃烧的产物
17.氢元素的质量分数相同的一组物质是( )
A. H SO 和H PO B. H SO 和Cu(OH) C. H O 和H S D. C H OH 和CH COOH
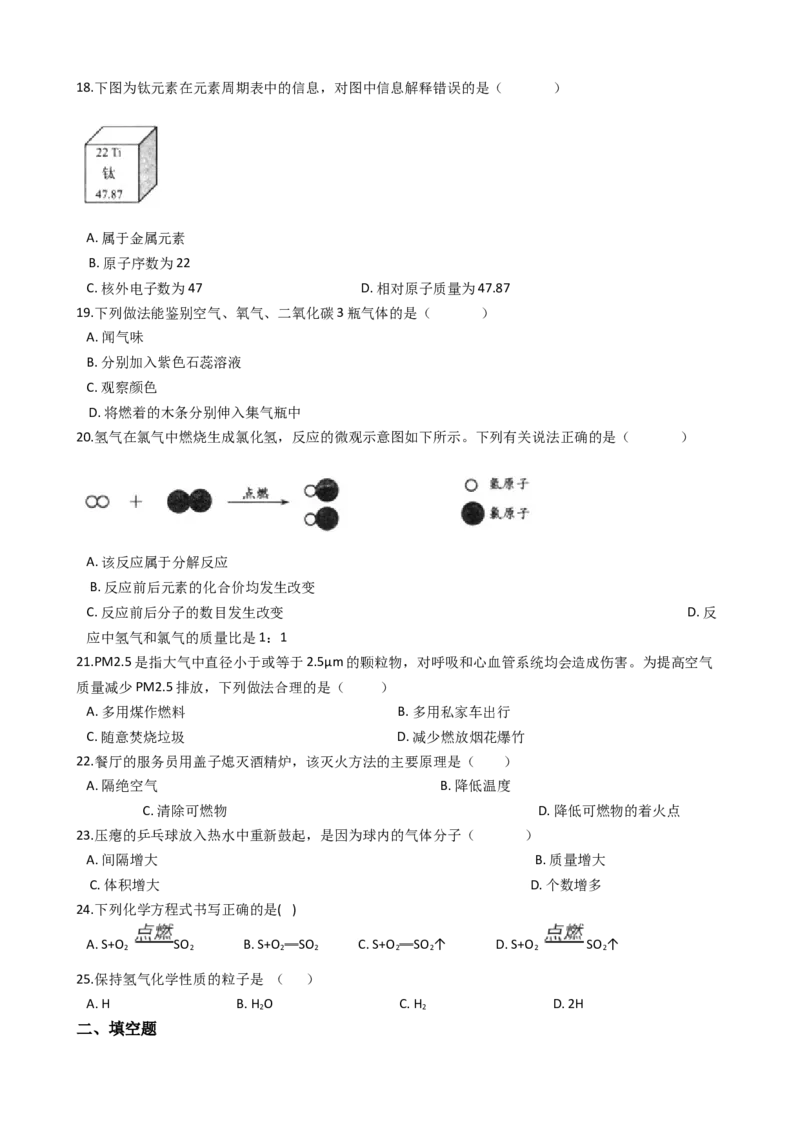
2 4 3 4 2 4 2 2 2 2 5 318.下图为钛元素在元素周期表中的信息,对图中信息解释错误的是( )
A. 属于金属元素
B. 原子序数为22
C. 核外电子数为47 D. 相对原子质量为47.87
19.下列做法能鉴别空气、氧气、二氧化碳3瓶气体的是( )
A. 闻气味
B. 分别加入紫色石蕊溶液
C. 观察颜色
D. 将燃着的木条分别伸入集气瓶中
20.氢气在氯气中燃烧生成氯化氢,反应的微观示意图如下所示。下列有关说法正确的是( )
A. 该反应属于分解反应
B. 反应前后元素的化合价均发生改变
C. 反应前后分子的数目发生改变 D. 反
应中氢气和氯气的质量比是1:1
21.PM2.5是指大气中直径小于或等于2.5μm的颗粒物,对呼吸和心血管系统均会造成伤害。为提高空气
质量减少PM2.5排放,下列做法合理的是( )
A. 多用煤作燃料 B. 多用私家车出行
C. 随意焚烧垃圾 D. 减少燃放烟花爆竹
22.餐厅的服务员用盖子熄灭酒精炉,该灭火方法的主要原理是( )
A. 隔绝空气 B. 降低温度
C. 清除可燃物 D. 降低可燃物的着火点
23.压瘪的乒乓球放入热水中重新鼓起,是因为球内的气体分子( )
A. 间隔增大 B. 质量增大
C. 体积增大 D. 个数增多
24.下列化学方程式书写正确的是( )
A. S+O SO B. S+O ═SO C. S+O ═SO ↑ D. S+O SO ↑
2 2 2 2 2 2 2 2
25.保持氢气化学性质的粒子是 ( )
A. H B. H O C. H D. 2H
2 2
二、填空题26.写出下列化学用语
(1)2 个铁原子________。
(2)5 个五氧化二磷分子________。
(3)氯化镁的化学式________。
(4)钙离子符号________。
(5)标出H O中氧的化合价________。
2
(6)画出钠原子结构示意图________。
(7)画出17 号元素的阴离子结构示意图________。
27.27、写出化学方程式:
(1)2004 年夏季奥运会将在奥林匹克发祥地希腊准典举行,传递奥运火炬已成为一项固定活动。1936
年由德国人许特韦克为柏林奥运会制作了第一把火炬。火炬由镁为主的燃料供燃。写出镁在空气中燃烧
的化学方程式________。
(2)过氧化氢在二氧化锰的作用下制取氧气________。
(3)实验室制取二氧化碳的化学方程式________。
(4)二氧化碳使石灰水变浑浊的化学方程式________。
(5)为了保护空气,很多公交车用“压缩天然气”作燃料。天然气的主要成分是________(化学式),其
充分燃烧的化学方程式是________。
28.在超市中常看到“高钙奶”、“铁强化酱油”等 食品,这里的“钙”和“铁”是指________(填“原
子”或“元素”)。
29.将浑浊的河水用如图所示的简易净水器进行净化,除过滤外,活性炭的主要作用是________,得到的
水是________ (填“混合物”或“纯净物”).生活中降低水的硬度可采用的方法是________净化。降低水
的硬度的方法中净化程度最高的方法是________。
三、简答题
30.水和水溶液在生产生活中起着重要作用。
(1)如图是研究水组成的电解水实验。图中与试管A相连的是电源的________(填“正极”或“负
极”),该反应的化学方程式是________。
(2)A、B 两试管中的气体体积之比是________,质量之比是________。四、实验题
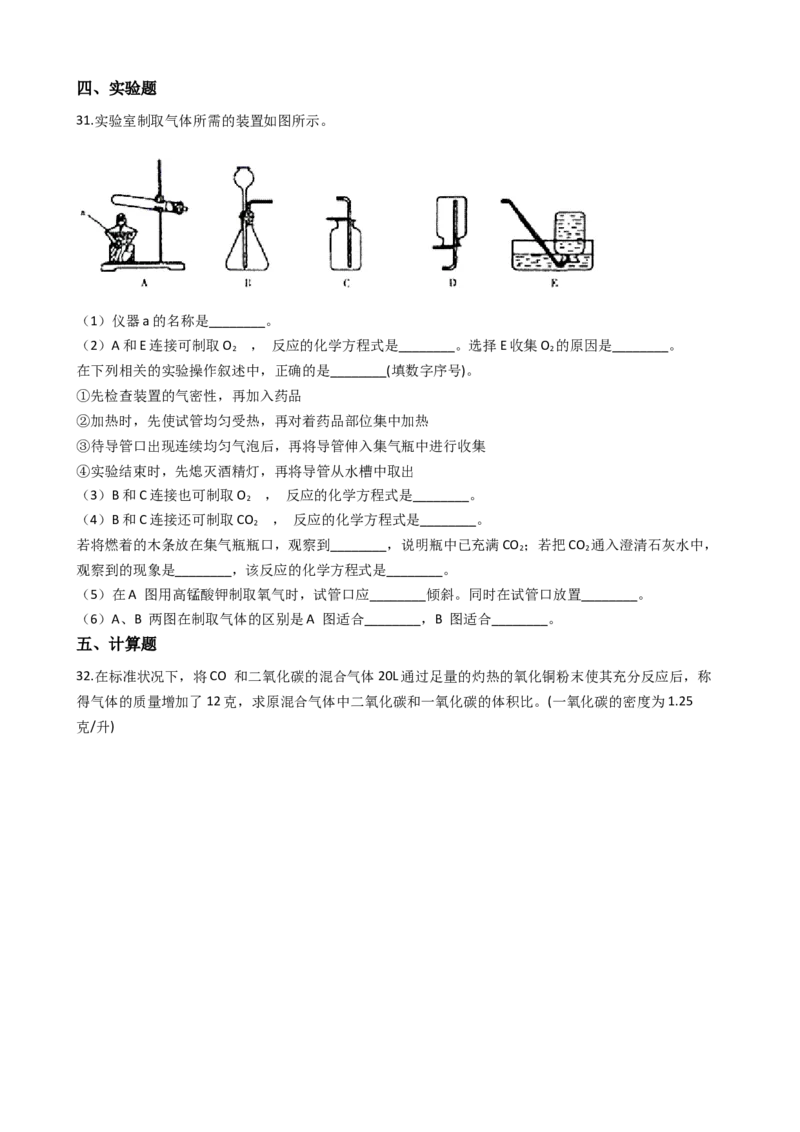
31.实验室制取气体所需的装置如图所示。
(1)仪器a的名称是________。
(2)A和E连接可制取O , 反应的化学方程式是________。选择E收集O 的原因是________。
2 2
在下列相关的实验操作叙述中,正确的是________(填数字序号)。
①先检查装置的气密性,再加入药品
②加热时,先使试管均匀受热,再对着药品部位集中加热
③待导管口出现连续均匀气泡后,再将导管伸入集气瓶中进行收集
④实验结束时,先熄灭酒精灯,再将导管从水槽中取出
(3)B和C连接也可制取O , 反应的化学方程式是________。
2
(4)B和C连接还可制取CO , 反应的化学方程式是________。
2
若将燃着的木条放在集气瓶瓶口,观察到________,说明瓶中已充满CO ;若把CO 通入澄清石灰水中,
2 2
观察到的现象是________,该反应的化学方程式是________。
(5)在A 图用高锰酸钾制取氧气时,试管口应________倾斜。同时在试管口放置________。
(6)A、B 两图在制取气体的区别是A 图适合________,B 图适合________。
五、计算题
32.在标准状况下,将CO 和二氧化碳的混合气体20L通过足量的灼热的氧化铜粉末使其充分反应后,称
得气体的质量增加了12克,求原混合气体中二氧化碳和一氧化碳的体积比。(一氧化碳的密度为1.25
克/升)答案解析部分
一、单选题
1.【答案】D
2.【答案】B
3.【答案】A
4.【答案】A
5.【答案】B
6.【答案】A
7.【答案】B
8.【答案】C
9.【答案】C
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】B
14.【答案】A
15.【答案】A
16.【答案】D
17.【答案】B
18.【答案】C
19.【答案】D
20.【答案】B
21.【答案】D
22.【答案】A
23.【答案】A
24.【答案】A
25.【答案】C
二、填空题
26.【答案】(1)2Fe
(2)5P O
2 5
(3)MgCl
2
(4)Ca2+
(5)(6)
(7)
27.【答案】(1)2Mg+O 2MgO
2
(2)2H O 2H O+O ↑
2 2 2 2
(3)CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
(4)Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
(5)CH ;CH +2O CO +2H O
4 4 2 2 2
28.【答案】元素
29.【答案】吸附;混合物;煮沸;蒸馏
三、简答题
30.【答案】(1)负极;2H O 2H ↑+O ↑
2 2 2
(2)2:1;1:8
四、实验题
31.【答案】(1)酒精灯
(2)2KMnO K MnO +MnO +O ↑;氧气不易溶于水;①②③
4 2 4 2 2
(3)2H O 2H O+O ↑
2 2 2 2
(4)CaCO +2HCl=CaCl +H O+CO ↑;木条熄灭;澄清的石灰水变浑浊;CO +Ca(OH) =CaCO ↓+H O
3 2 2 2 2 2 3 2
(5)向下;棉花团
(6)固固加热;固液不需要加热
五、计算题
32.【答案】解:设混合气体中一氧化碳的质量为x。
CuO+ CO Cu+ CO 气体增加的
2
质量为
28 44 44-24=16
x 12
x=21g
CO的体积为 =16.8L原混合气体中二氧化碳和一氧化碳的体积比(20-16.8)L:16.8L =4:21
答:原混合气体中二氧化碳和一氧化碳的体积比为4:21。