文档内容
邵阳市 2018 年初中毕业学业考试试题卷
化 学
温馨提示:
(1)本学科试卷分试题卷和答题卡两部分,考试时量为90分钟,满分为100分。
(2)请你将姓名、准考证号等相关信息按要求填涂在答题卡上。
(3)请你在答题卡上作答,答在本试题卷上无效。
试题很容易的哟,
可能用到的相对原子质量:H—1 C—12 O—16 你要充满信心哟!
Na—23 Mg—24 Al—27 Cl—35.5
一、选择题。(本大题共25个小题,每小题2分,
共50分。每小题只有一个选项符合题意)
1.下列过程发生化学变化的是
A.西瓜榨汁 B.滴水成冰 C.纸张燃烧 D.蜡烛熔化
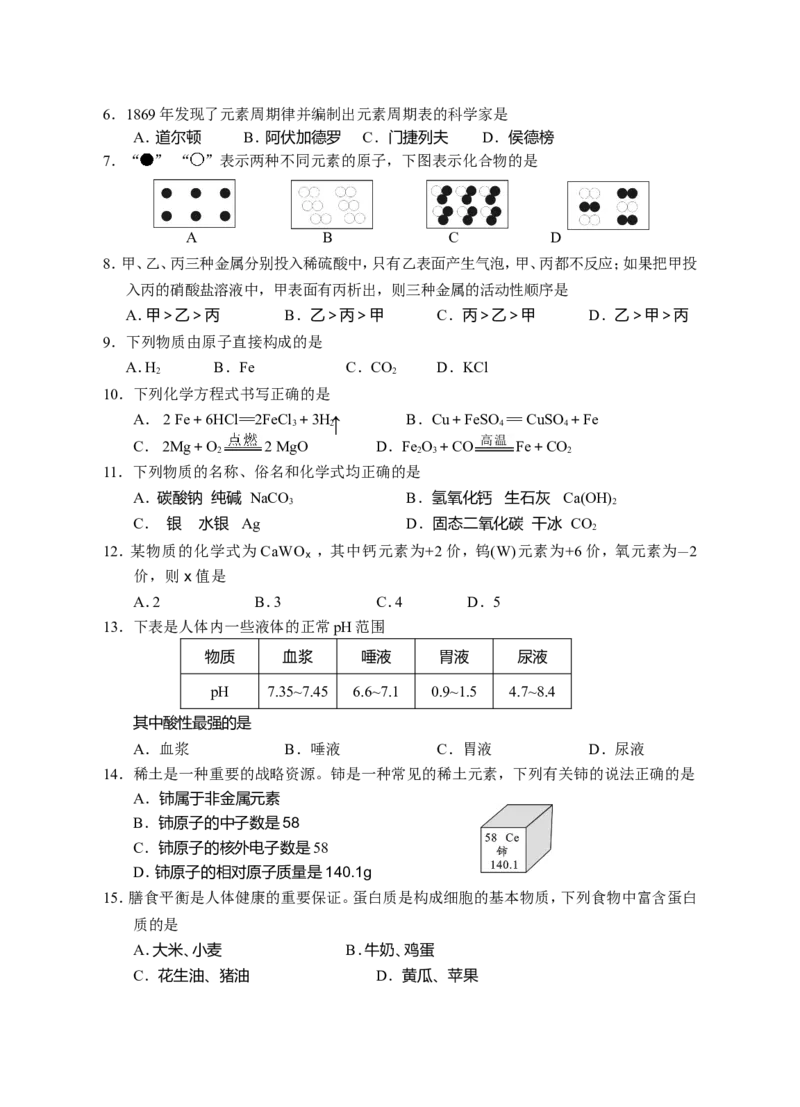
2.空气是一种宝贵的自然资源。右图为空气成分示意图,其中R指的是
A.氮气 B.氧气
C.稀有气体 D.二氧化碳
3.下列有关实验现象描述正确的是
A.硫在氧气中燃烧产生淡蓝色的火焰
B.红磷在空气中燃烧产生大量的白烟
C.碳在空气中燃烧生成二氧化碳
D.将铁丝伸入盛有氧气的集气瓶中剧烈燃烧
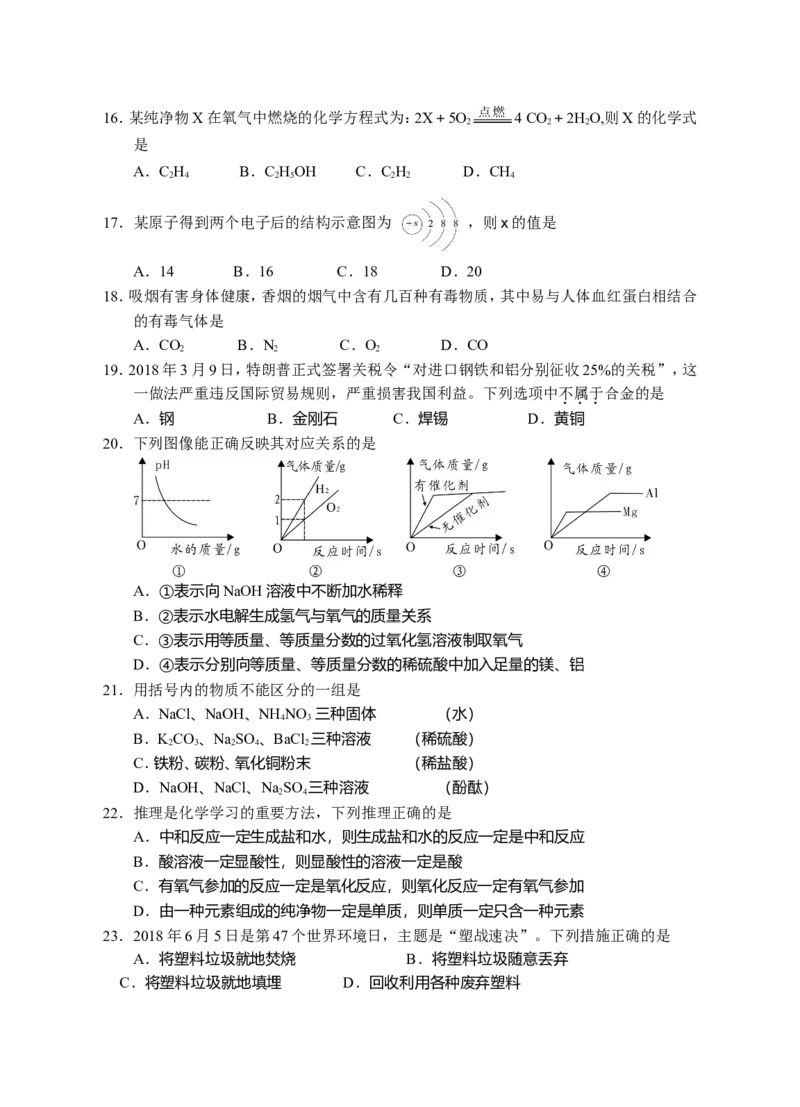
4.下列图示操作正确的是
A.浓硫酸的稀释 B.给液体加热
C.测定溶液的pH D.量取一定量的液体
5.下列说法正确的是
A.水变成水蒸气说明分子可以再分
B.八月丹桂飘香,说明分子在不停运动
C.保持水的化学性质的最小粒子是氢原子和氧原子
D.4000L氧气能压缩在40L的钢瓶中,说明分子的体积变小6.1869年发现了元素周期律并编制出元素周期表的科学家是
A.道尔顿 B.阿伏加德罗 C.门捷列夫 D.侯德榜
7.“ ” “ ”表示两种不同元素的原子,下图表示化合物的是
A B C D
8.甲、乙、丙三种金属分别投入稀硫酸中,只有乙表面产生气泡,甲、丙都不反应;如果把甲投
入丙的硝酸盐溶液中,甲表面有丙析出,则三种金属的活动性顺序是
A.甲>乙>丙 B.乙>丙>甲 C.丙>乙>甲 D.乙>甲>丙
9.下列物质由原子直接构成的是
A.H B.Fe C.CO D.KCl
2 2
10.下列化学方程式书写正确的是
A.2 Fe+6HCl==2FeCl +3H↑ B.Cu+FeSO == CuSO +Fe
3 2 4 4
C. 2Mg+O
2
2 MgO D.Fe
2
O
3
+CO Fe+CO
2
11.下列物质的名称、俗名和化学式均正确的是
A.碳酸钠 纯碱 NaCO B.氢氧化钙 生石灰 Ca(OH)
3 2
C. 银 水银 Ag D.固态二氧化碳 干冰 CO
2
12.某物质的化学式为CaWO
x
,其中钙元素为+2价,钨(W)元素为+6价,氧元素为—2
价,则x值是
A.2 B.3 C.4 D.5
13.下表是人体内一些液体的正常pH范围
物质 血浆 唾液 胃液 尿液
pH 7.35~7.45 6.6~7.1 0.9~1.5 4.7~8.4
其中酸性最强的是
A.血浆 B.唾液 C.胃液 D.尿液
14.稀土是一种重要的战略资源。铈是一种常见的稀土元素,下列有关铈的说法正确的是
A.铈属于非金属元素
B.铈原子的中子数是58
C.铈原子的核外电子数是58
D.铈原子的相对原子质量是140.1g
15.膳食平衡是人体健康的重要保证。蛋白质是构成细胞的基本物质,下列食物中富含蛋白
质的是
A.大米、小麦 B.牛奶、鸡蛋
C.花生油、猪油 D.黄瓜、苹果16.某纯净物X在氧气中燃烧的化学方程式为:2X+5O 4 CO+2HO,则X的化学式
2 2 2
是
A.C H B.C HOH C.C H D.CH
2 4 2 5 2 2 4
17.某原子得到两个电子后的结构示意图为 ,则x的值是
A.14 B.16 C.18 D.20
18.吸烟有害身体健康,香烟的烟气中含有几百种有毒物质,其中易与人体血红蛋白相结合
的有毒气体是
A.CO B.N C.O D.CO
2 2 2
19.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这
一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
20.下列图像能正确反映其对应关系的是
A.①表示向NaOH溶液中不断加水稀释
B.②表示水电解生成氢气与氧气的质量关系
C.③表示用等质量、等质量分数的过氧化氢溶液制取氧气
D.④表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝
21.用括号内的物质不能区分的一组是
A.NaCl、NaOH、NH NO 三种固体 (水)
4 3
B.KCO、NaSO 、BaCl 三种溶液 (稀硫酸)
2 3 2 4 2
C.铁粉、碳粉、氧化铜粉末 (稀盐酸)
D.NaOH、NaCl、NaSO 三种溶液 (酚酞)
2 4
22.推理是化学学习的重要方法,下列推理正确的是
A.中和反应一定生成盐和水,则生成盐和水的反应一定是中和反应
B.酸溶液一定显酸性,则显酸性的溶液一定是酸
C.有氧气参加的反应一定是氧化反应,则氧化反应一定有氧气参加
D.由一种元素组成的纯净物一定是单质,则单质一定只含一种元素
23.2018年6月5日是第47个世界环境日,主题是“塑战速决”。下列措施正确的是
A.将塑料垃圾就地焚烧 B.将塑料垃圾随意丢弃
C.将塑料垃圾就地填埋 D.回收利用各种废弃塑料24.向AgNO 溶液中加入一定质量铜和锌的混合物,充分反应后过滤得到无色溶液和滤渣,
3
下列说法正确的是
A.反应后所得的溶液中一定含有Zn(NO ),一定不含Cu(NO ) 和AgNO
3 2 3 2 3
B.反应后所得的溶液中一定含有Zn(NO ),可能含有Cu(NO ) 和AgNO
3 2 3 2 3
C.反应后所得的滤渣中一定含有Ag,一定不含Cu和Zn
D.反应后所得的滤渣中一定含有Cu,可能含有Zn和Ag
25.我国自主知识产权的抗癌新药“西达本胺”已全球上市。西达本胺的化学式为
C H FN O,下列有关西达本胺的说法正确的是
22 19 4 2
A.西达本胺由碳、氢、氟、氮、氧五种原子构成
B.一个西达本胺分子中含有一个氧分子
C.西达本胺由五种元素组成
D.西达本胺中C、H、F、N、O元素的质量比为22:19:1:4:2
二、填空题(本大题共7个小题,每个化学方程式2分,其余每空1分,共28分)
26.请按要求写出化学符号或符号表示的意义。
(1)2个氢分子 (2)铵根离子
(3)水中氢元素化合价为+1价 (4)2C
27.从①浓硫酸、②氢氧化钙、③碳酸氢钠、④硝酸钾中选择符合题意的物质(用序号填空)。
(1)可用作改良酸性土壤的是 。
(2)可用作复合肥的是 。
(3)可用作焙制糕点的是 。
(4)可用作某些气体干燥剂的是 。
28.化学源于生活,也服务与生活:
(1)冰箱中放入活性炭除异味,利用了活性炭的 性。
(2)炒菜时锅内油着火用锅盖盖灭,其灭火原理是 。
(3)稀盐酸除铁锈,其反应的化学方程式是 。
29.近年来,我国航空、航天、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标
志着我国的航空强国梦又迈出了一大步。大飞机使用的化学材料如甲图。请回答:
(1)橡胶属于 (填“金属”或“合
成”)材料。
(2)图乙是钛原子结构示意图,则x= ;
钛元素位于元素周期表第 周期。
(3)铁比铝的强度大,但制造飞机却用铝合金
而不用铁合金,主要原因是铝比铁的密度小且抗腐蚀性能强。铝具有很好的抗腐蚀
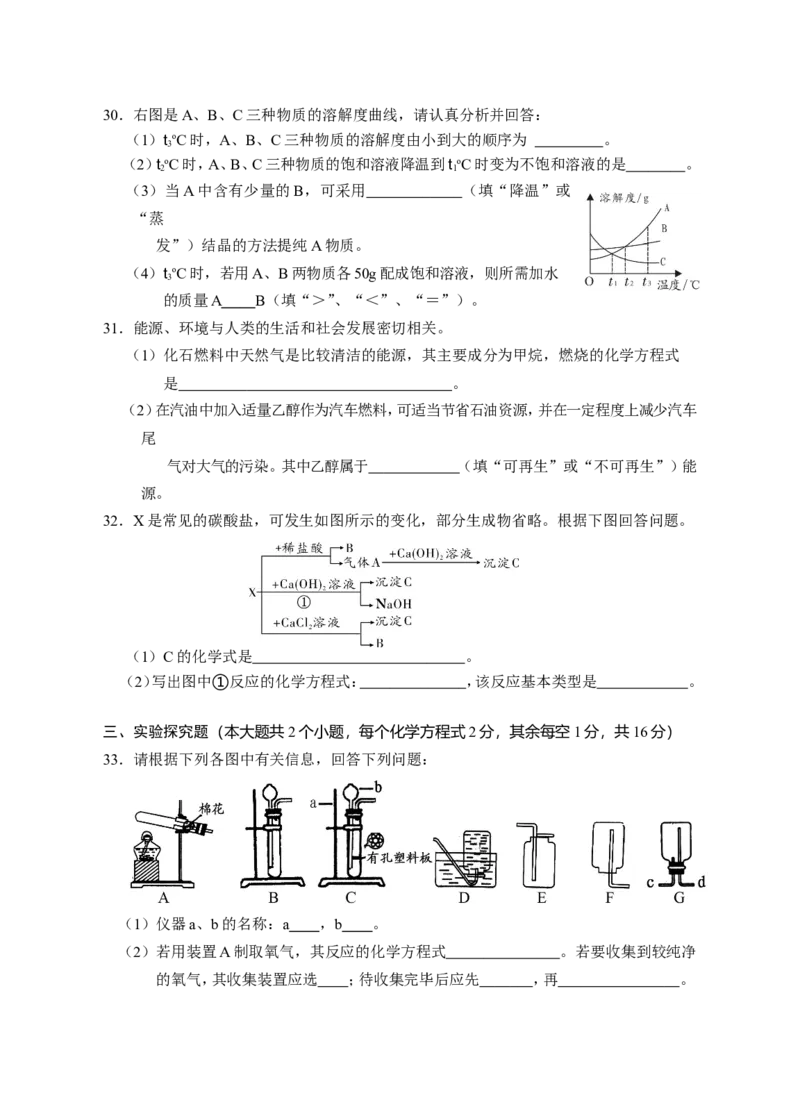
性的原因是 (用化学方程式表示)。30.右图是A、B、C三种物质的溶解度曲线,请认真分析并回答:
(1)toC时,A、B、C三种物质的溶解度由小到大的顺序为 。
3
(2)toC时,A、B、C三种物质的饱和溶液降温到t oC时变为不饱和溶液的是 。
2 l
(3)当A中含有少量的B,可采用 (填“降温”或
“蒸
发”)结晶的方法提纯A物质。
(4)toC时,若用A、B两物质各50g配成饱和溶液,则所需加水
3
的质量A B(填“>”、“<”、“=”)。
31.能源、环境与人类的生活和社会发展密切相关。
(1)化石燃料中天然气是比较清洁的能源,其主要成分为甲烷,燃烧的化学方程式
是 。
(2)在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源,并在一定程度上减少汽车
尾
气对大气的污染。其中乙醇属于 (填“可再生”或“不可再生”)能
源。
32.X是常见的碳酸盐,可发生如图所示的变化,部分生成物省略。根据下图回答问题。
(1)C的化学式是 。
(2)写出图中①反应的化学方程式: ,该反应基本类型是 。
三、实验探究题(本大题共2个小题,每个化学方程式2分,其余每空1分,共16分)
33.请根据下列各图中有关信息,回答下列问题:
(1)仪器a、b的名称:a ,b 。
(2)若用装置A制取氧气,其反应的化学方程式 。若要收集到较纯净
的氧气,其收集装置应选 ;待收集完毕后应先 ,再 。某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是 。
(3)实验制取CO,为了控制反应的发生与停止,选择最佳的发生装置是 ;
2
若用G装置收集CO 气体,气体应从 端(填“c”或“d”)进入。
2
34.在粗盐的提纯实验中
(1)其主要操作步骤顺序是 。
①过滤 ②溶解 ③蒸发 ④计算产率
(2)右下图是某同学过滤的操作图,指出图中明显错误 ;过滤后,如果滤
液仍然浑浊,其原因可能是 。(填一种)
(3)蒸发时,蒸发皿内出现 时应停止加热。
(4)通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂
质MgCl 、CaCl 得到纯净的NaCl,可采用如下图所示流程:
2 2
①上图中所用甲、乙、丙三种试剂依次是 。
A.NaOH溶液、NaCO 溶液、稀盐酸
2 3
B.NaCO 溶液、KOH溶液、稀盐酸
2 3
C.NaOH溶液、NaCO 溶液、稀硫酸
2 3
②反思交流:通过以上规范操作,制得氯化钠的质量比原粗盐样品中含氯化钠的质量
(填“增多”、“减少”、“不变”)。
四、计算题(本大题共6分)
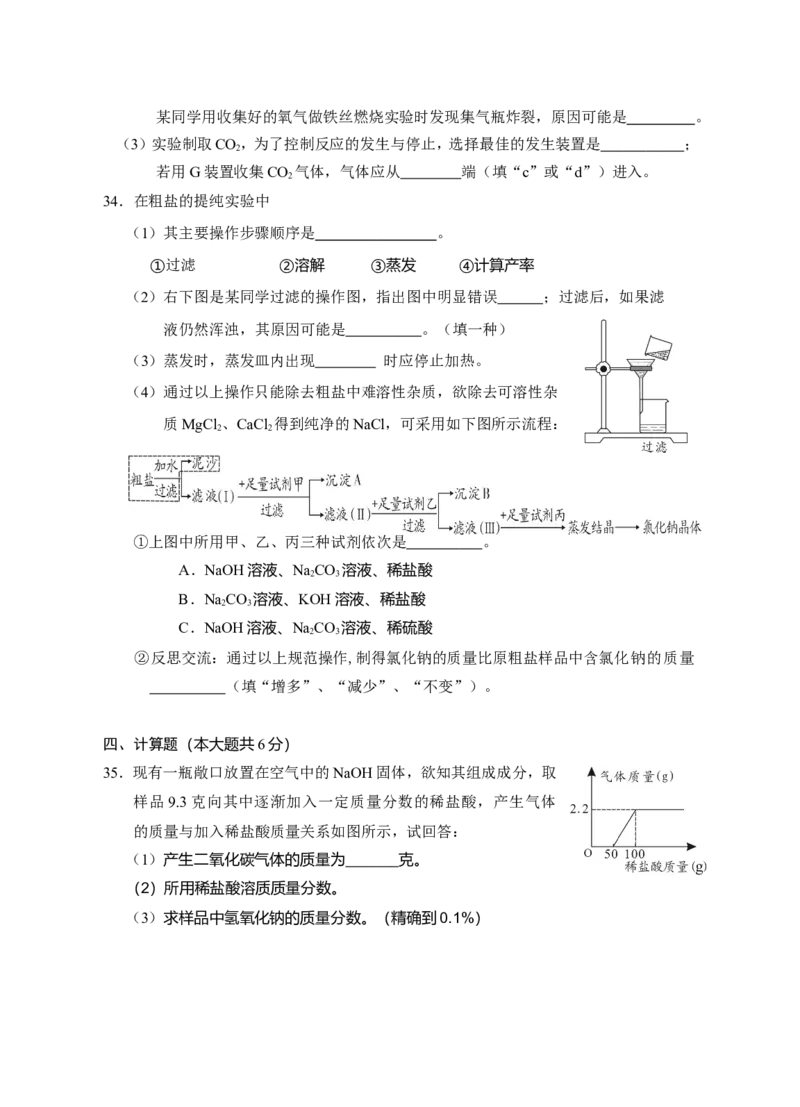
35.现有一瓶敞口放置在空气中的NaOH固体,欲知其组成成分,取
样品9.3克向其中逐渐加入一定质量分数的稀盐酸,产生气体
的质量与加入稀盐酸质量关系如图所示,试回答:
(1)产生二氧化碳气体的质量为 克。
(2)所用稀盐酸溶质质量分数。
(3)求样品中氢氧化钠的质量分数。(精确到0.1%)邵阳市 2018 年初中毕业学业考试参考答案及评分标
准
化 学
一、选择题(每小题2分,共50分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案 C B B A B C C D B C D C C
题号 14 15 16 17 18 19 20 21 22 23 24 25
答案 C B C B D B C D D D A C
二、填空题(每个化学方程式2分,其余每空1分,共28分。化学式写错或没配平不给分)
26.(1)2H (2)NH + (3) O (4)两个碳原子
2 4 2
27.(1)② (2)④ (3)③ (4) ①
28.(1)吸附 (2)隔绝空气(或氧气)
(3)6HCl+Fe O ==2FeCl +3H O
2 3 3 2
29.(1)合成 (2)8,四 (3)4Al+3O ==2 Al O
2 2 3
30.(1) C<B<A (2)C (3)降温 (4)<
31.(1) CH+2O CO+2H O (2)可再生
4 2 2 2
32.(1) CaCO (2)NaCO+Ca(OH) ==CaCO ↓+2NaOH 、复分解反应
3 2 3 2 3
三、实验探究题(每个化学方程式2分,其余每空1分,共16分。化学式写错或没配平不给
分)
33.(1)铁架台,长颈漏斗
(2)2KMnO == KMnO +MnO+ O↑ ,D,撤离水槽内的导管,熄灭酒精灯;
4 2 4 2 2
集气瓶中没有铺一层细砂(或集气瓶中没有存少量水或铁丝与集气瓶内壁接触)(3)C ,c
34.(1)②①③④
(2)没有用玻璃棒引流,液面高于滤纸边缘(或滤纸破损或承接的仪器不干净)
(3)较多固体
(4)A,增多
四、计算题(共6分)
35.(1)2.2(1分)
(2)解:设生成2.2g CO 所需HCl质量为x
2
NaCO+2HCl==2NaCl+2H O+CO↑…………………………(1分)
2 3 2 2
73 44
x 2.2g
…………………………(1分)
x=3.65 g
所用稀盐酸溶质质量分数为 ×100%=7.3% …………………(1分)
(3)解:设NaCO 质量为y
2 3
NaCO+2HCl==2NaCl+H O+CO↑
2 3 2 2
106 44
y 2.2g
y=5.3g …………………………(1分)
样品中NaOH质量为:9.3g-5.3g=4g
NaOH%为: %≈43.0% …………………………(1分)
答:略。
请 仔 细 检 查 , 祝 你 成 功 !