文档内容
作者:六指先生 qq:3099205099
绪言
1. 化学的概念:化学是研究物质的组成、结构、性质以及变化规律的科学。
2. 目前人类发现的元素只有一百多种,但人类发现和合成的物质已超过3000万种。
3. 到了近代,英国科学家道尔顿提出了近代原子学说;意大利物理学家、化学家阿伏伽德罗提出了分子
的概念。
4. 原子论和分子学说的创立,奠定了近代化学的基础。
5. 1869年,俄国化学家门捷列夫发现了元素周期律并编制出元素周期表。
第一单元 走进化学世界
第一节 物质的变化和性质
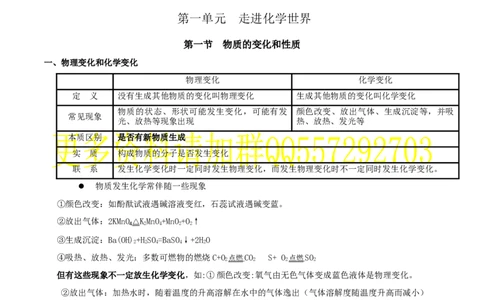
一、物理变化和化学变化
物理变化 化学变化
定 义 没有生成其他物质的变化叫物理变化 生成其他物质的变化叫化学变化
物质的状态、形状可能发生变化,可能有发 颜色改变、放出气体、生成沉淀等,并吸
常见现象
光、放热等现象出现 热、放热、发光等
本质区别 是否有新物质生成
实 质 构成物质的分子是否发生变化
联 系 发生化学变化时一定同时发生物理变化,而发生物理变化时不一定同时发生化学变化。
物质发生化学常伴随一些现象
①颜色改变:如酚酞试液遇碱溶液变红,石蕊试液遇碱变蓝。
②放出气体:2KMnO △KMnO+MnO+O↑
4 2 4 2 2
③生成沉淀:Ba(OH)+HSO=BaSO↓+2HO
2 2 4 4 2
④吸热、放热、发光:多数可燃物的燃烧C+O 点燃 CO S+ O 点燃 SO
2 2 2 2
但有这些现象不一定放生化学变化,如:①颜色改变:氧气由无色气体变成蓝色液体是物理变化。
②放出气体:加热水时,随着温度的升高溶解在水中的气体逸出(气体溶解度随温度升高而减小)
③生成沉淀:饱和的石灰水随着温度的升高有晶体析出(可说成有沉淀,氢氧化钙溶解度随温度升高
而减小)
④放热、发光:灯泡发光放热。
石墨变金刚石的变化是化学变化。“日照香炉生紫烟,遥看瀑布挂前川”指的是物理变化。
二、物理性质和化学性质
物理性质 化学性质
定 义 物质不需要发生化学变化就可以表现出来的性质 物质在化学变化中表现出来的性质作者:六指先生 qq:3099205099
颜色、状态、气味;硬度、密度、燃点、沸点、 可燃性、氧化性、还原性、稳定性、活泼
实 例
熔点、溶解性、挥发性、导电性、吸附性等 性、酸性、碱性、毒性等
区 别 这种性质是否需要经过化学变化才能表现出来
氮气和稀有气体可以做保护气。这虽然不包含化学变化,但利用了它们的化学性质(稳定性)。
第二节 化学是一门以实验为基础的科学
一、蜡烛
1. 石蜡不溶于水,石蜡密度小于水。
2. 蜡烛燃烧时的火焰分三层,包括外焰(温度最高)、内焰(最明亮)和
焰心。
用一火柴梗平放入火焰中发现,现象:两端先碳化,结论:外焰温度最高。
3. 检验产物 H O:用干冷烧杯罩火焰上方,烧杯内有水雾
2
CO :取下烧杯,倒入澄清石灰水,振荡,变浑浊
2
4. 熄灭蜡烛时产生的白烟是凝固的石蜡蒸气。
5. 蜡烛燃烧的表达式:石蜡+氧气点燃二氧化碳+水 C H +33O 点燃 25CO+16HO
25 32 2 2 2
二、做“对人体吸入的空气和呼出的气体的探究”实验时,最重要的是做对比实验。
结论:与吸入空气相比,呼出气体中O 的量减少,CO 和H O的量增多(吸入空气与呼出气体成分是相同
2 2 2
的)
第三节 走进化学实验室
一、托盘天平的使用
1. 托盘天平的精确度是 0. 1 g,即用天平测量出的物体质量只能精确到小数点后一位。
2. 托盘天平由托盘、指针、游码、标尺、分度盘和平衡螺母组成。
3. 物理使用方法(给物体测质量):
a) 将天平水平放置,游码放在标尺的零刻度处,调节平衡螺母,使天平平衡。
b) 将物放在左盘,砝码放在右盘。砝码必须用镊子夹取(防止砝码生锈造成称量的误差),
先加质量大的砝码,后加质量小的砝码,最后移动游码,直到天平平衡为止。
c) 记录所加砝码和游码的质量。
d) 称量完毕后,应把砝码放回砝码盒中,把游码移回0处。
4. 化学使用方法(给质量取物体):
a) 将天平水平放置,游码放在标尺的零刻度处,调节平衡螺母,使天平平衡。
b) 如果药品是粉末,在天平左右盘各放一张大小、质量相同的纸。如果药品易潮解或具有
腐蚀性,在天平上放玻璃器皿。(可以先放后调平衡,这样就不用记录它们的质量)
c) 用镊子夹取砝码并放在右盘,移动游码,使天平的读数等于要称量的药品的质量。作者:六指先生 qq:3099205099
d) 在左盘上添加药品,使天平平衡。如果天平不平衡,只能在左盘添加或减少药品,不能
动砝码或游码。
e) 称量完毕后,应把砝码放回砝码盒中,把游码移回0处。
5. “左物右码”时,物质的质量=砝码的质量+游码的示数 ;“左码右物”,物质的质量=砝
码的质量-游码的示数。“左码右物”的做法虽然也能称出物质的质量,但是这种做法是错误的。
6. 称量干燥的固体物品时,在两边托盘中各放一张大小、质量相同的纸,在纸上称量。潮湿的
或具有腐蚀性的药品(如氢氧化钠),放在加盖的玻璃器皿(如小烧杯、表面皿)中称量。
二、仪器的连接
1. 把玻璃管插入带孔橡皮塞:先把要插入塞子的玻璃的一端用水润湿,然后稍稍用力转动,使它插入。
2. 连接玻璃管和胶皮管:先把玻璃管口用水润湿,然后稍稍用力即可把玻璃管插入胶皮管。
3. 在容器口塞橡皮塞:应把橡皮塞慢慢转动塞进容器口。切不可把容器放在桌上再使劲塞进塞子,以免压
破容器。
4. 需要用力的事情都要由右手来做。
5. 连接一套装置顺序:先左后右,先下再上
三、实验室药品取用规则
1. “三不原则”:不能用手接触药品,不要把鼻孔凑到容器口去闻药品的气味,不得尝任何药
品的味道。
2. 注意节约药品。应该严格按照实验规定的用量取用药品。如果没有说明用量,一般应该按最
少量(1~2mL)取用液体。固体只需盖满试管底部。
3. 实验剩余的药品既不能放回原瓶,也不要随意丢弃,更不要拿出实验室,要放入指定的容器
内。
四、固体药品的取用
1. 固体药品通常保存在广口瓶里。
2. 固体粉末一般用药匙或纸槽取用。操作时先使试管倾斜,把药匙小心地送至试管底部,然后
使试管直立。(“一倾、二送、三直立”)
3. 块状药品一般用镊子夹取。操作时先横放容器,把药品或金属颗粒放入容器口以后,再把容
器慢慢竖立起来,使药品或金属颗粒缓缓地滑到容器的底部,以免打破容器。(“一横、二放、三慢
竖”)
4. 用过的药匙或镊子要立刻用干净的纸擦拭干净。
五、液体药品的取用
液体药品通常盛放在细口瓶中。广口瓶、细口瓶等都经过磨砂处理,目的是增大容器的气密性。作者:六指先生 qq:3099205099
1. 取用不定量(较多)液体——直接倾倒
使用时的注意事项(括号内为操作的目的):
a. 细口瓶的瓶塞必须倒放在桌面上【防止药品腐蚀实验台或污染药品】;
b. 瓶口必须紧挨试管口,并且缓缓地倒【防止药液损失】;
c. 细口瓶贴标签的一面必须朝向手心处【防止药液洒出腐蚀标签】;
d. 倒完液体后,要立即盖紧瓶塞,并把瓶子放回原处,标签朝向外面【防止药品潮解、变质】。
2. 取用不定量(较少)液体——使用胶头滴管
使用时的注意事项(括号内为操作的目的):
a. 应在容器的正上方垂直滴入;胶头滴管不要接触容器壁【防止沾污试管或污染试剂】;
b. 取液后的滴管,应保持橡胶胶帽在上,不要平放或倒置【防止液体倒流,沾污试剂或腐蚀橡胶胶
帽】;
c. 用过的试管要立即用清水冲洗干净;但滴瓶上的滴管不能用水冲洗,也不能交叉使用。
3. 取用一定量的液体——使用量筒
使用时的注意事项:
a. 当向量筒中倾倒液体接近所需刻度时,停止倾倒,余下部分用胶头滴管滴加药液至所需刻度线;
b. 读数时量筒必须放平稳,视线与凹液面的最低处保持水平【读数时若仰视,则读数偏低;读数时
若俯视,则读数偏高——倒液体时仰视,则量取的液体偏多;倒液体时俯视,则量取的液体偏少】。
六、物质的加热
1. 使用酒精灯时的注意事项(括号内为操作的目的)
a. 绝对禁止向燃着的酒精灯里添加酒精【防止失火】;
b. 绝对禁止用酒精灯引燃另一只酒精灯,应该用火柴点燃【防止失火】;
c. 用完酒精灯后,必须用灯帽盖灭,不可用嘴去吹【以免引起灯内酒精燃烧,发生危险】;
d. 如果洒出的酒精在桌上燃烧起来,应立刻用湿抹布扑盖。
e. 酒精灯内酒精含量不能少于酒精灯容量的 1/ 4 ,也不能多于酒精灯容量的 2/ 3 。
2. 用于加热的仪器
液体:试管、蒸发皿、锥形瓶、烧杯、烧瓶(使用后三者加热时需要石棉网)。
固体:试管、蒸发皿、燃烧匙。
3. 给试管加热的注意事项(括号内为操作的目的)
a. 试管外壁不能有水【防止试管炸裂】;
b. 加热时要有试管夹。夹持试管时,应将试管夹从试管底部往上套,夹持部位在距试管口近1/3处,握住作者:六指先生 qq:3099205099
试管夹的长柄,不要把拇指按在短柄上;
c. 如果加热固体,试管口应略向下倾斜【防止冷凝水回流到热的试管底部使试管炸裂】 ;如果加热液体,
试管口要向上倾斜,与桌面成45°角( 增 大受热面积,有利于液体回流 ) 。
d. 如果加热液体,液体体积不能超过试管容积的 1/ 3 【防止液体沸腾时溅出伤人】;
e. 加热时先预热,使试管在火焰上移动,待试管均匀受热后,再将火焰固定在盛放药品的部位加热【防
止试管炸裂】。
f. 试管底部不能和酒精灯的灯芯接触【防止试管炸裂】;
g. 烧得很热的试管不能用冷水立即冲洗【防止试管炸裂】;
h. 加热时试管不要对着有人的方向【防止液体沸腾时溅出伤人】。
i. 加热完毕时要将试管夹从试管口取出;
七、洗涤仪器
1. 洗涤方法:先将试管内的废液倒入废液缸中,再注入试管容积的 1/2的水,振荡后把水倒掉,
这样连洗几次。如果内壁附有不易洗掉的物质,要用试管刷刷洗。
2. 试管刷:刷洗时须转动或上下移动试管刷,但用力不能过猛,以防试管损坏。
3. 仪器洗干净的标准:洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下时,表示仪
器已洗干净。
4. 仪器洗干净后,不能乱放,要倒插在试管架上晾干。
5. 特殊情况
如果玻璃仪器中附有油脂,先用热的纯碱溶液或洗衣粉洗涤,再用水冲洗。
如果玻璃仪器中附有难溶于水的碱、碱性氧化物、碳酸盐,先用稀盐酸溶解,再用水冲
洗。
八、闻气体的方法:用手在瓶口轻轻扇动,仅使极少量的气体进入鼻孔。
九、几种特殊药品的存放:固体药品保存在广口瓶,液体药品保存在细口瓶中
1. 白磷放在盛水的广口瓶中。
白磷是固体,着火点低,易发生自燃保存于水中。(有人说因有水,应放在细口瓶中,这是错误的)
2. 浓硫酸、浓盐酸用磨口瓶盖严。浓硝酸用棕色磨口瓶盖严。------密封保存
浓硫酸具有吸水性,浓盐酸、浓硝酸具有挥发性,浓硝酸见光易分解保存在棕色瓶中。
3. 硝酸银溶液存放在棕色试剂瓶中。(硝酸银溶液见光易分解。)
4、 固体氢氧化钠、氢氧化钾应密封于干燥容器中,并用橡胶塞密封,不能用玻璃塞。
固体氢氧化钠、氢氧化钾具有吸水性,容易潮解,能与空气中二氧化碳反应,且与玻璃(含二氧化
硅)反应,使带有玻璃塞的瓶子难以打开。(SiO+2NaOH =NaSiO+HO)
2 2 3 2作者:六指先生 qq:3099205099
5、金属钾、钠、钙存放在煤油中。(金属钾、钠、钙非常活泼,能与空气中的氧气、水反应)
十、意外事故的处理
1. 失火:用湿抹布或沙子盖灭。
2. 如果不慎将浓硫酸沾到衣服或皮肤上,应立即用布擦拭,再用大量水冲洗,然后涂上3%~5%的碳酸氢
钠溶液。 稀硫酸沾到衣服或皮肤上也要处理,否则稀硫酸的水分蒸发,会变成浓硫酸。
3. 如果不慎将碱液滴到皮肤上,要用较多的水冲洗,然后再涂上 硼酸 ( H BO ) 溶液。
3 3
4. 生石灰沾在皮肤上,要先用布擦去,再用大量水冲洗。
十一、实验基本操作中的数据:
1、向酒精灯里添加酒精要使用漏斗,但酒精量不得超过灯身容积的 2/ 3
2、用试管给液体加热时,还应注意液体体积不宜超过试管容积的 1/ 3 。加热时试管宜倾斜,约与台面
成 4 5 0 角。
3、用试管盛装固体加热时,铁夹应夹在距管口的 1/ 3 处。
4、托盘天平只能用于粗略的称量,能称准到 0. 1 克。
5、用蒸发皿盛装液体时,其液体量不能超过其容积的 1/ 3 。
6、如果不慎将酸溶液沾到皮肤或衣物上,立即用较多的水冲洗(如果是浓硫酸,必须迅速用抹布擦拭,然
后用水冲洗),再用溶质质量分数为 3 ~ 5 % 的碳酸氢钠溶液来冲洗。
7、在实验时取用药品,如果没有说明用量,一般应该按最少量取用:液体取1-2 毫升,固体只需盖满试管
底部。
8、使用试管夹时,应该从试管的底部往上套,固定在离试管口的 1/ 3 处