文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 06 金属和金属材料
目 录
考点过关练 2
考点01 金属材料 2
考点02 合金 3
考点03 金属与氧气反应 4
考点04 金属与酸反应 4
考点05 金属与盐反应 4
考点06 置换反应 5
考点07 金属活动顺序及应用 5
考点08 金属的冶炼 7
考点09 金属锈蚀条件及探究 8
考点10 金属资源的保护 9
真题实战练 10
重难创新练 17
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点 01 金属材料
1. 中国国家博物馆珍藏着一枚“国玺”,即“中华人民共和国中央人民政府之印”,代表着熠熠生辉的共
和国符号。她由铜胎铸字,不易变形。选用这种材料作为印章胎体最大的优点是( )
A. 硬度较大 B. 熔点较高 C. 不溶于水 D. 形状美观
2. 今年6月4日,神州十五号载人飞船(模型图如下)的返回舱经过大气层时,经受住了一千多度的高温
考验,最终成功返回地面。下列说法错误的是( )
A. 太阳翼可将太阳能转化为电能
B. 飞船大量使用密度较小的合金材料,能减轻船体质量
C. 返回舱表面所用的材料具有熔点高、强度大等特点
D. 天线材料采用了钛镍合金,它属于有机合成材料
3. 天舟6号货运飞船在20235月成功发射,标志着我国航天事业可再进一步。科研人员在空间站做了多孔
铜、镁合金等材料性能实验,以及甲烷微重力燃烧实验。
(1)相同质量的镁和铜,含原子数更多的是_____,铜能拉成丝,说明铜具有良好的_____(填序号)。
A.导电性 B.导热性 C.延展性
(2)为了验证Mg(H)Cu的金属活动性顺序,小王同学做了如下两个实验:①将镁条和铜条分别放入相同的
稀硫酸中②将镁条放入CuSO 溶液中。下列有关叙述正确的是_____(填序号)。
4
A.只需要实验①就能得出结论
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.实验②中有红色物质析出
C.实验②反应后溶液的质量减轻
(3)利用甲烷、氧气和氢氧化钠溶液组成的燃料电池可供电。三种物质共同作用生成一种盐和水,该反应的
化学方程式为_____。
考点 02 合金
4. 在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )
A.合金中一定只含金属元素
B.生铁和钢都是铁的合金,且生铁的含碳量更高
C.金属单质在常温下都是固体
D.纯金属的硬度一般比它们组成合金的硬度更高
5. 下列关于合金的说法正确的是( )
A.合金中至少含有两种金属物质 B.合金一定不含有非金属
C.合金的硬度一般比各成分金属大 D.合金不能导电和导热
6. 北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下下列有关金属材料
的说法错误的是( )
A.纯金属和合金都是金属材料
B.生铁的主要成分是碳
C.金制成金箔是利用了金具有良好的延展性
D.一般来说,合金比组成它的纯金属硬度大
7. 氢能源是理想能源,氢能源开发一直是前沿科学研究的课题之一。科学家研发出一种以铝镓合金(镓:
Ca)和水为原料制取氢气的新工艺,流程如下图所示:
(1)氢气是一种能源,它在空气中燃烧的化学方程式是 。氢气被称为“绿色能源”的主要原因是
。
(2)反应①中镓的作用是 ,该反应的化学方程式是 。电解水制取氢气相比,用铝镓合金和水为
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
原料制取氢气的优点是(答出一点即可) 。
考点 03 金属与氧气反应
8.下列关于物质燃烧的现象描述不正确的是( )
A.镁带在空气中燃烧,发出耀眼的白光
B.红磷在空气中燃烧,产生大量白烟
C.铁丝在氧气中燃烧,火星四射
D.铜在空气中加热,生成红色物质
考点 04 金属与酸反应
9.(2022上·北京东城·九年级统考期末)下列金属不能与稀盐酸反应的是( )
A.Cu B.Mg C.Fe D.Al
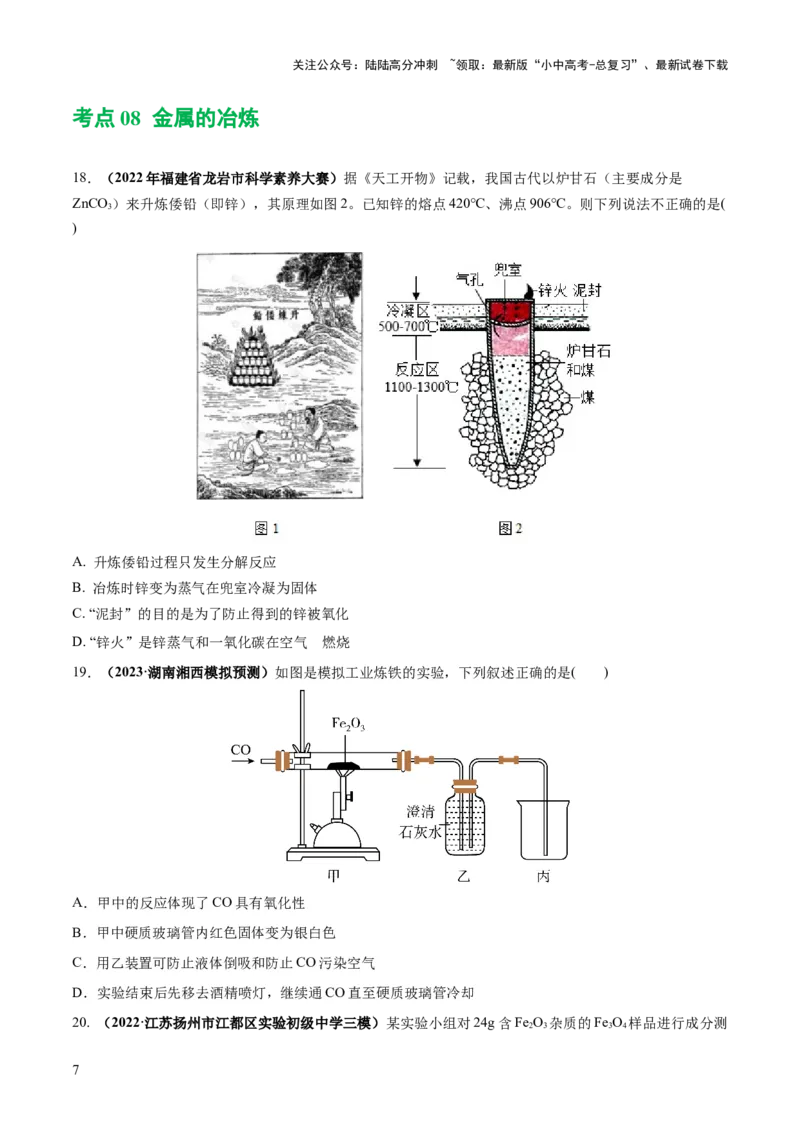
10.(2023·博山区三模)现将等质量且形状相同的甲、乙、丙三种金属,分别放入三份溶质质量分数相同
的足量稀硫酸中,产生氢气的质量随反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为
+2)。下列说法不正确的是( )
A.相对原子质量:甲<乙<丙
B.金属活动性:乙<丙<甲
C.消耗硫酸的质量:甲<乙<丙
D.甲、乙、丙可能分别是镁、铁、锌
考点 05 金属与盐反应
11.(2023·山东省青岛市中考化学真题)向含有硝酸银和硝酸铜的废液中加入—定质量的锌粉,充分反应
后过滤,将滤渣洗涤、干燥、称量,所得滤渣的质量与加入锌粉的质量相等。下列说法不正确的是( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.滤液可能呈蓝色 B.滤渣中至少含有两种物质
C.向滤渣中滴加稀盐酸,一定没有气泡产生 D.向滤液中滴加稀盐酸,一定没有白色沉淀生成
12.(2023·河北沧州校考模拟预测)将一定质量的锌粉加入含硝酸银和硝酸铜的混合溶液中,充分反应。
反应过程中固体质量与加入锌粉的质量关系如图所示。下列说法正确的是( )
A.a点固体为锌和银
B.b点固体中加入稀盐酸有气泡产生
C.c点溶液为无色
D.d点固体为银和铜
考点 06 置换反应
13.(2022·湖南株洲中考真题)下列反应中,属于置换反应的是( )
A.CaCO 3 +CO 2 +H 2 O=Ca(HCO 3 ) 2 B.CuCl 2Cu+Cl2 ↑
C.3CO+Fe 2 O 32Fe+3CO2 D.Fe+CuSO 4 =FeSO 4 +Cu
14.(2022·萧县模考)下列化合物可以通过金属与对应的酸发生置换反应获得的是( )
A.CuCl B.FeCl C.AgNO D.Al (SO )
2 3 3 2 4 3
考点 07 金属活动顺序及应用
15.(2023·山东聊城中考真题)为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的
是
A.将Fe、Cu、Ag分别放入稀盐酸中( )
B.将Cu分别放入FeCl 、AgNO 溶液中
2 3
C.将Cu、Ag分别放入FeSO 溶液中
4
D.将Fe放入稀盐酸、Cu放入AgNO 溶液中
3
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
16.(2023·河南中考真题)某化学小组用下图所示实验装置,探究铝、铜、银的金属活动性顺序。
(1)铝丝浸入溶液前需要先用砂纸打磨,其目的是什么?
(2)请写出装置A或B中发生反应的化学方程式。
(3)通过图示中的实验不能判断铜、银的金属活动性顺序,请补充实验继续探究。(简要叙述实验步骤)
17.(2023·山东省烟台市中考真题)垃圾是放错地方的资源,城市的废旧电器是一座“金属矿山”,某废
旧电器中含有锌、铜、镍(Ni)三种金属,兴趣小组的同学为了从中回收金属铜和镍,做了如下的探究。
已知:硫酸镍(化学式NiSO )能溶于水。
4
实验一:探究锌、铜、镍三种金属在溶液中的活动性强弱
【提出猜想】兴趣小组结合常见金属活动性顺序,提出了以下猜想。
猜想一:Zn>Ni>Cu;猜想二:Zn> Cu > Ni;猜想三: 。
【进行实验】兴趣小组进行了如下的实验,请完成实验报告。
实验步骤 实验现象 解释与结论
取三支试管,分别向其中加入等质量、等浓 锌片表面产生的气泡较 猜想 正确。镍与稀
度的稀硫酸,然后将大小、形状相同的锌、 快;镍片表面产生的气泡 硫酸反应的化学方程式是
铜、镍三种金属片分别插入三支试管中。 较慢;铜片无明显现象。 。
实验二:从含有锌、铜、镍三种金属的废旧电器中回收铜和镍
【设计方案】兴趣小组设计了如图所示的物质转化流程。
步骤①中得到的A是 。步骤②中生成C的化学方程式是 。
【反思评价】合理开发城市“金属矿山”的意义是 (答1条)。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点 08 金属的冶炼
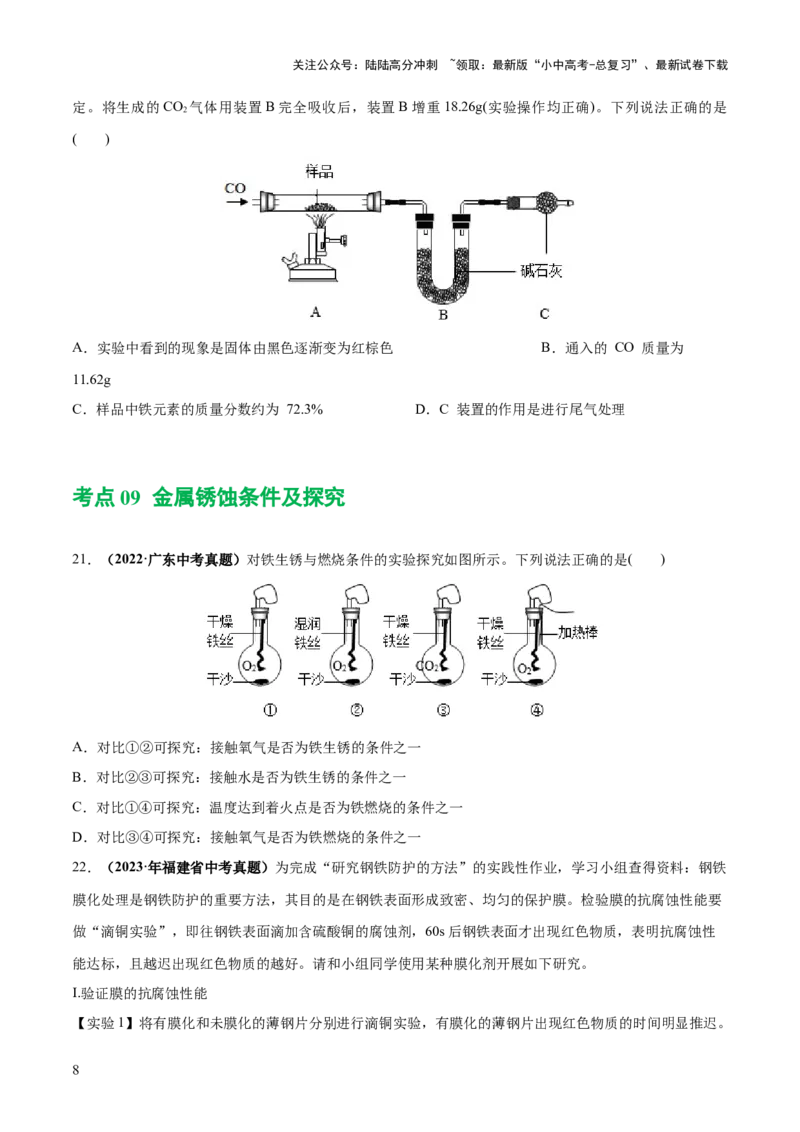
18.(2022年福建省龙岩市科学素养大赛)据《天工开物》记载,我国古代以炉甘石(主要成分是
ZnCO )来升炼倭铅(即锌),其原理如图2。已知锌的熔点420℃、沸点906℃。则下列说法不正确的是(
3
)
A. 升炼倭铅过程只发生分解反应
B. 冶炼时锌变为蒸气在兜室冷凝为固体
C. “泥封”的目的是为了防止得到的锌被氧化
D. “锌火”是锌蒸气和一氧化碳在空气 的燃烧
19.(2023·湖南湘西模拟预测)如图是模拟工业炼铁的实验,下列叙述正确的是( )
A.甲中的反应体现了CO具有氧化性
B.甲中硬质玻璃管内红色固体变为银白色
C.用乙装置可防止液体倒吸和防止CO污染空气
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
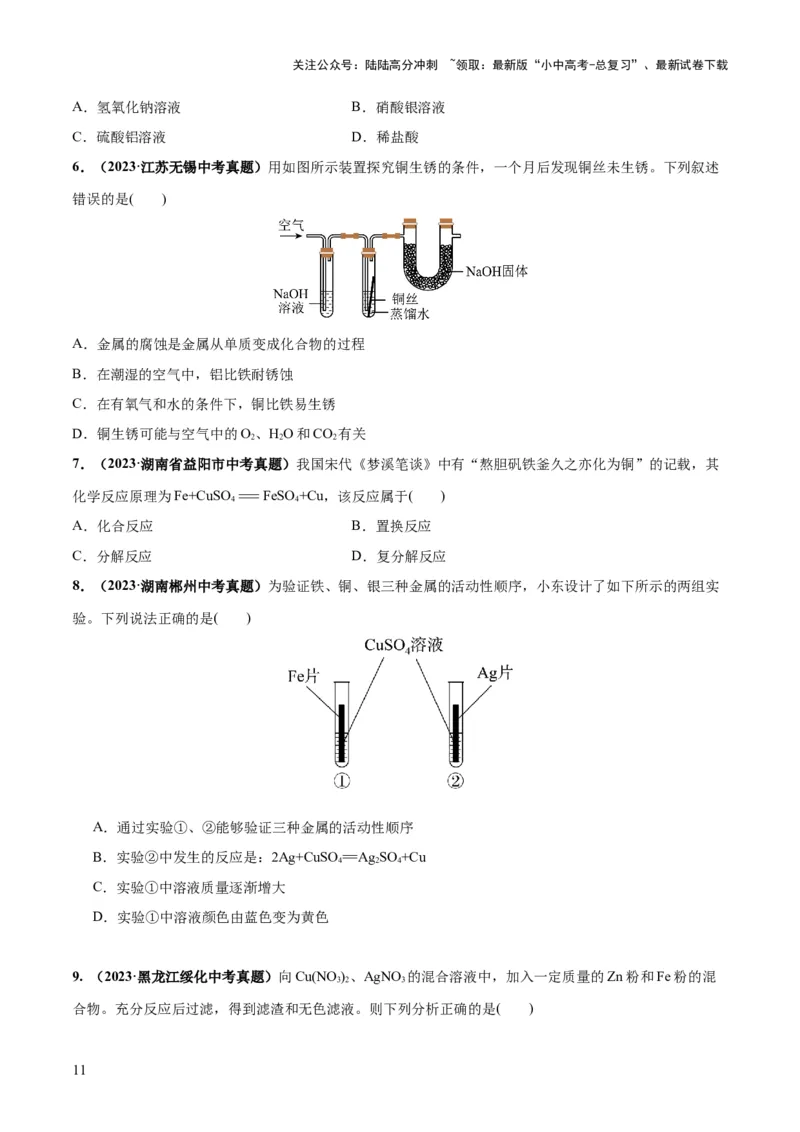
20. (2022·江苏扬州市江都区实验初级中学三模)某实验小组对24g含Fe O 杂质的Fe O 样品进行成分测
2 3 3 4
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
定。将生成的CO 气体用装置B完全吸收后,装置B增重18.26g(实验操作均正确)。下列说法正确的是
2
( )
A.实验中看到的现象是固体由黑色逐渐变为红棕色 B.通入的 CO 质量为
11.62g
C.样品中铁元素的质量分数约为 72.3% D.C 装置的作用是进行尾气处理
考点 09 金属锈蚀条件及探究
21.(2022·广东中考真题)对铁生锈与燃烧条件的实验探究如图所示。下列说法正确的是( )
A.对比①②可探究:接触氧气是否为铁生锈的条件之一
B.对比②③可探究:接触水是否为铁生锈的条件之一
C.对比①④可探究:温度达到着火点是否为铁燃烧的条件之一
D.对比③④可探究:接触氧气是否为铁燃烧的条件之一
22.(2023·年福建省中考真题)为完成“研究钢铁防护的方法”的实践性作业,学习小组查得资料:钢铁
膜化处理是钢铁防护的重要方法,其目的是在钢铁表面形成致密、均匀的保护膜。检验膜的抗腐蚀性能要
做“滴铜实验”,即往钢铁表面滴加含硫酸铜的腐蚀剂,60s后钢铁表面才出现红色物质,表明抗腐蚀性
能达标,且越迟出现红色物质的越好。请和小组同学使用某种膜化剂开展如下研究。
I.验证膜的抗腐蚀性能
【实验1】将有膜化和未膜化的薄钢片分别进行滴铜实验,有膜化的薄钢片出现红色物质的时间明显推迟。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)出现红色物质的原因是_________________(用化学方程式表示)。
的
(2)有膜化 薄钢片出现红色物质的时间明显推迟,其原因是_________________。
Ⅱ.探究膜化条件对膜层外观的影响
【实验2】其他条件相同时,将薄钢片放入pH=3、不同温度的膜化剂中浸泡20min,观察钢片表面形成的
膜层外观。结果如下:
温度℃ 50 60 70 80
膜层外观 粗糙 致密、均匀 致密、均匀 粗糙
【实验3】已知pH≥3.5时,膜化剂不稳定。其他条件相同时,将薄钢片放入60℃、不同pH的膜化剂中浸
泡20min,观察钢片表面形成的膜层外观。结果如下:
pH 1.5 2.0 2.5 3.0
膜层外观 易脱落 粗糙 致密、均匀 致密、均匀
(3)实验3的目的是_________________。
(4)根据实验2、实验3的结果,膜层外观符合要求的温度、pH的范围依次为_________、________。
Ⅲ.确定抗腐蚀性能较好的膜化条件
【实验4】依次选取实验2、实验3膜层外观符合要求的钢片进行对比实验,分别确定适宜的温度、pH。
的
(5)实验4中,确定适宜温度 实验方案是_________________。
IV.实践反思
(6)反思上述实践活动,提出一个关于钢铁膜化处理可进一步探究的问题。
答:_________________。
考点 10 金属资源的保护
23.(2023·山东青岛中考真题)防止金属锈蚀能有效保护金属资源。下列防锈方法中,与其它三种方法原
理不同的是( )
A.表面涂油 B.表面刷漆
C.覆盖塑料 D.制成合金
24.(2023·广西中考真题)下列做法不能有效保护金属资源的是( )
A.防止金属腐蚀 B.寻找金属的代用品
C.回收利用废旧金属 D.肆意开采金属矿物
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.(2023·江苏常州中考真题)同学们收集的下列矿石样品中,主要成分为Fe O 的是( )
3 4
A.赤铁矿 B.磁铁矿
C.孔雀石 D.铝土矿
2.(2023江苏苏州真题)中华文明源远流长,文物承载着文明的记忆。下列苏州博物馆馆藏文物中主要
由金属材料制成的是( )
A. 清代瓷盘 B. 明代书轴
C. 西周铜鼎 D. 宋代石函
3.(2023重庆中考真题B卷)铁和铜在自然环境中都能被腐蚀。下列不能说明铁比铜活泼的事实是( )
A. 历史上铜比铁使用更早 B. 铁的文物比铜的稀有
C. 氧化铁能与盐酸反应而铜单质不能 D. 铁能与硫酸铜溶液反应
4.(2023江苏省扬州市中考)下列对实验现象的解释不正确的是( )
选项 实验现象 解释
A 将50mL水和50mL酒精混合,总体积小于100mL 分子之间有空隙
B 向锌粒中加入稀硫酸,产生气泡 金属均能与酸反应产生H
2
C 将黄铜片和铜片相互刻画,铜片表面有明显划痕 合金的硬度往往比其成分金属大
D 铁丝在空气中不能燃烧,在氧气中可以燃烧 氧气的浓度对物质的燃烧有影响
A.A B.B C.C D.D
5.(2023·湖南省湘潭市中考化学真题)将光亮的铜丝插入下列溶液中,有明显现象的是( )
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.氢氧化钠溶液 B.硝酸银溶液
C.硫酸铝溶液 D.稀盐酸
6.(2023·江苏无锡中考真题)用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述
错误的是( )
A.金属的腐蚀是金属从单质变成化合物的过程
B.在潮湿的空气中,铝比铁耐锈蚀
C.在有氧气和水的条件下,铜比铁易生锈
D.铜生锈可能与空气中的O、HO和CO 有关
2 2 2
7.(2023·湖南省益阳市中考真题)我国宋代《梦溪笔谈》中有“熬胆矾铁釜久之亦化为铜”的记载,其
化学反应原理为Fe+CuSO=FeSO +Cu,该反应属于( )
4 4
A.化合反应 B.置换反应
C.分解反应 D.复分解反应
8.(2023·湖南郴州中考真题)为验证铁、铜、银三种金属的活动性顺序,小东设计了如下所示的两组实
验。下列说法正确的是( )
A.通过实验①、②能够验证三种金属的活动性顺序
B.实验②中发生的反应是:2Ag+CuSO =Ag SO +Cu
4 2 4
C.实验①中溶液质量逐渐增大
D.实验①中溶液颜色由蓝色变为黄色
9. (2023·黑龙江绥化中考真题)向Cu(NO )、AgNO 的混合溶液中,加入一定质量的Zn粉和Fe粉的混
3 2 3
合物。充分反应后过滤,得到滤渣和无色滤液。则下列分析正确的是( )
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.滤渣中一定有Ag、Cu、Fe,可能有Zn
B.滤渣中一定有Ag、Cu,可能有Fe
C.滤液中一定有Zn(NO ),可能有AgNO
3 2 3
D.滤液中一定有Zn(NO ),可能有Fe(NO )
3 2 3 2
10.(2023四川省眉山市中考)实验设计是实验探究的基本环节。下列实验设计能达到对应实验目的的是
( )
选
实验目的 实验设计
项
A 鉴别白酒和白糖水 观察颜色
B 除去KCl溶液中的少量KSO 加适量BaCl 溶液,过滤
2 4 2
C 除去氨气中的水蒸气 将气体通过浓硫酸
D 探究铜、银的金属活动性顺序 将铜丝、银丝分别浸入稀盐酸溶液中
A.A B.B C.C D.D
11.(2023湖南省湘潭市中考化学真题)中国传统文化对人类文明贡献巨大,很多诗句和典籍中都蕴含着
化学知识。
(1)“春蚕到死丝方尽”所描述的蚕丝属于 (填“天然”或“合成”)纤维。
(2)“千锤万凿出深山,烈火焚烧若等闲”中“烈火焚烧”是指高温煅烧石灰石,该反应的化学方程式是
。
(3)“千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”和“漉”相当于化学实验中的 操作,实验室里进
行该操作用到的玻璃仪器有烧杯、 和玻璃棒。
(4)《天工开物》中记载了“古法炼铁”如图1和“炒钢法”如图2
①在图1的炉中鼓入与矿物逆流而行的空气,“逆流而行”的目的是 ;再利用生成的一氧化碳和氧
化铁反应生成铁单质,该反应的化学方程式是 ,此反应中体现了一氧化碳的 (填“氧化”或
“还原”)性。
②“炒钢法”即“持柳棍疾搅即时炒成熟铁,炒过稍冷之时,或有就塘内斩划方块者”。不断翻炒液态生
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
铁,是为了降低生铁中 元素的含量。
12.(2023·山东省威海市中考真题)典籍里的化学
《天工开物》是我国古代劳动人民在长期生产生活实践中总结出来的宝贵财富,其中蕴含很多化学知识与
方法。
(1)颜料制取:“水银入石亭脂(天然硫),同研……得银朱(HgS)。” 银朱是古代作画的红色颜料。请写出
制取银朱的化学方程式 。
(2)池盐制取(图1):将盐池内清水(含有Na+、Cl-、Mg2+、SO等)引入旁边耕成畦垄的地里。“待夏秋之交,
南风(热风)大起,则一宵(一夜)结成,曰颗盐(粗盐)。”若盐析出时刮东北风(冷风),则味苦(含硫酸镁)色恶,
不堪食用。
请根据溶解度曲线(图2),解释刮东北风(冷风)时析出盐且味苦的原因 。
(3)生石灰的制取和应用(图3):“每煤饼一层,垒石(石灰石)一层,铺薪其底,灼火燔(灼烧)之,火力到后,
烧酥石性。以水沃之,亦自解散……成质之后,入水永劫不坏”。
①“灼火燔之”涉及的化学方程式为 ,该反应的基本反应类型是 。
②“解散”是因为生石灰遇水由块状变成粉末。该粉末的主要成分是 (填化学式)。粉末“成质之后,
入水永劫不坏”,可用于船只、墙壁的填缝防水。请写出“粉末成质”的化学方程式 ;根据“入
水永劫不坏”,推测“成质”后的产物具有的性质是 (写一条即可)。
13.(2023辽宁省丹东市中考真题)金属广泛应用于生活、生产中,其应用推动了社会发展。
(1)铁铸成铁锅是利用了铁具有良好的 性;铁锅用于烹饪食物是利用铁具有良好的 性;使用后
的铁锅最好洗净后 ,再涂上食用油以防生锈。
(2)世界上每年因腐蚀而报废的铁, 以上得到了回收利用。回收利用废旧金属的意义是 (答一点
即可)。
(3)早在春秋战国时期,我国就利用铁矿石与木炭为原料冶炼生铁,在冶炼过程中将铁矿石粉碎,其目的是
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。现代工业用赤铁矿(主要成分为 )与一氧化碳在高温条件下冶炼生铁,该反应的化学方程式是
。
(4)我国高铁技术在世界处于领先地位。铁轨材料用钢而不用纯铁,原因是钢的强度和硬度比纯铁
(填“大”或“小”)。
14.(2022·山东威海中考真题)物尽其用——金属之“铝”
社会发展离不开金属,生产生活中铁、铝及其合金制品随处可见。
(1)铝制易拉罐(如图1)
某品牌碳酸饮料的易拉罐是由铝合金制成的,内壁附着一层有机薄膜。该铝合金中铝的含量约为97%,还
含有镁、锰、铁、铟(In)等。
①将易拉罐剪成条状,打磨后与纯铝片相互刻画,发现纯铝片表面有划痕,说明 _____。
②请你推测组成有机薄膜的物质具有的性质:_____、_____(写两条即可)。
③“是否应该停止使用铝制易拉罐”是当前的一个社会性科学议题。有同学认为应该停止使用铝制易拉罐,
理由可能 _____(写一条即可);也有同学支持继续使用铝制易拉罐,请你结合铝的性质阐述理由 _____、
_____(写两条即可)。
④生活垃圾要分类投放,可与废弃易拉罐作为同一类投放的是 _____(填字母序号)。
A.废旧电池
B.废弃口罩
C.厨余垃圾
D.废旧铁锅
(2)储氢材料
储氢材料的研发是氢能源技术的关键之一。金属铝可用作储氢材料,储氢后生成氢化铝(AlH),其中氢
3
元素的化合价为 _____;释氢原理为氢化铝与水反应释放氢气,同时生成氢氧化铝,其反应的化学方程式
为 _____。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)制备铝
工业上常用电解氧化铝的方法制备金属铝,反应的化学方程式为 _____。
(4)铝合金中的铟(In)
如图2为铝、铟的原子结构示意图。某同学推测金属铟与铝的化学性质相似,理由是 _____。实验证明,
铟可以与稀盐酸反应,其反应的化学方程式为 _____。
15.(2023·江苏省苏州市中考真题)中国古代已掌握了铜冶炼和铸造技术,现代铜冶炼废气、废水需经过
处理后排放。
Ⅰ、铜的冶炼与防腐
(1)如图所示一氧化碳还原氧化铜的实验,硬质玻璃管内出现______(现象),证明反应已经发生。
(2)上述实验获得的Cu中含有少量黑色的CuO。请补充完整提纯铜的实验方案:
将所得固体置于烧杯中,______,干燥。(可选用的试剂:稀HSO 、AgNO 溶液、NaOH溶液,蒸馏
2 4 3
水)
(3)《周礼·考工记》中记载了铸造各类青铜器的配方。铜和青铜的相关性质见下表,推断铜冶炼过程中熔
入锡的作用有______
铜 青铜(含25%的锡)
熔点 1085℃ 800℃
硬度 3.0 5~6.6
注:硬度以金刚石的硬度10为标准,1表示很软,10表示很硬。
(4)某同学设计实验探究铜锈蚀产生铜绿[Cu (OH) CO]的条件(如图所示),图中铜片上最不易产生铜
2 2 3
绿的是______(填序号)。
A. B. C. D.
Ⅱ、湿法炼铜废水的处理
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
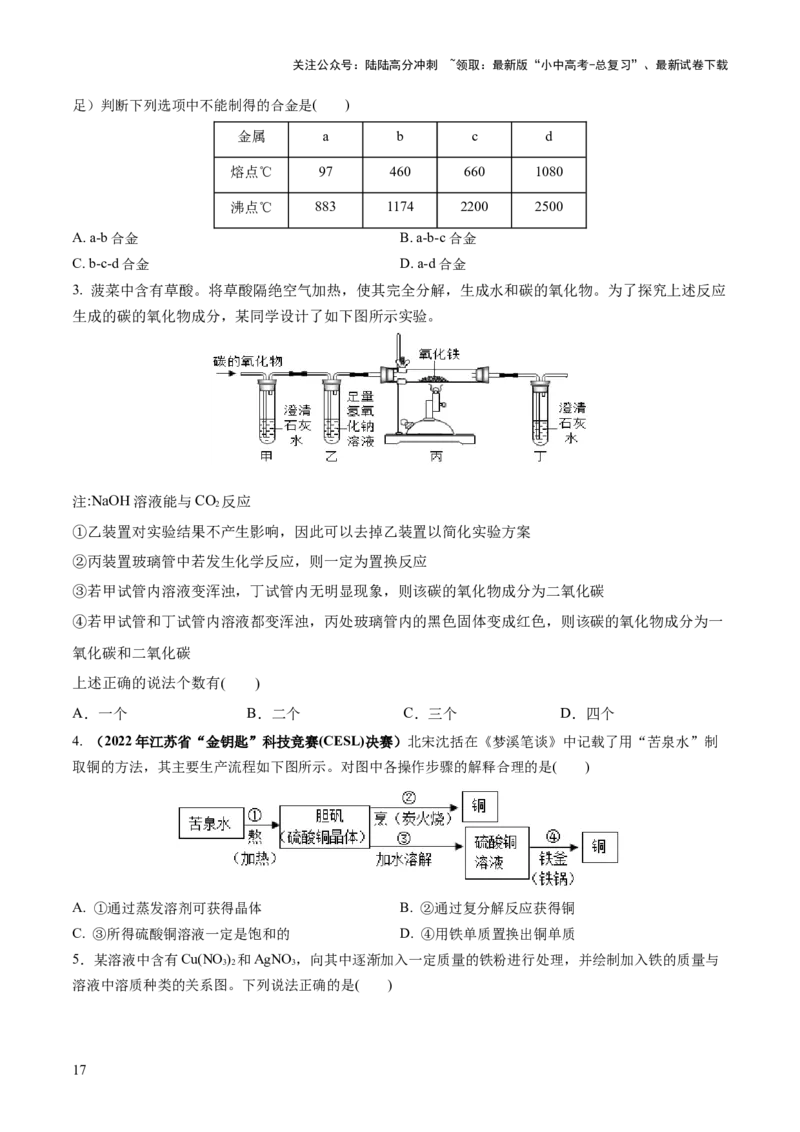
(5)湿法炼铜产生酸性废水,含有的CuSO 、ZnSO 可用铁炭混合物(铁粉和活性炭的混合物)除去。其他
4 4
条件不变,废水pH对 、 去除率的影响如图所示。
①pH<3时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为______。
②相同pH条件下, 的去除率远高于 的原因可能是______。
Ⅲ、工业铜冶炼废气的处理
(6)工业上利用反应Cu
2
O +O 22Cu+SO
2
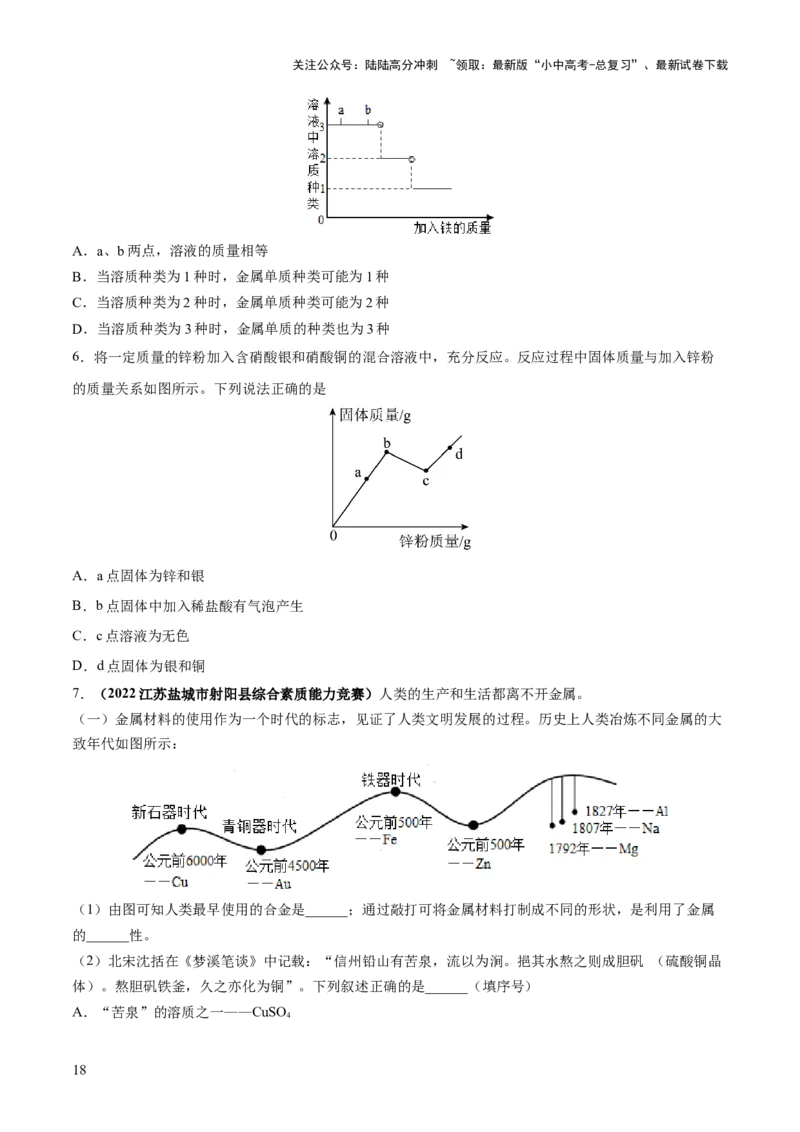
冶炼得到Cu,冶炼产生的烟气中含多种成分。经过水洗除尘后,烟
气中部分气体分子的百分含量(×100%)随温度变化如图所示。
①图中虚线表示SO 或O 的变化,其中曲线X表示的物质是______。
2 2
②当500℃烟气温度下降时,SO 含量降低的主要原因是______(用化学方程式表示)。
3
③温度低于200℃时,烟气中几乎不存在水分子的主要原因是______。
1.(2022年江苏省“金钥匙”科技竞赛(CESL)初赛)一般情况下,两种活动性不同的金属在潮湿的环
境中接触时,活动性强的金属首先被腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶
嵌的金属是( )
A. 银块 B. 铜块 C. 铁块 D. 锌块
2.(湖南怀化市2020-2021下学期6月化学竞赛)根据如表所列金属的溶点和沸点的数据(其他条件均已满
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
足)判断下列选项中不能制得的合金是( )
金属 a b c d
熔点℃ 97 460 660 1080
沸点℃ 883 1174 2200 2500
A. a-b合金 B. a-b-c合金
C. b-c-d合金 D. a-d合金
3. 菠菜中含有草酸。将草酸隔绝空气加热,使其完全分解,生成水和碳的氧化物。为了探究上述反应
生成的碳的氧化物成分,某同学设计了如下图所示实验。
注:NaOH溶液能与CO 反应
2
①乙装置对实验结果不产生影响,因此可以去掉乙装置以简化实验方案
②丙装置玻璃管中若发生化学反应,则一定为置换反应
③若甲试管内溶液变浑浊,丁试管内无明显现象,则该碳的氧化物成分为二氧化碳
④若甲试管和丁试管内溶液都变浑浊,丙处玻璃管内的黑色固体变成红色,则该碳的氧化物成分为一
氧化碳和二氧化碳
上述正确的说法个数有( )
A.一个 B.二个 C.三个 D.四个
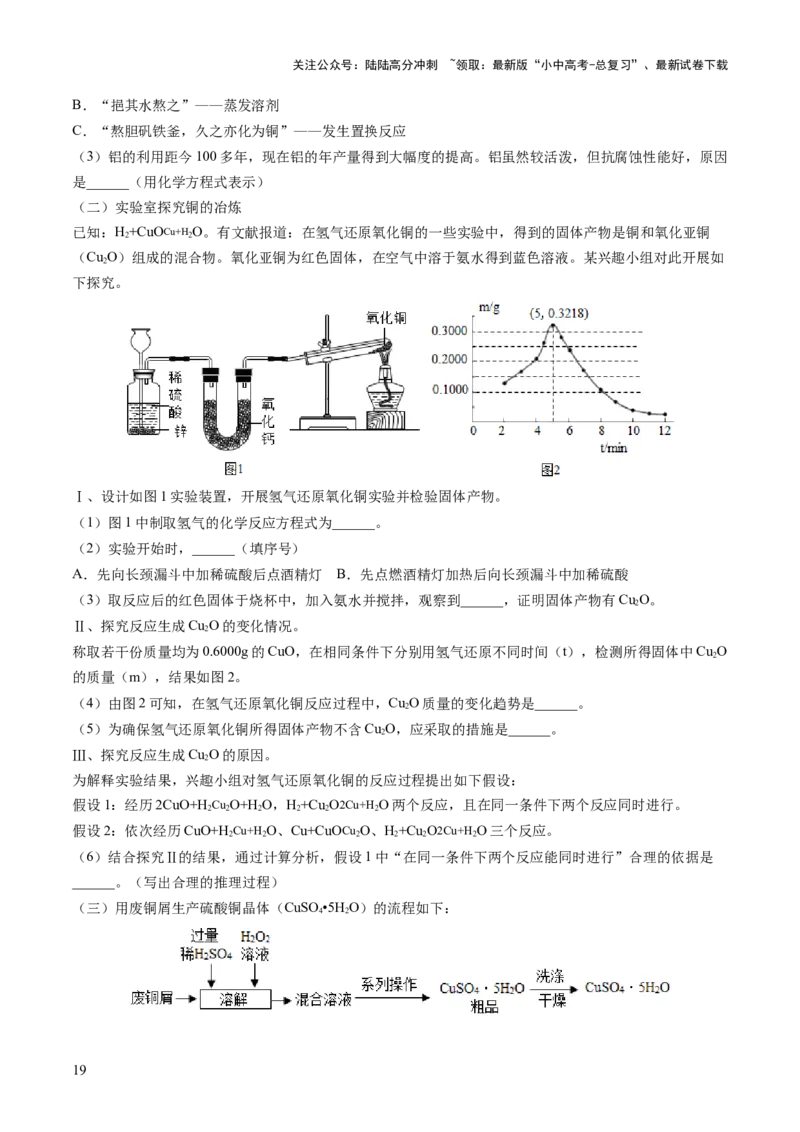
4. (2022年江苏省“金钥匙”科技竞赛(CESL)决赛)北宋沈括在《梦溪笔谈》中记载了用“苦泉水”制
取铜的方法,其主要生产流程如下图所示。对图中各操作步骤的解释合理的是( )
A. ①通过蒸发溶剂可获得晶体 B. ②通过复分解反应获得铜
C. ③所得硫酸铜溶液一定是饱和的 D. ④用铁单质置换出铜单质
5.某溶液中含有Cu(NO ) 和AgNO,向其中逐渐加入一定质量的铁粉进行处理,并绘制加入铁的质量与
3 2 3
溶液中溶质种类的关系图。下列说法正确的是( )
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.a、b两点,溶液的质量相等
B.当溶质种类为1种时,金属单质种类可能为1种
C.当溶质种类为2种时,金属单质种类可能为2种
D.当溶质种类为3种时,金属单质的种类也为3种
6.将一定质量的锌粉加入含硝酸银和硝酸铜的混合溶液中,充分反应。反应过程中固体质量与加入锌粉
的质量关系如图所示。下列说法正确的是
A.a点固体为锌和银
B.b点固体中加入稀盐酸有气泡产生
C.c点溶液为无色
D.d点固体为银和铜
7.(2022江苏盐城市射阳县综合素质能力竞赛)人类的生产和生活都离不开金属。
(一)金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。历史上人类冶炼不同金属的大
致年代如图所示:
(1)由图可知人类最早使用的合金是______;通过敲打可将金属材料打制成不同的形状,是利用了金属
的______性。
(2)北宋沈括在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾 (硫酸铜晶
体)。熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是______(填序号)
A.“苦泉”的溶质之一——CuSO
4
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.“挹其水熬之”——蒸发溶剂
C.“熬胆矾铁釜,久之亦化为铜”——发生置换反应
(3)铝的利用距今100多年,现在铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因
是______(用化学方程式表示)
(二)实验室探究铜的冶炼
已知:H+CuOCu+HO。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜
2 2
(Cu O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如
2
下探究。
Ⅰ、设计如图1实验装置,开展氢气还原氧化铜实验并检验固体产物。
(1)图1中制取氢气的化学反应方程式为______。
(2)实验开始时,______(填序号)
A.先向长颈漏斗中加稀硫酸后点酒精灯 B.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
(3)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到______,证明固体产物有Cu O。
2
Ⅱ、探究反应生成Cu O的变化情况。
2
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu O
2
的质量(m),结果如图2。
(4)由图2可知,在氢气还原氧化铜反应过程中,Cu O质量的变化趋势是______。
2
(5)为确保氢气还原氧化铜所得固体产物不含Cu O,应采取的措施是______。
2
Ⅲ、探究反应生成Cu O的原因。
2
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1:经历2CuO+HCu O+HO,H+Cu O2Cu+H O两个反应,且在同一条件下两个反应同时进行。
2 2 2 2 2 2
假设2:依次经历CuO+HCu+H O、Cu+CuOCu O、H+Cu O2Cu+H O三个反应。
2 2 2 2 2 2
(6)结合探究Ⅱ的结果,通过计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是
______。(写出合理的推理过程)
(三)用废铜屑生产硫酸铜晶体(CuSO •5H O)的流程如下:
4 2
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(7)“溶解”时发生的化学反应方程式为______。
(8)“洗涤、干燥”过程中常用95%的酒精做洗涤剂,优点是______。
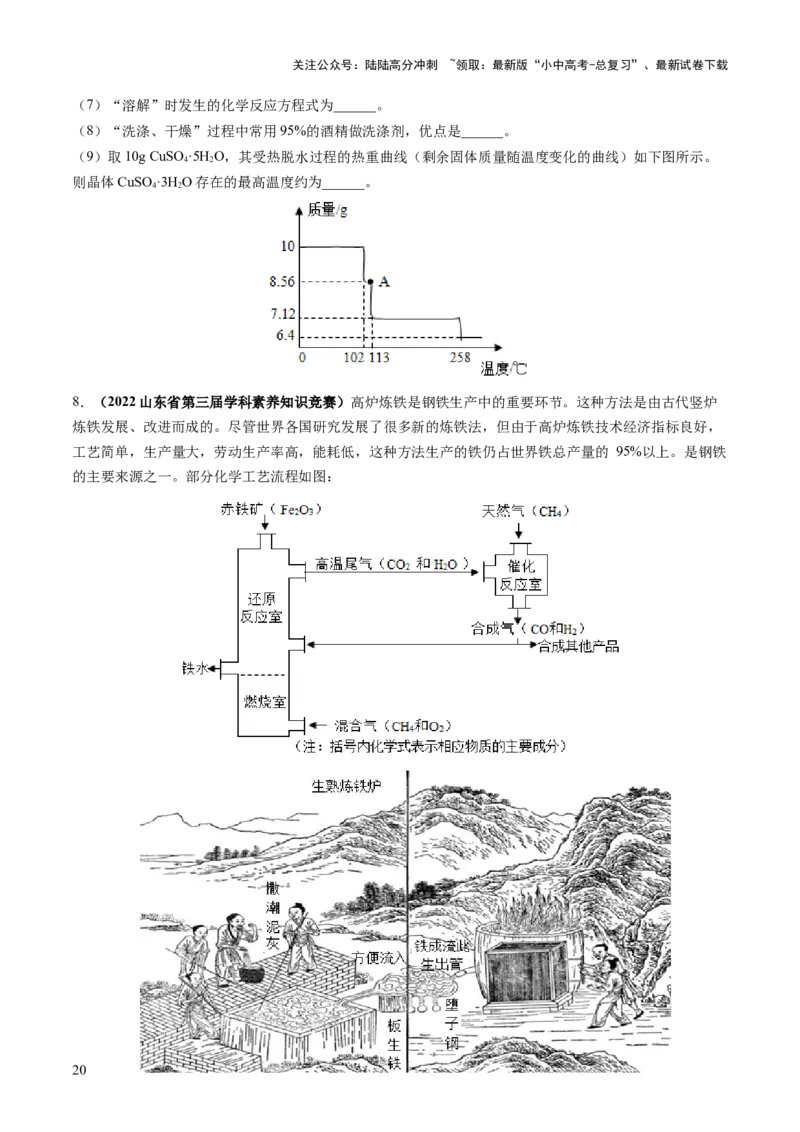
(9)取10g CuSO ·5H O,其受热脱水过程的热重曲线(剩余固体质量随温度变化的曲线)如下图所示。
4 2
则晶体CuSO ·3H O存在的最高温度约为______。
4 2
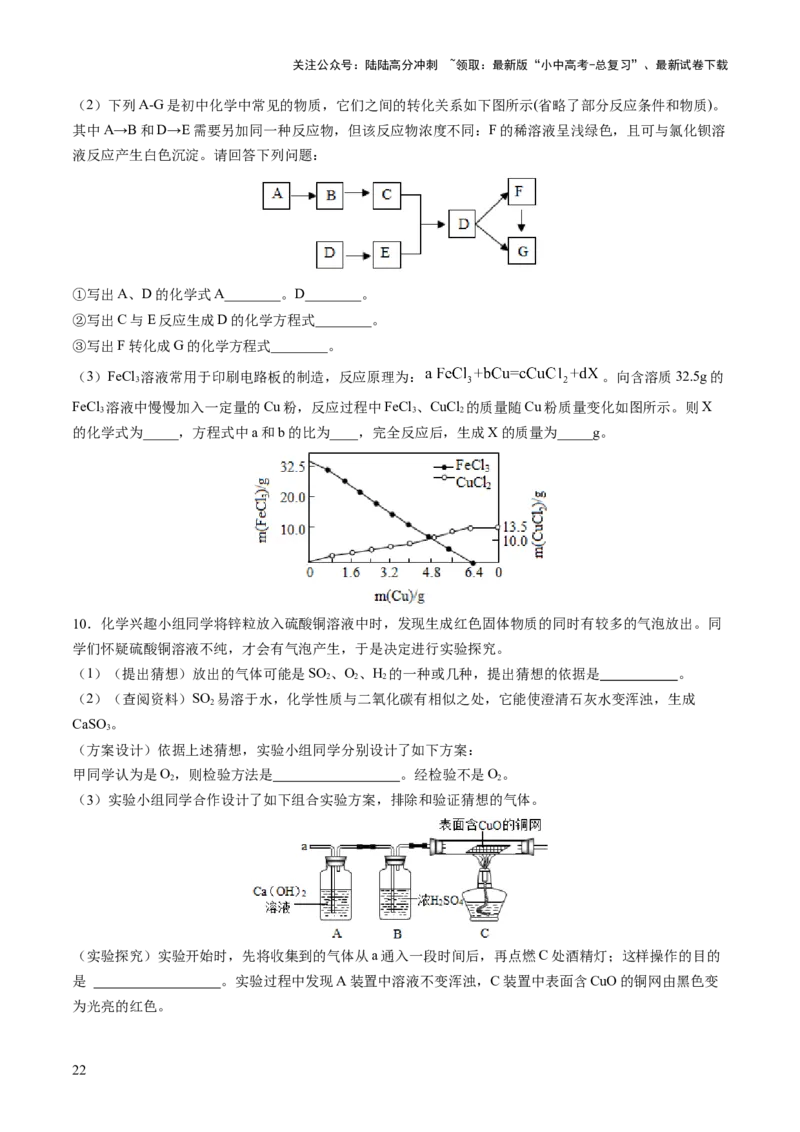
8.(2022山东省第三届学科素养知识竞赛)高炉炼铁是钢铁生产中的重要环节。这种方法是由古代竖炉
炼铁发展、改进而成的。尽管世界各国研究发展了很多新的炼铁法,但由于高炉炼铁技术经济指标良好,
工艺简单,生产量大,劳动生产率高,能耗低,这种方法生产的铁仍占世界铁总产量的 95%以上。是钢铁
的主要来源之一。部分化学工艺流程如图:
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)主要化学反应原理是: ________________。(用化学方程式表示)
(2)催化反应室的化学反应方程式为 ________________。
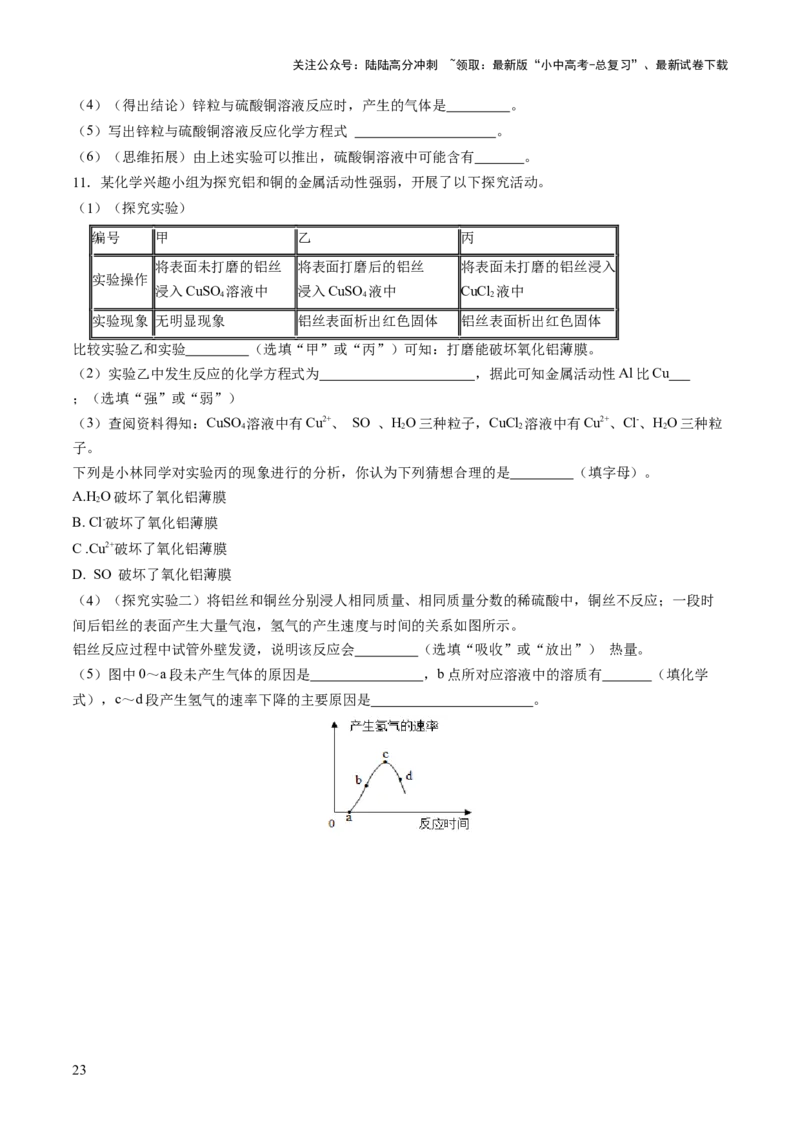
(3)明朝宋应星所著《天工开物》中我国古代炼铁图(如上图)。
①《天工开物》中炼铁的第一步与下图的________________原理相似。
②若原料为磁铁矿,生成“堕子钢”的化学反应方程式为________________。
③以下产物是混合物的是 _______________。(只用写字母即可,下同)
A 铁水 B碳的燃烧产物 C空气 D生铁 E熟铁 F纯铁
(4)提炼铜的方法主要有火法炼铜和湿法炼铜。火法炼铜包括熔炼、吹炼、精炼等工序。湿法炼铜是用
硫酸将铜矿中的铜置换出来。提炼铜的方法有 。
A. 精炼 B. 高炉 C. 吹炼 D. 化铜 E. 置换 F. 化合
9.(2022年江苏省“金钥匙”科技竞赛(CESL)决赛)金属的使用是人类社会文明发展的重要标志。金属
的治炼和金属性质的研究是化学研究的重要组成部分。
(1)地壳中含量最丰富的金属元素是______;从人类对自然资源利用的技术水平看,人类社会依次经历
了石器时代、_____、铁器时代:某金属及其合金有很好的抗腐蚀性能,熔点高、密度小,被广泛用于航
空航天器和人造关节等的制造,这种金属是______;在元素周期表中,有相邻的17种金属元素,被称为
“工业的维生素”,它们的性质非常相似,这类金属元素统称为______元素。
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)下列A-G是初中化学中常见的物质,它们之间的转化关系如下图所示(省略了部分反应条件和物质)。
其中A→B和D→E需要另加同一种反应物,但该反应物浓度不同:F的稀溶液呈浅绿色,且可与氯化钡溶
液反应产生白色沉淀。请回答下列问题:
①写出A、D的化学式A________。D________。
②写出C与E反应生成D的化学方程式________。
③写出F转化成G的化学方程式________。
(3)FeCl 溶液常用于印刷电路板的制造,反应原理为: 。向含溶质32.5g的
3
FeCl 溶液中慢慢加入一定量的Cu粉,反应过程中FeCl 、CuCl 的质量随Cu粉质量变化如图所示。则X
3 3 2
的化学式为_____,方程式中a和b的比为____,完全反应后,生成X的质量为_____g。
10.化学兴趣小组同学将锌粒放入硫酸铜溶液中时,发现生成红色固体物质的同时有较多的气泡放出。同
学们怀疑硫酸铜溶液不纯,才会有气泡产生,于是决定进行实验探究。
(1)(提出猜想)放出的气体可能是SO 、O、H 的一种或几种,提出猜想的依据是 。
2 2 2
(2)(查阅资料)SO 易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成
2
CaSO。
3
(方案设计)依据上述猜想,实验小组同学分别设计了如下方案:
甲同学认为是O,则检验方法是 。经检验不是O。
2 2
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
(实验探究)实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;这样操作的目的
是 。实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变
为光亮的红色。
22关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)(得出结论)锌粒与硫酸铜溶液反应时,产生的气体是 。
(5)写出锌粒与硫酸铜溶液反应化学方程式 。
(6)(思维拓展)由上述实验可以推出,硫酸铜溶液中可能含有 。
11.某化学兴趣小组为探究铝和铜的金属活动性强弱,开展了以下探究活动。
(1)(探究实验)
编号 甲 乙 丙
将表面未打磨的铝丝 将表面打磨后的铝丝 将表面未打磨的铝丝浸入
实验操作
浸入CuSO 溶液中 浸入CuSO 液中 CuCl 液中
4 4 2
实验现象 无明显现象 铝丝表面析出红色固体 铝丝表面析出红色固体
比较实验乙和实验 (选填“甲”或“丙”)可知:打磨能破坏氧化铝薄膜。
(2)实验乙中发生反应的化学方程式为 ,据此可知金属活动性Al比Cu
;(选填“强”或“弱”)
(3)查阅资料得知:CuSO 溶液中有Cu2+、 SO 、HO三种粒子,CuCl 溶液中有Cu2+、Cl-、HO三种粒
4 2 2 2
子。
下列是小林同学对实验丙的现象进行的分析,你认为下列猜想合理的是 (填字母)。
A.HO破坏了氧化铝薄膜
2
B. Cl-破坏了氧化铝薄膜
C .Cu2+破坏了氧化铝薄膜
D. SO 破坏了氧化铝薄膜
(4)(探究实验二)将铝丝和铜丝分别浸人相同质量、相同质量分数的稀硫酸中,铜丝不反应;一段时
间后铝丝的表面产生大量气泡,氢气的产生速度与时间的关系如图所示。
铝丝反应过程中试管外壁发烫,说明该反应会 (选填“吸收”或“放出”) 热量。
(5)图中0~a段未产生气体的原因是 ,b点所对应溶液中的溶质有 (填化学
式),c~d段产生氢气的速率下降的主要原因是 。
23