文档内容
第 62 讲 卤代烃 醇 酚
复习目标 1.掌握卤代烃的结构与性质,理解卤代烃在有机合成中的“桥梁”作用。2.掌握
醇、酚的结构、性质及应用。
考点一 卤代烃
1.卤代烃的概念
(1)卤代烃是烃分子中的氢原子被卤素原子取代后生成的化合物。通式可表示为R—X(其中R
—表示烃基)。
(2)官能团是卤素原子。
2.卤代烃的物理性质
(1)沸点:比同碳原子数的烃沸点要高。
(2)溶解性:水中难溶,有机溶剂中易溶。
(3)密度:一般一氟代烃、一氯代烃比水小,其余比水大。
3.卤代烃的化学性质
(1)水解反应
①反应条件:强碱的水溶液、加热。
②C HBr在碱性条件下水解的化学方程式为CHCHBr+NaOH――→CHCHOH+NaBr。
2 5 3 2 3 2
③用R—CH—X表示卤代烃,碱性条件下水解的化学方程式为R—CH—X+NaOH――→R—
2 2
CHOH+NaX。
2
(2)消去反应
①概念:有机化合物在一定条件下, 从一个分子中脱去一个或几个小分子 ( 如 H O 、 HX 等 ) ,
2
而生成含不饱和键的化合物的反应。
②反应条件:强碱的醇溶液、加热。
③溴乙烷发生消去反应的化学方程式为CHCHBr+NaOH――→CH==CH↑+NaBr+HO。
3 2 2 2 2
④用 R—CH—CH—X 表示卤代烃,消去反应的化学方程式为 R—CH—CH—X+
2 2 2 2
NaOH――→R—CH==CH+NaX+HO。
2 2
(1)消去反应的规律①没有邻位碳原子的卤代烃不能发生消去反应,如CHCl。
3
②邻位碳原子上无氢原子的卤代烃不能发生消去反应,如(CH)CCHCl。
3 3 2
③有两个邻位且不对称的碳原子上均有氢原子时,可得到两种不同产物。
④卤代烃发生消去反应可生成炔烃。如:
CHClCH Cl+2NaOH――→CH≡CH↑+2NaCl+2HO。
2 2 2
(2)卤代烃是发生水解反应还是消去反应,主要看反应条件——“无醇得醇,有醇得烯或
炔”。
1.常温下,卤代烃都为液体或固体( )
2.CHCHCl的沸点比CHCH 的沸点高( )
3 2 3 3
3.在溴乙烷中加入AgNO 溶液,立即产生淡黄色沉淀( )
3
4.卤代烃的密度一般随着烃基中碳原子数目的增加而减小,沸点也随着碳原子数目的增加
而减小( )
答案 1.× 2.√ 3.× 4.×
一、卤代烃的化学性质
1.设计一个完整的实验方案,检验溴乙烷中的溴原子。
答案 ①取少量溴乙烷于试管中;
②加入适量NaOH水溶液(或NaOH的乙醇溶液),加热;
③冷却后,加入稀硝酸至溶液呈酸性;
④加硝酸银溶液,产生浅黄色沉淀。
卤代烃(RX)中卤素原子的检验方法
(1)实验流程
(2)特别提醒
①卤代烃不能电离出X-,必须转化成X-,酸化后方可用AgNO 溶液来检验。
3
②将卤代烃中的卤素转化为X-,可用卤代烃的水解反应,也可用消去反应(与卤素原子相连
的碳原子的邻位碳原子上有氢)。
2.卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应。其实质是带负电的原
子团(例如OH-等阴离子)取代了卤代烃中的卤素原子。例如:CHCHCH—Br+OH-(或NaOH)―→CHCHCH—OH+Br-(或NaBr)
3 2 2 3 2 2
写出下列反应的化学方程式:
(1)溴乙烷跟NaHS反应。
(2)碘乙烷跟CHCOONa反应。
3
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH—O—C H)。
3 2 5
答案 (1)CH CHBr+NaHS―→CHCHSH+NaBr
3 2 3 2
(2)CH CHI+CHCOONa―→NaI+CHCHOOCCH
3 2 3 3 2 3
(3)2Na+2CHCHOH―→2CHCHONa+H↑,
3 2 3 2 2
CHI+CHCHONa―→CH—O—CH CH+NaI
3 3 2 3 2 3
二、卤代烃在有机合成中的“桥梁”作用
3.在有机反应中,反应物相同而条件不同,可得到不同的主产物,如:
请写出实现下列转变的合成路线图。
(1)由CHCHCHCHBr通过两步反应合成 。
3 2 2 2
(2)由CHCHCHCHBr通过三步反应合成 。
3 2 2 2
答案 (1)CH CHCHCHBr―――→CHCHCH==CH―――――→
3 2 2 2 3 2 2
(2)CH CHCHCHBr――――→CHCHCH==CH――→ ――→
3 2 2 2 3 2 2
4.已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应如下:
2CHCHBr+2Na―→CHCHCHCH+2NaBr
3 2 3 2 2 3
写出两种可以与钠发生反应,合成环丁烷的卤代烃的结构简式。
答案 、
卤代烃在有机合成中的“桥梁”作用主要体现在
(1)引入新官能团;
(2)实现官能团的移位;(3)增长碳链;
(4)成环等。
考点二 醇的结构和性质
1.醇的概述
(1)概念:醇是羟基与烃基或苯环侧链上的碳原子相连的化合物,饱和一元醇的通式为
C H OH(n≥1)。
n 2n+1
(2)分类
2.醇类物理性质的变化规律
物理性质 递变规律
密度 一元脂肪醇的密度一般小于1 g·cm-3
①直链饱和一元醇的沸点随着分子中碳原子数的递增而升高
沸点 ②醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相
比,醇的沸点远高于烷烃
低级脂肪醇易溶于水,饱和一元醇的溶解度随着分子中碳原
水溶性
子数的递增而逐渐减小
3.醇类的化学性质
(1)根据结构预测醇类的化学性质
醇的官能团羟基(—OH),决定了醇的主要化学性质,受羟基的影响,C—H的极性增强,一
定条件也可能断键发生化学反应。
(2)醇分子的断键部位及反应类型
以1-丙醇为例,完成下列条件下的化学方程式,并指明断键部位。
a.与Na反应2CHCHCHOH+2Na―→2CHCHCHONa+H↑,①。
3 2 2 3 2 2 2
b.催化氧化
2CHCHCHOH+O――→2CHCHCHO+2HO,①③。
3 2 2 2 3 2 2
c.与HBr的取代
CHCHCHOH+HBr――→CHCHCHBr+HO,②。
3 2 2 3 2 2 2
d.浓硫酸,加热,分子内脱水
CHCHCHOH――→CHCH==CH↑+HO,②⑤。
3 2 2 3 2 2
e.与乙酸的酯化反应
CHCHCHOH+CHCOOH
3 2 2 3
CHCOOCH CHCH + H O , ① 。
3 2 2 3 2
1.CHOH和 都属于醇类,且二者互为同系物( )
3
2.CHOH、CHCHOH、 的沸点逐渐升高( )
3 3 2
3.钠与乙醇反应时因断裂C—O失去—OH官能团( )
4.所有的醇都能发生催化氧化反应和消去反应( )
5.由于醇分子中含有—OH,醇类都易溶于水( )
答案 1.× 2.√ 3.× 4.× 5.×
一、醇的消去反应和催化氧化反应规律
1.下列四种有机物的分子式均为C H O。
4 10
①CHCHCHCHOH ②
3 2 2 2
③ ④
分析其结构特点,用序号解答下列问题:
(1)其中能与钠反应产生H 的有________。
2
(2)能被氧化成含相同碳原子数的醛的是____________________________________。
(3)能被氧化成酮的是__________。
(4)能发生消去反应且生成两种产物的是____________________________________。
答案 (1)①②③④ (2)①③ (3)② (4)②
解析 (1)所有的醇都能与活泼金属钠反应产生H 。(2)能被氧化成醛的醇分子中必含有基团
2“—CHOH”,①和③符合题意。(3)能被氧化成酮的醇分子中必含有基团“ ”,
2
②符合题意。(4)若与羟基相连的碳原子的邻位碳原子上的氢原子类型不同,则发生消去反
应时,可以得到两种产物,②符合题意。
(1)醇能否发生催化氧化及氧化产物类型取决于醇分子中是否有α-H及其个数:
(2)醇能否发生消去反应取决于醇分子中是否有β-H,若β碳原子上没有氢原子,则不能发生
消去反应。
二、类比法在探究其他醇类化学性质中的应用
2.有一种有机物的键线式酷似牛形(如图所示),故称为牛式二烯炔醇。
(1)写出该醇的分子式:________________________________________________。
(2)预测该醇在一定条件下,可能具有的化学性质有________(填序号)。
①能与金属钠反应生成氢气
②能与乙酸发生酯化反应
③能被氧气氧化为醛类物质
④能与HBr发生取代反应
⑤能发生分子内消去反应
答案 (1)C H O (2)①②④
29 44
考点三 酚的结构与性质
1.酚的概念酚是羟基与苯环直接相连而形成的化合物,最简单的酚为苯酚( )。
2.苯酚的物理性质
3.苯酚的化学性质
(1)酚羟基的反应(弱酸性)
+HO +HO+
2 3
苯酚具有弱酸性,俗称石炭酸。酸性:HCO> >HCO,苯酚不能使酸碱指示剂
2 3
变色,其酸性仅表现在与金属、强碱的反应中。
与NaOH反应:
+NaOH―→ +HO;
2
与NaCO 反应:
2 3
+NaCO―→ +NaHCO 。
2 3 3
(2)与溴水的取代反应
苯酚滴入过量浓溴水中的现象为生成白色沉淀。
化学方程式:
+3Br ―→ +3HBr。
2
(3)显色反应:苯酚与FeCl 溶液作用显紫色。
3
(4)苯酚与甲醛在催化剂作用下,可发生缩聚反应,化学方程式:n +nHCHO――→
(5)氧化反应:易被空气氧化为粉红色。
注意:苯酚有毒,浓溶液对皮肤有强腐蚀性,如皮肤不慎沾上苯酚溶液,应立即用酒精洗涤,
再用水冲洗。1.苯酚的水溶液呈酸性,说明酚羟基的活泼性大于水中羟基的活泼性( )
2. 和 互为同系物( )
3.除去苯中的苯酚,加入浓溴水再过滤( )
4. 和 含有的官能团相同,二者的化学性质相似( )
5.鉴别苯酚溶液与乙醇溶液可滴加FeCl 溶液( )
3
答案 1.√ 2.× 3.× 4.× 5.√
乙醇、苯甲醇、苯酚的性质比较
物质 CHCHOH
3 2
—OH与苯环侧链碳原
结构特点 —OH与链烃基相连 —OH与苯环直接相连
子相连
①弱酸性;
①与钠反应;
②取代反应;
②取代反应;
主要化 ③显色反应;
③消去反应(苯甲醇不可以);
学性质 ④加成反应;
④催化氧化生成醛;
⑤与钠反应;
⑤酯化反应
⑥氧化反应
特性 灼热的铜丝插入醇中,有刺激性气味物质产生 遇FeCl 溶液显紫色
3
一、类比法在探究其他酚类化学性质的应用
1.白藜芦醇具有抗癌性,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中。其结构简式
如图所示:
(1)能够跟1 mol该化合物反应的NaOH的最大物质的量是__________。
(2)能够跟1 mol该化合物反应的Br 、H 的最大物质的量分别是__________、__________。
2 2
答案 (1)3 mol (2)6 mol 7 mol
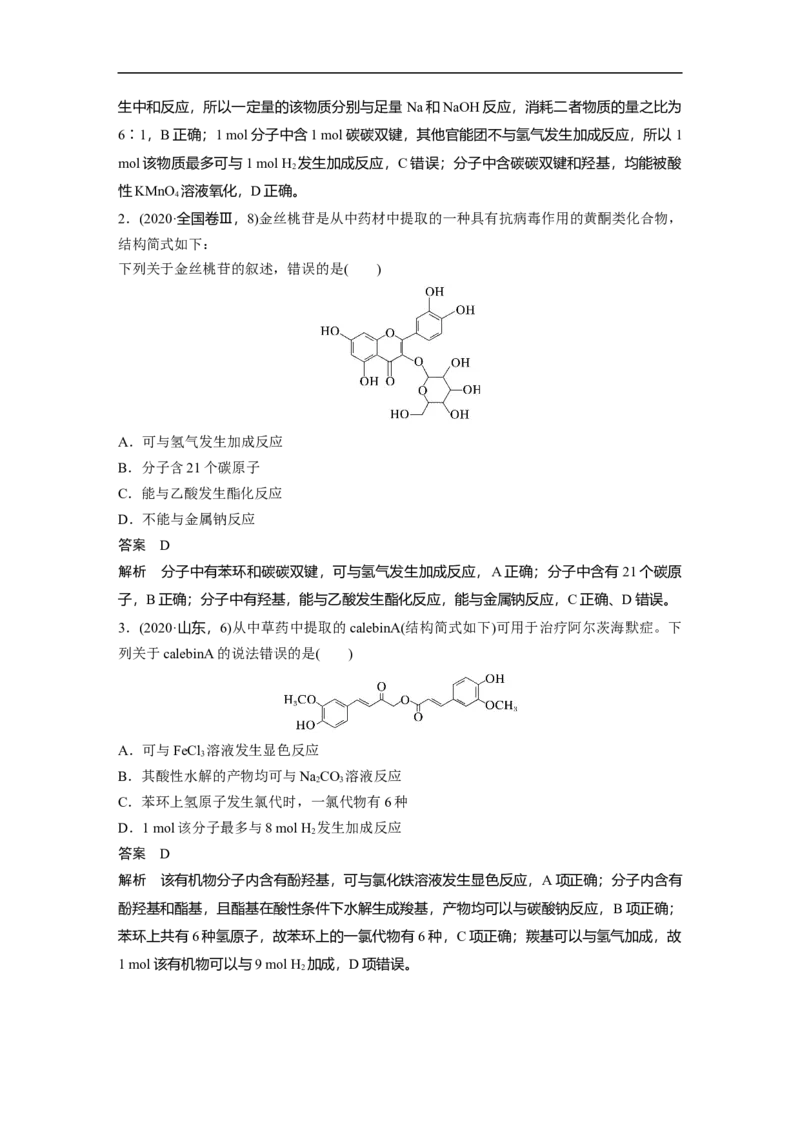
二、含酚废水的处理2.含苯酚的工业废水处理的流程图如图所示
(1)上述流程里,设备Ⅰ中进行的是__________操作(填写操作名称),实验室里这一步操作可
以用__________进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质 A 是__________,由设备Ⅲ进入设备Ⅳ的物质 B 是
__________。
(3)在设备Ⅲ中发生反应的化学方程式为_______________________________________。
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、HO和____________,通
2
过____________操作(填写操作名称),可以使产物相互分离。
(5)流程图中,能循环使用的物质是C H、CaO、____________、____________。
6 6
答案 (1)萃取 分液漏斗 (2)苯酚钠 碳酸氢钠
(3)C HONa+CO+HO―→C HOH+NaHCO
6 5 2 2 6 5 3
(4)CaCO 过滤 (5)NaOH溶液 CO
3 2
解析 苯酚易溶于苯中,可利用苯从废水中萃取出苯酚。分液后,即可得到不含苯酚的水和
含苯酚的苯溶液,然后再利用苯酚的性质从混合物中把苯酚分离出来。
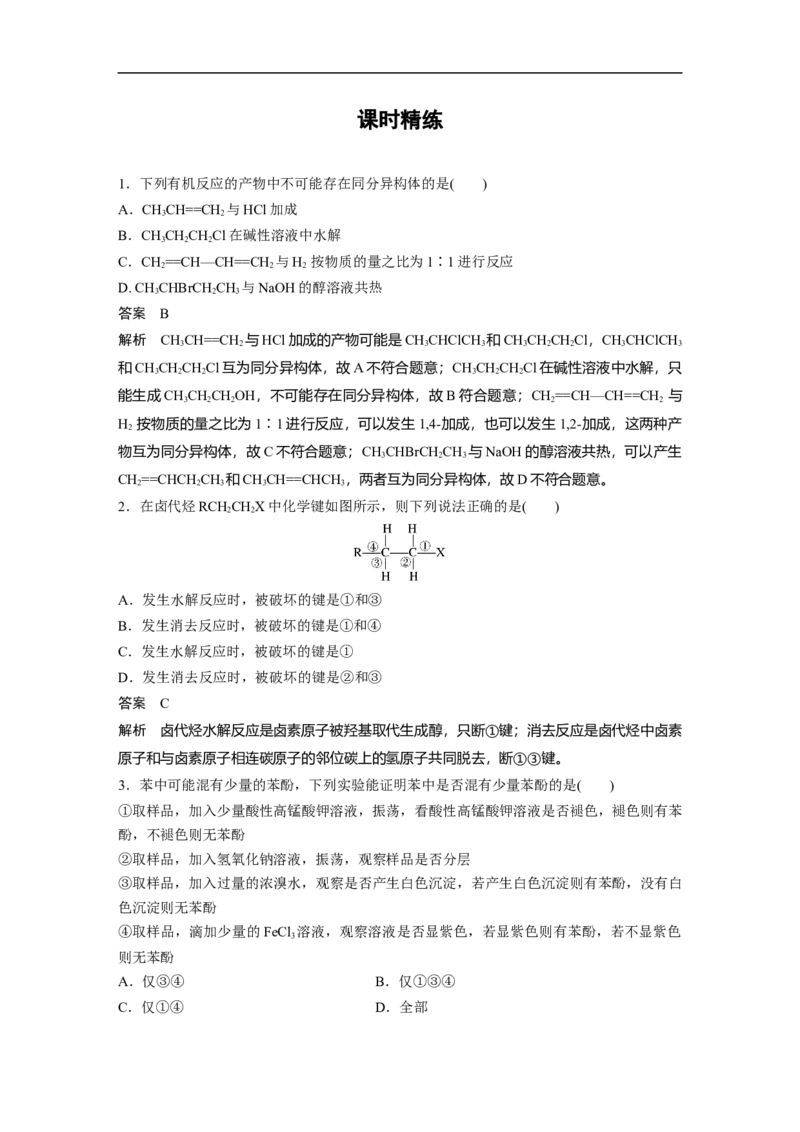
1.(2021·河北,12改编)番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法错误
的是( )
A.1 mol该物质与足量饱和NaHCO 溶液反应,可放出22.4 L(标准状况)CO
3 2
B.一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为6∶1
C.1 mol该物质最多可与2 mol H 发生加成反应
2
D.该物质可被酸性KMnO 溶液氧化
4
答案 C
解析 根据分子的结构简式可知,1 mol该分子中含有1 mol —COOH,可与NaHCO 溶液反
3
应生成1 mol CO ,在标准状况下其体积为22.4 L,A正确;1 mol分子中含5 mol羟基和1
2
mol羧基,其中羟基和羧基均能与Na发生置换反应产生氢气,而只有羧基可与氢氧化钠发生中和反应,所以一定量的该物质分别与足量Na和NaOH反应,消耗二者物质的量之比为
6∶1,B正确;1 mol分子中含1 mol碳碳双键,其他官能团不与氢气发生加成反应,所以1
mol该物质最多可与1 mol H 发生加成反应,C错误;分子中含碳碳双键和羟基,均能被酸
2
性KMnO 溶液氧化,D正确。
4
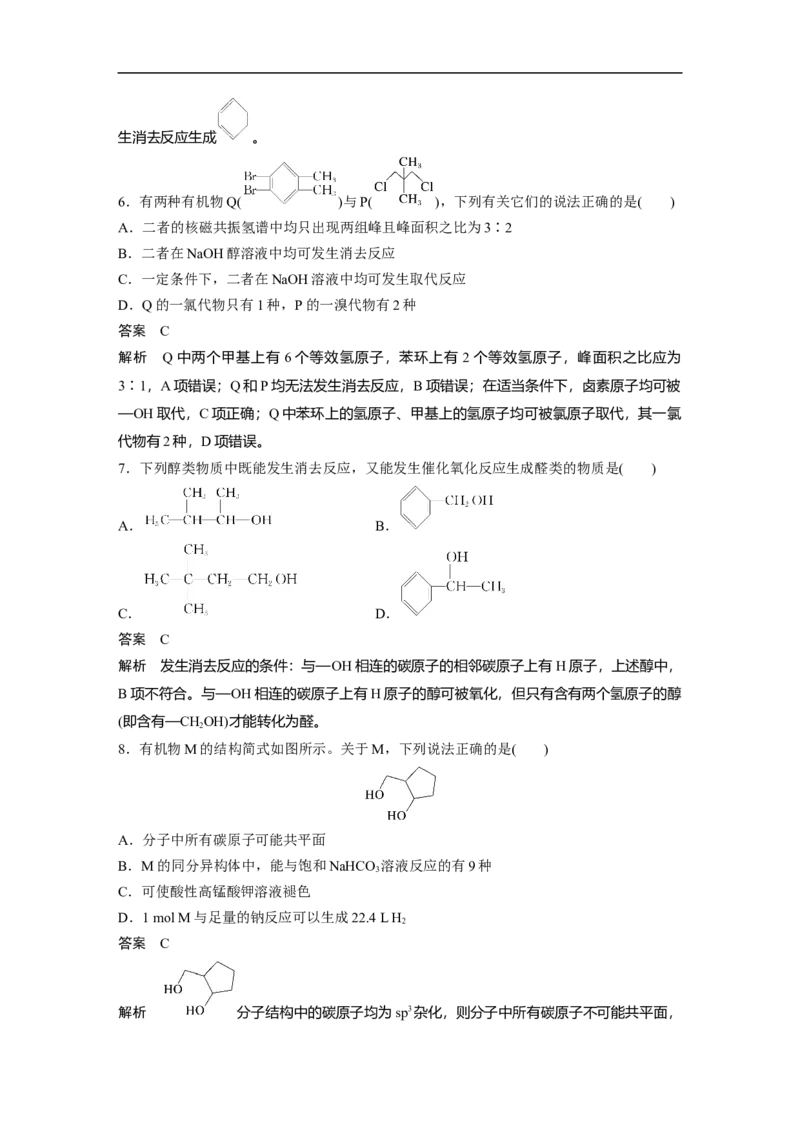
2.(2020·全国卷Ⅲ,8)金丝桃苷是从中药材中提取的一种具有抗病毒作用的黄酮类化合物,
结构简式如下:
下列关于金丝桃苷的叙述,错误的是( )
A.可与氢气发生加成反应
B.分子含21个碳原子
C.能与乙酸发生酯化反应
D.不能与金属钠反应
答案 D
解析 分子中有苯环和碳碳双键,可与氢气发生加成反应,A正确;分子中含有21个碳原
子,B正确;分子中有羟基,能与乙酸发生酯化反应,能与金属钠反应,C正确、D错误。
3.(2020·山东,6)从中草药中提取的calebinA(结构简式如下)可用于治疗阿尔茨海默症。下
列关于calebinA的说法错误的是( )
A.可与FeCl 溶液发生显色反应
3
B.其酸性水解的产物均可与NaCO 溶液反应
2 3
C.苯环上氢原子发生氯代时,一氯代物有6种
D.1 mol该分子最多与8 mol H 发生加成反应
2
答案 D
解析 该有机物分子内含有酚羟基,可与氯化铁溶液发生显色反应,A项正确;分子内含有
酚羟基和酯基,且酯基在酸性条件下水解生成羧基,产物均可以与碳酸钠反应,B项正确;
苯环上共有6种氢原子,故苯环上的一氯代物有6种,C项正确;羰基可以与氢气加成,故
1 mol该有机物可以与9 mol H 加成,D项错误。
2课时精练
1.下列有机反应的产物中不可能存在同分异构体的是( )
A.CHCH==CH 与HCl加成
3 2
B.CHCHCHCl在碱性溶液中水解
3 2 2
C.CH==CH—CH==CH 与H 按物质的量之比为1∶1进行反应
2 2 2
D. CH CHBrCH CH 与NaOH的醇溶液共热
3 2 3
答案 B
解析 CHCH==CH 与HCl加成的产物可能是CHCHClCH 和CHCHCHCl,CHCHClCH
3 2 3 3 3 2 2 3 3
和CHCHCHCl互为同分异构体,故A不符合题意;CHCHCHCl在碱性溶液中水解,只
3 2 2 3 2 2
能生成CHCHCHOH,不可能存在同分异构体,故B符合题意;CH==CH—CH==CH 与
3 2 2 2 2
H 按物质的量之比为1∶1进行反应,可以发生1,4-加成,也可以发生1,2-加成,这两种产
2
物互为同分异构体,故C不符合题意;CHCHBrCH CH 与NaOH的醇溶液共热,可以产生
3 2 3
CH==CHCH CH 和CHCH==CHCH ,两者互为同分异构体,故D不符合题意。
2 2 3 3 3
2.在卤代烃RCHCHX中化学键如图所示,则下列说法正确的是( )
2 2
A.发生水解反应时,被破坏的键是①和③
B.发生消去反应时,被破坏的键是①和④
C.发生水解反应时,被破坏的键是①
D.发生消去反应时,被破坏的键是②和③
答案 C
解析 卤代烃水解反应是卤素原子被羟基取代生成醇,只断①键;消去反应是卤代烃中卤素
原子和与卤素原子相连碳原子的邻位碳上的氢原子共同脱去,断①③键。
3.苯中可能混有少量的苯酚,下列实验能证明苯中是否混有少量苯酚的是( )
①取样品,加入少量酸性高锰酸钾溶液,振荡,看酸性高锰酸钾溶液是否褪色,褪色则有苯
酚,不褪色则无苯酚
②取样品,加入氢氧化钠溶液,振荡,观察样品是否分层
③取样品,加入过量的浓溴水,观察是否产生白色沉淀,若产生白色沉淀则有苯酚,没有白
色沉淀则无苯酚
④取样品,滴加少量的FeCl 溶液,观察溶液是否显紫色,若显紫色则有苯酚,若不显紫色
3
则无苯酚
A.仅③④ B.仅①③④
C.仅①④ D.全部答案 C
解析 ①苯酚能使酸性高锰酸钾褪色,但是苯不能,所以取样品,加入少量酸性高锰酸钾溶
液,振荡,看酸性高锰酸钾溶液是否褪色,褪色则有苯酚,不褪色则无苯酚,故正确;②不
管苯中是否有苯酚,加入NaOH溶液都会分层,因此无法鉴别,故错误;③产生的2,4,6-三
溴苯酚能溶于苯,因此不能鉴别,故错误;④苯酚遇到氯化铁显紫色,但是苯不能,取样品,
滴加少量的FeCl 溶液,观察溶液是否显紫色,若显紫色则有苯酚,若不显紫色则无苯酚,
3
故正确。
4.某有机物的结构简式为 ,下列关于该物质的说法不正确的是( )
A.该物质不能发生消去反应,但能在一定条件下发生加聚反应
B.该物质不能和AgNO 溶液反应产生AgBr沉淀
3
C.该物质在NaOH的醇溶液中加热可转化为醇类
D.该物质可使溴水褪色
答案 C
解析 该有机物分子中与溴原子相连的碳原子的邻位碳上没有H,不能发生消去反应,含有
碳碳双键,一定条件下能发生加聚反应,故A正确;该物质中的溴原子必须水解成Br-,才
能和AgNO 溶液反应生成AgBr沉淀,故B正确;该物质在NaOH的醇溶液中加热,不发生
3
消去反应,若发生水解反应生成醇类,应在氢氧化钠的水溶液中进行,故C错误;含有碳
碳双键,能与溴发生加成反应,使溴水褪色,故D正确。
5.用有机物甲可制备环己二烯( ),其反应路线如图所示:甲―――――→ ―――――→
乙――――――→丙――――――→ 。下列有关判断不正确的是( )
A.甲的分子式为C H
6 12
B.反应①②③分别为取代反应、消去反应、加成反应
C.乙与环己二烯互为同系物
D.丙的同分异构体中含有六元碳环结构的还有3种
答案 C
解析 由流程图知,甲与Cl 在光照条件下发生取代反应生成 ,则甲为 ; 发
2
生消去反应生成乙( ),乙可以与Br 的CCl 溶液发生加成反应生成丙( ),丙发
2 4生消去反应生成 。
6.有两种有机物Q( )与P( ),下列有关它们的说法正确的是( )
A.二者的核磁共振氢谱中均只出现两组峰且峰面积之比为3∶2
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种,P的一溴代物有2种
答案 C
解析 Q中两个甲基上有 6个等效氢原子,苯环上有 2个等效氢原子,峰面积之比应为
3∶1,A项错误;Q和P均无法发生消去反应,B项错误;在适当条件下,卤素原子均可被
—OH取代,C项正确;Q中苯环上的氢原子、甲基上的氢原子均可被氯原子取代,其一氯
代物有2种,D项错误。
7.下列醇类物质中既能发生消去反应,又能发生催化氧化反应生成醛类的物质是( )
A. B.
C. D.
答案 C
解析 发生消去反应的条件:与—OH相连的碳原子的相邻碳原子上有H原子,上述醇中,
B项不符合。与—OH相连的碳原子上有H原子的醇可被氧化,但只有含有两个氢原子的醇
(即含有—CHOH)才能转化为醛。
2
8.有机物M的结构简式如图所示。关于M,下列说法正确的是( )
A.分子中所有碳原子可能共平面
B.M的同分异构体中,能与饱和NaHCO 溶液反应的有9种
3
C.可使酸性高锰酸钾溶液褪色
D.1 mol M与足量的钠反应可以生成22.4 L H
2
答案 C
解析 分子结构中的碳原子均为sp3杂化,则分子中所有碳原子不可能共平面,故A错误;M的分子式为C H O ,同分异构体中,能与饱和NaHCO 溶液反应,说明含有
6 12 2 3
—COOH,则相当于C H 的烷烃中氢原子被—COOH取代,其中CHCHCHCHCH 有三
5 12 3 2 2 2 3
种等效氢,CH(CH )CHCH 有4种等效氢,C(CH) 有1种等效氢,故满足条件的同分异构
3 2 2 3 3 4
体共有8种,故B错误;M分子结构中的醇羟基能被酸性高锰酸钾溶液氧化,使酸性高锰
酸钾溶液褪色,故C正确;1 mol M与足量的钠反应可以生成1 mol H ,标准状况下体积为
2
22.4 L,选项中未标明是否是标准状况,故D错误。
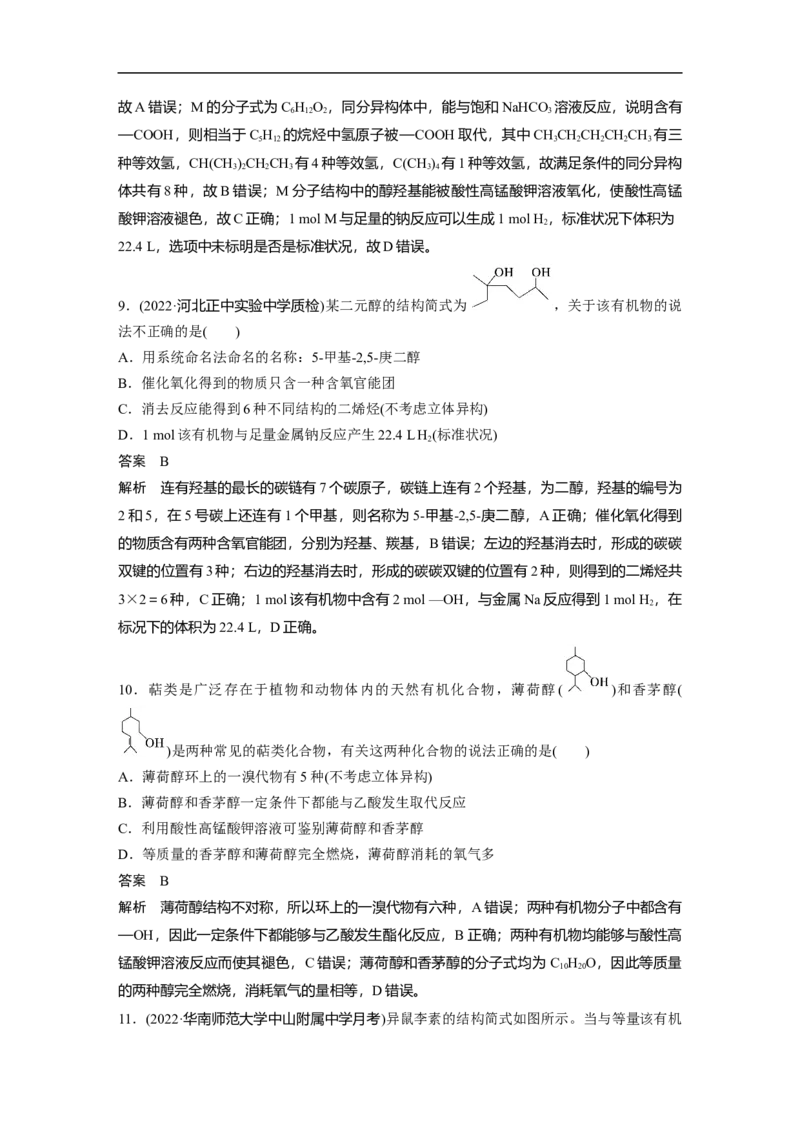
9.(2022·河北正中实验中学质检)某二元醇的结构简式为 ,关于该有机物的说
法不正确的是( )
A.用系统命名法命名的名称:5-甲基-2,5-庚二醇
B.催化氧化得到的物质只含一种含氧官能团
C.消去反应能得到6种不同结构的二烯烃(不考虑立体异构)
D.1 mol该有机物与足量金属钠反应产生22.4 L H (标准状况)
2
答案 B
解析 连有羟基的最长的碳链有7个碳原子,碳链上连有2个羟基,为二醇,羟基的编号为
2和5,在5号碳上还连有1个甲基,则名称为5-甲基-2,5-庚二醇,A正确;催化氧化得到
的物质含有两种含氧官能团,分别为羟基、羰基,B错误;左边的羟基消去时,形成的碳碳
双键的位置有3种;右边的羟基消去时,形成的碳碳双键的位置有2种,则得到的二烯烃共
3×2=6种,C正确;1 mol该有机物中含有2 mol —OH,与金属Na反应得到1 mol H ,在
2
标况下的体积为22.4 L,D正确。
10.萜类是广泛存在于植物和动物体内的天然有机化合物,薄荷醇( )和香茅醇(
)是两种常见的萜类化合物,有关这两种化合物的说法正确的是( )
A.薄荷醇环上的一溴代物有5种(不考虑立体异构)
B.薄荷醇和香茅醇一定条件下都能与乙酸发生取代反应
C.利用酸性高锰酸钾溶液可鉴别薄荷醇和香茅醇
D.等质量的香茅醇和薄荷醇完全燃烧,薄荷醇消耗的氧气多
答案 B
解析 薄荷醇结构不对称,所以环上的一溴代物有六种,A错误;两种有机物分子中都含有
—OH,因此一定条件下都能够与乙酸发生酯化反应,B正确;两种有机物均能够与酸性高
锰酸钾溶液反应而使其褪色,C错误;薄荷醇和香茅醇的分子式均为 C H O,因此等质量
10 20
的两种醇完全燃烧,消耗氧气的量相等,D错误。
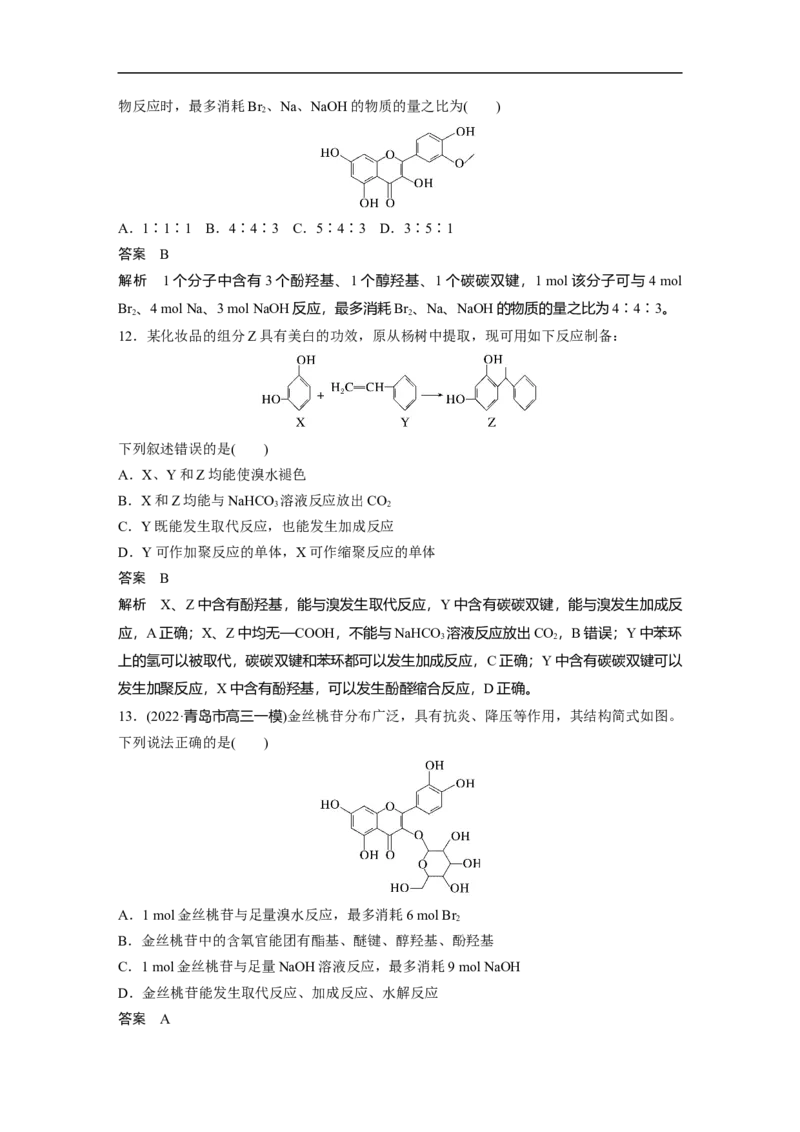
11.(2022·华南师范大学中山附属中学月考)异鼠李素的结构简式如图所示。当与等量该有机物反应时,最多消耗Br 、Na、NaOH的物质的量之比为( )
2
A.1∶1∶1 B.4∶4∶3 C.5∶4∶3 D.3∶5∶1
答案 B
解析 1个分子中含有3个酚羟基、1个醇羟基、1个碳碳双键,1 mol该分子可与4 mol
Br 、4 mol Na、3 mol NaOH反应,最多消耗Br 、Na、NaOH的物质的量之比为4∶4∶3。
2 2
12.某化妆品的组分Z具有美白的功效,原从杨树中提取,现可用如下反应制备:
下列叙述错误的是( )
A.X、Y和Z均能使溴水褪色
B.X和Z均能与NaHCO 溶液反应放出CO
3 2
C.Y既能发生取代反应,也能发生加成反应
D.Y可作加聚反应的单体,X可作缩聚反应的单体
答案 B
解析 X、Z中含有酚羟基,能与溴发生取代反应,Y中含有碳碳双键,能与溴发生加成反
应,A正确;X、Z中均无—COOH,不能与NaHCO 溶液反应放出CO,B错误;Y中苯环
3 2
上的氢可以被取代,碳碳双键和苯环都可以发生加成反应,C正确;Y中含有碳碳双键可以
发生加聚反应,X中含有酚羟基,可以发生酚醛缩合反应,D正确。
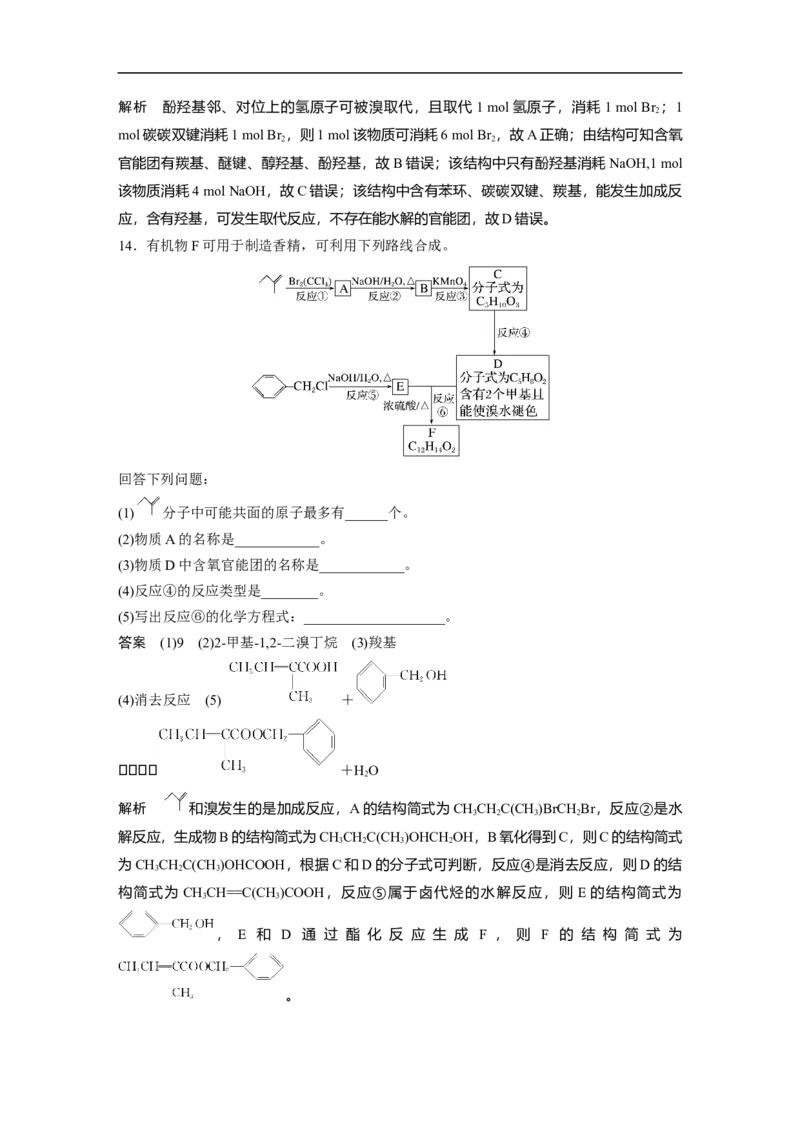
13.(2022·青岛市高三一模)金丝桃苷分布广泛,具有抗炎、降压等作用,其结构简式如图。
下列说法正确的是( )
A.1 mol金丝桃苷与足量溴水反应,最多消耗6 mol Br
2
B.金丝桃苷中的含氧官能团有酯基、醚键、醇羟基、酚羟基
C.1 mol金丝桃苷与足量NaOH溶液反应,最多消耗9 mol NaOH
D.金丝桃苷能发生取代反应、加成反应、水解反应
答案 A解析 酚羟基邻、对位上的氢原子可被溴取代,且取代1 mol氢原子,消耗1 mol Br ;1
2
mol碳碳双键消耗1 mol Br ,则1 mol该物质可消耗6 mol Br ,故A正确;由结构可知含氧
2 2
官能团有羰基、醚键、醇羟基、酚羟基,故B错误;该结构中只有酚羟基消耗NaOH,1 mol
该物质消耗4 mol NaOH,故C错误;该结构中含有苯环、碳碳双键、羰基,能发生加成反
应,含有羟基,可发生取代反应,不存在能水解的官能团,故D错误。
14.有机物F可用于制造香精,可利用下列路线合成。
回答下列问题:
(1) 分子中可能共面的原子最多有______个。
(2)物质A的名称是____________。
(3)物质D中含氧官能团的名称是____________。
(4)反应④的反应类型是________。
(5)写出反应⑥的化学方程式:____________________。
答案 (1)9 (2)2-甲基-1,2-二溴丁烷 (3)羧基
(4)消去反应 (5) +
+HO
2
解析 和溴发生的是加成反应,A的结构简式为CHCHC(CH)BrCHBr,反应②是水
3 2 3 2
解反应,生成物B的结构简式为CHCHC(CH)OHCHOH,B氧化得到C,则C的结构简式
3 2 3 2
为CHCHC(CH)OHCOOH,根据C和D的分子式可判断,反应④是消去反应,则D的结
3 2 3
构简式为 CHCH==C(CH)COOH,反应⑤属于卤代烃的水解反应,则 E 的结构简式为
3 3
, E 和 D 通 过 酯 化 反 应 生 成 F , 则 F 的 结 构 简 式 为
。(1) 分子中的五个C、双键上的两个H、两个甲基上各有一个H可能共面,故可能共面
的原子最多有9个。
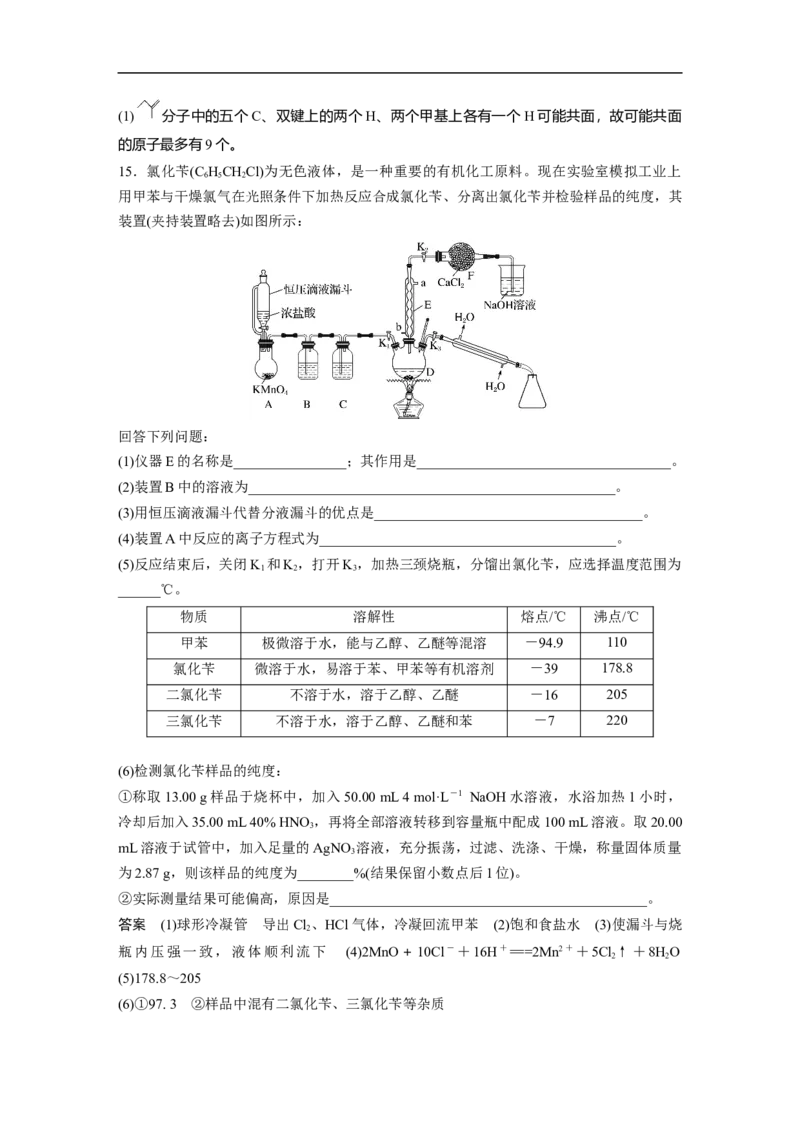
15.氯化苄(C HCHCl)为无色液体,是一种重要的有机化工原料。现在实验室模拟工业上
6 5 2
用甲苯与干燥氯气在光照条件下加热反应合成氯化苄、分离出氯化苄并检验样品的纯度,其
装置(夹持装置略去)如图所示:
回答下列问题:
(1)仪器E的名称是________________;其作用是____________________________________。
(2)装置B中的溶液为____________________________________________________。
(3)用恒压滴液漏斗代替分液漏斗的优点是______________________________________。
(4)装置A中反应的离子方程式为__________________________________________。
(5)反应结束后,关闭K 和K,打开K,加热三颈烧瓶,分馏出氯化苄,应选择温度范围为
1 2 3
______℃。
物质 溶解性 熔点/℃ 沸点/℃
甲苯 极微溶于水,能与乙醇、乙醚等混溶 -94.9 110
氯化苄 微溶于水,易溶于苯、甲苯等有机溶剂 -39 178.8
二氯化苄 不溶于水,溶于乙醇、乙醚 -16 205
三氯化苄 不溶于水,溶于乙醇、乙醚和苯 -7 220
(6)检测氯化苄样品的纯度:
①称取13.00 g样品于烧杯中,加入50.00 mL 4 mol·L-1 NaOH水溶液,水浴加热1小时,
冷却后加入35.00 mL 40% HNO ,再将全部溶液转移到容量瓶中配成100 mL溶液。取20.00
3
mL溶液于试管中,加入足量的AgNO 溶液,充分振荡,过滤、洗涤、干燥,称量固体质量
3
为2.87 g,则该样品的纯度为________%(结果保留小数点后1位)。
②实际测量结果可能偏高,原因是_____________________________________________。
答案 (1)球形冷凝管 导出Cl 、HCl气体,冷凝回流甲苯 (2)饱和食盐水 (3)使漏斗与烧
2
瓶内压强一致,液体顺利流下 (4)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO
2 2
(5)178.8~205
(6)①97. 3 ②样品中混有二氯化苄、三氯化苄等杂质解析 (2)装置A制取的氯气中含有杂质氯化氢,装置B的作用是除去氯气中的氯化氢,所
以B中的试剂是饱和食盐水。(5)分馏出氯化苄的温度应高于氯化苄的沸点,低于二氯化苄
的沸点,所以应选择温度范围是178.8~205 ℃。(6)设样品中C HCHCl的质量为x g,则:
6 5 2
C HCHCl~AgCl
6 5 2
126.5 g 143.5 g
x g 2.87× g
x=12.65,样品纯度为×100%≈97.3%;二氯化苄、三氯化苄中氯元素的质量分数大于氯化
苄,样品中若混有二氯化苄、三氯化苄等杂质会使测量结果偏高。