文档内容
2015 年贵州省遵义市中考化学试卷
一、选择题(每小题2分,共20分)
1.(2分)材料是人类发展中的重要物质,陶瓷属于( )
A.合成材料 B.无机非金属材料
C.复合材料 D.金属材料
2.(2分)下列净化水的方法中,净化程度最高的是( )
A.静置 B.吸附 C.过滤 D.蒸馏
3.(2分)物质的性质决定用途,下列说法不正确的是( )
A.用甲醛溶液浸泡食品保鲜
B.用熟石灰改良酸性土壤
C.干冰用于人工降雨
D.一氧化碳可用作燃料
4.(2分)分类是学习和研究化学的常用方法,下列分类正确的是( )
A.有机物:甲烷、碳酸钡
B.化石燃料:石油、天然气
C.混合物:氮气、空气
D.复合肥料:硝酸钾、氯化铵
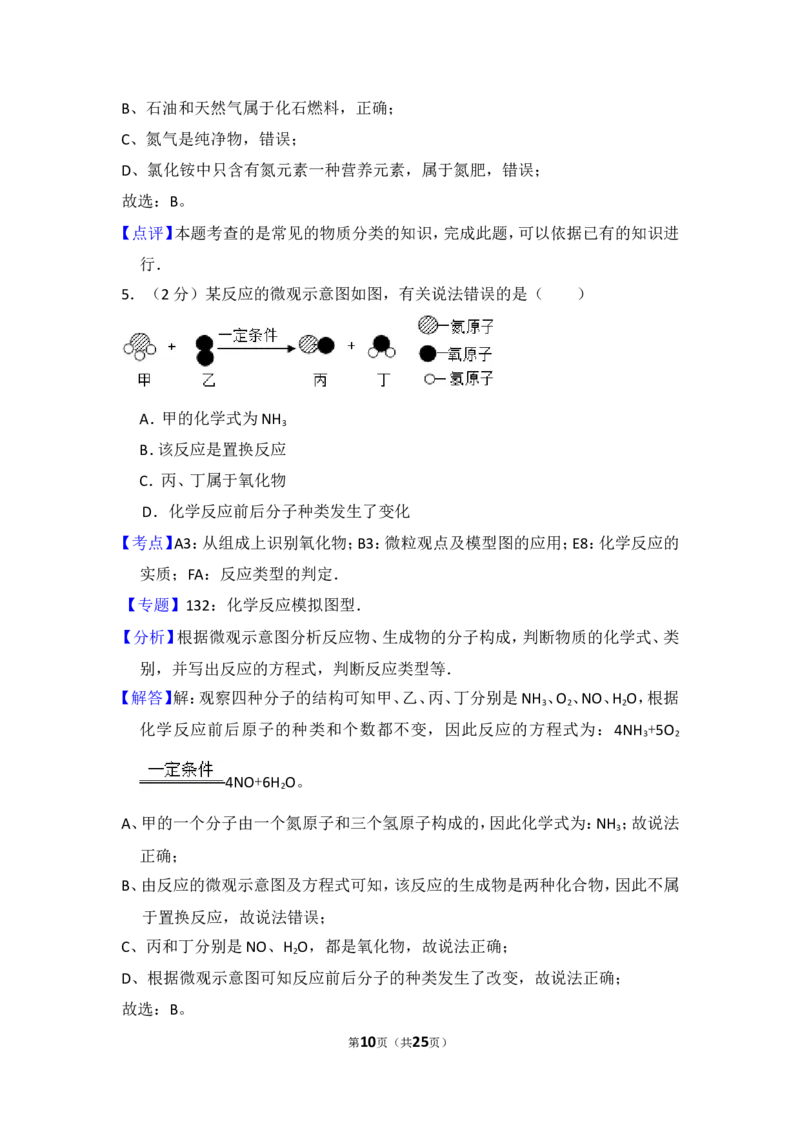
5.(2分)某反应的微观示意图如图,有关说法错误的是( )
A.甲的化学式为NH
3
B.该反应是置换反应
C.丙、丁属于氧化物
D.化学反应前后分子种类发生了变化
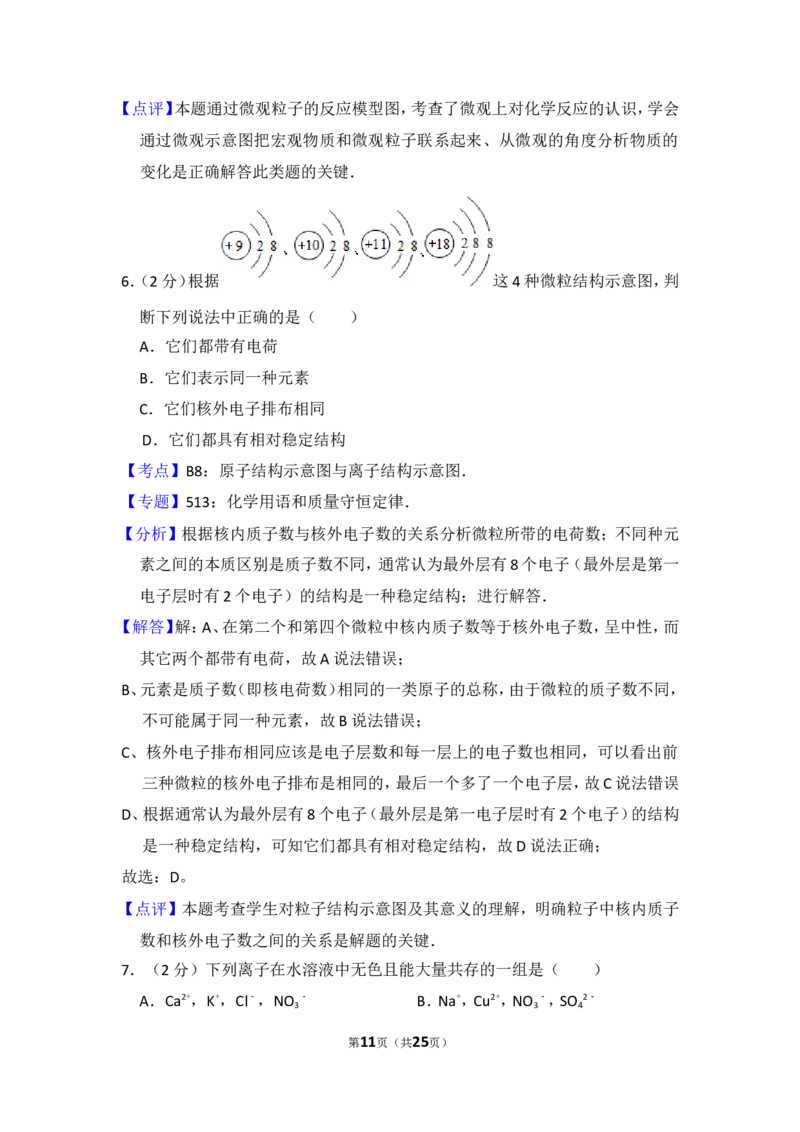
6.(2分)根据 这4种微粒结构示意图,判
第1页(共25页)断下列说法中正确的是( )
A.它们都带有电荷
B.它们表示同一种元素
C.它们核外电子排布相同
D.它们都具有相对稳定结构
7.(2分)下列离子在水溶液中无色且能大量共存的一组是( )
A.Ca2+,K+,Cl﹣,NO ﹣ B.Na+,Cu2+,NO ﹣,SO 2﹣
3 3 4
C.Fe3+,Na+,OH﹣,NO ﹣ D.K+,H+,SO 2﹣,CO 2﹣
3 4 3
8.(2分)质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反
应aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
9.(2分)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐
酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
10.(2分)下列各项实验(括号内为相应的操作或方法),能达到实验目的是(
)
A.除去CO 中的少量CO(点燃)
2
B.验证硫酸铵溶液(取样,加氢氧化钠溶液)
C.检验CaO中混有的CaCO 溶液(滴加稀盐酸)
3
D.鉴别氢氧化钠和碳酸钠(取样,溶解,滴加酚酞)
二、非选择题(11-17小题每空1分,18小题4分,共40分)
11.(4分)用化学用语填空:
(1)氢原子
第2页(共25页)(2)2个二氧化硫分子
(3)3个铵根离子
(4)氧化铁中铁元素的化合价 .
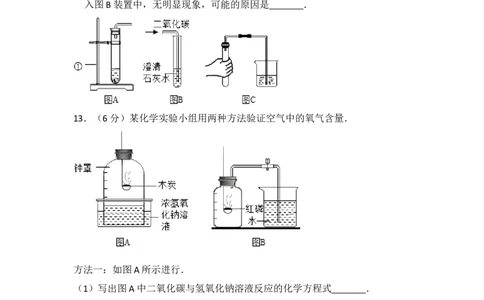
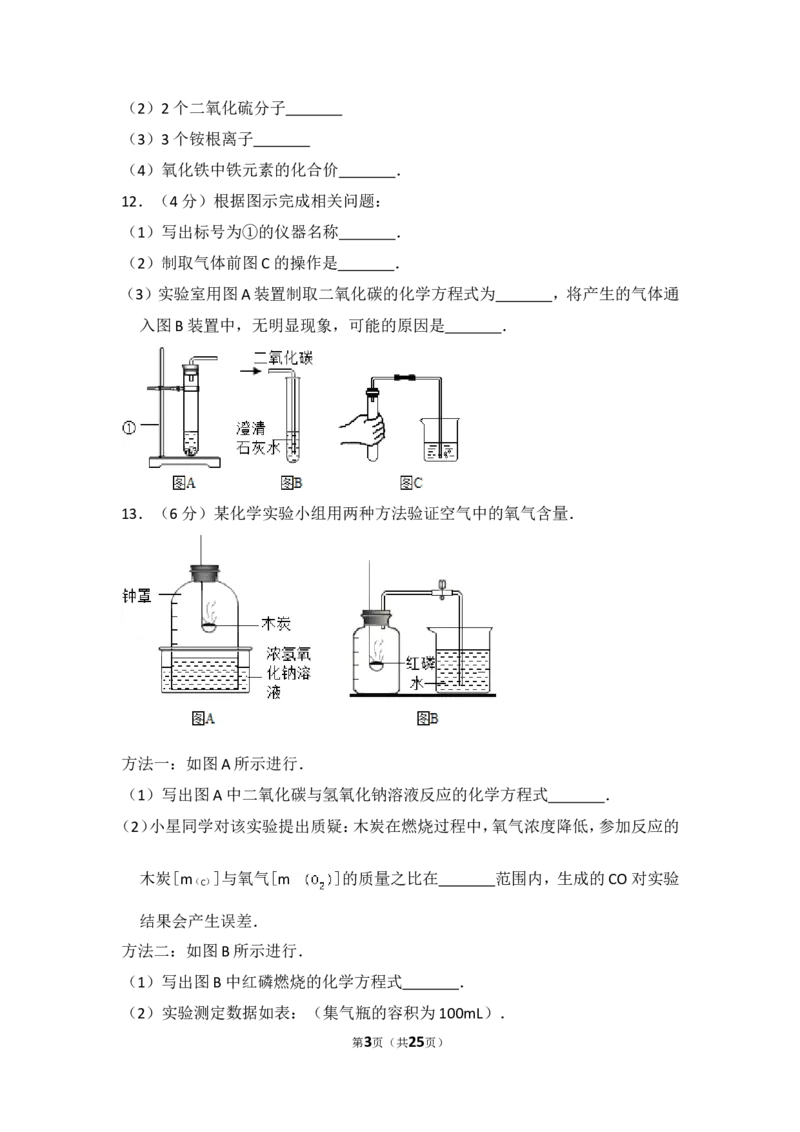
12.(4分)根据图示完成相关问题:
(1)写出标号为①的仪器名称 .
(2)制取气体前图C的操作是 .
(3)实验室用图A装置制取二氧化碳的化学方程式为 ,将产生的气体通
入图B装置中,无明显现象,可能的原因是 .
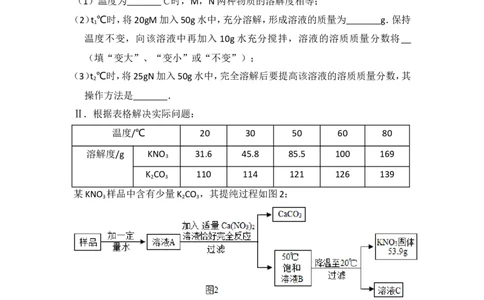
13.(6分)某化学实验小组用两种方法验证空气中的氧气含量.
方法一:如图A所示进行.
(1)写出图A中二氧化碳与氢氧化钠溶液反应的化学方程式 .
(2)小星同学对该实验提出质疑:木炭在燃烧过程中,氧气浓度降低,参加反应的
木炭[m ]与氧气[m ]的质量之比在 范围内,生成的CO对实验
(C)
结果会产生误差.
方法二:如图B所示进行.
(1)写出图B中红磷燃烧的化学方程式 .
(2)实验测定数据如表:(集气瓶的容积为100mL).
第3页(共25页)组别 1 2 3 4 5 6
进入集气瓶中水的 30 21 19 22 15 20
体积/mL
分析实验数据,第2,3,4,6组验证出氧气约占空气体积的 ,第5组出现
较大偏差的原因可能是 .
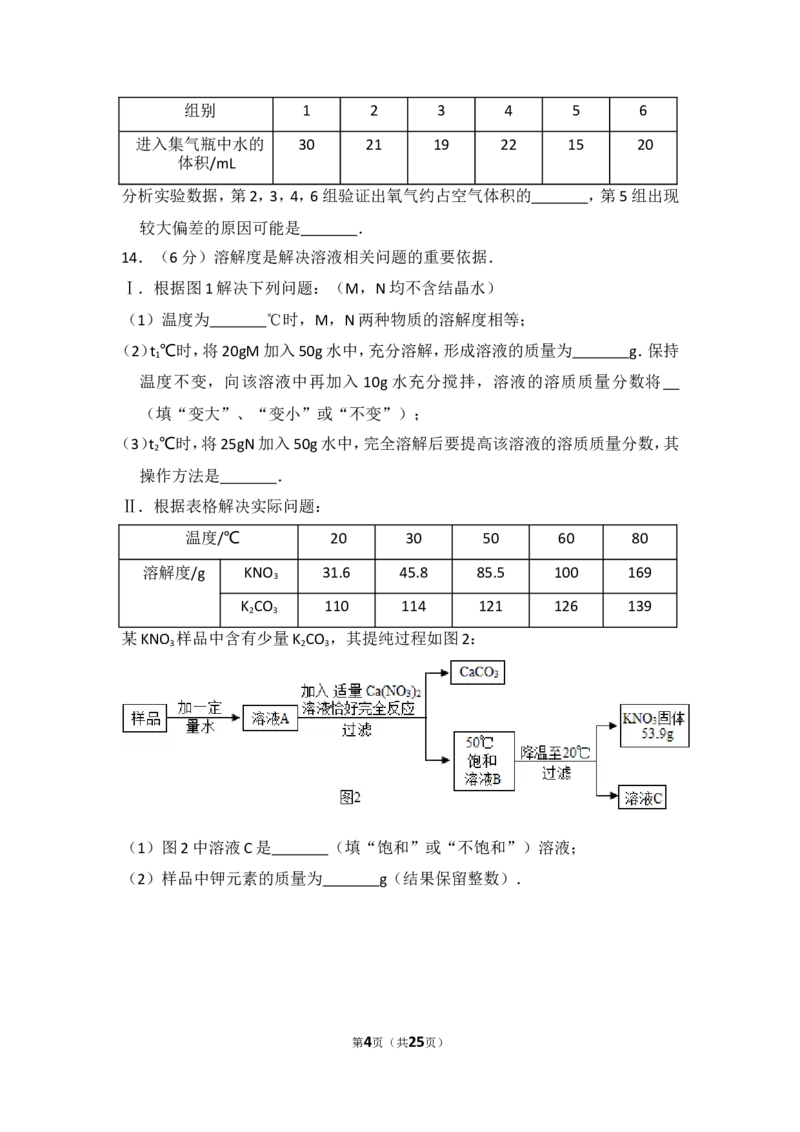
14.(6分)溶解度是解决溶液相关问题的重要依据.
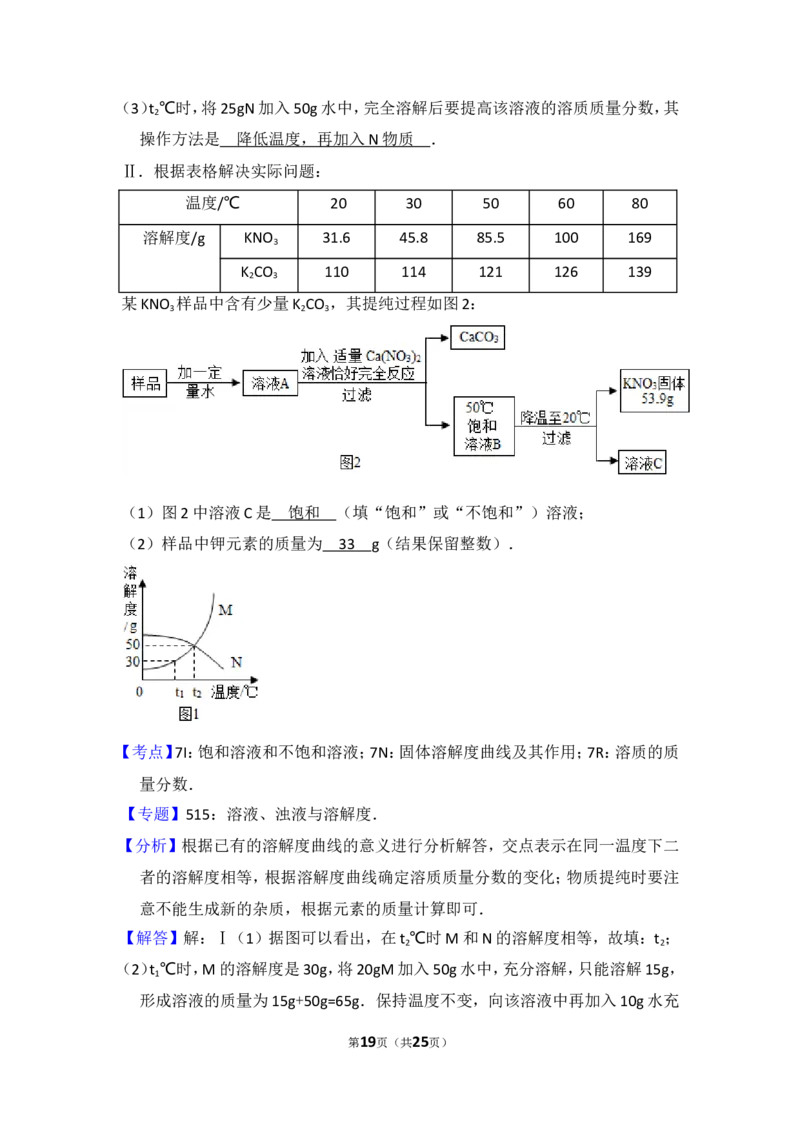
Ⅰ.根据图1解决下列问题:(M,N均不含结晶水)
(1)温度为 ℃时,M,N两种物质的溶解度相等;
(2)t ℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为 g.保持
1
温度不变,向该溶液中再加入 10g 水充分搅拌,溶液的溶质质量分数将
(填“变大”、“变小”或“不变”);
(3)t ℃时,将25gN加入50g水中,完全溶解后要提高该溶液的溶质质量分数,其
2
操作方法是 .
Ⅱ.根据表格解决实际问题:
温度/℃ 20 30 50 60 80
溶解度/g KNO 31.6 45.8 85.5 100 169
3
K CO 110 114 121 126 139
2 3
某KNO 样品中含有少量K CO ,其提纯过程如图2:
3 2 3
(1)图2中溶液C是 (填“饱和”或“不饱和”)溶液;
(2)样品中钾元素的质量为 g(结果保留整数).
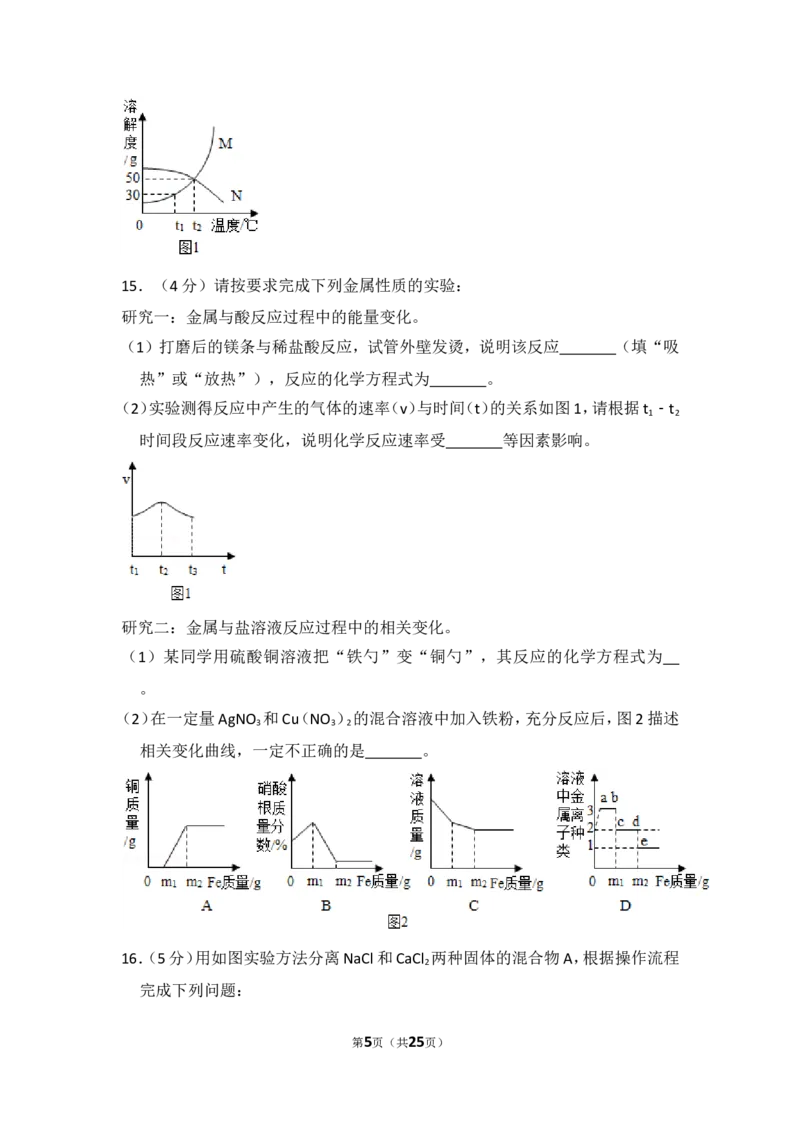
第4页(共25页)15.(4分)请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应 (填“吸
热”或“放热”),反应的化学方程式为 。
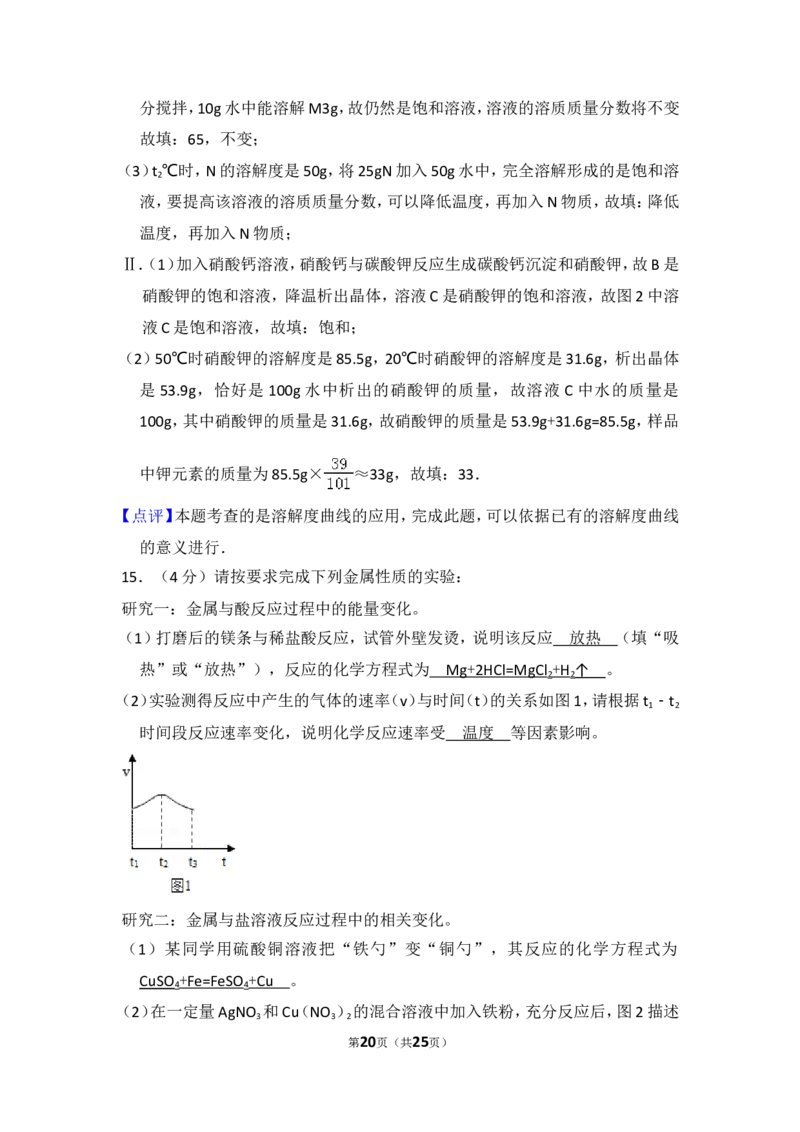
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图1,请根据t ﹣t
1 2
时间段反应速率变化,说明化学反应速率受 等因素影响。
研究二:金属与盐溶液反应过程中的相关变化。
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为
。
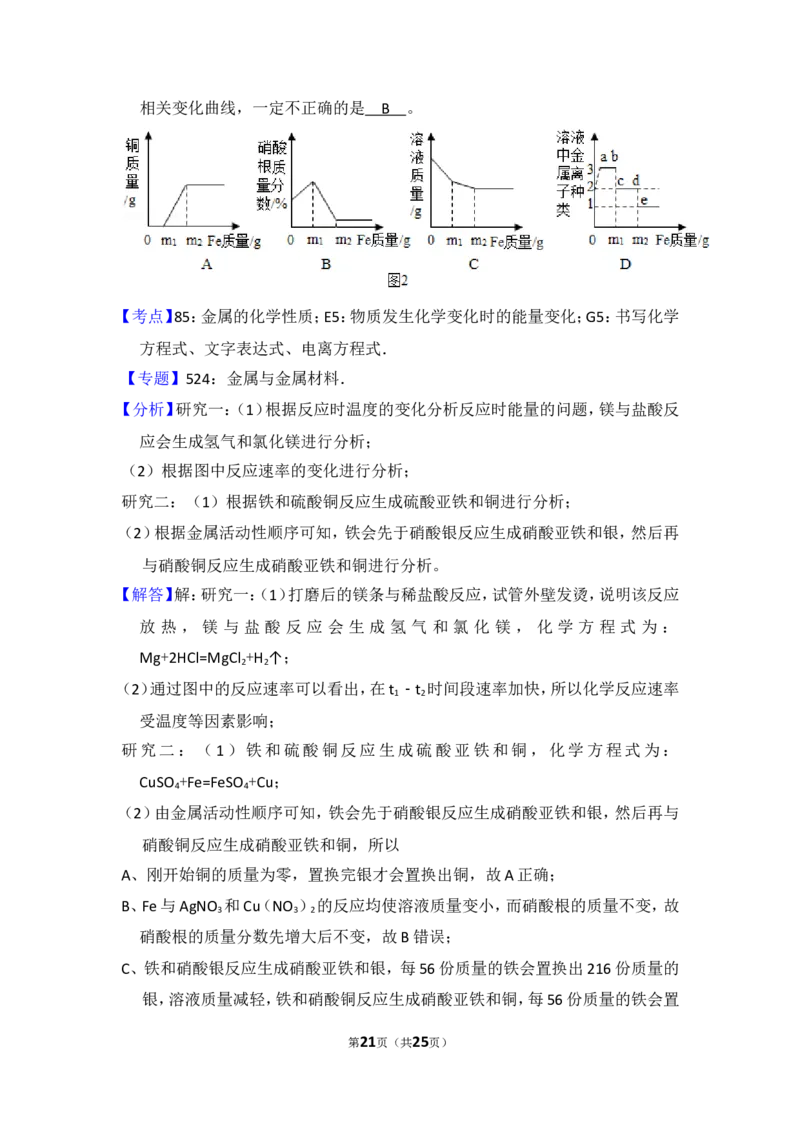
(2)在一定量AgNO 和Cu(NO )的混合溶液中加入铁粉,充分反应后,图2描述
3 3 2
相关变化曲线,一定不正确的是 。
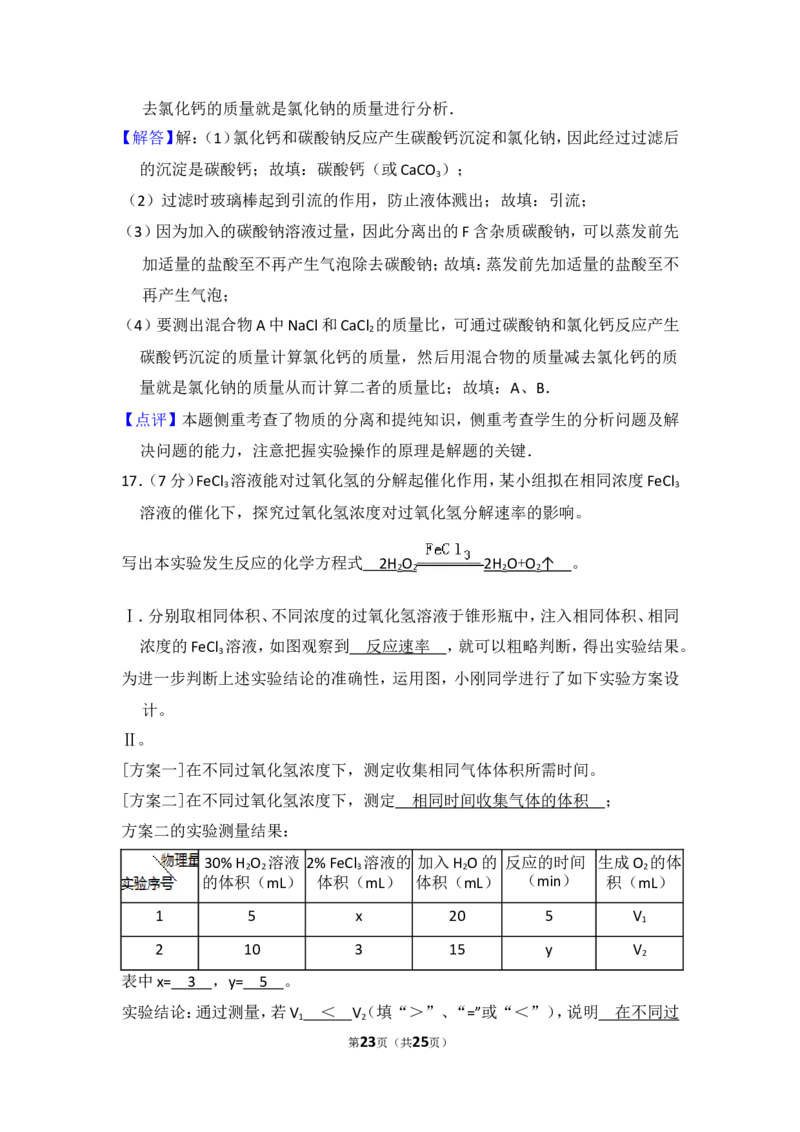
16.(5分)用如图实验方法分离NaCl和CaCl 两种固体的混合物A,根据操作流程
2
完成下列问题:
第5页(共25页)(1)B物质是 .
(2)过滤操作中玻璃棒的作用是 .
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善 .
(4)若用原操作方法,要测出混合物A中NaCl和CaCl 的质量比,不称量D,可通
2
过称量 和 的质量求解.
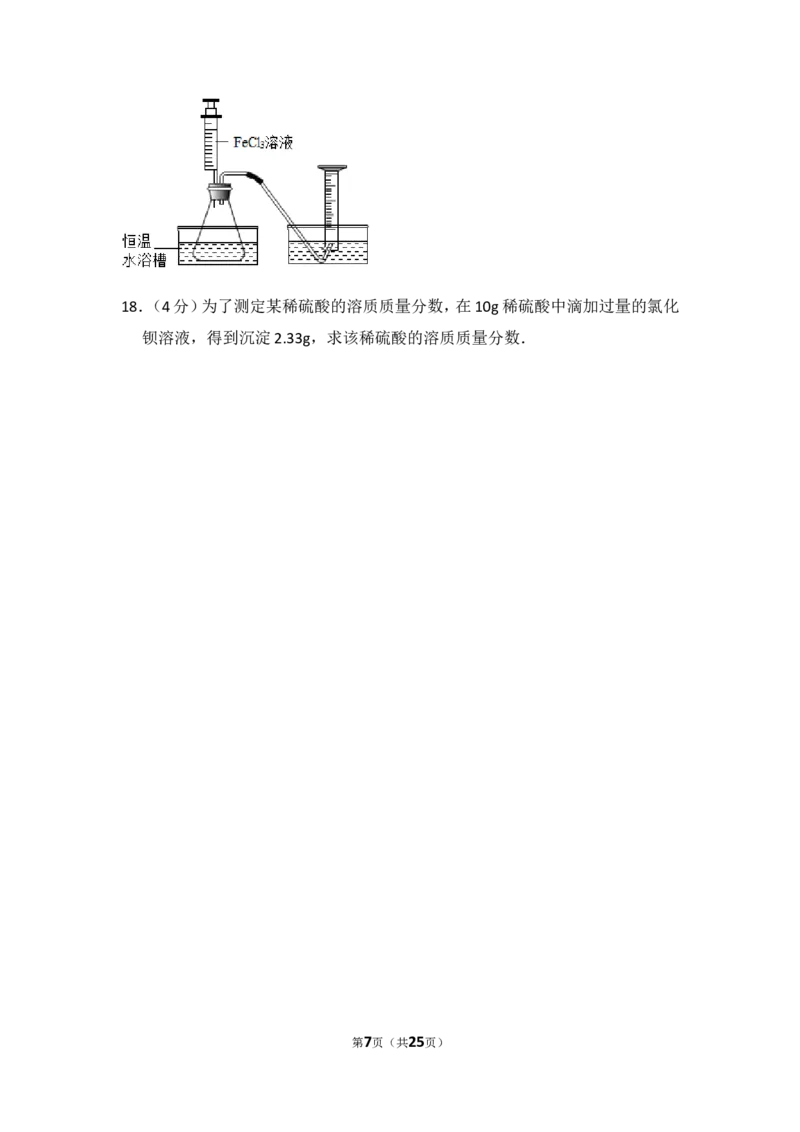
17.(7分)FeCl 溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl
3 3
溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。
写出本实验发生反应的化学方程式 。
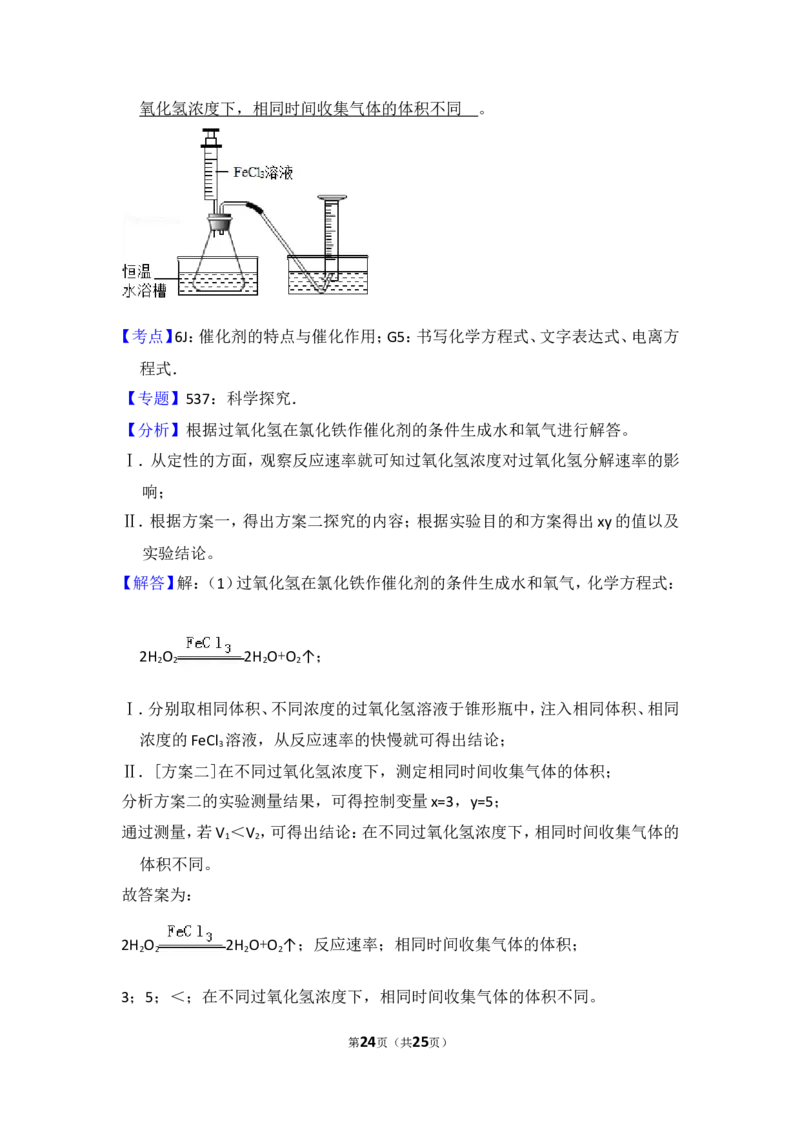
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同
浓度的FeCl 溶液,如图观察到 ,就可以粗略判断,得出实验结果。
3
为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设
计。
Ⅱ。
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间。
[方案二]在不同过氧化氢浓度下,测定 ;
方案二的实验测量结果:
30% H O 溶液 2% FeCl 溶液的 加入H O的 反应的时间 生成O 的体
2 2 3 2 2
的体积(mL) 体积(mL) 体积(mL) (min) 积(mL)
1 5 x 20 5 V
1
2 10 3 15 y V
2
表中x= ,y= 。
实验结论:通过测量,若V V(填“>”、“=”或“<”),说明 。
1 2
第6页(共25页)18.(4分)为了测定某稀硫酸的溶质质量分数,在10g稀硫酸中滴加过量的氯化
钡溶液,得到沉淀2.33g,求该稀硫酸的溶质质量分数.
第7页(共25页)2015 年贵州省遵义市中考化学试卷
参考答案与试题解析
一、选择题(每小题2分,共20分)
1.(2分)材料是人类发展中的重要物质,陶瓷属于( )
A.合成材料 B.无机非金属材料
C.复合材料 D.金属材料
【考点】89:金属材料及其应用;I7:合成材料的使用及其对人和环境的影响;I8:
新材料的开发与社会发展的密切关系;IA:复合材料、纳米材料.
【专题】528:化学与生活.
【分析】根据已有的材料的类别进行分析解答即可,陶瓷属于无机硅酸盐材料,据
此解答.
【解答】解:陶瓷属于无机硅酸盐材料,硅酸盐属于非金属材料。
故选:B。
【点评】本题考查的是材料的类别,完成此题,可以依据已有的材料的成分进行.
2.(2分)下列净化水的方法中,净化程度最高的是( )
A.静置 B.吸附 C.过滤 D.蒸馏
【考点】75:水的净化.
【专题】521:空气与水.
【分析】根据已有的水的净化的知识进行分析解答,蒸馏得到的水中不含有任何
杂质,是净水程度最高的方法,据此解答.
【解答】解:蒸馏得到的水中不含有任何杂质,是净水程度最高的方法。
故选:D。
【点评】本题考查的是水的净化的知识,完成此题,可以依据已有的知识进行.
3.(2分)物质的性质决定用途,下列说法不正确的是( )
A.用甲醛溶液浸泡食品保鲜
B.用熟石灰改良酸性土壤
C.干冰用于人工降雨
第8页(共25页)D.一氧化碳可用作燃料
【考点】6R:二氧化碳的用途;6U:一氧化碳的化学性质;94:常见碱的特性和用途;
J3:亚硝酸钠、甲醛等化学品的性质与人体健康.
【专题】528:化学与生活.
【分析】A、根据甲醛可破坏蛋白质的结构性质解答;
B、根据熟石灰的性质和用途解答;
C、根据干冰升华时吸热的性质判断;
D、根据一氧化碳的可燃性解答.
【解答】解:A、甲醛有毒,能破坏蛋白质的结构,不但对人体有害,而且降低了食
品的质量,故A错误;
B、利用了熟石灰的能和显酸性的物质反应,熟石灰用于改良酸性土壤,故B正确;
C、干冰用于人工降雨利用了干冰升华时吸热,故C正确;
D、一氧化碳可用作燃料利用了一氧化碳的可燃性,故D正确。
故选:A。
【点评】物质的性质在一定程度上决定了物质的用途,在判断物质的用途时,首先
要考虑物质相关的性质,所以掌握物质的性质以及性质和用途的关系是解题
的关键.
4.(2分)分类是学习和研究化学的常用方法,下列分类正确的是( )
A.有机物:甲烷、碳酸钡
B.化石燃料:石油、天然气
C.混合物:氮气、空气
D.复合肥料:硝酸钾、氯化铵
【考点】9J:常见化肥的种类和作用;A5:纯净物和混合物的判别;AC:有机物与无
机物的区别;H7:化石燃料及其综合利用.
【专题】516:物质的分类.
【分析】根据已有的物质的类别进行分析解答,有机物是指含有碳元素的化合物,
化石燃料包括煤、石油和天然气,混合物是指含有多种物质的物质,复合肥料
是指含有氮、磷、钾三种元素中至少两种元素的肥料,据此解答.
【解答】解:A、碳酸钡虽然含有碳元素,但是性质与无机物相似,属于无机物,错
误;
第9页(共25页)B、石油和天然气属于化石燃料,正确;
C、氮气是纯净物,错误;
D、氯化铵中只含有氮元素一种营养元素,属于氮肥,错误;
故选:B。
【点评】本题考查的是常见的物质分类的知识,完成此题,可以依据已有的知识进
行.
5.(2分)某反应的微观示意图如图,有关说法错误的是( )
A.甲的化学式为NH
3
B.该反应是置换反应
C.丙、丁属于氧化物
D.化学反应前后分子种类发生了变化
【考点】A3:从组成上识别氧化物;B3:微粒观点及模型图的应用;E8:化学反应的
实质;FA:反应类型的判定.
【专题】132:化学反应模拟图型.
【分析】根据微观示意图分析反应物、生成物的分子构成,判断物质的化学式、类
别,并写出反应的方程式,判断反应类型等.
【解答】解:观察四种分子的结构可知甲、乙、丙、丁分别是NH 、O 、NO、H O,根据
3 2 2
化学反应前后原子的种类和个数都不变,因此反应的方程式为:4NH +5O
3 2
4NO+6H O。
2
A、甲的一个分子由一个氮原子和三个氢原子构成的,因此化学式为:NH ;故说法
3
正确;
B、由反应的微观示意图及方程式可知,该反应的生成物是两种化合物,因此不属
于置换反应,故说法错误;
C、丙和丁分别是NO、H O,都是氧化物,故说法正确;
2
D、根据微观示意图可知反应前后分子的种类发生了改变,故说法正确;
故选:B。
第10页(共25页)【点评】本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会
通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的
变化是正确解答此类题的关键.
6.(2分)根据 这4种微粒结构示意图,判
断下列说法中正确的是( )
A.它们都带有电荷
B.它们表示同一种元素
C.它们核外电子排布相同
D.它们都具有相对稳定结构
【考点】B8:原子结构示意图与离子结构示意图.
【专题】513:化学用语和质量守恒定律.
【分析】根据核内质子数与核外电子数的关系分析微粒所带的电荷数;不同种元
素之间的本质区别是质子数不同,通常认为最外层有8个电子(最外层是第一
电子层时有2个电子)的结构是一种稳定结构;进行解答.
【解答】解:A、在第二个和第四个微粒中核内质子数等于核外电子数,呈中性,而
其它两个都带有电荷,故A说法错误;
B、元素是质子数(即核电荷数)相同的一类原子的总称,由于微粒的质子数不同,
不可能属于同一种元素,故B说法错误;
C、核外电子排布相同应该是电子层数和每一层上的电子数也相同,可以看出前
三种微粒的核外电子排布是相同的,最后一个多了一个电子层,故C说法错误
D、根据通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构
是一种稳定结构,可知它们都具有相对稳定结构,故D说法正确;
故选:D。
【点评】本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子
数和核外电子数之间的关系是解题的关键.
7.(2分)下列离子在水溶液中无色且能大量共存的一组是( )
A.Ca2+,K+,Cl﹣,NO ﹣ B.Na+,Cu2+,NO ﹣,SO 2﹣
3 3 4
第11页(共25页)C.Fe3+,Na+,OH﹣,NO ﹣ D.K+,H+,SO 2﹣,CO 2﹣
3 4 3
【考点】9R:离子或物质的共存问题.
【专题】533:物质的分离、除杂、提纯与共存问题.
【分析】根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子
不能大量共存,据此进行分析判断即可。本题还要注意溶液呈无色透明,不能
含有明显有颜色的铜离子、铁离子和亚铁离子等。
【解答】解:A、四种离子间不能结合成沉淀、气体或水,能大量共存,且不存在有
色离子,故选项正确。
B、四种离子间不能结合成沉淀、气体或水,能大量共存,但Cu2+的水溶液蓝色,故
选项错误。
C、Fe3+、OH﹣两种离子能结合成氢氧化铁沉淀,不能大量共存,故选项错误。
D、H+、CO 2﹣两种离子能结合成水和二氧化碳,不能大量共存,故选项错误。
3
故选:A。
【点评】本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液
中的各离子之间能否发生反应生成沉淀、气体、水;还要注意特定离子的颜色。
8.(2分)质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学反
应aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
【考点】9I:复分解反应及其发生的条件;G1:质量守恒定律及其应用.
【专题】513:化学用语和质量守恒定律.
【分析】化学计量数a与b之和不一定等于c与d之和;物质参加化学反应按一定
的质量比进行,故可以判断B、C是否正确;若A和C都是盐,则该反应可能是
复分解反应,质也可能是置换反应.
【解答】解:A、参加反应的AB的质量总和一定等于生成的CD的质量总和,但化学
计量数a与b之和不一定等于c与d之和,故A错误。
B、若A和C都是盐,则该反应不一定是复分解反应,若BD是单质也可能是置换
反应,故B错误。
第12页(共25页)C、参加反应的AB的质量总和一定等于生成的CD的质量总和,但反应物A和B
的质量比不一定等于生成物C和D的质量比,故C错误。
D、物质参加化学反应按一定的质量比进行,由于参加反应的AB的质量比不一定
是1:1,故若取zgA和zgB反应,生成C和D的质量总和不一定是2zg,故D正
确。
故选:D。
【点评】本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同
变化过程中相同点和不同点,有效地寻找出它们之间的内在联系以及融合点
和嫁接点,从而培养了学生的创新思维能力.
9.(2分)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐
酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
【考点】93:酸的化学性质.
【专题】525:常见的酸 酸的通性.
【分析】根据酸溶液中都含有H+,因此不同的酸表现出一些共同的性质,如酸能与
酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应等,据此进行分析判断
【解答】解:A、盐酸能使紫色石蕊溶液变红,其它酸也能使紫色石蕊溶液变红,属
于酸的共同性质,故选项错误;
B、盐酸能与氢氧化钠溶液反应生成水,酸能与碱发生中和反应,其它酸也能与氢
氧化钠溶液反应生成水,属于酸的共同性质,故选项错误;
C、盐酸能与硝酸银溶液反应生成氯化银沉淀,表现为氯离子的特征,因此硫酸、
硝酸等不能与硝酸银溶液反应生成氯化银沉淀,则该性质不属于酸的共同性
质,故选项正确;
D、盐酸能与活泼金属反应产生氢气,其它的酸也能与活泼金属反应产生氢气,属
于酸的共同性质,故选项错误;
故选:C。
【点评】本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化
第13页(共25页)物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.
10.(2分)下列各项实验(括号内为相应的操作或方法),能达到实验目的是(
)
A.除去CO 中的少量CO(点燃)
2
B.验证硫酸铵溶液(取样,加氢氧化钠溶液)
C.检验CaO中混有的CaCO 溶液(滴加稀盐酸)
3
D.鉴别氢氧化钠和碳酸钠(取样,溶解,滴加酚酞)
【考点】34:化学实验方案设计与评价;4Q:常见气体的检验与除杂方法;9H:盐的
化学性质;9L:铵态氮肥的检验;9U:酸、碱、盐的鉴别.
【专题】535:简单实验方案的设计与评价.
【分析】A、根据一氧化碳和二氧化碳均匀混合,不能被点燃进行分析;
B、根据硫酸铵和氢氧化钠会生成氨气进行分析;
C、根据碳酸钙和盐酸会生成二氧化碳气体进行分析;
D、根据碳酸钠和氢氧化钠溶液都显碱性进行分析.
【解答】解:A、一氧化碳和二氧化碳均匀混合,不能被点燃,故A错误;
B、取样品,加入氢氧化钠溶液,会生成刺激性气味的气体,可以鉴别铵根离子,但
不能鉴别硫酸根离子,故B错误;
C、取样品,滴入盐酸,会产生气体,证明含有碳酸钙,故C正确;
D、碳酸钠和氢氧化钠溶液都显碱性,都能是酚酞显红色,故D错误。
故选:C。
【点评】在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,
出现不同的现象即可鉴别.
二、非选择题(11-17小题每空1分,18小题4分,共40分)
11.(4分)用化学用语填空:
(1)氢原子 H
(2)2个二氧化硫分子 2SO
2
(3)3个铵根离子 3NH +
4
(4)氧化铁中铁元素的化合价 O .
2 3
第14页(共25页)【考点】DF:化学符号及其周围数字的意义.
【专题】513:化学用语和质量守恒定律.
【分析】(1)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就
在其元素符号前加上相应的数字.
(2)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前
加上相应的数字.
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负
电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离
子,就在其离子符号前加上相应的数字.
(4)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号
在前,数字在后.
【解答】解:(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,
就在其元素符号前加上相应的数字,故氢原子表示为:H.
(2)由分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式
前加上相应的数字,2个二氧化硫分子可表示为:2SO .
2
(3)由离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正
负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该
离子,就在其元素符号前加上相应的数字;3个铵根离子可表示为:3NH +.
4
(4)氧化铁中氧元素显﹣2价,铁元素显+3价;由化合价的表示方法,在其化学式
该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化铁中铁元
素的化合价为+3价可表示为: O .
2 3
故答案为:(1)H;(2)2SO ;(3)3NH +;(4) O .
2 4 2 3
【点评】本题难度不大,掌握常见化学用语(原子符号、分子符号、化合价、离子符
号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的
关键.
12.(4分)根据图示完成相关问题:
(1)写出标号为①的仪器名称 铁架台 .
(2)制取气体前图C的操作是 检查装置的气密性 .
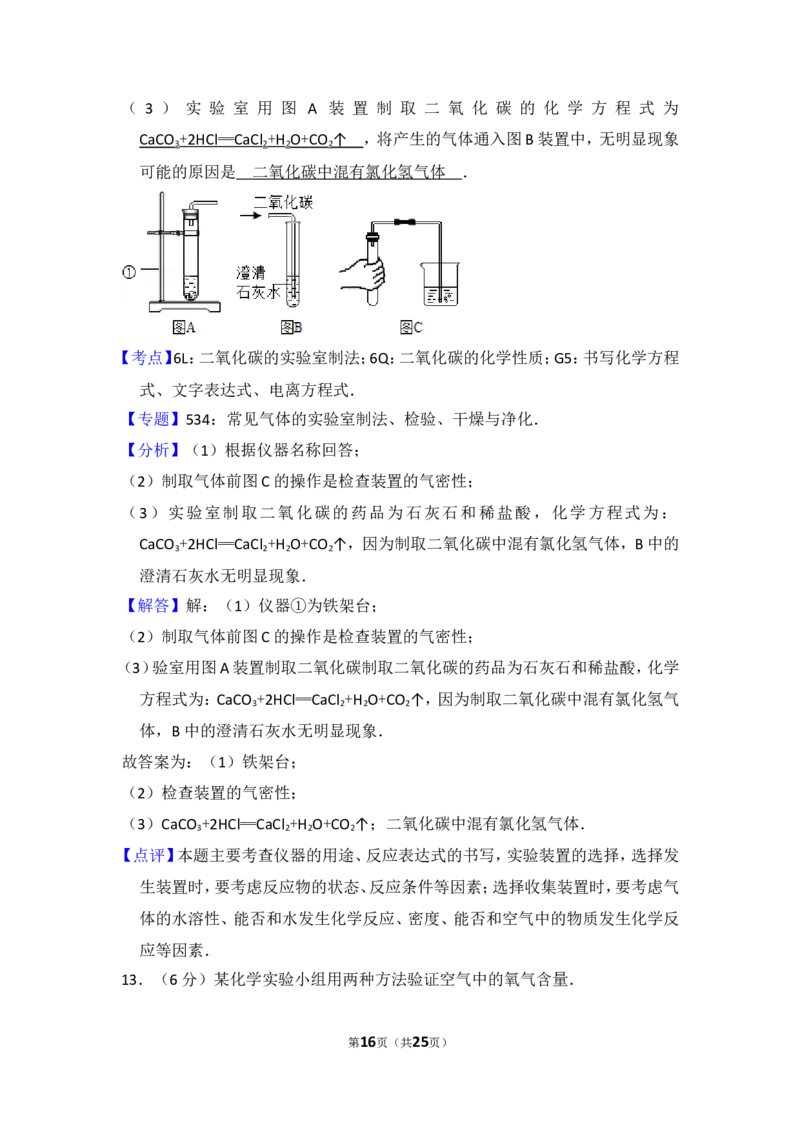
第15页(共25页)( 3 ) 实 验 室 用 图 A 装 置 制 取 二 氧 化 碳 的 化 学 方 程 式 为
CaCO + 2HC l ═ CaC l + H O + CO ↑ ,将产生的气体通入图B装置中,无明显现象
3 2 2 2
可能的原因是 二氧化碳中混有氯化氢气体 .
【考点】6L:二氧化碳的实验室制法;6Q:二氧化碳的化学性质;G5:书写化学方程
式、文字表达式、电离方程式.
【专题】534:常见气体的实验室制法、检验、干燥与净化.
【分析】(1)根据仪器名称回答;
(2)制取气体前图C的操作是检查装置的气密性;
(3)实验室制取二氧化碳的药品为石灰石和稀盐酸,化学方程式为:
CaCO +2HCl═CaCl +H O+CO ↑,因为制取二氧化碳中混有氯化氢气体,B中的
3 2 2 2
澄清石灰水无明显现象.
【解答】解:(1)仪器①为铁架台;
(2)制取气体前图C的操作是检查装置的气密性;
(3)验室用图A装置制取二氧化碳制取二氧化碳的药品为石灰石和稀盐酸,化学
方程式为:CaCO +2HCl═CaCl +H O+CO ↑,因为制取二氧化碳中混有氯化氢气
3 2 2 2
体,B中的澄清石灰水无明显现象.
故答案为:(1)铁架台;
(2)检查装置的气密性;
(3)CaCO +2HCl═CaCl +H O+CO ↑;二氧化碳中混有氯化氢气体.
3 2 2 2
【点评】本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发
生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气
体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反
应等因素.
13.(6分)某化学实验小组用两种方法验证空气中的氧气含量.
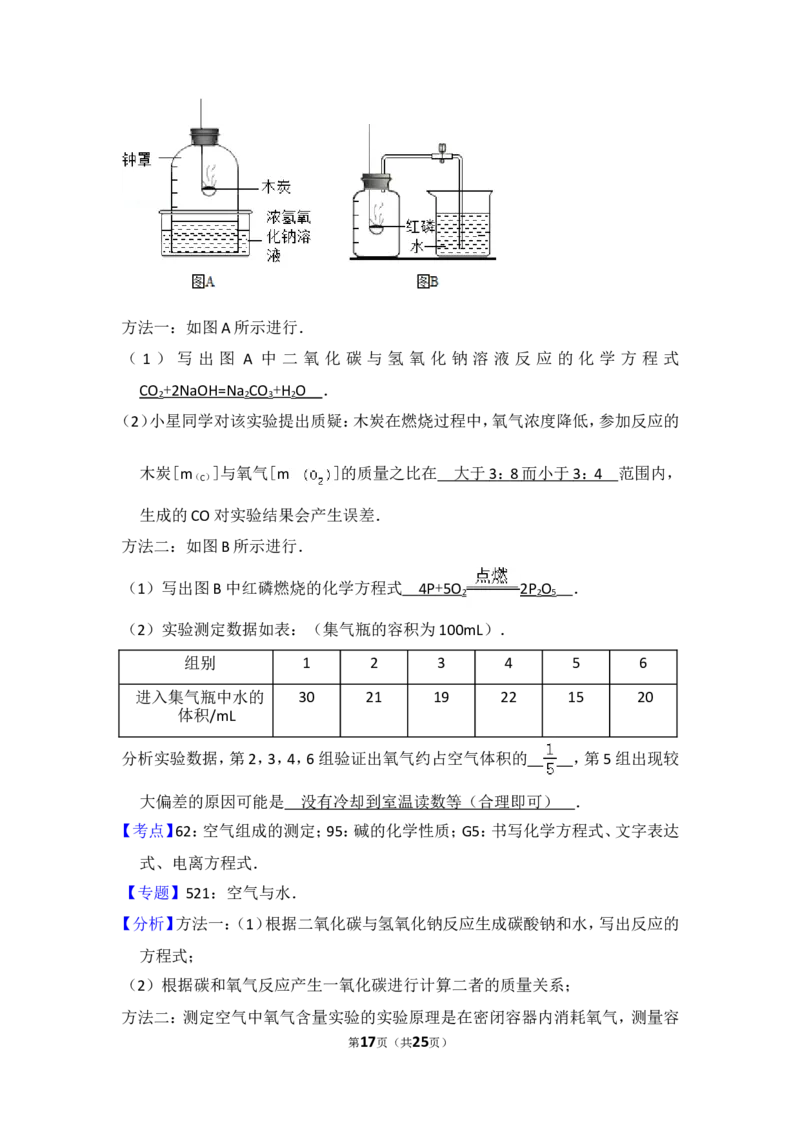
第16页(共25页)方法一:如图A所示进行.
( 1 ) 写 出 图 A 中 二 氧 化 碳 与 氢 氧 化 钠 溶 液 反 应 的 化 学 方 程 式
CO + 2NaOH=N a CO + H O .
2 2 3 2
(2)小星同学对该实验提出质疑:木炭在燃烧过程中,氧气浓度降低,参加反应的
木炭[m ]与氧气[m ]的质量之比在 大于 3 : 8 而小于 3 : 4 范围内,
(C)
生成的CO对实验结果会产生误差.
方法二:如图B所示进行.
(1)写出图B中红磷燃烧的化学方程式 4P + 5O 2P O .
2 2 5
(2)实验测定数据如表:(集气瓶的容积为100mL).
组别 1 2 3 4 5 6
进入集气瓶中水的 30 21 19 22 15 20
体积/mL
分析实验数据,第2,3,4,6组验证出氧气约占空气体积的 ,第5组出现较
大偏差的原因可能是 没有冷却到室温读数等(合理即可) .
【考点】62:空气组成的测定;95:碱的化学性质;G5:书写化学方程式、文字表达
式、电离方程式.
【专题】521:空气与水.
【分析】方法一:(1)根据二氧化碳与氢氧化钠反应生成碳酸钠和水,写出反应的
方程式;
(2)根据碳和氧气反应产生一氧化碳进行计算二者的质量关系;
方法二:测定空气中氧气含量实验的实验原理是在密闭容器内消耗氧气,测量容
第17页(共25页)器内气体体积的减少量确定氧气的含量.因此在选择消耗氧气的药品时,应考
虑能与空气中的氧气反应,生成物为固体不能为气体,还应注意装置不漏气,
药品的量要足,读数时温度要回到原来的温度等.最后得出氧气约占空气体积
的五分之一.
【解答】解:方法一:(1)根据二氧化碳与氢氧化钠反应生成碳酸钠和水,故反应的
方程式为:CO +2NaOH=Na CO +H O;
2 2 3 2
(2)若碳完全燃烧,生成气体全部为二氧化碳时,碳与氧气的质量比为3:8,其中
产生的二氧化碳可以完全被氢氧化钠溶液吸收,通过液面上升的体积可以计
算氧气的体积分数;若碳不完全燃烧,生成气体全部为一氧化碳时,碳与氧气
的质量比为3:4,由于一氧化碳不能被氢氧化钠溶液吸收,不能测定出氧气的
含量;因此要产生一氧化碳,其中参加反应的碳和氧气的质量比必须满足的条
件为大于3:8而小于3:4;
故答案为:大于3:8而小于3:4;
方法二:(1)红磷燃烧产生五氧化二磷,故反应的方程式为:4P+5O 2P O ;
2 2 5
(2)第2,3,4,6组的水的体积就是消耗的氧气的体积,与空气的体积100mL进行
比较,结果得出氧气约占空气体积的 ;而第五组的结果会偏小,可能是没有
冷却到室温读数、红磷量不足、装置漏气等的原因;
故填: ;没有冷却到室温读数等(合理即可).
【点评】本考点考查了用红磷及木炭测定氧气在空气中的体积分数和化学方程式
的书写,属于实验方法和过程的探究,明确测定的原理及实验的注意事项是解
题的关键.
14.(6分)溶解度是解决溶液相关问题的重要依据.
Ⅰ.根据图1解决下列问题:(M,N均不含结晶水)
(1)温度为 t ℃时,M,N两种物质的溶解度相等;
2
(2)t ℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为 6 5 g.保持
1
温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将 不变
(填“变大”、“变小”或“不变”);
第18页(共25页)(3)t ℃时,将25gN加入50g水中,完全溶解后要提高该溶液的溶质质量分数,其
2
操作方法是 降低温度,再加入 N 物质 .
Ⅱ.根据表格解决实际问题:
温度/℃ 20 30 50 60 80
溶解度/g KNO 31.6 45.8 85.5 100 169
3
K CO 110 114 121 126 139
2 3
某KNO 样品中含有少量K CO ,其提纯过程如图2:
3 2 3
(1)图2中溶液C是 饱和 (填“饱和”或“不饱和”)溶液;
(2)样品中钾元素的质量为 3 3 g(结果保留整数).
【考点】7I:饱和溶液和不饱和溶液;7N:固体溶解度曲线及其作用;7R:溶质的质
量分数.
【专题】515:溶液、浊液与溶解度.
【分析】根据已有的溶解度曲线的意义进行分析解答,交点表示在同一温度下二
者的溶解度相等,根据溶解度曲线确定溶质质量分数的变化;物质提纯时要注
意不能生成新的杂质,根据元素的质量计算即可.
【解答】解:Ⅰ(1)据图可以看出,在t ℃时M和N的溶解度相等,故填:t ;
2 2
(2)t ℃时,M的溶解度是30g,将20gM加入50g水中,充分溶解,只能溶解15g,
1
形成溶液的质量为15g+50g=65g.保持温度不变,向该溶液中再加入10g水充
第19页(共25页)分搅拌,10g水中能溶解M3g,故仍然是饱和溶液,溶液的溶质质量分数将不变
故填:65,不变;
(3)t ℃时,N的溶解度是50g,将25gN加入50g水中,完全溶解形成的是饱和溶
2
液,要提高该溶液的溶质质量分数,可以降低温度,再加入N物质,故填:降低
温度,再加入N物质;
Ⅱ.(1)加入硝酸钙溶液,硝酸钙与碳酸钾反应生成碳酸钙沉淀和硝酸钾,故B是
硝酸钾的饱和溶液,降温析出晶体,溶液C是硝酸钾的饱和溶液,故图2中溶
液C是饱和溶液,故填:饱和;
(2)50℃时硝酸钾的溶解度是85.5g,20℃时硝酸钾的溶解度是31.6g,析出晶体
是 53.9g,恰好是 100g 水中析出的硝酸钾的质量,故溶液 C 中水的质量是
100g,其中硝酸钾的质量是31.6g,故硝酸钾的质量是53.9g+31.6g=85.5g,样品
中钾元素的质量为85.5g× ≈33g,故填:33.
【点评】本题考查的是溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线
的意义进行.
15.(4分)请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应 放热 (填“吸
热”或“放热”),反应的化学方程式为 M g + 2HCl=MgC l + H ↑ 。
2 2
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图1,请根据t ﹣t
1 2
时间段反应速率变化,说明化学反应速率受 温度 等因素影响。
研究二:金属与盐溶液反应过程中的相关变化。
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为
CuSO + Fe=FeSO + Cu 。
4 4
(2)在一定量AgNO 和Cu(NO )的混合溶液中加入铁粉,充分反应后,图2描述
3 3 2
第20页(共25页)相关变化曲线,一定不正确的是 B 。
【考点】85:金属的化学性质;E5:物质发生化学变化时的能量变化;G5:书写化学
方程式、文字表达式、电离方程式.
【专题】524:金属与金属材料.
【分析】研究一:(1)根据反应时温度的变化分析反应时能量的问题,镁与盐酸反
应会生成氢气和氯化镁进行分析;
(2)根据图中反应速率的变化进行分析;
研究二:(1)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(2)根据金属活动性顺序可知,铁会先于硝酸银反应生成硝酸亚铁和银,然后再
与硝酸铜反应生成硝酸亚铁和铜进行分析。
【解答】解:研究一:(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应
放 热 , 镁 与 盐 酸 反 应 会 生 成 氢 气 和 氯 化 镁 , 化 学 方 程 式 为 :
Mg+2HCl=MgCl +H ↑;
2 2
(2)通过图中的反应速率可以看出,在t ﹣t 时间段速率加快,所以化学反应速率
1 2
受温度等因素影响;
研究二:(1)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:
CuSO +Fe=FeSO +Cu;
4 4
(2)由金属活动性顺序可知,铁会先于硝酸银反应生成硝酸亚铁和银,然后再与
硝酸铜反应生成硝酸亚铁和铜,所以
A、刚开始铜的质量为零,置换完银才会置换出铜,故A正确;
B、Fe与AgNO 和Cu(NO )的反应均使溶液质量变小,而硝酸根的质量不变,故
3 3 2
硝酸根的质量分数先增大后不变,故B错误;
C、铁和硝酸银反应生成硝酸亚铁和银,每56份质量的铁会置换出216份质量的
银,溶液质量减轻,铁和硝酸铜反应生成硝酸亚铁和铜,每56份质量的铁会置
第21页(共25页)换出64份质量的铜,溶液质量也会减轻,但是没有前面减小的幅度大,故C正
确;
D、铁刚与硝酸银反应生成硝酸亚铁和银,溶液中会出现银离子、亚铁离子、铜离
子三种离子,然后会出现亚铁离子和铜离子,然后只剩下亚铁离子,故D正确
故选:B。
故答案为:研究一:(1)放热,Mg+2HCl=MgCl +H ↑;
2 2
(2)温度;
研究二:(1)CuSO +Fe=FeSO +Cu;
4 4
(2)B。
【点评】本题难度不大,要找准题中考查的知识点即可解答。
16.(5分)用如图实验方法分离NaCl和CaCl 两种固体的混合物A,根据操作流程
2
完成下列问题:
(1)B物质是 碳酸钙(或 CaCO ) .
3
(2)过滤操作中玻璃棒的作用是 引流 .
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善 蒸发前先加
适量的盐酸至不再产生气泡 .
(4)若用原操作方法,要测出混合物A中NaCl和CaCl 的质量比,不称量D,可通
2
过称量 A 和 B 的质量求解.
【考点】4F:混合物的分离方法;4G:过滤的原理、方法及其应用;9H:盐的化学性
质.
【专题】167:物质的分离和提纯.
【分析】(1)根据氯化钙和碳酸钠反应产生碳酸钙沉淀和氯化钠分析沉淀B;
(2)根据过滤时玻璃棒的作用回答;
(3)根据过量的盐酸会增加新的杂质结合除去碳酸钠的方法分析;
(4)根据氯化钙反应产生碳酸钙沉淀质量计算氯化钙的质量,用混合物的质量减
第22页(共25页)去氯化钙的质量就是氯化钠的质量进行分析.
【解答】解:(1)氯化钙和碳酸钠反应产生碳酸钙沉淀和氯化钠,因此经过过滤后
的沉淀是碳酸钙;故填:碳酸钙(或CaCO );
3
(2)过滤时玻璃棒起到引流的作用,防止液体溅出;故填:引流;
(3)因为加入的碳酸钠溶液过量,因此分离出的F含杂质碳酸钠,可以蒸发前先
加适量的盐酸至不再产生气泡除去碳酸钠;故填:蒸发前先加适量的盐酸至不
再产生气泡;
(4)要测出混合物A中NaCl和CaCl 的质量比,可通过碳酸钠和氯化钙反应产生
2
碳酸钙沉淀的质量计算氯化钙的质量,然后用混合物的质量减去氯化钙的质
量就是氯化钠的质量从而计算二者的质量比;故填:A、B.
【点评】本题侧重考查了物质的分离和提纯知识,侧重考查学生的分析问题及解
决问题的能力,注意把握实验操作的原理是解题的关键.
17.(7分)FeCl 溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl
3 3
溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。
写出本实验发生反应的化学方程式 2H O 2H O + O ↑ 。
2 2 2 2
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同
浓度的FeCl 溶液,如图观察到 反应速率 ,就可以粗略判断,得出实验结果。
3
为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设
计。
Ⅱ。
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间。
[方案二]在不同过氧化氢浓度下,测定 相同时间收集气体的体积 ;
方案二的实验测量结果:
30% H O 溶液 2% FeCl 溶液的 加入H O的 反应的时间 生成O 的体
2 2 3 2 2
的体积(mL) 体积(mL) 体积(mL) (min) 积(mL)
1 5 x 20 5 V
1
2 10 3 15 y V
2
表中x= 3 ,y= 5 。
实验结论:通过测量,若V < V(填“>”、“=”或“<”),说明 在不同过
1 2
第23页(共25页)氧化氢浓度下,相同时间收集气体的体积不同 。
【考点】6J:催化剂的特点与催化作用;G5:书写化学方程式、文字表达式、电离方
程式.
【专题】537:科学探究.
【分析】根据过氧化氢在氯化铁作催化剂的条件生成水和氧气进行解答。
Ⅰ.从定性的方面,观察反应速率就可知过氧化氢浓度对过氧化氢分解速率的影
响;
Ⅱ.根据方案一,得出方案二探究的内容;根据实验目的和方案得出xy的值以及
实验结论。
【解答】解:(1)过氧化氢在氯化铁作催化剂的条件生成水和氧气,化学方程式:
2H O 2H O+O ↑;
2 2 2 2
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同
浓度的FeCl 溶液,从反应速率的快慢就可得出结论;
3
Ⅱ.[方案二]在不同过氧化氢浓度下,测定相同时间收集气体的体积;
分析方案二的实验测量结果,可得控制变量x=3,y=5;
通过测量,若V <V ,可得出结论:在不同过氧化氢浓度下,相同时间收集气体的
1 2
体积不同。
故答案为:
2H O 2H O+O ↑;反应速率;相同时间收集气体的体积;
2 2 2 2
3;5;<;在不同过氧化氢浓度下,相同时间收集气体的体积不同。
第24页(共25页)【点评】培养观察记录实验现象,分析实验结果和处理实验数据,得出正确结论的
能力;学会归纳总结、对比分析。
18.(4分)为了测定某稀硫酸的溶质质量分数,在10g稀硫酸中滴加过量的氯化
钡溶液,得到沉淀2.33g,求该稀硫酸的溶质质量分数.
【考点】7U:有关溶质质量分数的简单计算;G6:根据化学反应方程式的计算.
【专题】194:溶质质量分数与化学方程式相结合的计算.
【分析】根据化学方程式,由沉淀的质量求出稀硫酸的溶质质量,进而求得该稀硫
酸的溶质质量分数.
【解答】解:设该稀硫酸的溶质质量为x
BaCl +H SO =BaSO ↓+2HCl
2 2 4 4
98 233
x 2.33g
,解得x=0.98g
∴该稀硫酸的溶质质量分数= =9.8%
答:该稀硫酸的溶质质量分数为9.8%.
【点评】根据化学方程式进行计算的步骤一般为设出未知数,写出配平的化学方
程式,求出相关物质的质量比,列出比例式,求解,答,共六步.
第25页(共25页)