文档内容
2017年贵州省遵义市中考化学试卷
一、选择题(本大题包括10个小题,每小题2分,共20分.每小题只有一个正确
答案,请在答题卡选择题栏内用2B铅笔将对应题目答案的标号涂黑.)
1.(2分)下列变化属于化学变化的是( )
A.海水晒盐 B.红磷燃烧 C.葡萄榨汁 D.玻璃破碎
2.(2分)下列材料属于有机合成材料的是( )
A.陶瓷B.黄铜 C.羊毛 D.塑料
3.(2分)为了防止缺铁性贫血,人体必须摄入的元素是( )
A.铁 B.钙 C.碘 D.锌
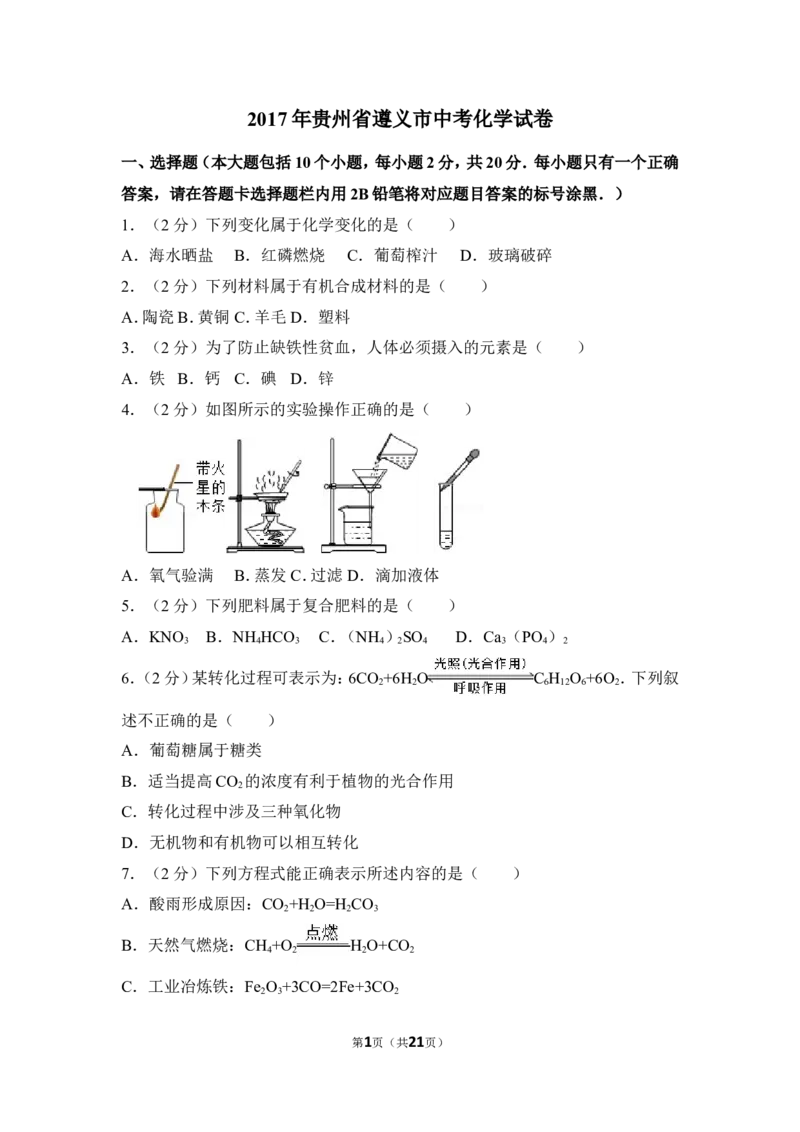
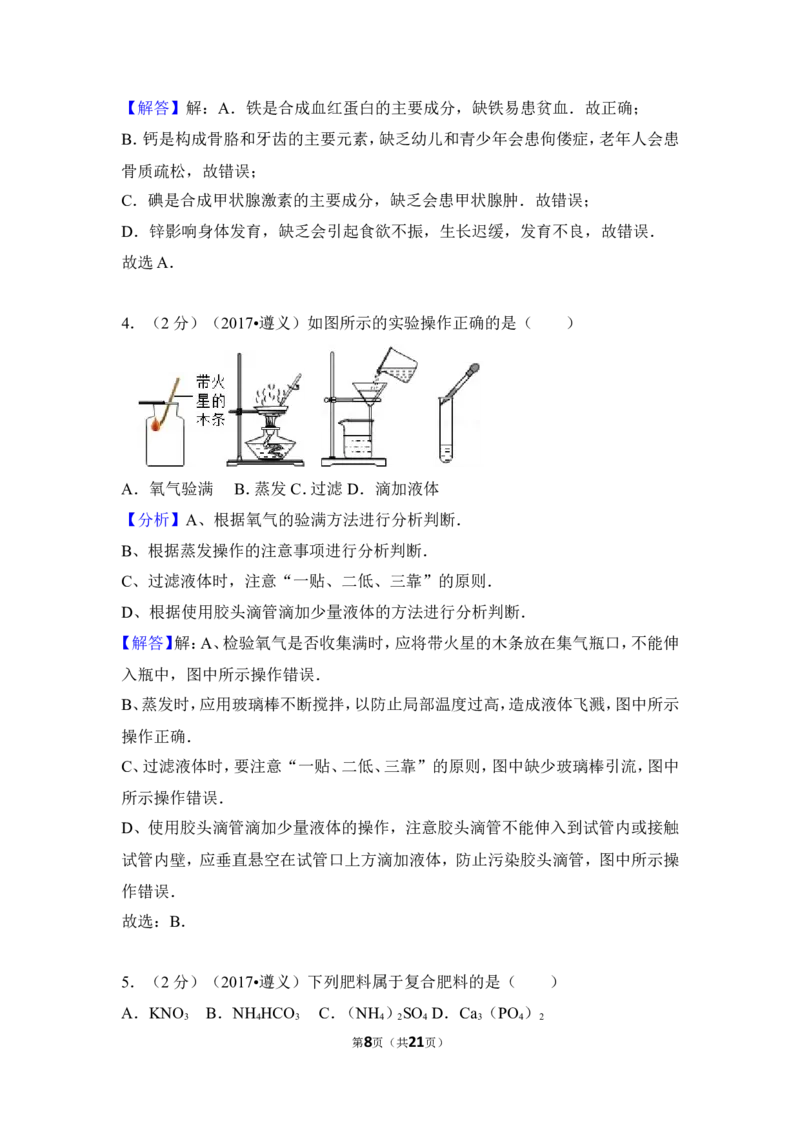
4.(2分)如图所示的实验操作正确的是( )
A.氧气验满 B.蒸发 C.过滤 D.滴加液体
5.(2分)下列肥料属于复合肥料的是( )
A.KNO B.NH HCO C.(NH )SO D.Ca (PO )
3 4 3 4 2 4 3 4 2
6.(2分)某转化过程可表示为:6CO +6H O C H O +6O .下列叙
2 2 6 12 6 2
述不正确的是( )
A.葡萄糖属于糖类
B.适当提高CO 的浓度有利于植物的光合作用
2
C.转化过程中涉及三种氧化物
D.无机物和有机物可以相互转化
7.(2分)下列方程式能正确表示所述内容的是( )
A.酸雨形成原因:CO +H O=H CO
2 2 2 3
B.天然气燃烧:CH +O H O+CO
4 2 2 2
C.工业冶炼铁:Fe O +3CO=2Fe+3CO
2 3 2
第1页(共21页)D.碱式碳酸铜受热:Cu (OH) CO 2CuO+CO ↑+H O
2 2 3 2 2
8.(2分)关于H O和H O 的比较,不正确的是( )
2 2 2
A.都含有氢、氧元素
B.都由氢、氧原子构成,结构相同
C.一定条件下都能分解产生氧气
D.H O是常见的溶剂,H O 溶液可用于医疗消毒
2 2 2
9.(2分)除去下列物质中少量杂质(括号内为杂质)的方法,叙述正确的是
( )
A.一氧化碳(二氧化碳)﹣﹣通过灼热的氧化铜
B.水(植物油)﹣﹣加洗洁精,搅拌振荡
C.Na CO (NaHCO )固体﹣﹣充分加热至固体质量不变
2 3 3
D.NaCl溶液(CaCl )﹣﹣滴加适量K CO 溶液、过滤
2 2 3
10.(2分)根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是(
)
A.氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法
B.30℃氯酸钾饱和溶液的溶质质量分数为10%
C.80℃时7gNaCl和20g水能形成饱和溶液
D.控制温度,图中氯酸钠和氯化钾能发生化学反应
二、非选择题(本大题包括7个小题,每空1分,共40分.请将下列各题应答内容,
填写到答题卡相应题号的空格内.)
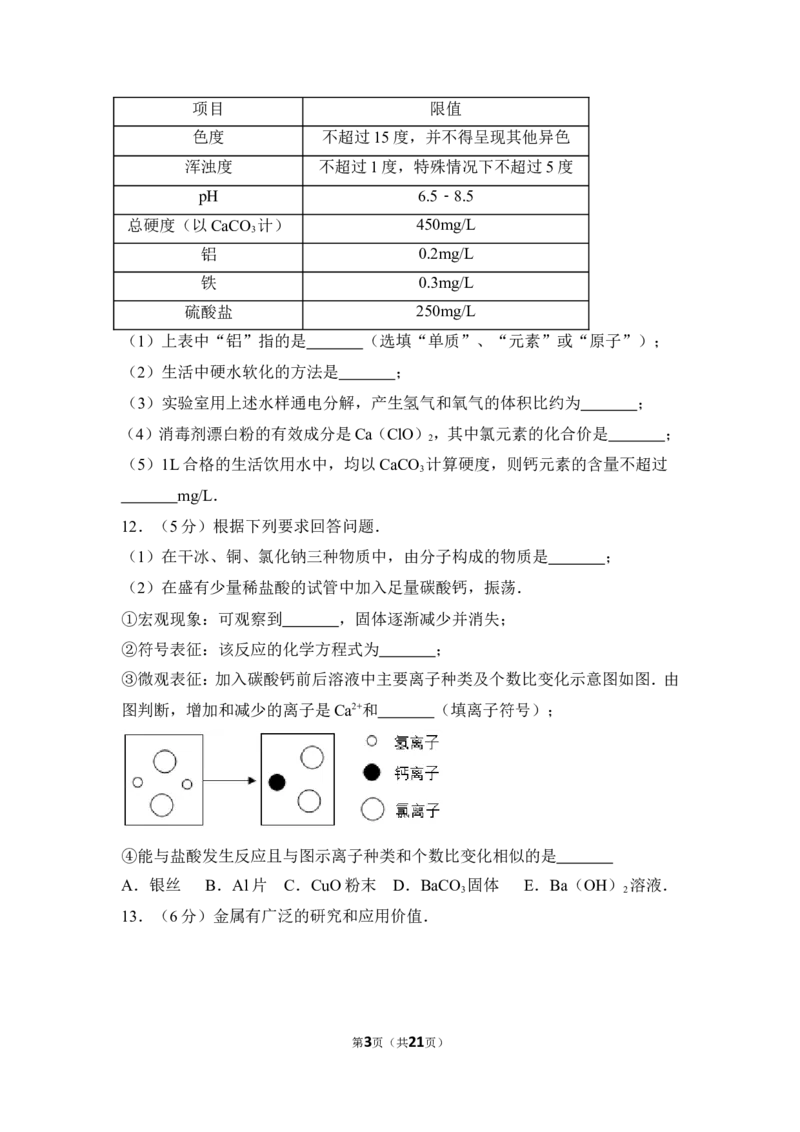
11.(5分)下表是生活饮用水国家标准的部分内容.
生活饮用水水质常规检验项目及限值(部分)
第2页(共21页)项目 限值
色度 不超过15度,并不得呈现其他异色
浑浊度 不超过1度,特殊情况下不超过5度
pH 6.5﹣8.5
总硬度(以CaCO 计) 450mg/L
3
铝 0.2mg/L
铁 0.3mg/L
硫酸盐 250mg/L
(1)上表中“铝”指的是 (选填“单质”、“元素”或“原子”);
(2)生活中硬水软化的方法是 ;
(3)实验室用上述水样通电分解,产生氢气和氧气的体积比约为 ;
(4)消毒剂漂白粉的有效成分是Ca(ClO),其中氯元素的化合价是 ;
2
(5)1L合格的生活饮用水中,均以CaCO 计算硬度,则钙元素的含量不超过
3
mg/L.
12.(5分)根据下列要求回答问题.
(1)在干冰、铜、氯化钠三种物质中,由分子构成的物质是 ;
(2)在盛有少量稀盐酸的试管中加入足量碳酸钙,振荡.
①宏观现象:可观察到 ,固体逐渐减少并消失;
②符号表征:该反应的化学方程式为 ;
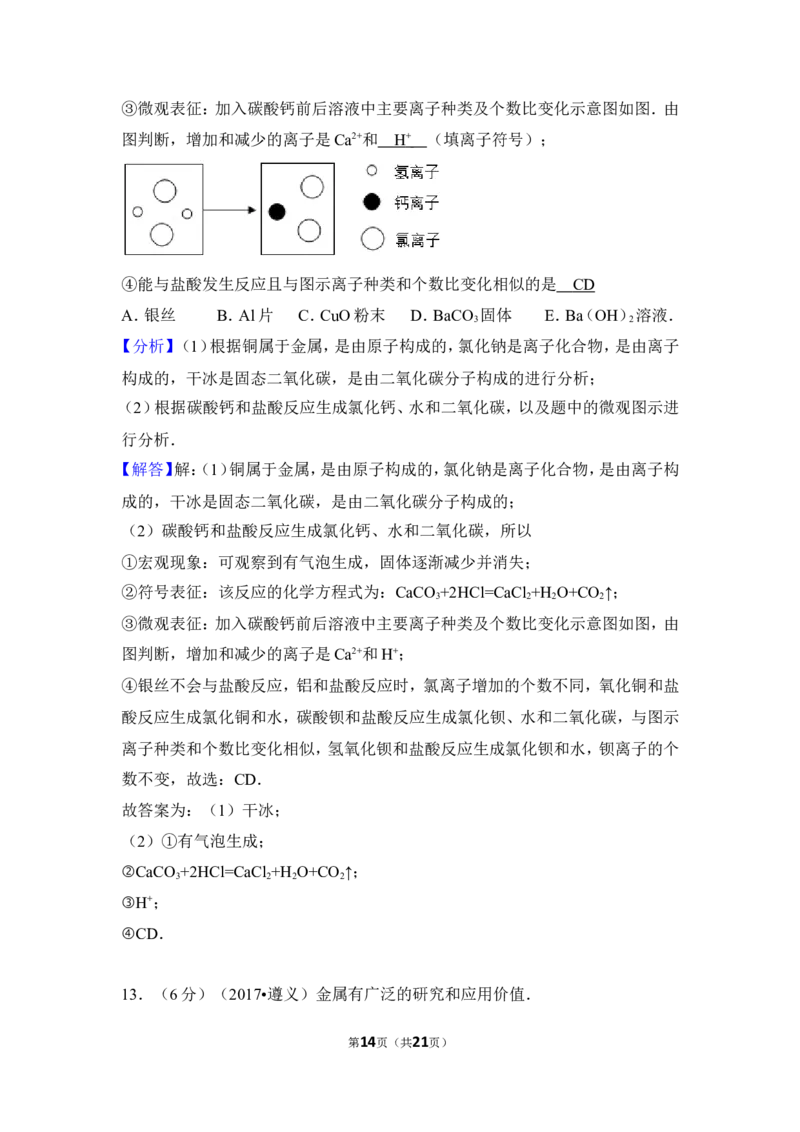
③微观表征:加入碳酸钙前后溶液中主要离子种类及个数比变化示意图如图.由
图判断,增加和减少的离子是Ca2+和 (填离子符号);
④能与盐酸发生反应且与图示离子种类和个数比变化相似的是
A.银丝 B.Al片 C.CuO粉末 D.BaCO 固体 E.Ba(OH) 溶液.
3 2
13.(6分)金属有广泛的研究和应用价值.
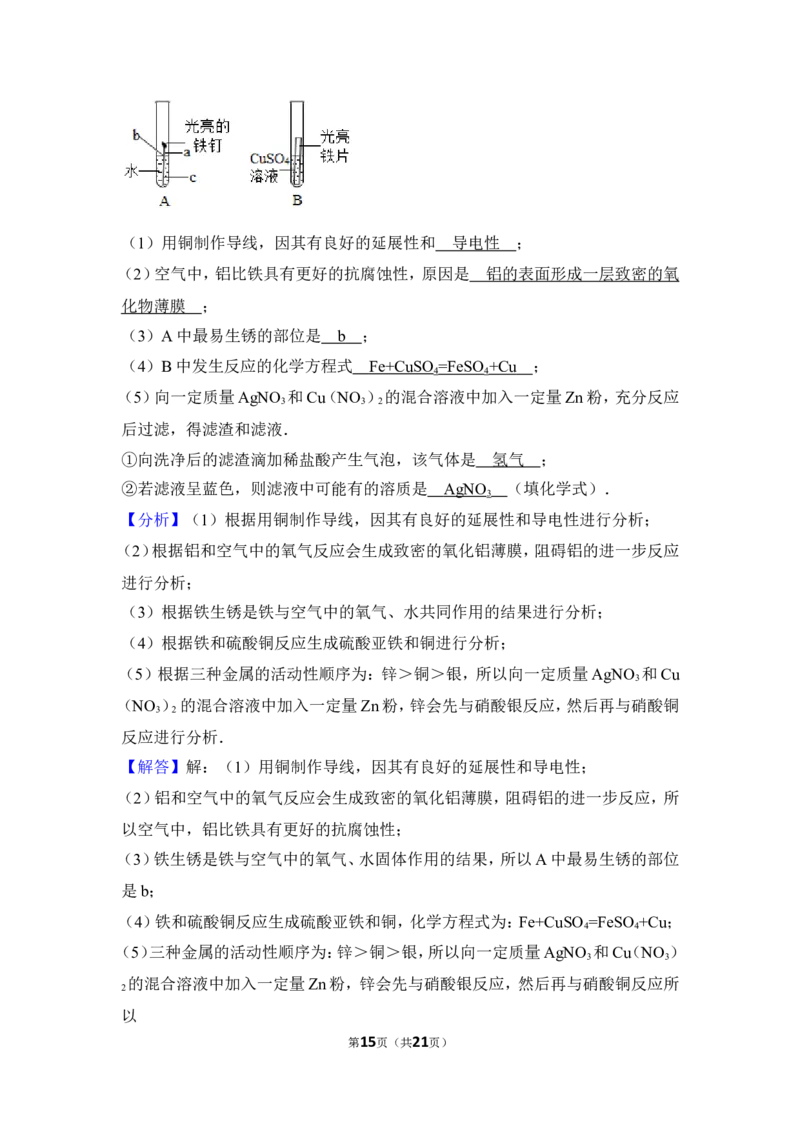
第3页(共21页)(1)用铜制作导线,因其有良好的延展性和 ;
(2)空气中,铝比铁具有更好的抗腐蚀性,原因是 ;
(3)A中最易生锈的部位是 ;
(4)B中发生反应的化学方程式 ;
(5)向一定质量AgNO 和Cu(NO )的混合溶液中加入一定量Zn粉,充分反应
3 3 2
后过滤,得滤渣和滤液.
①向洗净后的滤渣滴加稀盐酸产生气泡,该气体是 ;
②若滤液呈蓝色,则滤液中可能有的溶质是 (填化学式).
14.(7分)Na CO 是一种常见的盐,多角度看物质可以提高对该物质的认识.
2 3
(1)Na CO 俗称 ;
2 3
(2)从类别看,Na CO 可以看作是某种碱和某种氧化物反应的产物.该反应的化
2 3
学方程式: ;
(3)从用途看,Na CO 可制备某些物质,如Na CO +M→NaOH+N,写出该反应的
2 3 2 3
化学方程式: ;
(4)从组成看,Na CO 、NaCl均属钠盐,NaCl溶于水显中性,但Na CO 溶于水显
2 3 2 3
碱性.请完善实验方案,探析上述性质差异的初步原因:
实验步骤 实现现象 实验结论
取适量NaCl溶液于试管中,滴加石蕊试 ① Na+和Cl﹣与溶
液,振荡 液的酸碱性无关
取适量滴有酚酞试液的Na CO 溶液少许 ③ ④
2 3
于试管中,滴加②
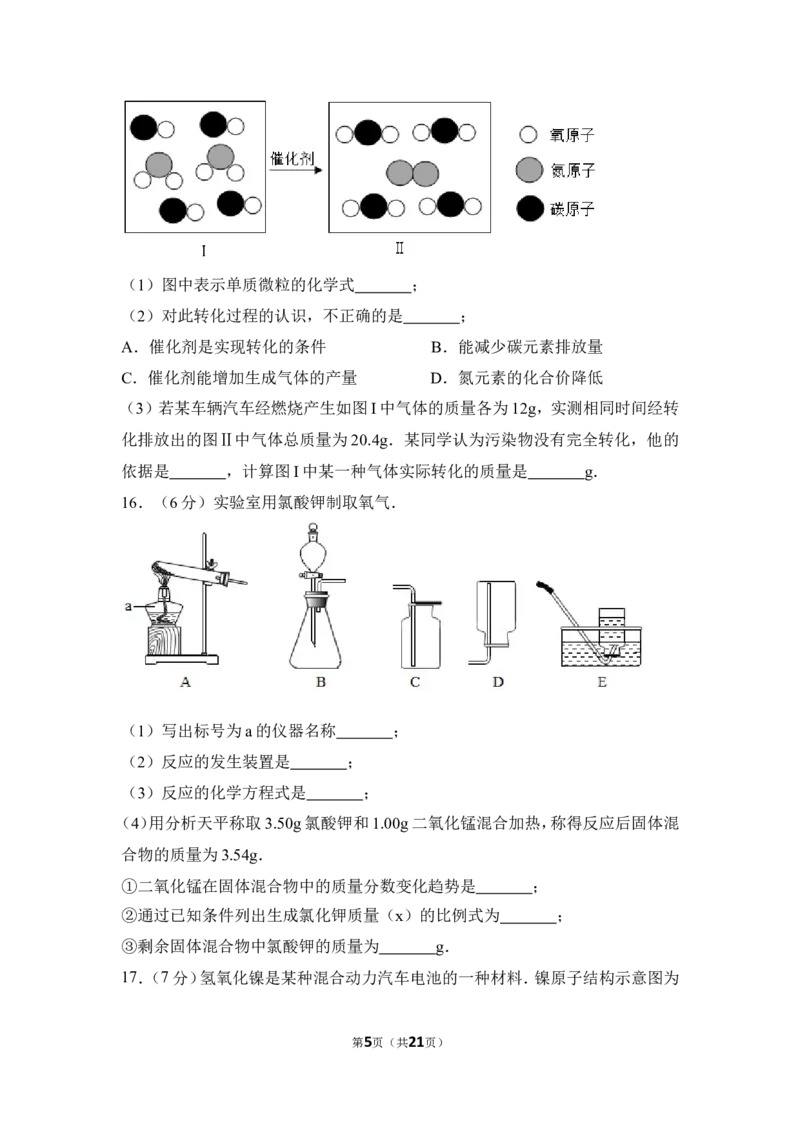
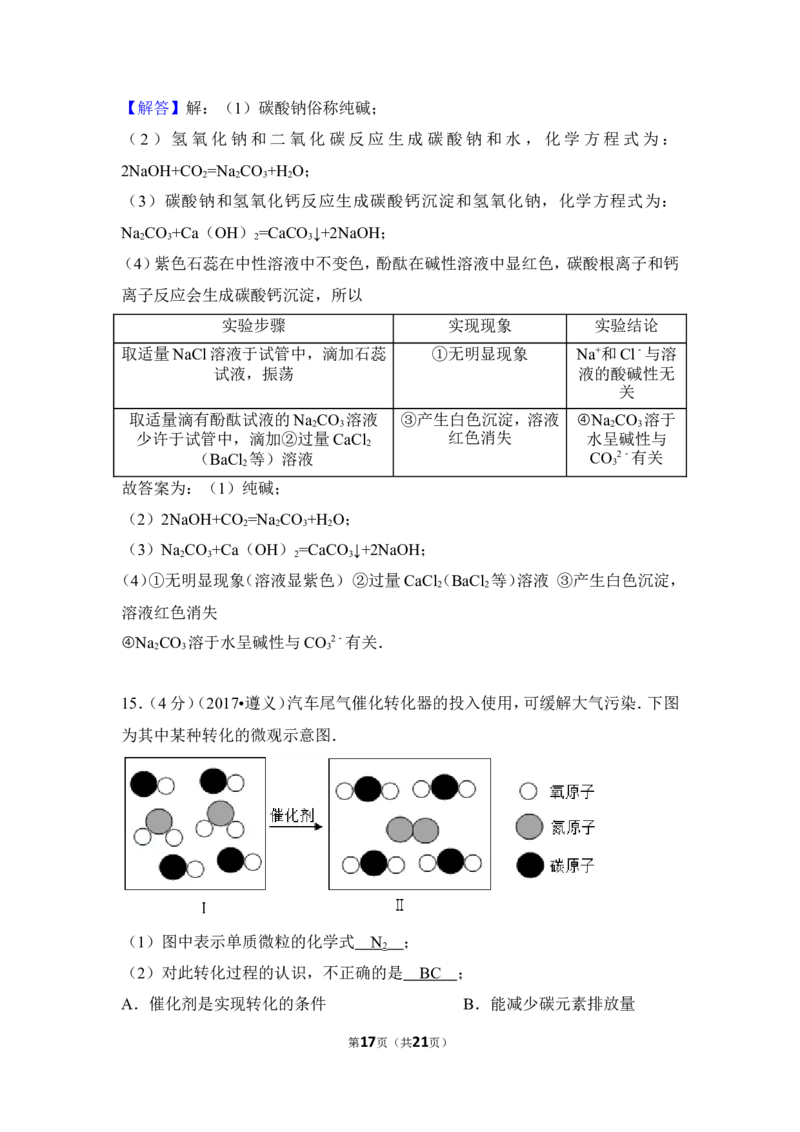
15.(4分)汽车尾气催化转化器的投入使用,可缓解大气污染.下图为其中某种
转化的微观示意图.
第4页(共21页)(1)图中表示单质微粒的化学式 ;
(2)对此转化过程的认识,不正确的是 ;
A.催化剂是实现转化的条件 B.能减少碳元素排放量
C.催化剂能增加生成气体的产量 D.氮元素的化合价降低
(3)若某车辆汽车经燃烧产生如图I中气体的质量各为12g,实测相同时间经转
化排放出的图Ⅱ中气体总质量为20.4g.某同学认为污染物没有完全转化,他的
依据是 ,计算图I中某一种气体实际转化的质量是 g.
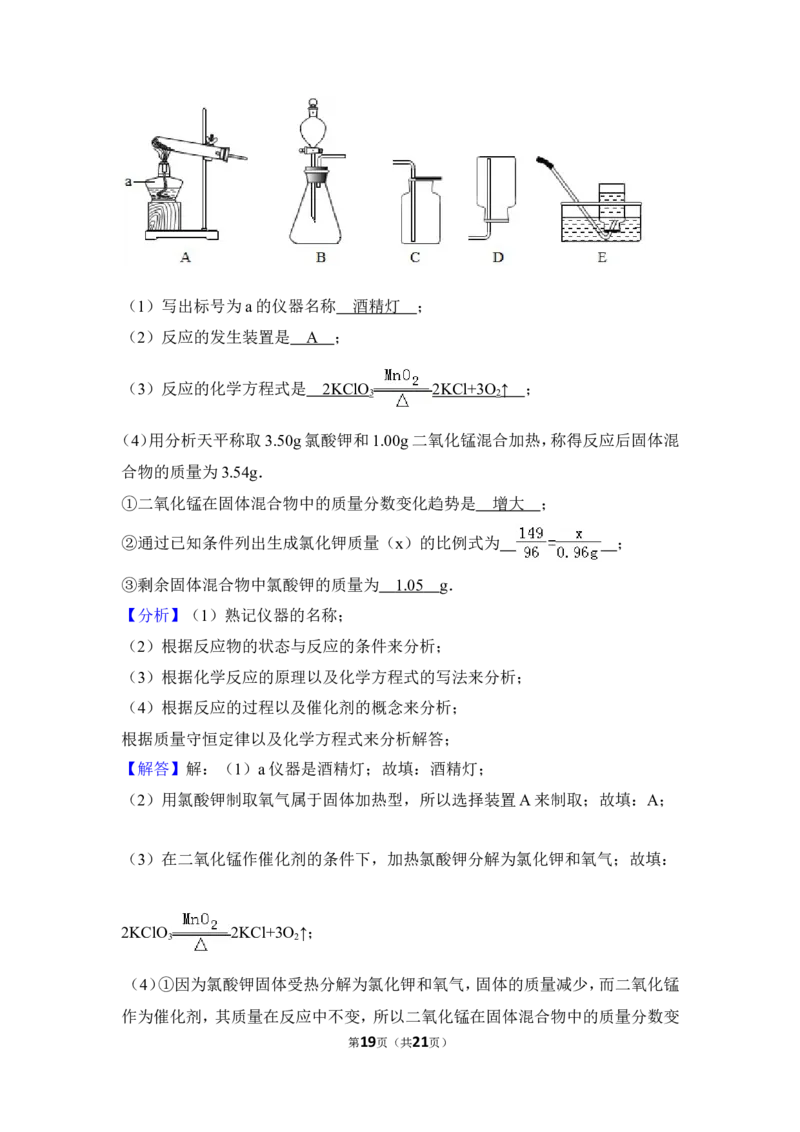
16.(6分)实验室用氯酸钾制取氧气.
(1)写出标号为a的仪器名称 ;
(2)反应的发生装置是 ;
(3)反应的化学方程式是 ;
(4)用分析天平称取3.50g氯酸钾和1.00g二氧化锰混合加热,称得反应后固体混
合物的质量为3.54g.
①二氧化锰在固体混合物中的质量分数变化趋势是 ;
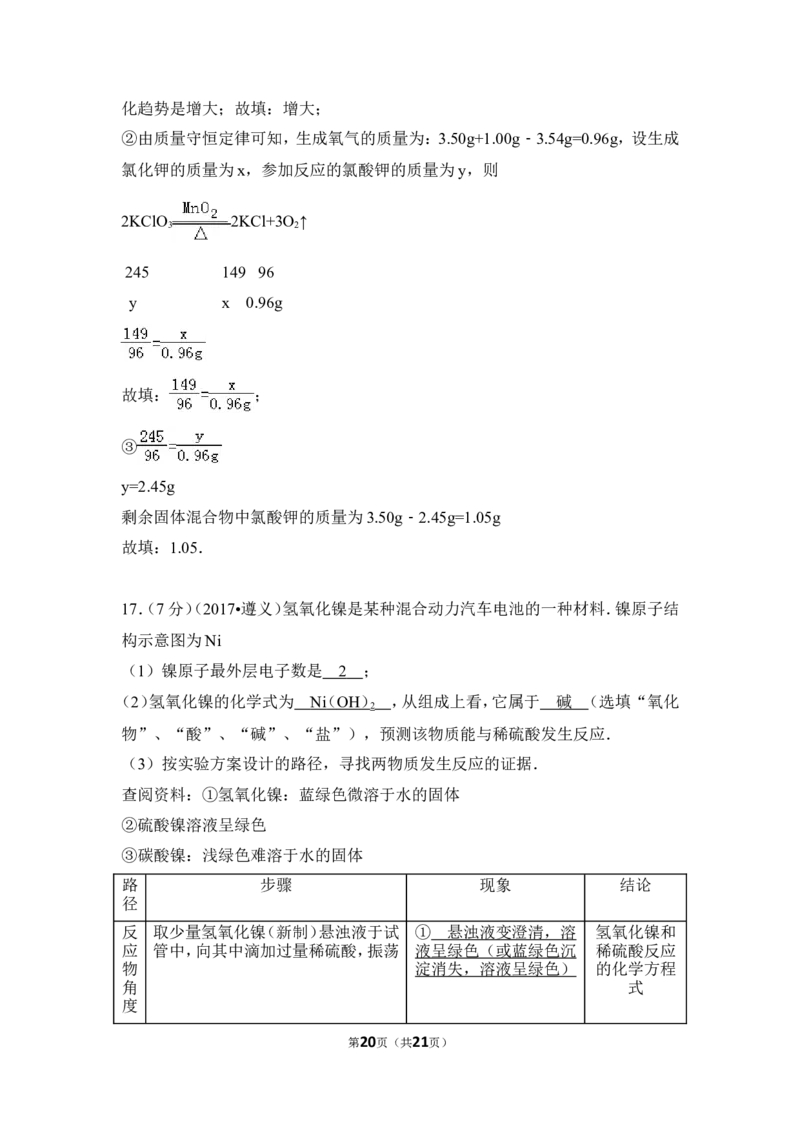
②通过已知条件列出生成氯化钾质量(x)的比例式为 ;
③剩余固体混合物中氯酸钾的质量为 g.
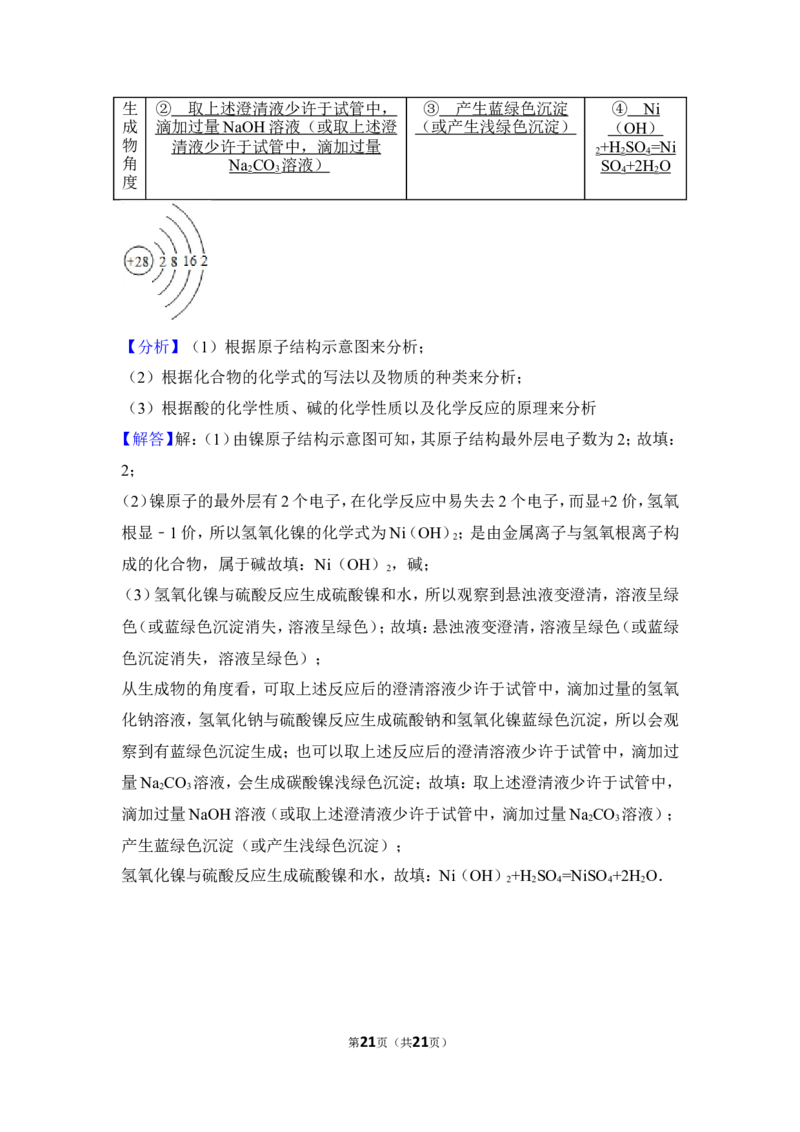
17.(7分)氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结构示意图为
第5页(共21页)Ni
(1)镍原子最外层电子数是 ;
(2)氢氧化镍的化学式为 ,从组成上看,它属于 (选填“氧化物”、
“酸”、“碱”、“盐”),预测该物质能与稀硫酸发生反应.
(3)按实验方案设计的路径,寻找两物质发生反应的证据.
查阅资料:①氢氧化镍:蓝绿色微溶于水的固体
②硫酸镍溶液呈绿色
③碳酸镍:浅绿色难溶于水的固体
路径 步骤 现象 结论
反应物 取少量氢氧化镍(新制)悬浊液于试管 氢氧化镍和稀
角度 中,向其中滴加过量稀硫酸,振荡 硫酸反应的化
①
学方程式
生成物
④
角度
② ③
第6页(共21页)2017 年贵州省遵义市中考化学试卷
参考答案与试题解析
一、选择题(本大题包括10个小题,每小题2分,共20分.每小题只有一个正确
答案,请在答题卡选择题栏内用2B铅笔将对应题目答案的标号涂黑.)
1.(2分)(2017•遵义)下列变化属于化学变化的是( )
A.海水晒盐 B.红磷燃烧 C.葡萄榨汁 D.玻璃破碎
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、海水晒盐过程中只是状态发生改变,没有新物质生成,属于物理变
化.
B、红磷燃烧的过程中有新物质五氧化二磷生成,属于化学变化.
C、葡萄榨汁的过程中没有新物质生成,属于物理变化.
D、玻璃破碎的过程中只是形状发生变化,没有新物质生成,属于物理变化.
故选B.
2.(2分)(2017•遵义)下列材料属于有机合成材料的是( )
A.陶瓷B.黄铜 C.羊毛 D.塑料
【分析】有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:
有机物、合成、高分子化合物,据此常见材料的分类进行分析判断.
【解答】解:A、陶瓷是用瓷土烧制而成的,属于无机非金属材料,故选项错误.
B、黄铜是铜的合金,属于金属材料,故选项错误.
C、羊毛属于天然材料,故选项错误.
D、塑料属于三大合成材料之一,故选项正确.
故选:D.
3.(2分)(2017•遵义)为了防止缺铁性贫血,人体必须摄入的元素是( )
A.铁 B.钙 C.碘 D.锌
【分析】从各种元素的生理作用、缺乏症等角度进行分析解答.
第7页(共21页)【解答】解:A.铁是合成血红蛋白的主要成分,缺铁易患贫血.故正确;
B.钙是构成骨胳和牙齿的主要元素,缺乏幼儿和青少年会患佝偻症,老年人会患
骨质疏松,故错误;
C.碘是合成甲状腺激素的主要成分,缺乏会患甲状腺肿.故错误;
D.锌影响身体发育,缺乏会引起食欲不振,生长迟缓,发育不良,故错误.
故选A.
4.(2分)(2017•遵义)如图所示的实验操作正确的是( )
A.氧气验满 B.蒸发 C.过滤 D.滴加液体
【分析】A、根据氧气的验满方法进行分析判断.
B、根据蒸发操作的注意事项进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据使用胶头滴管滴加少量液体的方法进行分析判断.
【解答】解:A、检验氧气是否收集满时,应将带火星的木条放在集气瓶口,不能伸
入瓶中,图中所示操作错误.
B、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示
操作正确.
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中
所示操作错误.
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触
试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操
作错误.
故选:B.
5.(2分)(2017•遵义)下列肥料属于复合肥料的是( )
A.KNO B.NH HCO C.(NH )SO D.Ca (PO )
3 4 3 4 2 4 3 4 2
第8页(共21页)【分析】含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的
肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复
合肥.
【解答】解:A、KNO 中含有钾元素和氮元素,属于复合肥;
3
B、NH HCO 中含有氮元素,属于氮肥,故选项错误;
4 3
C、(NH ) SO 中含有氮元素,属于氮肥,故选项错误;
4 2 4
D、Ca (PO ) 中含有磷元素,属于磷肥,故选项错误.
3 4 2
故选A.
6.(2 分)(2017•遵义)某转化过程可表示为:6CO +6H O
2 2
C H O +6O .下列叙述不正确的是( )
6 12 6 2
A.葡萄糖属于糖类
B.适当提高CO 的浓度有利于植物的光合作用
2
C.转化过程中涉及三种氧化物
D.无机物和有机物可以相互转化
【分析】根据反应的化学方程式以及物质的类别进行分析解答即可.
【解答】解:
A、葡萄糖属于糖类物质,故正确;
B、适当提高CO 浓度,能促进植物的光合作用,故正确;
2
C、该反应中的二氧化碳、水属于氧化物,只有两种物质,不是三种物质,故错误;
D、此反应说明有机物和无机物可以相互转化,故正确;
故选C.
7.(2分)(2017•遵义)下列方程式能正确表示所述内容的是( )
A.酸雨形成原因:CO +H O=H CO
2 2 2 3
B.天然气燃烧:CH +O H O+CO
4 2 2 2
C.工业冶炼铁:Fe O +3CO=2Fe+3CO
2 3 2
D.碱式碳酸铜受热:Cu (OH) CO 2CuO+CO ↑+H O
2 2 3 2 2
第9页(共21页)【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书
写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】解:A.空气中含有二氧化碳,与水反应生成碳酸,所以正常的雨水显酸性;
但是酸雨的形成主要是由二氧化硫与水反应生成亚硫酸造成的,方程式为
SO +H O=H SO ,故错误;
2 2 2 3
B.该化学方程式没有配平,正确的为CH +2O 2H O+CO ,故错误;
4 2 2 2
C.工业炼铁是在高温的条件下进行的,正确的化学方程式为Fe O +3CO
2 3
2Fe+3CO ,故错误;
2
D.碱式碳酸铜在加热的条件下分解为氧化铜、水和二氧化碳,化学方程式书写正
确,故正确.
故选D.
8.(2分)(2017•遵义)关于H O和H O 的比较,不正确的是( )
2 2 2
A.都含有氢、氧元素
B.都由氢、氧原子构成,结构相同
C.一定条件下都能分解产生氧气
D.H O是常见的溶剂,H O 溶液可用于医疗消毒
2 2 2
【分析】A.根据物质的组成来分析;
B.根据物质的构成来分析;
C.根据物质的化学性质来分析;
D.根据物质的性质与用途来分析.
【解答】解:A.H O和H O 的中都含有氢元素和氧元素,故选项说法正确.
2 2 2
B.水是由水分子构成的,过氧化氢是由过氧化氢分子构成的,故选项说法错误.
C.H O和H O 在一定条件下都能发生分解反应,水在通电条件下生成氢气和氧
2 2 2
气,过氧化氢在二氧化锰的催化作用下生成水和氧气,上述反应均属于分解反应
故选项说法正确.
D.水是最常用的一种溶剂;过氧化氢溶液是一种常用的消毒剂,故选项说法正确.
故选B.
第10页(共21页)9.(2分)(2017•遵义)除去下列物质中少量杂质(括号内为杂质)的方法,叙述正
确的是( )
A.一氧化碳(二氧化碳)﹣﹣通过灼热的氧化铜
B.水(植物油)﹣﹣加洗洁精,搅拌振荡
C.Na CO (NaHCO )固体﹣﹣充分加热至固体质量不变
2 3 3
D.NaCl溶液(CaCl )﹣﹣滴加适量K CO 溶液、过滤
2 2 3
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提
纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:
①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质
【解答】解:A、CO 能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除
去,不符合除杂原则,故选项所采取的方法错误.
B、洗洁精具有乳化作用,能将植物油分散成细小的液滴,搅拌振荡,形成稳定的
乳浊液,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、NaHCO 充分加热生成碳酸钠、水和二氧化碳,至固体质量不变,能除去杂质
3
且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、CaCl 能与适量K CO 溶液反应生成碳酸钙沉淀和氯化钾,能除去杂质但引入
2 2 3
了新的杂质氯化钾,不符合除杂原则,故选项所采取的方法错误.
故选:C.
10.(2分)(2017•遵义)根据如图提供的几种物质的溶解度曲线,判断下列说法正
确的是( )
A.氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法
B.30℃氯酸钾饱和溶液的溶质质量分数为10%
第11页(共21页)C.80℃时7gNaCl和20g水能形成饱和溶液
D.控制温度,图中氯酸钠和氯化钾能发生化学反应
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和
溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从
而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:A、氯酸钾的溶解度受温度变化影响较大,所以氯酸钾中混有少量氯
化钠,提纯氯酸钾最好用降温结晶的方法,故A错误;
B、30℃时,氯酸钾的溶解度是10g,所以氯酸钾饱和溶液的溶质质量分数为:
×100%=9.1%,故B错误;
C、80℃时,氯化钠的溶解度是40g,所以7gNaCl和20g水不能形成饱和溶液,故
C错误;
D、氯酸钠和氯化钾交换成分可以得到氯酸钾和氯化钠,控制温度在10﹣30℃之
间,氯化钠的溶解度较大,氯酸钾的溶解度较小,会以晶体形式析出,所以图中氯
酸钠和氯化钾能发生化学反应,故D正确.
故选:D.
二、非选择题(本大题包括7个小题,每空1分,共40分.请将下列各题应答内容,
填写到答题卡相应题号的空格内.)
11.(5分)(2017•遵义)下表是生活饮用水国家标准的部分内容.
生活饮用水水质常规检验项目及限值(部分)
项目 限值
色度 不超过15度,并不得呈现其他异色
浑浊度 不超过1度,特殊情况下不超过5度
pH 6.5﹣8.5
总硬度(以CaCO 计) 450mg/L
3
铝 0.2mg/L
铁 0.3mg/L
硫酸盐 250mg/L
第12页(共21页)(1)上表中“铝”指的是 元素 (选填“单质”、“元素”或“原子”);
(2)生活中硬水软化的方法是 煮沸 ;
(3)实验室用上述水样通电分解,产生氢气和氧气的体积比约为 2 : 1 ;
(4)消毒剂漂白粉的有效成分是Ca(ClO),其中氯元素的化合价是 + 1 价 ;
2
(5)1L合格的生活饮用水中,均以CaCO 计算硬度,则钙元素的含量不超过
3
180 mg/L.
【分析】(1)食品、药品、营养品、矿泉水等物质中的“铁、铝”等不是以单质、分
子、原子、离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来
描述.
(2)根据硬水软化的方法来分析;
(3)根据电解水反应进行分析;
(4)根据化合物中元素正负化合价的代数和为零进行分析;
(5)根据题目信息及化合物中元素质量分数的计算方法分析;
【解答】解:(1)食品、药品、营养品、矿泉水等物质中的“铁、铝”等不是以单质、
分子、原子、离子等形式存在,这里所指的“铝”是强调存在的元素,与具体形态
无关.故填:元素;
(2)加热煮沸能减少水中钙、镁离子的化合物的含量.所以,生活中常用的硬水软
化的方法是煮沸;故填:煮沸;
(3)实验室用中将水通电分解,产生氢气和氧气的体积比约为2:1;故填:2:1;
(4)在Ca(ClO)中,钙为+2价,氧为﹣2价,设氯元素的化合价为x,则(+2)+2x+
2
(﹣2)×2=0,x=1;故填:+1价;
(5)由题目信息可知,1L合格的生活饮用水中,CaCO 的质量不能超过450mg,则
3
钙元素的含量应不超过:450mg× =180mg;故填:180;
12.(5分)(2017•遵义)根据下列要求回答问题.
(1)在干冰、铜、氯化钠三种物质中,由分子构成的物质是 干冰 ;
(2)在盛有少量稀盐酸的试管中加入足量碳酸钙,振荡.
①宏观现象:可观察到 有气泡生成 ,固体逐渐减少并消失;
②符号表征:该反应的化学方程式为 CaCO +2HCl=CaCl +H O+CO ↑ ;
3 2 2 2
第13页(共21页)③微观表征:加入碳酸钙前后溶液中主要离子种类及个数比变化示意图如图.由
图判断,增加和减少的离子是Ca2+和 H + (填离子符号);
④能与盐酸发生反应且与图示离子种类和个数比变化相似的是 CD
A.银丝 B.Al片 C.CuO粉末 D.BaCO 固体 E.Ba(OH)溶液.
3 2
【分析】(1)根据铜属于金属,是由原子构成的,氯化钠是离子化合物,是由离子
构成的,干冰是固态二氧化碳,是由二氧化碳分子构成的进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,以及题中的微观图示进
行分析.
【解答】解:(1)铜属于金属,是由原子构成的,氯化钠是离子化合物,是由离子构
成的,干冰是固态二氧化碳,是由二氧化碳分子构成的;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以
①宏观现象:可观察到有气泡生成,固体逐渐减少并消失;
②符号表征:该反应的化学方程式为:CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
③微观表征:加入碳酸钙前后溶液中主要离子种类及个数比变化示意图如图,由
图判断,增加和减少的离子是Ca2+和H+;
④银丝不会与盐酸反应,铝和盐酸反应时,氯离子增加的个数不同,氧化铜和盐
酸反应生成氯化铜和水,碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,与图示
离子种类和个数比变化相似,氢氧化钡和盐酸反应生成氯化钡和水,钡离子的个
数不变,故选:CD.
故答案为:(1)干冰;
(2)①有气泡生成;
②CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
③H+;
④CD.
13.(6分)(2017•遵义)金属有广泛的研究和应用价值.
第14页(共21页)(1)用铜制作导线,因其有良好的延展性和 导电性 ;
(2)空气中,铝比铁具有更好的抗腐蚀性,原因是 铝的表面形成一层致密的氧
化物薄膜 ;
(3)A中最易生锈的部位是 b ;
(4)B中发生反应的化学方程式 Fe+CuSO =FeSO +Cu ;
4 4
(5)向一定质量AgNO 和Cu(NO )的混合溶液中加入一定量Zn粉,充分反应
3 3 2
后过滤,得滤渣和滤液.
①向洗净后的滤渣滴加稀盐酸产生气泡,该气体是 氢气 ;
②若滤液呈蓝色,则滤液中可能有的溶质是 AgNO (填化学式).
3
【分析】(1)根据用铜制作导线,因其有良好的延展性和导电性进行分析;
(2)根据铝和空气中的氧气反应会生成致密的氧化铝薄膜,阻碍铝的进一步反应
进行分析;
(3)根据铁生锈是铁与空气中的氧气、水共同作用的结果进行分析;
(4)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(5)根据三种金属的活动性顺序为:锌>铜>银,所以向一定质量AgNO 和Cu
3
(NO )的混合溶液中加入一定量Zn粉,锌会先与硝酸银反应,然后再与硝酸铜
3 2
反应进行分析.
【解答】解:(1)用铜制作导线,因其有良好的延展性和导电性;
(2)铝和空气中的氧气反应会生成致密的氧化铝薄膜,阻碍铝的进一步反应,所
以空气中,铝比铁具有更好的抗腐蚀性;
(3)铁生锈是铁与空气中的氧气、水固体作用的结果,所以A中最易生锈的部位
是b;
(4)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO =FeSO +Cu;
4 4
(5)三种金属的活动性顺序为:锌>铜>银,所以向一定质量AgNO 和Cu(NO )
3 3
的混合溶液中加入一定量Zn粉,锌会先与硝酸银反应,然后再与硝酸铜反应所
2
以
第15页(共21页)①向洗净后的滤渣滴加稀盐酸产生气泡,锌过量,锌和硝酸银、硝酸铜完全反应,
滤渣中含有锌、铜、银,则该气体是氢气;
②若滤液呈蓝色,滤液中一定含有硝酸铜和硝酸锌,则滤液中可能有的溶质是
AgNO .
3
故答案为:(1)导电性;
(2)铝的表面形成一层致密的氧化物薄膜;
(3)b;
(4)Fe+CuSO =FeSO +Cu;
4 4
(5)①H (氢气);
2
②AgNO .
3
14.(7分)(2017•遵义)Na CO 是一种常见的盐,多角度看物质可以提高对该物
2 3
质的认识.
(1)Na CO 俗称 纯碱 ;
2 3
(2)从类别看,Na CO 可以看作是某种碱和某种氧化物反应的产物.该反应的化
2 3
学方程式: 2NaOH+CO =Na CO +H O ;
2 2 3 2
(3)从用途看,Na CO 可制备某些物质,如Na CO +M→NaOH+N,写出该反应的
2 3 2 3
化学方程式: N a CO +Ca ( OH ) =CaCO ↓+2NaOH ;
2 3 2 3
(4)从组成看,Na CO 、NaCl均属钠盐,NaCl溶于水显中性,但Na CO 溶于水显
2 3 2 3
碱性.请完善实验方案,探析上述性质差异的初步原因:
实验步骤 实现现象 实验结论
取适量NaCl溶液于试管中,滴加石蕊 ① 无明显现象 Na+和Cl﹣与溶
试液,振荡 液的酸碱性无
关
取适量滴有酚酞试液的Na CO 溶液 ③ 产生白色沉淀,溶 ④ N a CO 溶
2 3 2 3
少许于试管中,滴加② 过量 CaC l 液红色消失 于水呈碱性与
2
( BaC l 等)溶液 CO 2﹣ 有关
2 3
【分析】(1)根据碳酸钠俗称纯碱进行分析;
(2)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(3)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠进行分析;
(4)根据紫色石蕊在中性溶液中不变色,酚酞在碱性溶液中显红色,碳酸根离子
和钙离子反应会生成碳酸钙沉淀进行分析.
第16页(共21页)【解答】解:(1)碳酸钠俗称纯碱;
(2)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:
2NaOH+CO =Na CO +H O;
2 2 3 2
(3)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:
Na CO +Ca(OH) =CaCO ↓+2NaOH;
2 3 2 3
(4)紫色石蕊在中性溶液中不变色,酚酞在碱性溶液中显红色,碳酸根离子和钙
离子反应会生成碳酸钙沉淀,所以
实验步骤 实现现象 实验结论
取适量NaCl溶液于试管中,滴加石蕊 ①无明显现象 Na+和Cl﹣与溶
试液,振荡 液的酸碱性无
关
取适量滴有酚酞试液的Na CO 溶液 ③产生白色沉淀,溶液 ④Na CO 溶于
2 3 2 3
少许于试管中,滴加②过量CaCl 红色消失 水呈碱性与
2
(BaCl 等)溶液 CO 2﹣有关
2 3
故答案为:(1)纯碱;
(2)2NaOH+CO =Na CO +H O;
2 2 3 2
(3)Na CO +Ca(OH) =CaCO ↓+2NaOH;
2 3 2 3
(4)①无明显现象(溶液显紫色) ②过量CaCl(BaCl 等)溶液 ③产生白色沉淀,
2 2
溶液红色消失
④Na CO 溶于水呈碱性与CO 2﹣有关.
2 3 3
15.(4分)(2017•遵义)汽车尾气催化转化器的投入使用,可缓解大气污染.下图
为其中某种转化的微观示意图.
(1)图中表示单质微粒的化学式 N ;
2
(2)对此转化过程的认识,不正确的是 BC ;
A.催化剂是实现转化的条件 B.能减少碳元素排放量
第17页(共21页)C.催化剂能增加生成气体的产量 D.氮元素的化合价降低
(3)若某车辆汽车经燃烧产生如图I中气体的质量各为12g,实测相同时间经转
化排放出的图Ⅱ中气体总质量为20.4g.某同学认为污染物没有完全转化,他的
依据是 质量守恒定律 ,计算图I中某一种气体实际转化的质量是 9.2 (或
11.2 ) g.
【分析】根据反应的微观示意图,写出反应的化学方程式,根据方程式的意义进行
有关的分析与计算.
【解答】解:由反应的微观示意图可知,反应物为NO 和CO,生成物为为CO 和
2 2
N ,因此反应的化学方程式为:2NO +4CO 4CO +N ;
2 2 2 2
(1)图中表示单质微粒的化学式为N ;
2
(2)A.由图示可知:催化剂是实现转化的条件,故正确;
B、根据质量守恒定律,反应前后元素的质量和种类不变,不能减少碳元素排放量,
故错误;
C、催化剂只是改变反应速率,不能增加生成气体的产量,故错误;
D、氮元素的化合价由+2价,变为0价,化合价降低,故正确.
(3)若某车辆汽车经燃烧产生如图I中气体的质量各为12g,实测相同时间经转
化排放出的图Ⅱ中气体总质量为20.4g.某同学认为污染物没有完全转化,他的
依据是质量守恒定律,实际转化的质量为20.4g;
由反应的化学方程式:2NO +4CO 4CO +N ;
2 2 2
92 112
则二氧化氮气体实际转化的质量是:20.4g× 100%=9.2g;
则一氧化碳气体实际转化的质量是:20.4g× 100%=11.2g;
答案:
(1)N ;(2)B C;(3)质量守恒定律;9.2(或11.2)
2
16.(6分)(2017•遵义)实验室用氯酸钾制取氧气.
第18页(共21页)(1)写出标号为a的仪器名称 酒精灯 ;
(2)反应的发生装置是 A ;
(3)反应的化学方程式是 2KClO 2KCl+3O ↑ ;
3 2
(4)用分析天平称取3.50g氯酸钾和1.00g二氧化锰混合加热,称得反应后固体混
合物的质量为3.54g.
①二氧化锰在固体混合物中的质量分数变化趋势是 增大 ;
②通过已知条件列出生成氯化钾质量(x)的比例式为 ;
③剩余固体混合物中氯酸钾的质量为 1.0 5 g.
【分析】(1)熟记仪器的名称;
(2)根据反应物的状态与反应的条件来分析;
(3)根据化学反应的原理以及化学方程式的写法来分析;
(4)根据反应的过程以及催化剂的概念来分析;
根据质量守恒定律以及化学方程式来分析解答;
【解答】解:(1)a仪器是酒精灯;故填:酒精灯;
(2)用氯酸钾制取氧气属于固体加热型,所以选择装置A来制取;故填:A;
(3)在二氧化锰作催化剂的条件下,加热氯酸钾分解为氯化钾和氧气;故填:
2KClO 2KCl+3O ↑;
3 2
(4)①因为氯酸钾固体受热分解为氯化钾和氧气,固体的质量减少,而二氧化锰
作为催化剂,其质量在反应中不变,所以二氧化锰在固体混合物中的质量分数变
第19页(共21页)化趋势是增大;故填:增大;
②由质量守恒定律可知,生成氧气的质量为:3.50g+1.00g﹣3.54g=0.96g,设生成
氯化钾的质量为x,参加反应的氯酸钾的质量为y,则
2KClO 2KCl+3O ↑
3 2
245 149 96
y x 0.96g
故填: ;
③
y=2.45g
剩余固体混合物中氯酸钾的质量为3.50g﹣2.45g=1.05g
故填:1.05.
17.(7分)(2017•遵义)氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结
构示意图为Ni
(1)镍原子最外层电子数是 2 ;
(2)氢氧化镍的化学式为 N (i OH ) ,从组成上看,它属于 碱 (选填“氧化
2
物”、“酸”、“碱”、“盐”),预测该物质能与稀硫酸发生反应.
(3)按实验方案设计的路径,寻找两物质发生反应的证据.
查阅资料:①氢氧化镍:蓝绿色微溶于水的固体
②硫酸镍溶液呈绿色
③碳酸镍:浅绿色难溶于水的固体
路 步骤 现象 结论
径
反 取少量氢氧化镍(新制)悬浊液于试 ① 悬浊液变澄清,溶 氢氧化镍和
应 管中,向其中滴加过量稀硫酸,振荡 液呈绿色(或蓝绿色沉 稀硫酸反应
物 淀消失,溶液呈绿色) 的化学方程
角 式
度
第20页(共21页)生 ② 取上述澄清液少许于试管中, ③ 产生蓝绿色沉淀 ④ N i
成 滴加过量 NaOH 溶液(或取上述澄 (或产生浅绿色沉淀) ( OH )
物 清液少许于试管中,滴加过量 +H SO =Ni
2 2 4
角 Na CO 溶液) SO +2H O
2 3 4 2
度
【分析】(1)根据原子结构示意图来分析;
(2)根据化合物的化学式的写法以及物质的种类来分析;
(3)根据酸的化学性质、碱的化学性质以及化学反应的原理来分析
【解答】解:(1)由镍原子结构示意图可知,其原子结构最外层电子数为2;故填:
2;
(2)镍原子的最外层有2个电子,在化学反应中易失去2个电子,而显+2价,氢氧
根显﹣1价,所以氢氧化镍的化学式为Ni(OH);是由金属离子与氢氧根离子构
2
成的化合物,属于碱故填:Ni(OH) ,碱;
2
(3)氢氧化镍与硫酸反应生成硫酸镍和水,所以观察到悬浊液变澄清,溶液呈绿
色(或蓝绿色沉淀消失,溶液呈绿色);故填:悬浊液变澄清,溶液呈绿色(或蓝绿
色沉淀消失,溶液呈绿色);
从生成物的角度看,可取上述反应后的澄清溶液少许于试管中,滴加过量的氢氧
化钠溶液,氢氧化钠与硫酸镍反应生成硫酸钠和氢氧化镍蓝绿色沉淀,所以会观
察到有蓝绿色沉淀生成;也可以取上述反应后的澄清溶液少许于试管中,滴加过
量Na CO 溶液,会生成碳酸镍浅绿色沉淀;故填:取上述澄清液少许于试管中,
2 3
滴加过量NaOH溶液(或取上述澄清液少许于试管中,滴加过量Na CO 溶液);
2 3
产生蓝绿色沉淀(或产生浅绿色沉淀);
氢氧化镍与硫酸反应生成硫酸镍和水,故填:Ni(OH)+H SO =NiSO +2H O.
2 2 4 4 2
第21页(共21页)