文档内容
2021 年贵州省安顺市中考化学试卷
附相对原子质量:H-1;C-12;N-14;O-16;Mg-24;Na-23;Si-28;S-32;
一、选择题:本题包括6个小题,每小题2分,共12分。每题只有一个选项符合题意。
1. 空气是人人都离不开的重要物质,其中体积分数约为21%并能供给人类呼吸的气体是
A. N B. O C. Ne D. CO
2 2 2
2. 2021年世界环境日的主题为“人与自然和谐共生”。下列做法不符合该主题的是
A. 大量燃放烟花爆竹 B. 工业废水净化达标排放
C. 生活垃圾分类回收 D. 农药、化肥合理使用
3. 学习化学,树立健康生活新观念。下列观念或行为不正确的是
A. 毒品对肝、肾和脑会造成永久性损害,我们应珍爱生命、远离毒品
B. 香烟的烟气中含有几百种对人体有害的物质,青少年一定不要吸烟
C. 维生素可以调节新陈代谢、预防疾病和维持身体健康
D. 人体所摄入必需元素越多越有利于健康
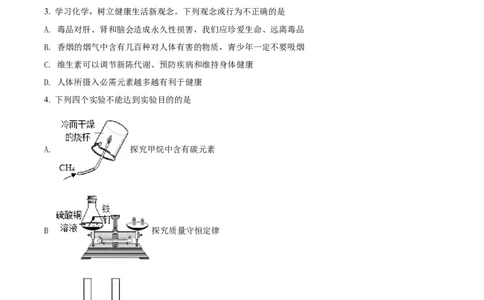
4. 下列四个实验不能达到实验目的的是
A. 探究甲烷中含有碳元素
B 探究质量守恒定律
.
C. 探究不同物质在同种溶剂中的溶解性
学科网(北京)股份有限公司D. 探究木炭 还原性
的
5. 燃烧是人类最早利用的化学反应之一。下列说法正确的是
A. 可燃物的温度达到着火点即可燃烧
B. 燃烧属于化学反应,爆炸也一定属于化学反应
C. 化学反应常伴随能量变化,燃烧是一种发光放热的化学反应
D. 在氧气中能燃烧 的物质在空气中也一定能燃烧
6. 取等质量的NaCO 和NaHCO 固体分别置于两个体积相同的密闭容器中,分别一次性加入等浓度等体
2 3 3
积的过量稀硫酸,用压强传感器测得两容器内压强随时间的变化关系如图所示。下列说法正确的是
A. 曲线a表示NaCO 与稀硫酸反应过程中压强随时间的变化关系
2 3
B. 反应过程中两容器内溶液的pH均逐渐减小
C. 反应结束后,两容器中HSO 的质量相等,NaSO 的质量也相等
2 4 2 4
的
D. 反应结束后,向两容器中加入过量BaCl 溶液,产生沉淀 质量相等
2
四、非选择题:本题共7个小题,共48分。
7. 化学与我们的生活、生产息息相关。
(1)小满时节,为促进农作物生长,可施用的化肥有:尿素[CO(NH )]、硝酸钠(NaNO )、硫酸钾
2 2 3
(KSO ),其中属于钾肥的是 _____。
2 4
(2)目前我国已掌握在﹣269℃下加压,将氦气转化为液氦的技术,该转化过程属于 _____(填“物理变
化”或“化学变化”)。
(3)文房四宝承载着优秀的中华传统文化。我国古代用墨书写或绘制的书画能长久保存,是因为常温下
碳的化学性质 _____(填“活泼”或“不活泼”)。而在高温下,碳能与很多物质发生反应,碳充分燃烧的化
学方程式为 _____。
学科网(北京)股份有限公司(4)“中国粮食•中国饭碗”。米饭中富含的营养素有 _____。
(5)口罩是防疫的必备品,其生产原料中用到的聚丙烯属于 _____(填“合成材料”或“金属材料”)。
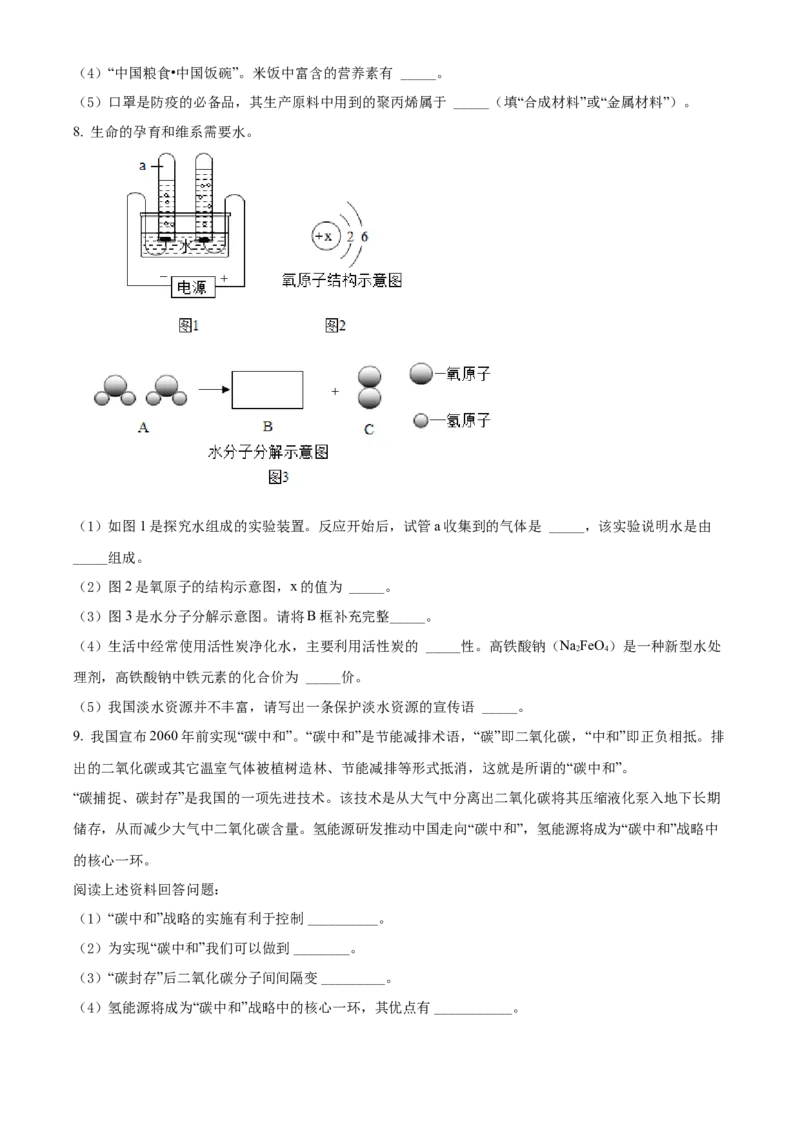
8. 生命的孕育和维系需要水。
(1)如图1是探究水组成的实验装置。反应开始后,试管a收集到的气体是 _____,该实验说明水是由
_____组成。
(2)图2是氧原子的结构示意图,x的值为 _____。
(3)图3是水分子分解示意图。请将B框补充完整_____。
(4)生活中经常使用活性炭净化水,主要利用活性炭的 _____性。高铁酸钠(NaFeO)是一种新型水处
2 4
理剂,高铁酸钠中铁元素的化合价为 _____价。
(5)我国淡水资源并不丰富,请写出一条保护淡水资源的宣传语 _____。
9. 我国宣布2060年前实现“碳中和”。“碳中和”是节能减排术语,“碳”即二氧化碳,“中和”即正负相抵。排
出的二氧化碳或其它温室气体被植树造林、节能减排等形式抵消,这就是所谓的“碳中和”。
“碳捕捉、碳封存”是我国的一项先进技术。该技术是从大气中分离出二氧化碳将其压缩液化泵入地下长期
储存,从而减少大气中二氧化碳含量。氢能源研发推动中国走向“碳中和”,氢能源将成为“碳中和”战略中
的核心一环。
阅读上述资料回答问题:
(1)“碳中和”战略的实施有利于控制 __________。
(2)为实现“碳中和”我们可以做到 ________。
(3)“碳封存”后二氧化碳分子间间隔变 _________。
(4)氢能源将成为“碳中和”战略中的核心一环,其优点有 ___________。
学科网(北京)股份有限公司(5)利用一种新型“人造树叶”在光照条件下进行光合作用可将二氧化碳和水转化为乙醇(C HOH)和氧
2 5
气,化学方程式为 ______________。
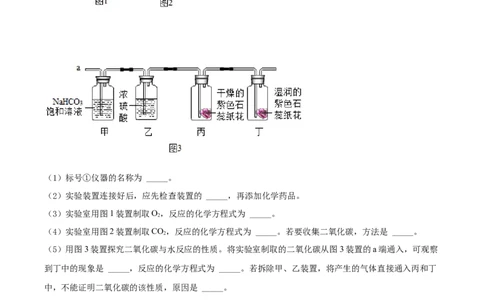
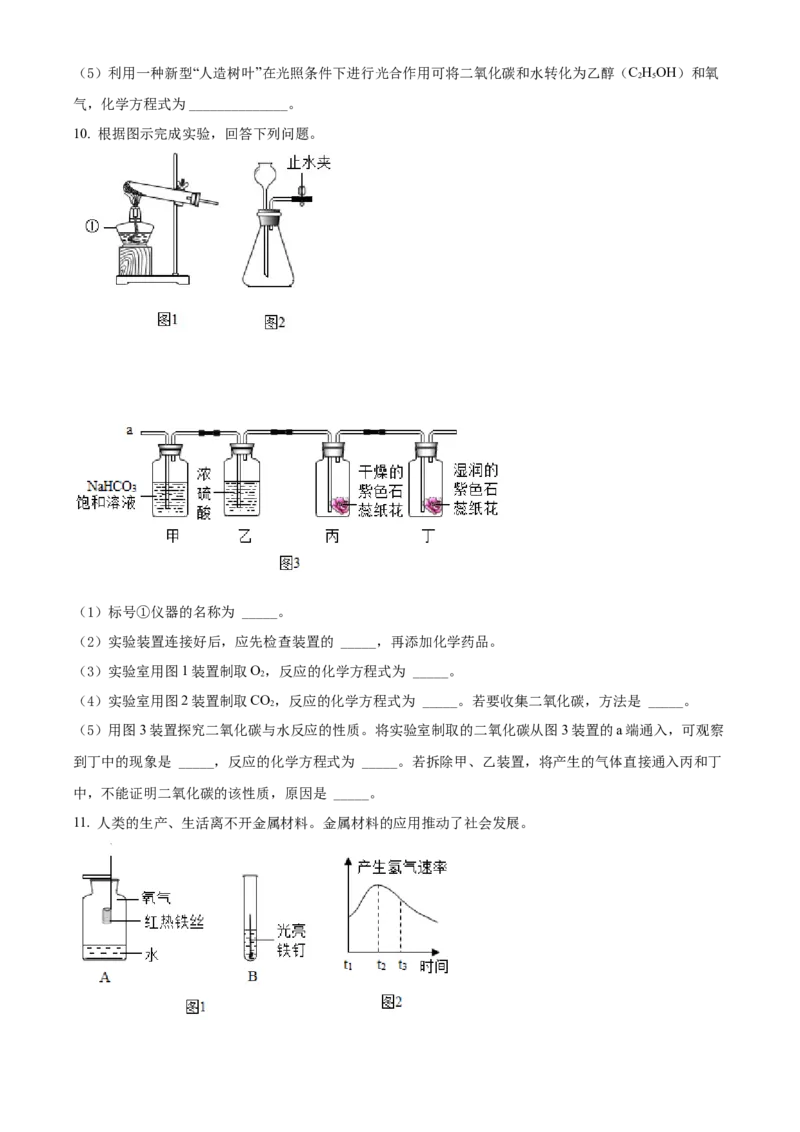
10. 根据图示完成实验,回答下列问题。
(1)标号①仪器的名称为 _____。
(2)实验装置连接好后,应先检查装置的 _____,再添加化学药品。
(3)实验室用图1装置制取O,反应的化学方程式为 _____。
2
(4)实验室用图2装置制取CO,反应的化学方程式为 _____。若要收集二氧化碳,方法是 _____。
2
(5)用图3装置探究二氧化碳与水反应的性质。将实验室制取的二氧化碳从图3装置的a端通入,可观察
到丁中的现象是 _____,反应的化学方程式为 _____。若拆除甲、乙装置,将产生的气体直接通入丙和丁
中,不能证明二氧化碳的该性质,原因是 _____。
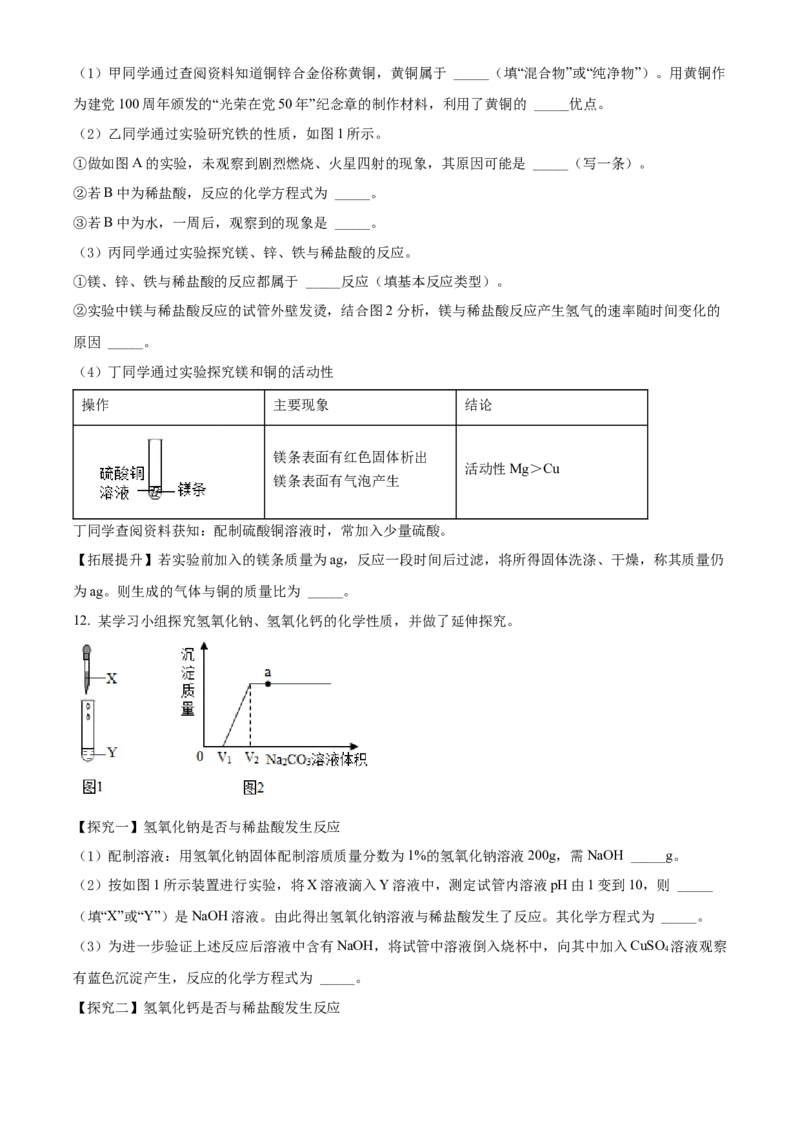
11. 人类的生产、生活离不开金属材料。金属材料的应用推动了社会发展。
学科网(北京)股份有限公司(1)甲同学通过查阅资料知道铜锌合金俗称黄铜,黄铜属于 _____(填“混合物”或“纯净物”)。用黄铜作
为建党100周年颁发的“光荣在党50年”纪念章的制作材料,利用了黄铜的 _____优点。
(2)乙同学通过实验研究铁的性质,如图1所示。
①做如图A的实验,未观察到剧烈燃烧、火星四射的现象,其原因可能是 _____(写一条)。
②若B中为稀盐酸,反应的化学方程式为 _____。
③若B中为水,一周后,观察到的现象是 _____。
(3)丙同学通过实验探究镁、锌、铁与稀盐酸的反应。
①镁、锌、铁与稀盐酸的反应都属于 _____反应(填基本反应类型)。
②实验中镁与稀盐酸反应的试管外壁发烫,结合图2分析,镁与稀盐酸反应产生氢气的速率随时间变化的
原因 _____。
(4)丁同学通过实验探究镁和铜的活动性
操作 主要现象 结论
镁条表面有红色固体析出
活动性Mg>Cu
镁条表面有气泡产生
丁同学查阅资料获知:配制硫酸铜溶液时,常加入少量硫酸。
【拓展提升】若实验前加入的镁条质量为ag,反应一段时间后过滤,将所得固体洗涤、干燥,称其质量仍
为ag。则生成的气体与铜的质量比为 _____。
12. 某学习小组探究氢氧化钠、氢氧化钙的化学性质,并做了延伸探究。
【探究一】氢氧化钠是否与稀盐酸发生反应
(1)配制溶液:用氢氧化钠固体配制溶质质量分数为1%的氢氧化钠溶液200g,需NaOH _____g。
(2)按如图1所示装置进行实验,将X溶液滴入Y溶液中,测定试管内溶液pH由1变到10,则 _____
(填“X”或“Y”)是NaOH溶液。由此得出氢氧化钠溶液与稀盐酸发生了反应。其化学方程式为 _____。
(3)为进一步验证上述反应后溶液中含有NaOH,将试管中溶液倒入烧杯中,向其中加入CuSO 溶液观察
4
有蓝色沉淀产生,反应的化学方程式为 _____。
【探究二】氢氧化钙是否与稀盐酸发生反应
学科网(北京)股份有限公司若再按如图1所示装置进行实验,若X溶液为稀盐酸,Y溶液为澄清石灰水,将X溶液滴入Y溶液中。
【提出问题】反应后试管内溶液中的溶质成分是什么?
【查阅资料】CaCl 溶液呈中性。
2
【作出猜想】溶液中溶质成分可能有三种情况:
①CaCl
2
②CaCl 和HCl
2
③CaCl 和Ca(OH)
2 2
【设计实验】将试管内溶液倒入烧杯中,向其中逐滴加入稀碳酸钠溶液的同时,充分搅拌,直至过量。
【分析讨论】
(4)实验过程中产生沉淀质量与碳酸钠溶液体积之间的关系如图2所示。写出实验过程中的现象 _____。
【得出结论】
(5)猜想 _____正确(填序号)。
【反思讨论】
(6)结合图2分析,下列说法正确的是 (填序号)。
A. 溶液质量逐渐增大
B. a点对应溶液中含有的微粒只有Na+、Cl﹣、HO
2
C. 氯化钙 的质量先增大后减小
D. 氯化钠的质量逐渐增大至碳酸钠溶液体积为V 后不变
2
(7)图2中加入碳酸钠溶液体积从V 到V 过程中发生反应的化学方程式为 _____。
1 2
13. 位于我省的“中国天眼”FAST,其“眼镜片”由金刚砂(SiC)制造。生产SiC的化学方程式为SiO+3C
2
SiC+2CO↑,消耗C的质量为36kg时,理论上可生产SiC的质量为多少?
学科网(北京)股份有限公司