文档内容
2017 年陕西省初中毕业学业考试(副题)
第一部分(选择题 共14分)
一、选择题(共7小题,每小题2分,计14分。每小题只有一个选项是符合题意的)
1. 学以致用既能加深对知识的理解,也能体现知识的价值。某同学结合所学知识,向家长提出下列建议,
其中不合理的是( )
A. 向硬水中加入明矾,可降低水的硬度
B. 被蚊虫叮咬后,可涂抹肥皂液减轻痛痒
C. 多吃水果蔬菜,可补充人体所需的维生素
D. 用燃烧的方法,可区分羊毛纤维和合成纤维
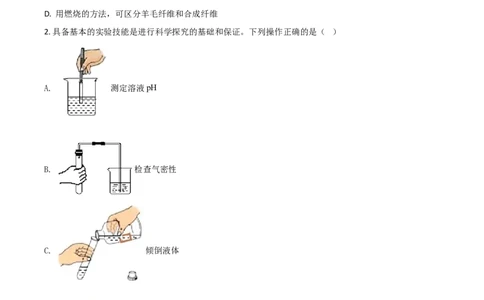
2. 具备基本的实验技能是进行科学探究的基础和保证。下列操作正确的是( )
A. 测定溶液pH
B. 检查气密性
C. 倾倒液体
D. CO 的验满
2
3. 下列对相关知识的分析不正确的是( )
.
A 用海水晒制粗盐,其过程发生了物理变化
B. 用过滤的方法分离混合物,是利用物质的物理性质不同C. 用生石灰作干燥剂,其过程发生了化学变化
D. 硫酸能与氯化钡溶液反应产生沉淀,是因为其具有酸性
4. 硝酸铵可用作氮肥。其受热易分解,易溶于水,且水溶液显酸性。下列有关硝酸铵的说法不正确的是(
)
A. 应置于阴凉干燥处保存
B. 和碱性物质混合使用会降低肥效
C. 长期施用会导致土壤酸化板结
D. 施用后可使植物根系发达
5. 用不同的观念分析物质,可以更全面准确地认识物质。下列关于氢气(H)、甲烷(CH)、酒精
2 4
(C HO)的说法正确的是( )
2 6
.
A 从变化角度分析:都能燃烧生成HO和CO
2 2
B. 从物质分类分析:都属于含氢化合物
C. 从元素组成分析:都含氢元素
D. 从构成微粒分析:都含氢分子
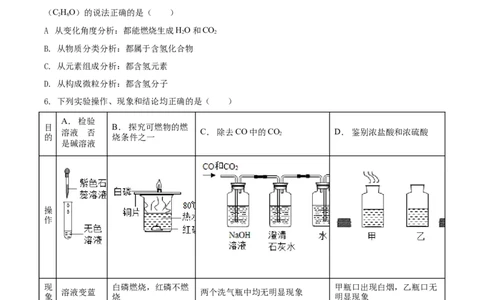
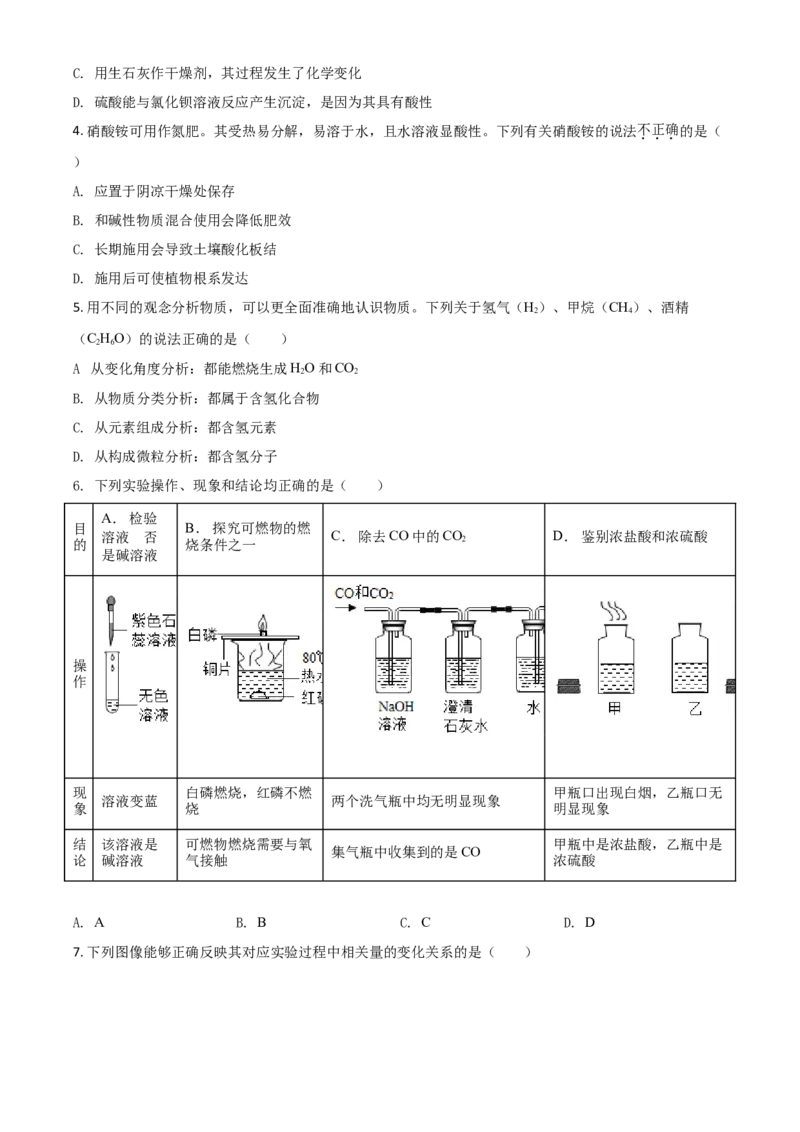
6. 下列实验操作、现象和结论均正确的是( )
A. 检验
目 B. 探究可燃物的燃
溶液 是否 C. 除去CO中的CO D. 鉴别浓盐酸和浓硫酸
的 烧条件之一 2
是碱溶液
操
作
现 白磷燃烧,红磷不燃 甲瓶口出现白烟,乙瓶口无
溶液变蓝 两个洗气瓶中均无明显现象
象 烧 明显现象
结 该溶液是 可燃物燃烧需要与氧 甲瓶中是浓盐酸,乙瓶中是
集气瓶中收集到的是CO
论 碱溶液 气接触 浓硫酸
A. A B. B C. C D. D
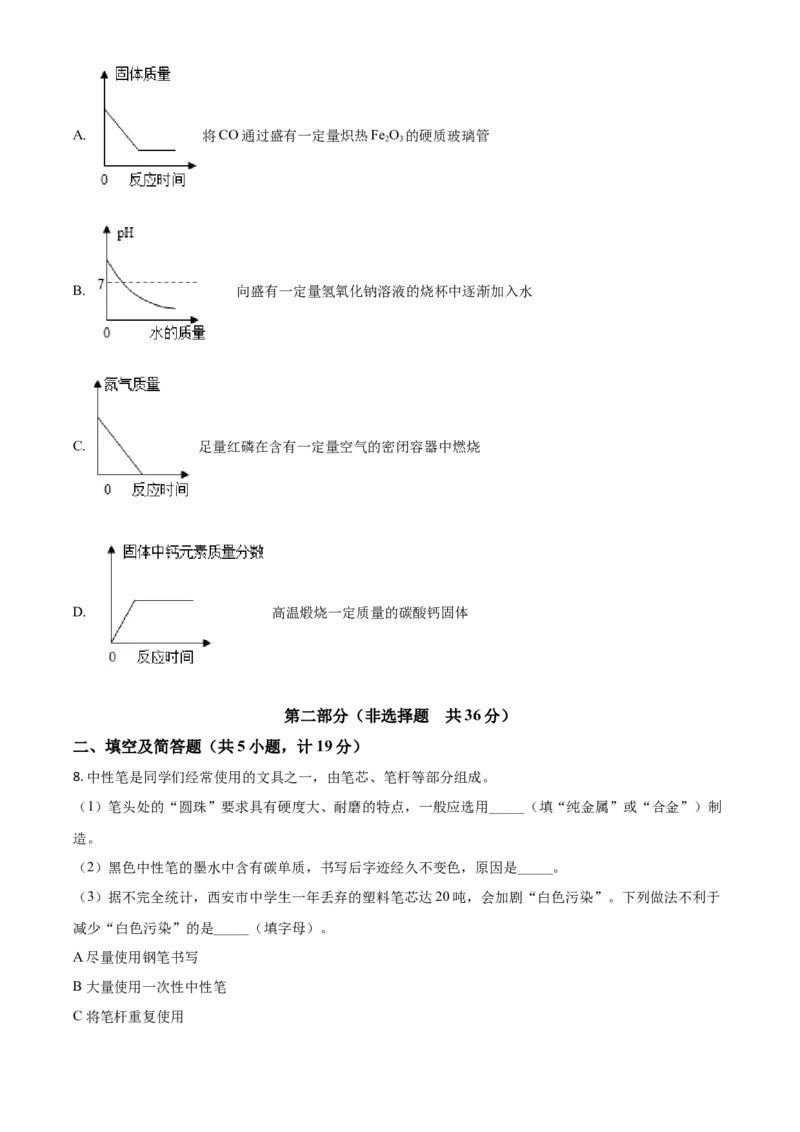
7. 下列图像能够正确反映其对应实验过程中相关量的变化关系的是( )A. 将CO通过盛有一定量炽热Fe O 的硬质玻璃管
2 3
B. 向盛有一定量氢氧化钠溶液的烧杯中逐渐加入水
C. 足量红磷在含有一定量空气的密闭容器中燃烧
D. 高温煅烧一定质量的碳酸钙固体
第二部分(非选择题 共36分)
二、填空及简答题(共5小题,计19分)
8. 中性笔是同学们经常使用的文具之一,由笔芯、笔杆等部分组成。
(1)笔头处的“圆珠”要求具有硬度大、耐磨的特点,一般应选用_____(填“纯金属”或“合金”)制
造。
(2)黑色中性笔的墨水中含有碳单质,书写后字迹经久不变色,原因是_____。
(3)据不完全统计,西安市中学生一年丢弃的塑料笔芯达20吨,会加剧“白色污染”。下列做法不利于
减少“白色污染”的是_____(填字母)。
A 尽量使用钢笔书写
B 大量使用一次性中性笔
C 将笔杆重复使用D 将废弃笔芯、笔杆回收利用
9. A、B、C、D分别为1~18号元素中的一种,且原子序数依次增大。A、B元素组成的化合物常温时为
液态,且是最常用的溶剂;C元素原子核内有11个质子;D元素的原子易得到一个电子形成稳定结构。
(1)B元素的原子最外层有_____个电子。
(2)C、D元素组成的化合物由_____构成(填“分子”“原子”或“离子”)。
(3)A、B、C三种元素组成的化合物的俗称是_____。
的
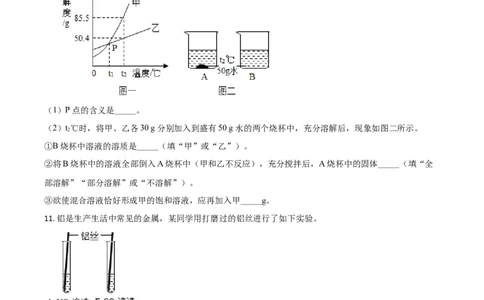
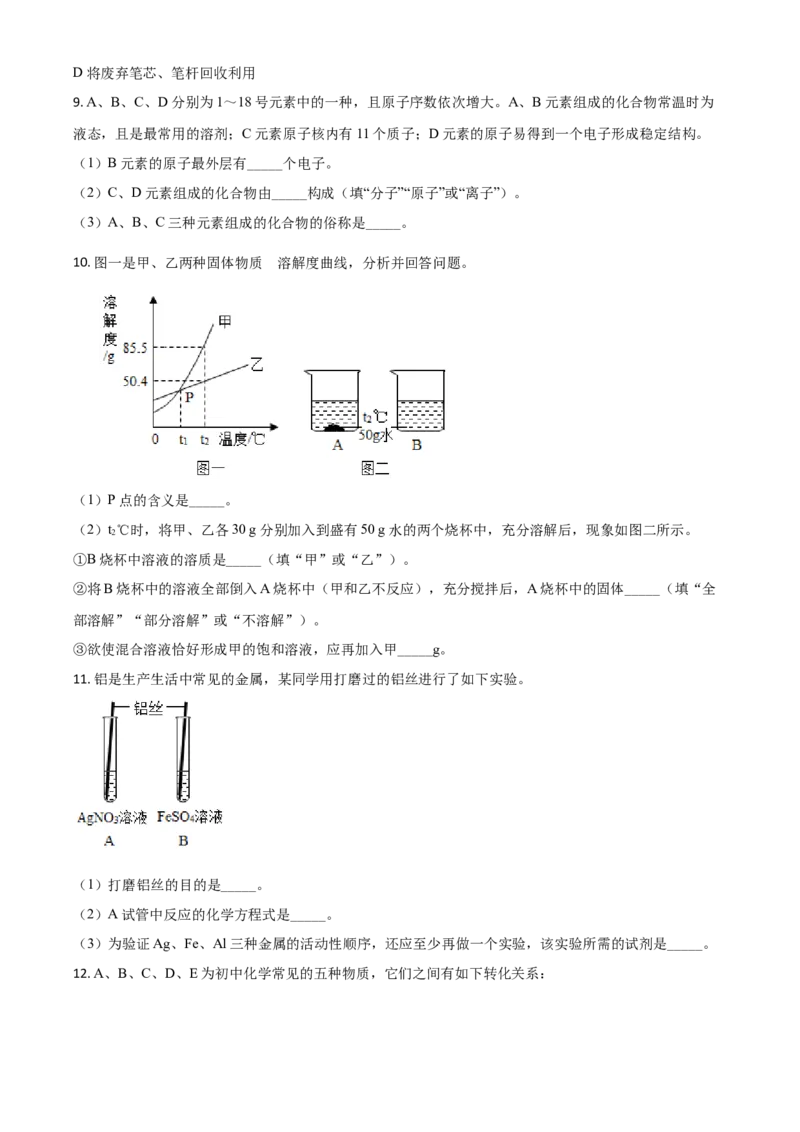
10. 图一是甲、乙两种固体物质 溶解度曲线,分析并回答问题。
(1)P点的含义是_____。
(2)t℃时,将甲、乙各30 g分别加入到盛有50 g水的两个烧杯中,充分溶解后,现象如图二所示。
2
①B烧杯中溶液的溶质是_____(填“甲”或“乙”)。
②将B烧杯中的溶液全部倒入A烧杯中(甲和乙不反应),充分搅拌后,A烧杯中的固体_____(填“全
部溶解”“部分溶解”或“不溶解”)。
③欲使混合溶液恰好形成甲的饱和溶液,应再加入甲_____g。
11. 铝是生产生活中常见的金属,某同学用打磨过的铝丝进行了如下实验。
(1)打磨铝丝的目的是_____。
(2)A试管中反应的化学方程式是_____。
(3)为验证Ag、Fe、Al三种金属的活动性顺序,还应至少再做一个实验,该实验所需的试剂是_____。
12. A、B、C、D、E为初中化学常见的五种物质,它们之间有如下转化关系:(1)若A为黑色粉末,C的溶液呈蓝色,E的溶液呈浅绿色,则B的溶液中所含的阳离子是_____(填离
子符号);反应②的基本反应类型是_____反应。
(2)若A为红色粉末,E为红褐色沉淀,反应②的化学方程式是_____。
三、实验及探究题(共2小题,计12分)
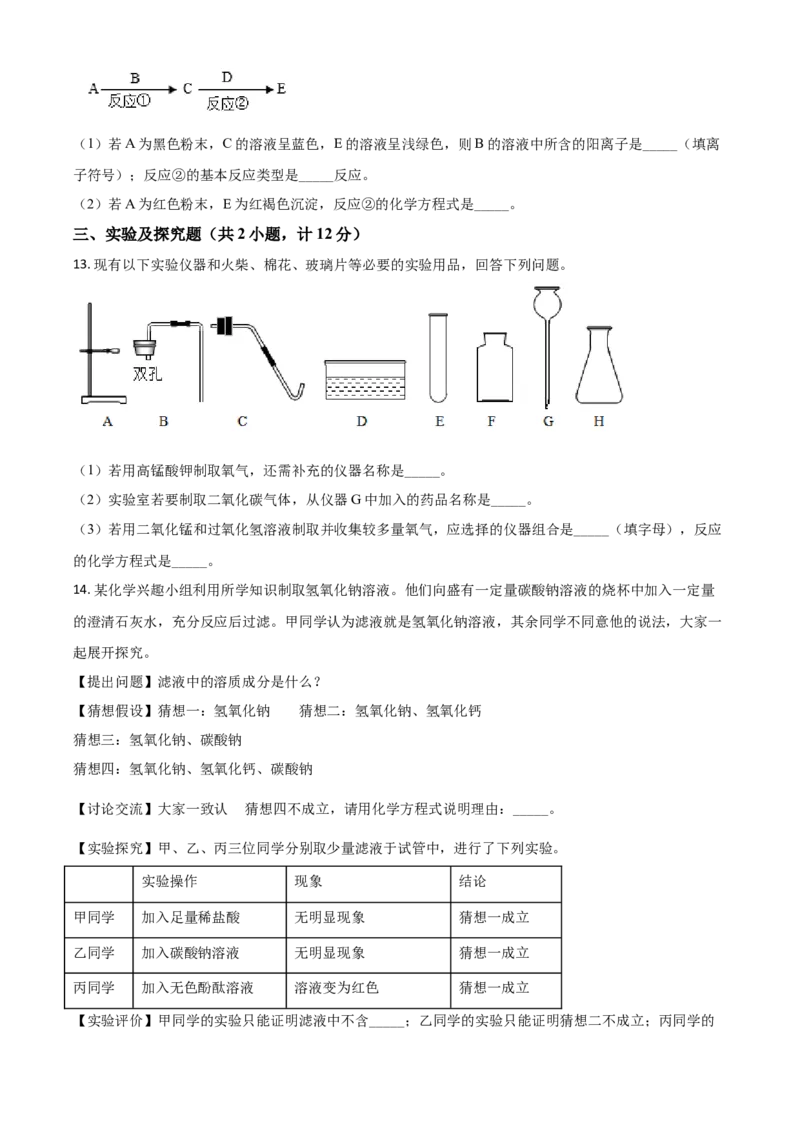
13. 现有以下实验仪器和火柴、棉花、玻璃片等必要的实验用品,回答下列问题。
(1)若用高锰酸钾制取氧气,还需补充的仪器名称是_____。
(2)实验室若要制取二氧化碳气体,从仪器G中加入的药品名称是_____。
(3)若用二氧化锰和过氧化氢溶液制取并收集较多量氧气,应选择的仪器组合是_____(填字母),反应
的化学方程式是_____。
14. 某化学兴趣小组利用所学知识制取氢氧化钠溶液。他们向盛有一定量碳酸钠溶液的烧杯中加入一定量
的澄清石灰水,充分反应后过滤。甲同学认为滤液就是氢氧化钠溶液,其余同学不同意他的说法,大家一
起展开探究。
【提出问题】滤液中的溶质成分是什么?
【猜想假设】猜想一:氢氧化钠 猜想二:氢氧化钠、氢氧化钙
猜想三:氢氧化钠、碳酸钠
猜想四:氢氧化钠、氢氧化钙、碳酸钠
为
【讨论交流】大家一致认 猜想四不成立,请用化学方程式说明理由:_____。
【实验探究】甲、乙、丙三位同学分别取少量滤液于试管中,进行了下列实验。
实验操作 现象 结论
甲同学 加入足量稀盐酸 无明显现象 猜想一成立
乙同学 加入碳酸钠溶液 无明显现象 猜想一成立
丙同学 加入无色酚酞溶液 溶液变为红色 猜想一成立
【实验评价】甲同学的实验只能证明滤液中不含_____;乙同学的实验只能证明猜想二不成立;丙同学的实验错误,原因是_____。
【得出结论】综合_____两位同学的实验和现象,可证明猜想一成立。
【反思迁移】①同学们经过讨论,提出用两种盐溶液及相应的实验操作,也可确定所得滤液中溶质的成分,
这两种盐溶液可以是_____。
②在制取某物质时,除了根据反应原理设计实验,还需要注意_____。
四、计算与分析题
15. 为测定某盐酸的溶质质量分数,同学们进行了如下实验:将该盐酸逐滴加入到盛有20 g 4%的氢氧化钠
溶液的烧杯中,用玻璃棒不断搅拌,并测定溶液的pH。当pH=7时,共用去该盐酸14.6 g。
(1)实验过程中,搅拌的目的是_____。
(2)计算该盐酸的溶质质量分数。