文档内容
实验仪器连接及现象作用描述
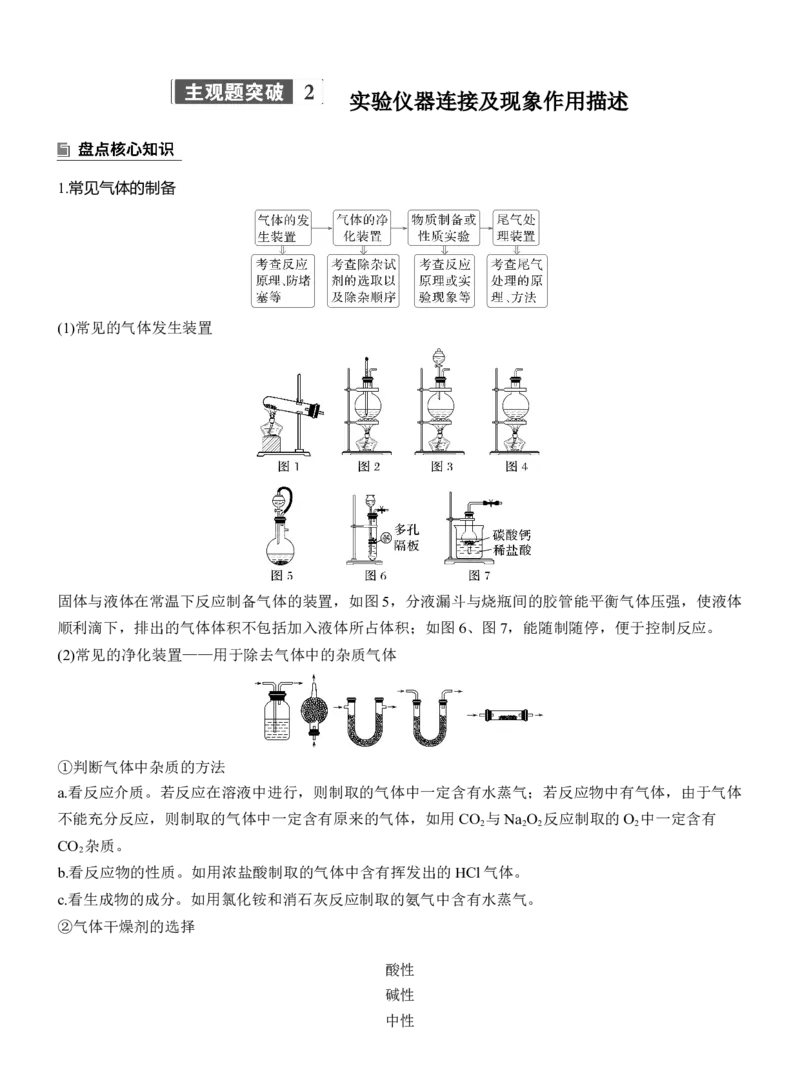
1.常见气体的制备
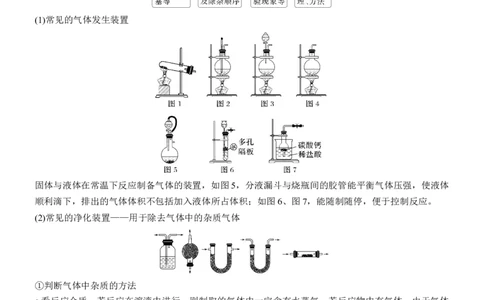
(1)常见的气体发生装置
固体与液体在常温下反应制备气体的装置,如图5,分液漏斗与烧瓶间的胶管能平衡气体压强,使液体
顺利滴下,排出的气体体积不包括加入液体所占体积;如图6、图7,能随制随停,便于控制反应。
(2)常见的净化装置——用于除去气体中的杂质气体
①判断气体中杂质的方法
a.看反应介质。若反应在溶液中进行,则制取的气体中一定含有水蒸气;若反应物中有气体,由于气体
不能充分反应,则制取的气体中一定含有原来的气体,如用CO 与Na O 反应制取的O 中一定含有
2 2 2 2
CO 杂质。
2
b.看反应物的性质。如用浓盐酸制取的气体中含有挥发出的HCl气体。
c.看生成物的成分。如用氯化铵和消石灰反应制取的氨气中含有水蒸气。
②气体干燥剂的选择
酸性
碱性
中性干燥剂
浓硫酸、P O
2 5
碱石灰、CaO
CaCl
2
气体
CO 、SO 、Cl 、NO
2 2 2 2
NH
3
H 、CO、N 、NO、CH
2 2 4
特别提醒 选取干燥剂时,除了常规的从酸碱性角度考虑外,还要考虑特殊反应,如浓硫酸不能干燥还原
性气体(H S、HI等),可用P O 干燥;中性干燥剂CaCl 不能干燥NH ,因为二者会发生络合反应(这些知
2 2 5 2 3
识可能会成为高考的设题点)。
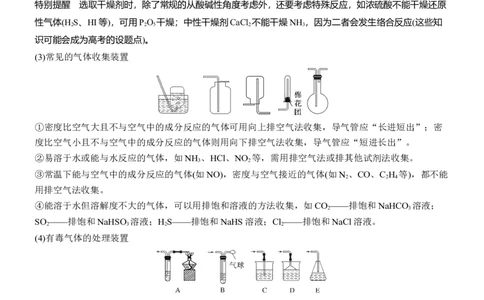
(3)常见的气体收集装置
①密度比空气大且不与空气中的成分反应的气体可用向上排空气法收集,导气管应“长进短出”;密
度比空气小且不与空气中的成分反应的气体则用向下排空气法收集,导气管应“短进长出”。
②易溶于水或能与水反应的气体,如NH 、HCl、NO 等,需用排空气法或排其他试剂法收集。
3 2
③常温下能与空气中的成分反应的气体(如NO),密度与空气接近的气体(如N 、CO、C H 等),都不能
2 2 4
用排空气法收集。
④能溶于水但溶解度不大的气体,可以用排饱和溶液的方法收集,如CO ——排饱和NaHCO 溶液;
2 3
SO ——排饱和NaHSO 溶液;H S——排饱和NaHS溶液;Cl ——排饱和NaCl溶液。
2 3 2 2
(4)有毒气体的处理装置
①装置C适用于溶解度较小的有毒气体,如Cl 、NO 、H S等。
2 2 2
②装置D、E适用于溶解度较大的气体,如HCl、NH 等。
3
③装置A适用于某些可燃性气体,如CO等。
④装置B采用收集法处理尾气,适用于NO、CO等。
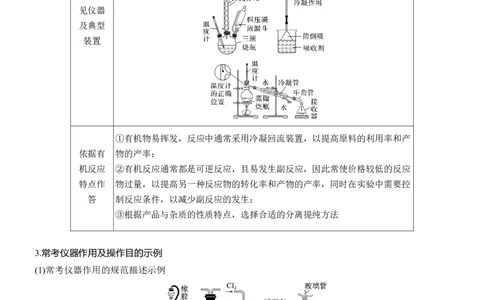
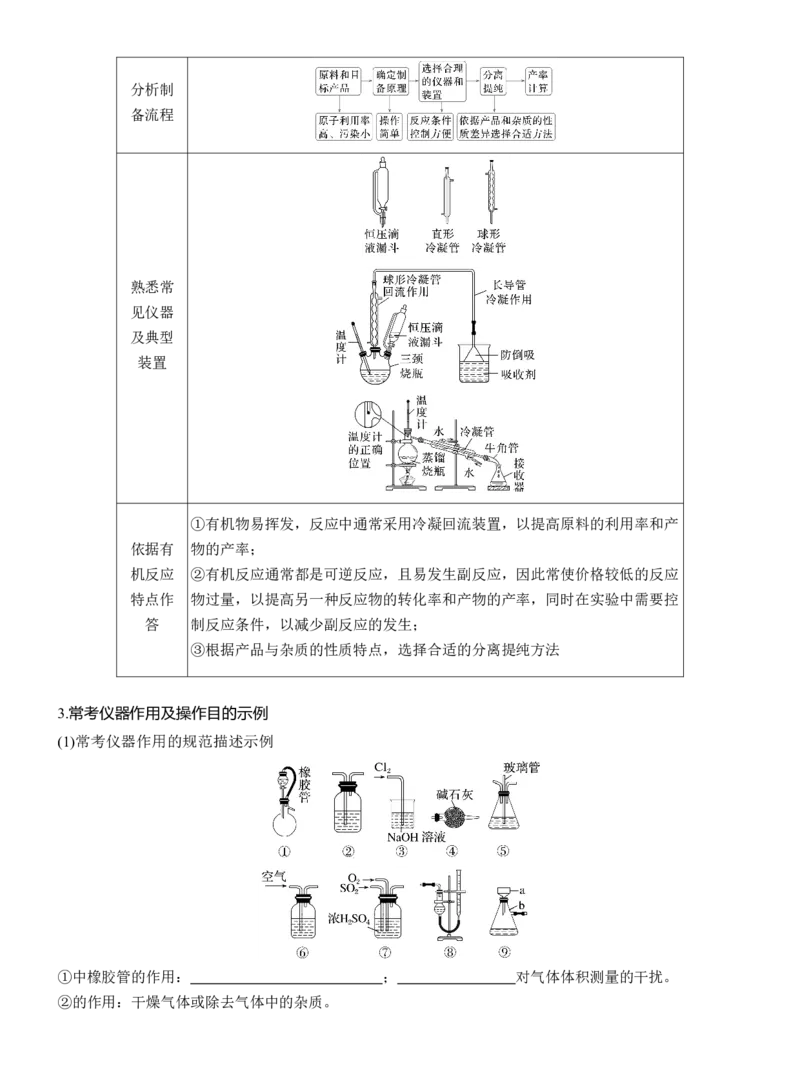
2.有机物的制备
有机物的制备实验装置的选择分析制
备流程
熟悉常
见仪器
及典型
装置
①有机物易挥发,反应中通常采用冷凝回流装置,以提高原料的利用率和产
依据有 物的产率;
机反应 ②有机反应通常都是可逆反应,且易发生副反应,因此常使价格较低的反应
特点作 物过量,以提高另一种反应物的转化率和产物的产率,同时在实验中需要控
答 制反应条件,以减少副反应的发生;
③根据产品与杂质的性质特点,选择合适的分离提纯方法
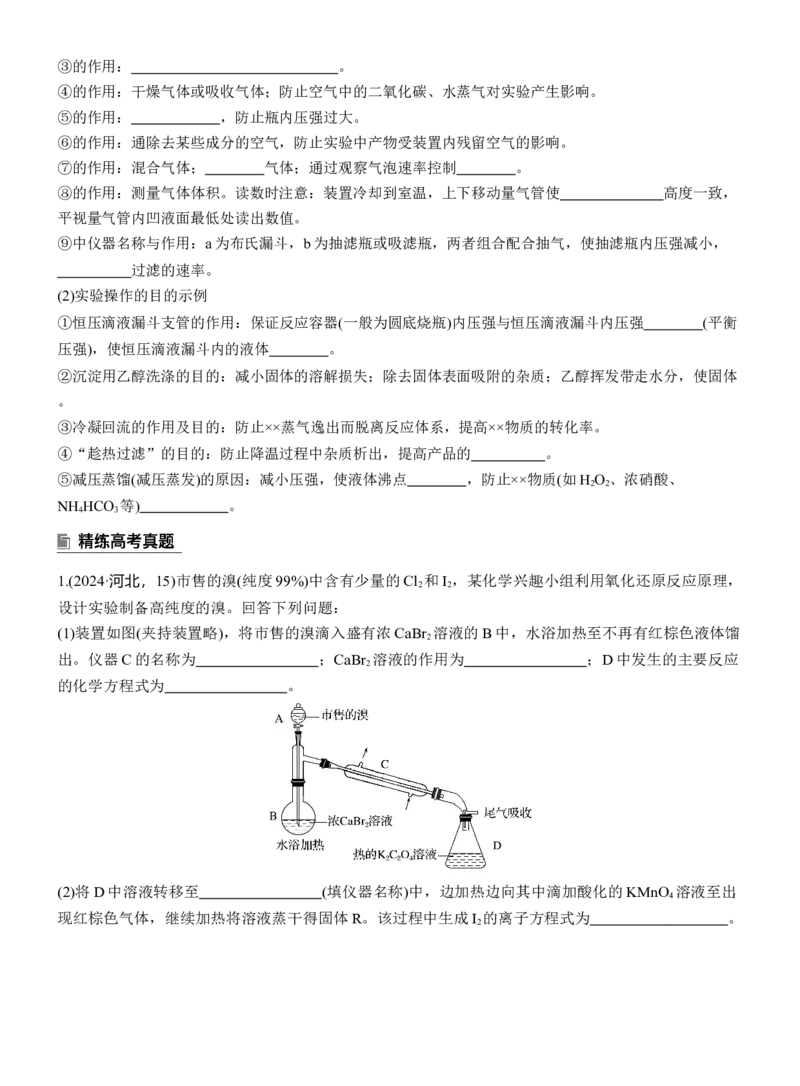
3.常考仪器作用及操作目的示例
(1)常考仪器作用的规范描述示例
①中橡胶管的作用: ; 对气体体积测量的干扰。
②的作用:干燥气体或除去气体中的杂质。③的作用: 。
④的作用:干燥气体或吸收气体;防止空气中的二氧化碳、水蒸气对实验产生影响。
⑤的作用: ,防止瓶内压强过大。
⑥的作用:通除去某些成分的空气,防止实验中产物受装置内残留空气的影响。
⑦的作用:混合气体; 气体;通过观察气泡速率控制 。
⑧的作用:测量气体体积。读数时注意:装置冷却到室温,上下移动量气管使 高度一致,
平视量气管内凹液面最低处读出数值。
⑨中仪器名称与作用:a为布氏漏斗,b为抽滤瓶或吸滤瓶,两者组合配合抽气,使抽滤瓶内压强减小,
过滤的速率。
(2)实验操作的目的示例
①恒压滴液漏斗支管的作用:保证反应容器(一般为圆底烧瓶)内压强与恒压滴液漏斗内压强 (平衡
压强),使恒压滴液漏斗内的液体 。
②沉淀用乙醇洗涤的目的:减小固体的溶解损失;除去固体表面吸附的杂质;乙醇挥发带走水分,使固体
。
③冷凝回流的作用及目的:防止××蒸气逸出而脱离反应体系,提高××物质的转化率。
④“趁热过滤”的目的:防止降温过程中杂质析出,提高产品的 。
⑤减压蒸馏(减压蒸发)的原因:减小压强,使液体沸点 ,防止××物质(如H O 、浓硝酸、
2 2
NH HCO 等) 。
4 3
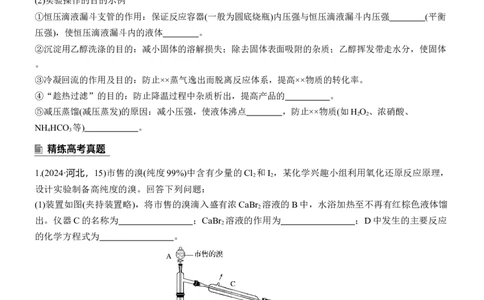
1.(2024·河北,15)市售的溴(纯度99%)中含有少量的Cl 和I ,某化学兴趣小组利用氧化还原反应原理,
2 2
设计实验制备高纯度的溴。回答下列问题:
(1)装置如图(夹持装置略),将市售的溴滴入盛有浓CaBr 溶液的B中,水浴加热至不再有红棕色液体馏
2
出。仪器C的名称为 ;CaBr 溶液的作用为 ;D中发生的主要反应
2
的化学方程式为 。
(2)将D中溶液转移至 (填仪器名称)中,边加热边向其中滴加酸化的KMnO 溶液至出
4
现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成I 的离子方程式为 。
2(3)利用图示相同装置,将R和K Cr O 固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴
2 2 7
加适量浓H SO ,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏
2 4
水的作用为 和 。
3
(4)为保证溴的纯度,步骤(3)中K Cr O 固体的用量按理论所需量的 计算,若固体R质量为m克(以
2 2 7 4
KBr计),则需称取 g K Cr O (M=294 g·mol-1)(用含m的代数式表示)。
2 2 7
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内
壁,转移溶液时用 ,滤液沿烧杯壁流下。
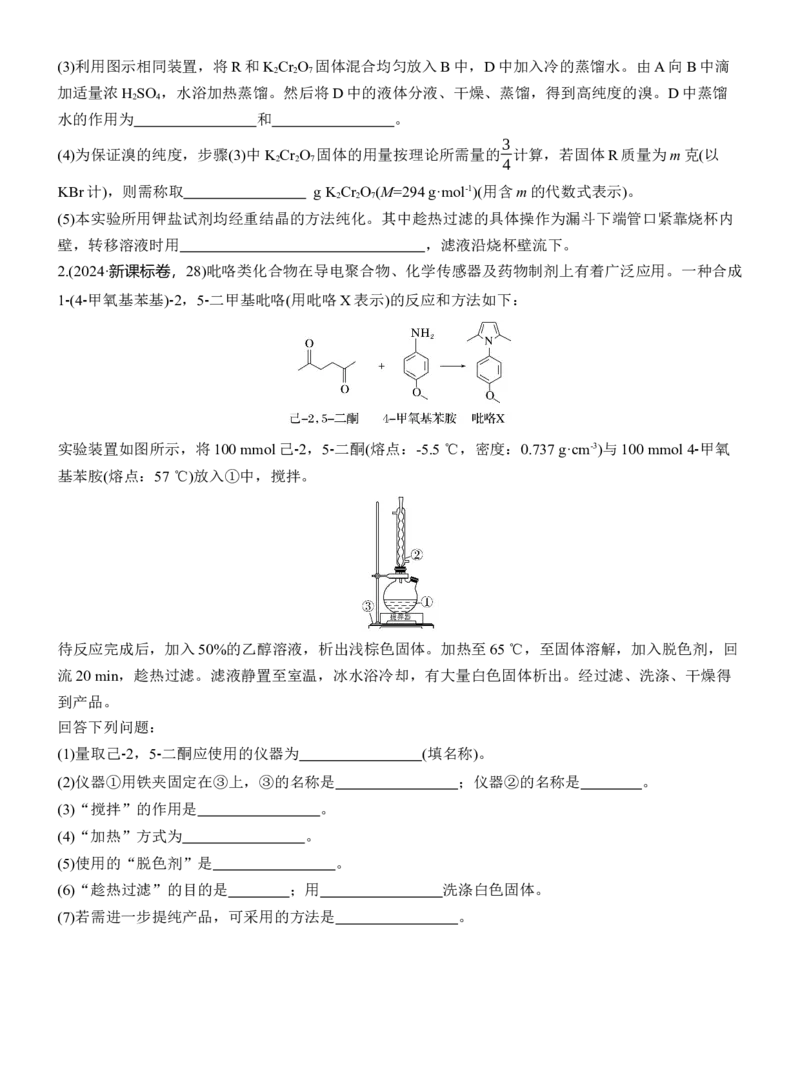
2.(2024·新课标卷,28)吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用。一种合成
1⁃(4⁃ 甲氧基苯基)⁃2,5⁃ 二甲基吡咯(用吡咯X表示)的反应和方法如下:
实验装置如图所示,将100 mmol己 ⁃2,5⁃ 二酮(熔点:-5.5 ℃,密度:0.737 g·cm-3)与100 mmol 4⁃ 甲氧
基苯胺(熔点:57 ℃)放入①中,搅拌。
待反应完成后,加入50%的乙醇溶液,析出浅棕色固体。加热至65 ℃,至固体溶解,加入脱色剂,回
流20 min,趁热过滤。滤液静置至室温,冰水浴冷却,有大量白色固体析出。经过滤、洗涤、干燥得
到产品。
回答下列问题:
(1)量取己 ⁃2,5⁃ 二酮应使用的仪器为 (填名称)。
(2)仪器①用铁夹固定在③上,③的名称是 ;仪器②的名称是 。
(3)“搅拌”的作用是 。
(4)“加热”方式为 。
(5)使用的“脱色剂”是 。
(6)“趁热过滤”的目的是 ;用 洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是 。答案精析
盘点核心知识
3.(1)①平衡压强,使液体能顺利滴下 减小液体体积
③吸收尾气,防止污染空气 ⑤安全瓶 ⑦干燥 流量
⑧左右两液面 ⑨加快 (2)①相等 顺利滴下
②快速干燥 ④纯度 ⑤降低 受热分解
精练高考真题
1.(1)直形冷凝管 除去市售的溴中少量的Cl
2
Br +K C O 2KBr+2CO ↑ (2)蒸发皿
2 2 2 4 2
2Mn
O-
+10I-+16H+ 2Mn2++5I +8H O
4 2 2
(3)液封 降低温度 (4)0.31m
(5)玻璃棒引流,玻璃棒下端靠在三层滤纸处
解析 (1)仪器C为直形冷凝管,用于冷凝蒸气;市售的溴(纯度99%)中含有少量的Cl 和I ,Cl 可与CaBr
2 2 2 2
发生氧化还原反应而除去;水浴加热时,Br 、I 蒸发进入装置D中,分别与K C O 发生氧化还原反应,
2 2 2 2 4
由于I 少量,故主要反应的化学方程式为Br +K C O 2KBr+2CO ↑。(2)将D中溶液转移至蒸发皿中,
2 2 2 2 4 2
边加热边向其中滴加酸化的KMnO 溶液至出现红棕色气体(Br ),因为I-的还原性强于Br-,说明KMnO 已
4 2 4
将KI全部氧化,发生反应的离子方程式为2Mn
O-
4
+10I-+16H+ 2Mn2++5I
2
+8H
2
O;KBr几乎未被氧化,继
续加热将溶液蒸干所得固体R的主要成分为KBr。(3)密度:Br >H O,D中冷的蒸馏水起到液封的作用,
2 2
m
同时冷的蒸馏水温度较低,均可减少溴的挥发。(4)m g KBr固体的物质的量为 mol,根据得失电子守
119
1 m
恒可得关系式6KBr~6e-~K Cr O ,则理论上需要K Cr O 的物质的量为 × mol,实际所需称取K Cr O
2 2 7 2 2 7 6 119 2 2 7
1 m 3
的质量为 × mol× ×294 g·mol-1≈0.31m g。
6 119 4
2.(1)酸式滴定管 (2)铁架台 球形冷凝管 (3)使固液充分接触,加快反应速率 (4)水浴加热 (5)活性炭
(6)防止产品结晶损失,提高产率 50%的乙醇溶液 (7)重结晶
解析 在制备吡咯X的过程中,利用球形冷凝管进行冷凝回流提高原料利用率,通过搅拌来提高反应速率,
反应完成后,加入50%的乙醇溶液,析出浅棕色固体(即含杂质的产品),加热至65 ℃,至固体溶解,加入
脱色剂(脱色剂为不溶于水和乙醇等溶剂的固体,如活性炭),回流20 min,趁热过滤,使产品尽可能多地
进入滤液,滤液静置至室温,冰水浴冷却,有大量白色固体析出,经过滤、洗涤、干燥得到产品。
(1)己⁃2,5⁃二酮的熔点:-5.5 ℃,可知常温下该物质为液体,摩尔质量为114 g·mol-1,根据题中所给数据
100×10-3mol×114 g·mol-1
可知,所需己⁃2,5⁃二酮的体积为 ≈15.47 cm3=15.47 mL,又因为酮类对橡
0.737 g·cm-3胶有腐蚀性,所以选用酸式滴定管量取己⁃2,5⁃二酮。(3)己⁃2,5⁃二酮常温下为液体,4⁃甲氧基苯胺的熔
点为57 ℃,常温下为固体,搅拌可使固液反应物充分接触,加快反应速率。(4)由题给信息“加热至65
℃”可知,应用水浴加热,这样便于控制温度,且受热更均匀。(5)“脱色剂”的作用是吸附反应过程中产
生的有色物质,结合题中信息,加入脱色剂后回流,趁热过滤,保留滤液,即脱色剂为不溶于水和乙醇等
溶剂的固体,所以可以选用活性炭作脱色剂。(6)由“加入50%的乙醇溶液,析出浅棕色固体”可知,常温
下产品不溶于50%的乙醇溶液;“加热至65 ℃,至固体溶解”,所以需趁热过滤,使产品尽可能多地进
入滤液,防止产品结晶损失,提高产率。为减少溶解损失,洗涤时可用50%的乙醇溶液。(7)由产品的分离
提纯过程可知,若需进一步提纯,可采用的方法为重结晶。