文档内容
实验仪器连接及现象作用描述
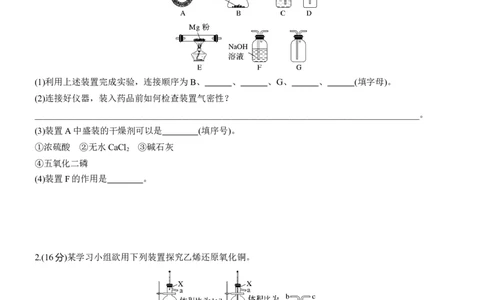
1.(5分)Mg能在NO 中燃烧,产物为Mg N 、MgO和N ,某科学小组通过实验验证部分产物并探究产物的
2 3 2 2
比例关系。用如下装置进行实验(夹持装置省略)。
资料信息:Mg N +6H O===3Mg(OH) +2NH ↑
3 2 2 2 3
(1)利用上述装置完成实验,连接顺序为B、 、 、G、 、 (填字母)。
(2)连接好仪器,装入药品前如何检查装置气密性?
______________________________________________________________________________________。
(3)装置A中盛装的干燥剂可以是 (填序号)。
①浓硫酸 ②无水CaCl ③碱石灰
2
④五氧化二磷
(4)装置F的作用是 。
2.(16分)某学习小组欲用下列装置探究乙烯还原氧化铜。
已知:ⅰ.乙醇在170 ℃、浓硫酸的作用下能产生乙烯,化学方程式为CH CH OH
3 2
CH ==CH ↑+H O;
2 2 2ⅱ.加热条件下,少量乙醇被浓硫酸炭化。
(1)仪器X的名称为 。
(2)制备乙烯时应选用装置 (填“A”或“B”);反应开始后,仪器X中观察到的现象为 。
(3)实验时装置的连接顺序是a→ →尾气处理(按气流方向,用小写字母表示);其中NaOH溶液的
作用为 。
(4)实验时,装置F应 (填“先加热”或“后加热”),原因为 。
(5)能证明乙烯还原氧化铜的实验现象为 。
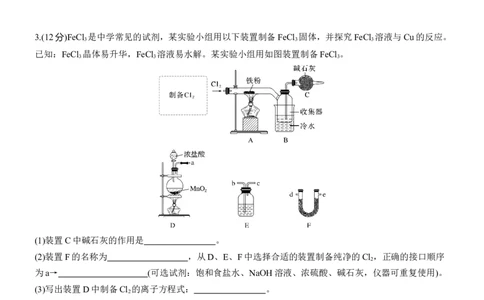
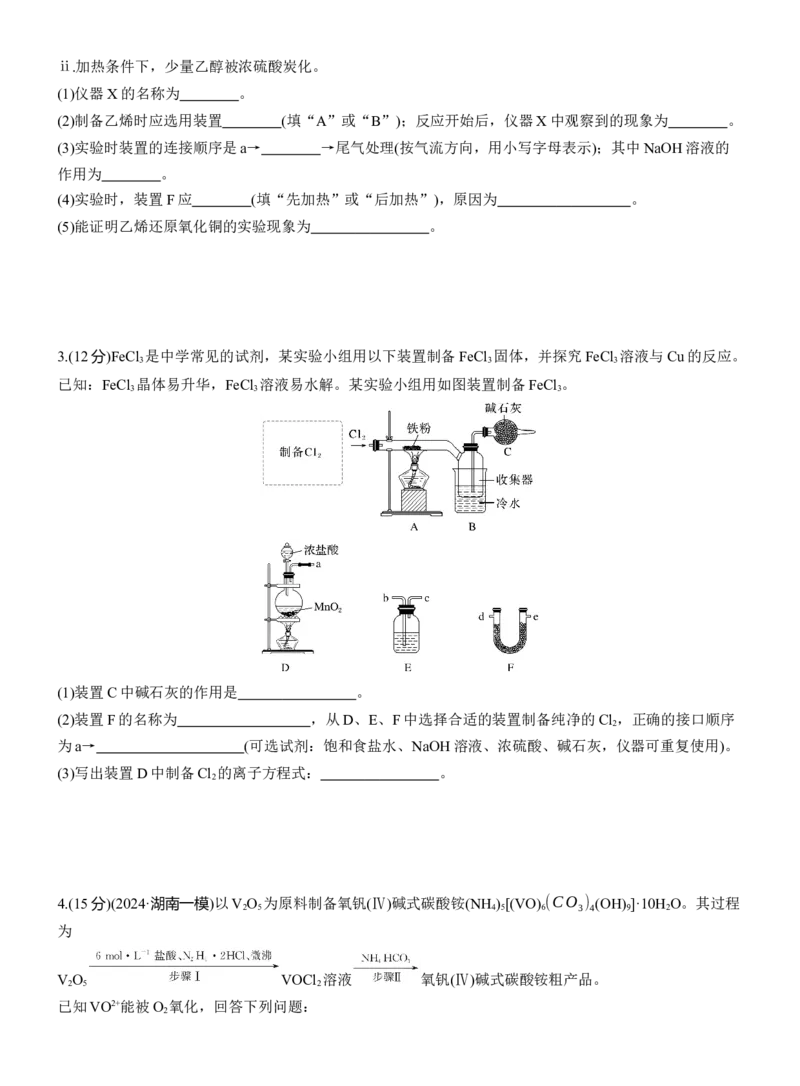
3.(12分)FeCl 是中学常见的试剂,某实验小组用以下装置制备FeCl 固体,并探究FeCl 溶液与Cu的反应。
3 3 3
已知:FeCl 晶体易升华,FeCl 溶液易水解。某实验小组用如图装置制备FeCl 。
3 3 3
(1)装置C中碱石灰的作用是 。
(2)装置F的名称为 ,从D、E、F中选择合适的装置制备纯净的Cl ,正确的接口顺序
2
为a→ (可选试剂:饱和食盐水、NaOH溶液、浓硫酸、碱石灰,仪器可重复使用)。
(3)写出装置D中制备Cl 的离子方程式: 。
2
4.(15分)(2024·湖南一模)以V O 为原料制备氧钒(Ⅳ)碱式碳酸铵(NH ) [(VO) (CO ) (OH) ]·10H O。其过程
2 5 4 5 6 3 4 9 2
为
V O VOCl 溶液 氧钒(Ⅳ)碱式碳酸铵粗产品。
2 5 2
已知VO2+能被O 氧化,回答下列问题:
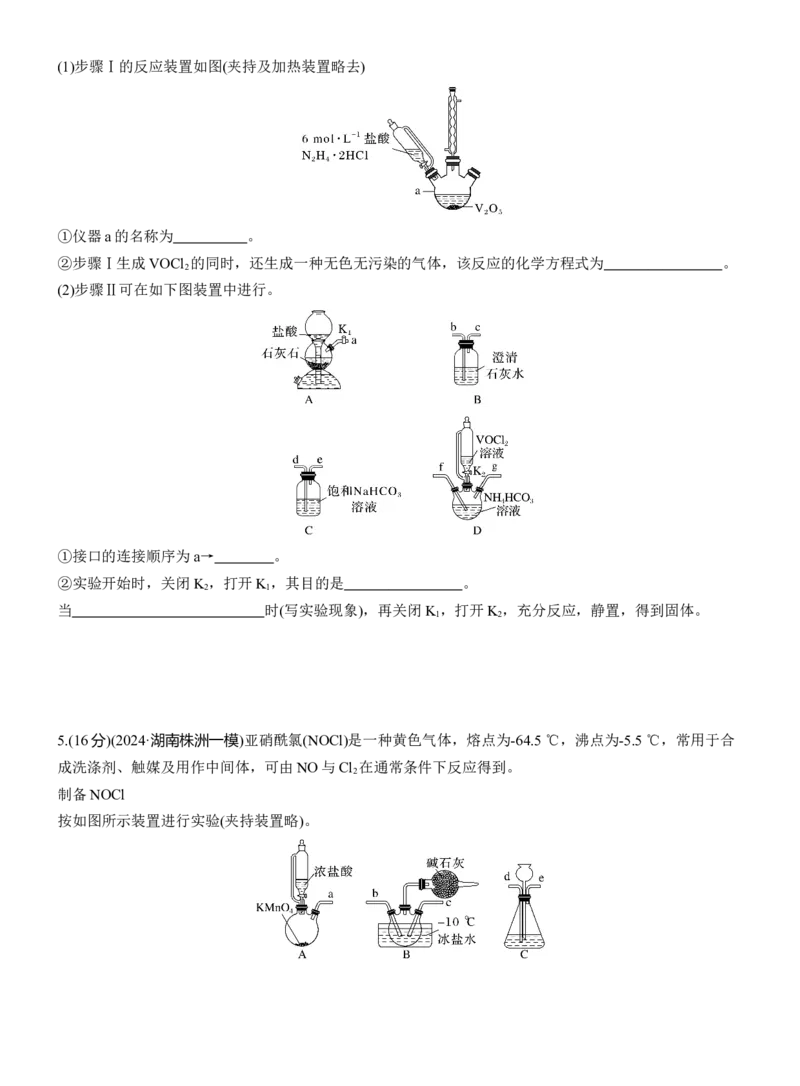
2(1)步骤Ⅰ的反应装置如图(夹持及加热装置略去)
①仪器a的名称为 。
②步骤Ⅰ生成VOCl 的同时,还生成一种无色无污染的气体,该反应的化学方程式为 。
2
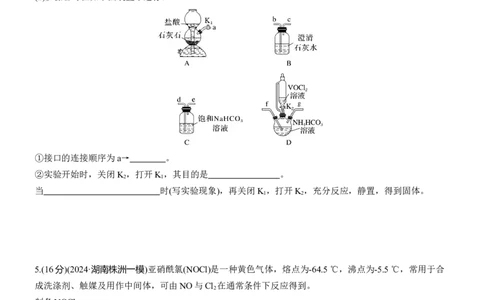
(2)步骤Ⅱ可在如下图装置中进行。
①接口的连接顺序为a→ 。
②实验开始时,关闭K ,打开K ,其目的是 。
2 1
当 时(写实验现象),再关闭K ,打开K ,充分反应,静置,得到固体。
1 2
5.(16分)(2024·湖南株洲一模)亚硝酰氯(NOCl)是一种黄色气体,熔点为-64.5 ℃,沸点为-5.5 ℃,常用于合
成洗涤剂、触媒及用作中间体,可由NO与Cl 在通常条件下反应得到。
2
制备NOCl
按如图所示装置进行实验(夹持装置略)。已知:2NOCl+H O===2H++2Cl-+NO↑+NO ↑。
2 2
(1)装置B中盛放碱石灰的仪器名称为 ;装置A中发生反应的离子方程式为
。
(2)仪器连接的顺序为a→ →b,c← ←h(仪器可重复使用);装置C中所盛试剂的名称是
;若装置B中压强过大,可以观察到的现象是 。
(3)实验时,待装置B中三颈烧瓶内充满黄绿色气体时,再将NO通入三颈烧瓶中,这样做的目的是
。
(4)该制备装置中存在的一处缺陷是 。
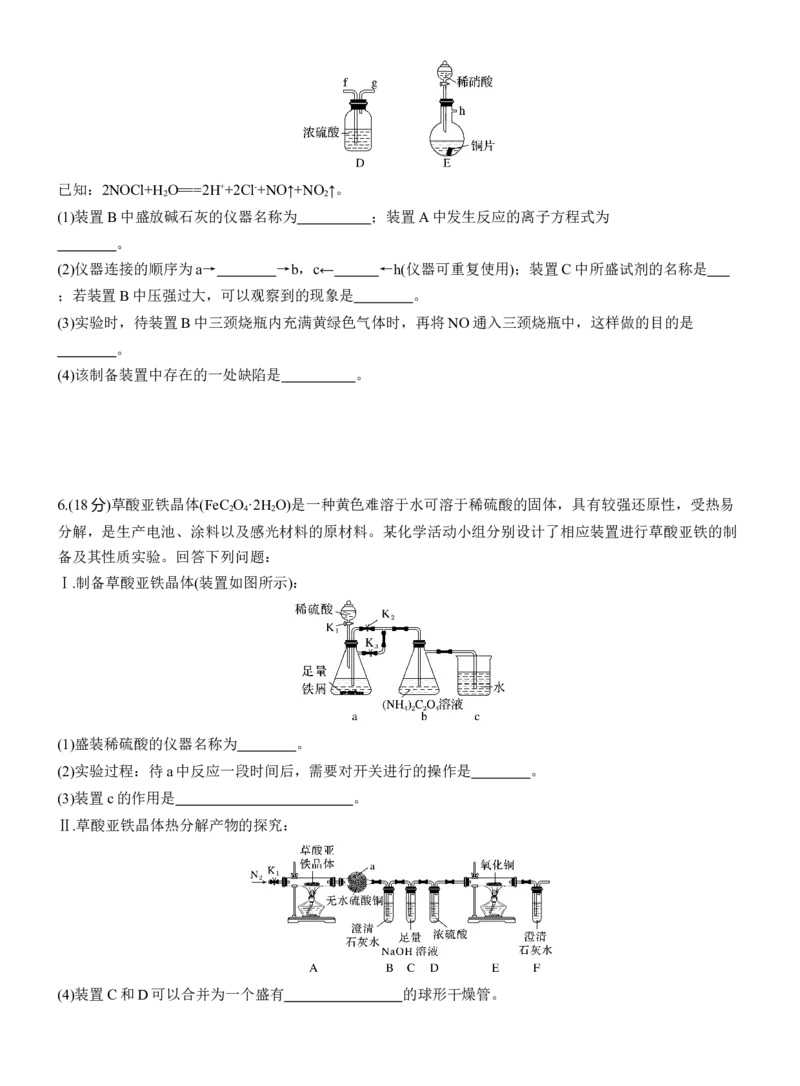
6.(18分)草酸亚铁晶体(FeC O ·2H O)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易
2 4 2
分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制
备及其性质实验。回答下列问题:
Ⅰ.制备草酸亚铁晶体(装置如图所示):
(1)盛装稀硫酸的仪器名称为 。
(2)实验过程:待a中反应一段时间后,需要对开关进行的操作是 。
(3)装置c的作用是 。
Ⅱ.草酸亚铁晶体热分解产物的探究:
(4)装置C和D可以合并为一个盛有 的球形干燥管。(5)从绿色化学考虑,该套装置存在的明显缺陷是 。
(6)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸铜变为蓝色,A中残留
FeO,则A处反应管中发生反应的化学方程式为 。
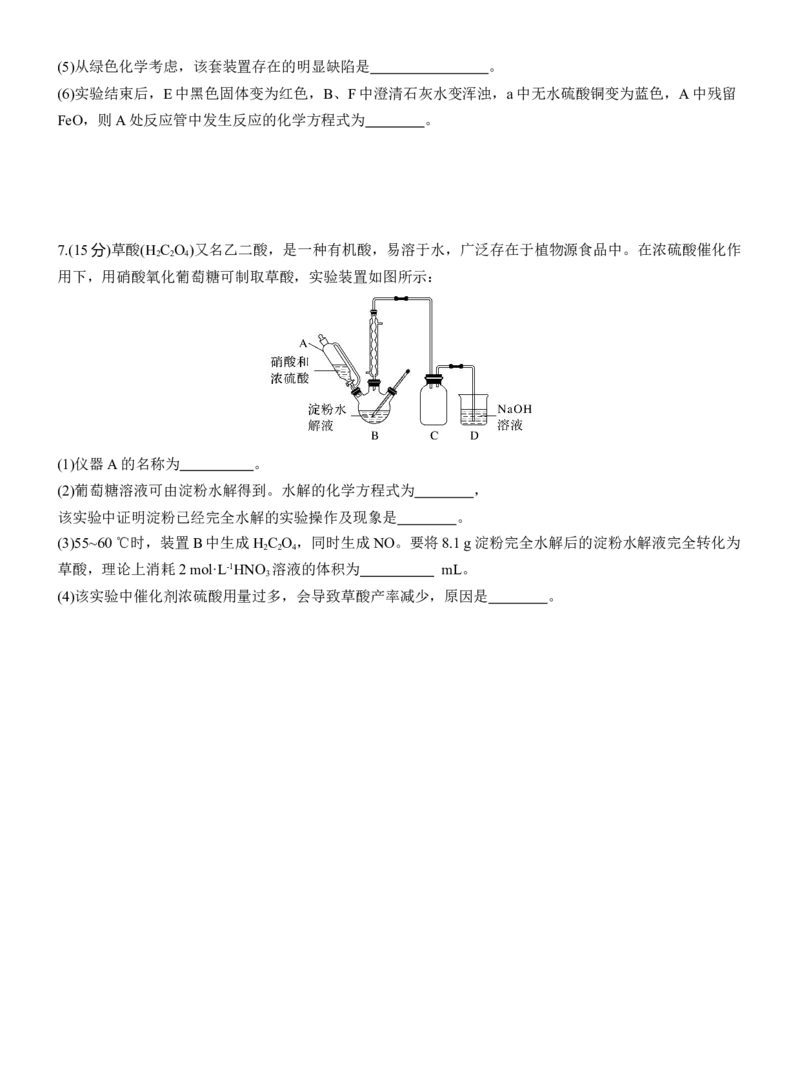
7.(15分)草酸(H C O )又名乙二酸,是一种有机酸,易溶于水,广泛存在于植物源食品中。在浓硫酸催化作
2 2 4
用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示:
(1)仪器A的名称为 。
(2)葡萄糖溶液可由淀粉水解得到。水解的化学方程式为 ,
该实验中证明淀粉已经完全水解的实验操作及现象是 。
(3)55~60 ℃时,装置B中生成H C O ,同时生成NO。要将8.1 g淀粉完全水解后的淀粉水解液完全转化为
2 2 4
草酸,理论上消耗2 mol·L-1HNO 溶液的体积为 mL。
3
(4)该实验中催化剂浓硫酸用量过多,会导致草酸产率减少,原因是 。答案精析
1.(1)A E F C(CD) (2)关闭分液漏斗活塞,将D中导气管末端插入水中,对B中锥形瓶微热,若导管
口有气泡冒出,停止加热,导气管中形成一段水柱,则装置气密性良好 (3)②④ (4)吸收过量的二氧化氮
气体
2.(1)蒸馏烧瓶 (2)B 溶液变黑,有气泡产生 (3)e→d→f→g→h→i(或i→h)→b→c 吸收乙烯中的CO 和
2
SO (4)后加热 应先用乙烯排尽装置中的空气,避免乙烯与空气混合加热爆炸 (5)装置F中黑色粉末变
2
为红色,装置C中溶液变浑浊
解析 本实验探究乙烯还原氧化铜,实验原理是C H +6CuO 6Cu+2CO +2H O,根据已知信息,制备乙
2 4 2 2
烯时反应温度应在170 ℃,温度计需要插入到溶液中,即用装置B制备乙烯,加热条件下,少量乙醇被浓
硫酸炭化,碳在加热条件下与浓硫酸反应生成CO 、SO ,需要除去,装置B连接装置D,然后装置E干
2 2
燥乙烯,再连接装置F,最后连接装置C,据此分析解答。
3.(1)吸收多余的Cl ,用于尾气处理,同时可以防止空气中的水蒸气进入收集器中,防止FeCl 水解变质
2 3
(2)U形干燥管 b→c→b→c (3)MnO +4H++2Cl- Mn2++Cl ↑+2H O
2 2 2
解析 由题干实验装置图可知,装置D为实验室制备Cl 的发生装置,原理为MnO +4HCl(浓)
2 2
MnCl +Cl ↑+2H O,装置E为盛有饱和食盐水的洗气瓶,用于除去Cl 中的HCl,装置E还可盛浓硫酸,
2 2 2 2
用于干燥Cl ,然后将干燥的Cl 通入装置A中,装置A为制备FeCl 的发生装置,装置B中的收集器用于
2 2 3
收集FeCl ,装置C中的碱石灰用于吸收多余的Cl ,用于尾气处理,同时可以防止空气中的水蒸气进入收
3 2
集器中,防止FeCl 水解变质,据此分析解题。
3
4.(1)①三颈烧瓶 ②2V O +N H ·2HCl+6HCl 4VOCl +N ↑+6H O (2)①d→e→f→g→b→c ②排尽装
2 5 2 4 2 2 2
置中的空气 装置B中澄清石灰水变浑浊
解析 (2)①首先通过装置A制取CO ,利用装置C除去CO 中的HCl后,将CO 通入装置D中,排尽装置
2 2 2
中的空气以防止产物被氧化,待装置B中澄清石灰水变浑浊,确保空气被排尽后,再打开D中K ,开始实
2
验,接口的连接顺序为a→d→e→f→g→b→c。
5.(1)球形干燥管
2MnO-
+10Cl-+16H+===2Mn2++5Cl ↑+8H O (2)d→e→f→g g←f 饱和NaCl溶液
4 2 2
装置C中长颈漏斗液面上升 (3)排尽装置内的空气,防止NO被氧化 (4)缺少尾气处理装置
解析 (2)A中得到的Cl 中含有HCl,用装置C除去Cl 中的HCl且起安全瓶的作用,C中溶液为饱和NaCl
2 2
溶液,根据已知,NOCl能和水反应,所以B中发生反应的氯气必须是干燥的,所以装置D的作用是干燥
氯气;装置E用于生成NO,且需要干燥,所以连接顺序为a→d→e→f→g→b,c←g←f←h,若装置B中
压强过大,可以观察到的现象为装置C中长颈漏斗液面上升。
6.(1)分液漏斗 (2)打开K ,关闭K 、K (3)隔离空气,防止生成的草酸亚铁晶体被空气中的氧气氧化
2 3 1
(4)碱石灰 (5)缺少处理CO尾气的装置 (6)FeC O ·2H O FeO+CO ↑+CO↑+2H O
2 4 2 2 2解析 Ⅰ.由实验装置图可知,制备草酸亚铁晶体的操作为组装好装置后,检查装置的气密性,添加试剂后,
先关闭K ,打开K 、K ,将一定量稀硫酸加入锥形瓶中,利用反应生成的氢气排尽装置中的空气,一段
2 3 1
时间后,打开K ,关闭K 、K ,再利用反应生成的氢气将装置a中的硫酸亚铁溶液压入装置b中,使硫酸
2 3 1
亚铁溶液与草酸铵溶液混合反应制得草酸亚铁,装置c中盛有的水用于隔离空气,防止生成的草酸亚铁晶
体被空气中的氧气氧化,装置b中制得的草酸亚铁溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到草
酸亚铁晶体。
Ⅱ.由实验装置图可知,装置A为草酸亚铁晶体受热分解装置,盛有无水硫酸铜的干燥管用于检验生成的水
蒸气,装置B中盛有的澄清石灰水用于检验生成的二氧化碳,装置C中盛有的氢氧化钠溶液用于吸收二氧
化碳,防止二氧化碳干扰一氧化碳的检验,装置D中盛有的浓硫酸用于干燥气体,装置E和装置F用于检
验生成的一氧化碳,该装置的设计缺陷是缺少处理一氧化碳尾气的装置。
7.(1)恒压滴液漏斗 (2)(C H O ) (淀粉)+nH O nC H O (葡萄糖) 取水解液少许于试管中,向试管中加
6 10 5 n 2 6 12 6
入碘水,溶液不变蓝色 (3)150 (4)浓硫酸具有强氧化性,会将部分有机物氧化成CO ;浓硫酸具有脱水
2
性,会使部分有机物脱水炭化