文档内容
绝密*启用并使用完毕前 试卷类型:A
2013 年山东省日照市初中学业考试
化 学 试 题
本试卷分第I卷和第II卷两部分,共8页,满分100分,考试用时90分钟。答卷前,考生
务必用0.5毫米黑色签字笔将自己的姓名、座号、准考证号填写在答题卡规定的位置上。考试
结束后,将本试卷和答题卡一并交回。
注意事项:
1.第I卷每小题选出答案后,用2B铅笔把答题卡上对应题号的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。不涂在答题卡上,答在试卷上无效。
2.第II卷必须用0.5毫米黑色签字笔作答,答案须写在答题卡各题目指定的区域内,在
试卷上答题不得分;如需改动,先划掉原来的答案,然后再写上新的答案。
相对原子质量:H 1 C 12 N14 O 16 S 32 Cl 35.5 Cu 64 Zn 65
第I卷(选择题,共44分)
[来源:Zxxk.Com]
一、选择题(本题包括22小题,每小题2分,共44分。每小题只有一个选项符合题意)
1.科学家成功地利用精密仪器从石墨中分离出单层的石墨片,这是目前世界上人工制得的
最薄的材料,如图所示。下列有关石墨片说法错误的是
A.石墨片是一种单质
B.石墨片与C 是同种物质,具有导电性
60
C.在一定条件下,石墨片可还原氧化铜
D.石墨片在氧气中完全燃烧的产物是CO
2
2.“酸雨”的形成主要是由于
A.工业上大量燃烧含硫燃料 B.大气中二氧化碳的含量增多
C.汽车排出大量尾气 D.森林遭到乱砍滥伐,破坏了生态平衡
3.化学与生活密切相关,下列说法不正确的是
A.蔬菜、水果中富含维生素 B.糖类和油脂都能为人体提供能量
C.人体缺锌易患贫血病 D.人体缺钙会发生骨质疏松,容易骨折
4.净化水的方法有:①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌。要将混有泥沙的天然
水净化成生活用的自来水,应选用的方法和顺序为
A.①②③④ B.②④①③ C.①③④ D.②①④
5.镁是一种化学性质活泼的金属,在空气中常温下就能被缓慢氧化。下列有关镁条燃烧实验
的说法不正确的是
A.实验前,应先用砂纸打磨镁条至表面出现银白色
B.实验时,应使用石棉网
C.实验时,应用坩埚钳夹持镁条,在酒精灯上点燃
D.镁条在空气中缓慢燃烧,发出耀眼的黄光,有大量蓝紫烟生成6.《中华人民共和国食品安全法》于2009年6月1日起实施。下列做法对人体健康无害的是
A.用聚氯乙烯塑料袋包装食品
B.在食盐中添加适量的碘酸钾
C.工业用盐亚硝酸钠代替食盐,当调味品用
D.用福尔马林(甲醛的水溶液)保鲜鱼肉等食品
7.根据你所学过的化学知识,判断下列说法错误的是
A.我们使用的铅笔笔芯是金属铅制成的
B.温度计中的水银不是银,是金属汞
C.干冰不是冰,是固体二氧化碳
D.纯碱在物质分类中不是碱,是盐
8.有甲、乙、丙三种金属,将甲投入丙的硫酸盐溶液中,有丙析出。将乙、丙两种金属分别投
入硫酸铜溶液中,丙的表面有红色物质析出,乙的表面没有明显变化。
则甲、乙、丙三种金属活动性顺序
排列正确的是
A.甲>乙>丙 B.甲>丙>乙 C.丙>乙>甲 D.丙>甲>乙
9.某些金属氢化物与水反应可生成碱和氢气,如:NaH + H O=NaOH+ H ↑。CaH 与足量
2 2 2
NaCO 溶液之间发生反应的产物有
2 3
A.Ca(OH) 和H B.CaCO 、NaOH和H
2 2 3 2
C.NaOH和Ca(OH) D.Ca(OH) 、CaCO 和H
2 2 3 2
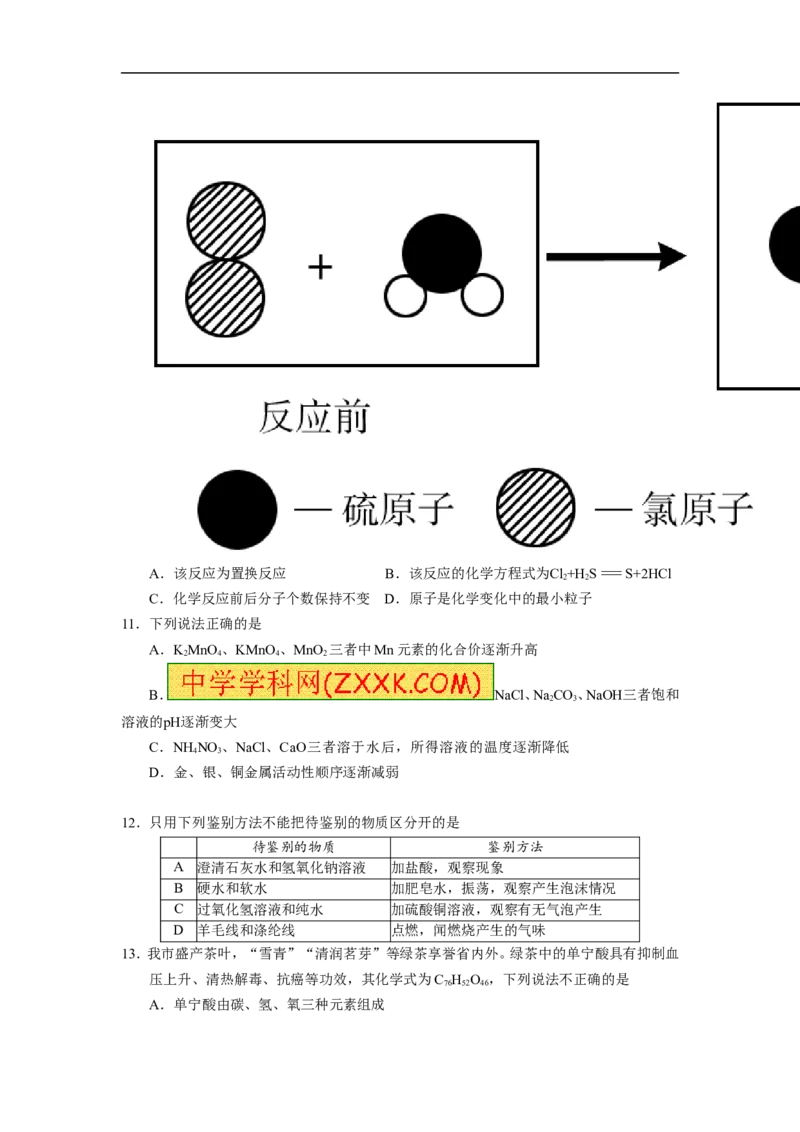
10. 下图为某反应在同一容器中反应
前后微粒示意图。下列说法不正确的是A.该反应为置换反应 B.该反应的化学方程式为Cl+H S=S+2HCl
2 2
C.化学反应前后分子个数保持不变 D.原子是化学变化中的最小粒子
11.下列说法正确的是
A.KMnO 、KMnO 、MnO 三者中Mn元素的化合价逐渐升高
2 4 4 2
B. NaCl、NaCO、NaOH三者饱和
2 3
溶液的pH逐渐变大
C.NH NO 、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低
4 3
D.金、银、铜金属活动性顺序逐渐减弱
12.只用下列鉴别方法不能把待鉴别的物质区分开的是
待鉴别的物质 鉴别方法
A 澄清石灰水和氢氧化钠溶液 加盐酸,观察现象
B 硬水和软水 加肥皂水,振荡,观察产生泡沫情况
C 过氧化氢溶液和纯水 加硫酸铜溶液,观察有无气泡产生
D 羊毛线和涤纶线 点燃,闻燃烧产生的气味
13.我市盛产茶叶,“雪青”“清润茗芽”等绿茶享誉省内外。绿茶中的单宁酸具有抑制血
压上升、清热解毒、抗癌等功效,其化学式为C H O ,下列说法不正确的是
76 52 46
A.单宁酸由碳、氢、氧三种元素组成B.一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸分子中碳、氢、氧原子个数比为38︰26︰23
D.一个单宁酸分子中含26个氢分子
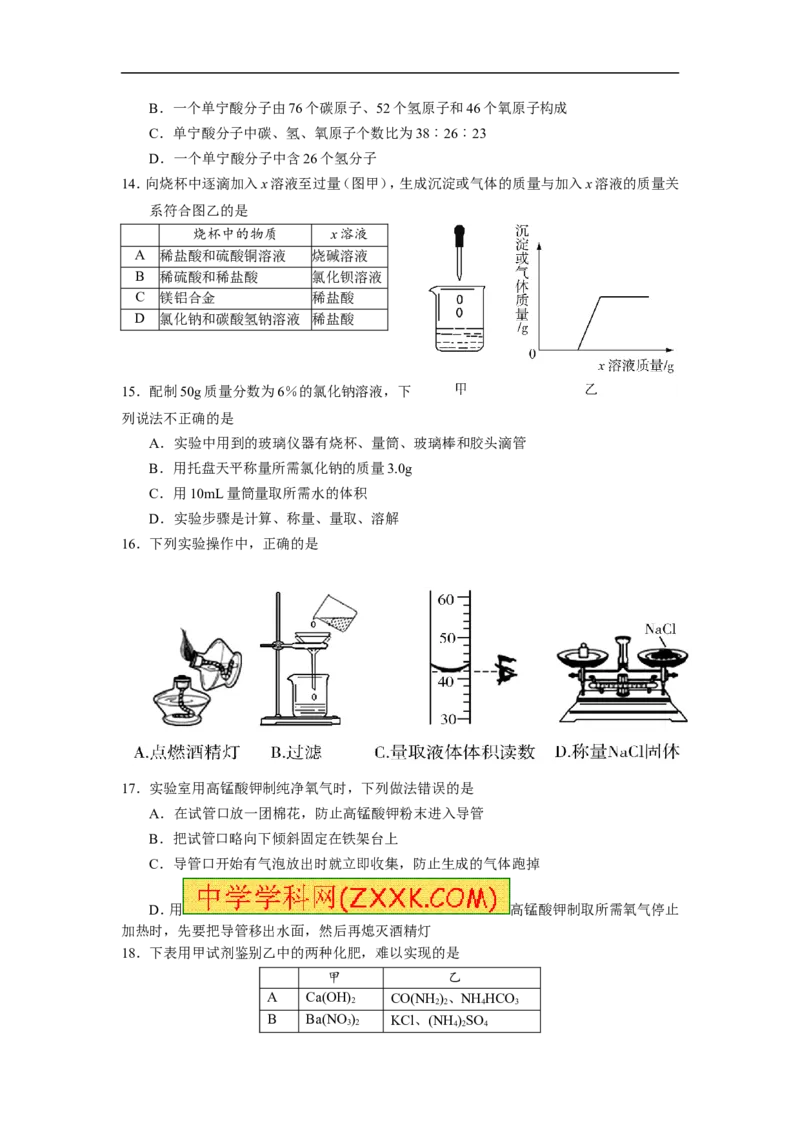
14.向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关
系符合图乙的是
烧杯中的物质 x溶液
A 稀盐酸和硫酸铜溶液 烧碱溶液
B 稀硫酸和稀盐酸 氯化钡溶液
C 镁铝合金 稀盐酸
D 氯化钠和碳酸氢钠溶液 稀盐酸
15.配制50g质量分数为6%的氯化钠溶液,下
列说法不正确的是
A.实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管
B.用托盘天平称量所需氯化钠的质量3.0g
C.用10mL量筒量取所需水的体积
D.实验步骤是计算、称量、量取、溶解
16.下列实验操作中,正确的是
17.实验室用高锰酸钾制纯净氧气时,下列做法错误的是
A.在试管口放一团棉花,防止高锰酸钾粉末进入导管
B.把试管口略向下倾斜固定在铁架台上
C.导管口开始有气泡放出时就立即收集,防止生成的气体跑掉
D.用 高锰酸钾制取所需氧气停止
加热时,先要把导管移出水面,然后再熄灭酒精灯
18.下表用甲试剂鉴别乙中的两种化肥,难以实现的是
甲 乙
A Ca(OH) CO(NH)、NH HCO
2 2 2 4 3
B Ba(NO ) KCl、(NH )SO
3 2 4 2 4C AgNO NH Cl、NH NO
3 4 4 3
D NaCl KSO 、KNO
2 4 3
19.进行化学实验必须注意安全,下列做法符合实际的是
A.不慎将浓硫酸沾到皮肤上,应立即用稀氨水冲洗,再涂上硼酸溶液
B.氢氧化钠有强烈的腐蚀性,实验使用时,最好戴上防护眼镜
C.在实验室里可用品尝的办法区别食盐和蔗糖晶体
D.配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌
20.如图所示,实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度
变化对实验结果的影响。经数小时实验后,U形管A、B两处的液面会出现下列哪种情况
A.A处下降,B处上升
B.A、B两处都下降
C.A处上升,B处下降
D.A、B两处都不变
21.某无色混合气体可能由CH 、H 、
4 2
CO、CO 和HCl中的某几种气体组成。将此混合气体通过过量的澄清石灰水,未见变浑
2
浊,但混合气体的总体积减小,把剩余气体导出后,在O 中能够点燃,燃烧产物不能使
2
白色CuSO 粉末变蓝色。则原混合气体的成份是
4
A.HCl和CO B.HCl、H 和CO C.CH 和H D.CO和CO
2 2 4 2 2
22.地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO,主要用于
2
饮用水消毒。实验测得该氧化物中R与O的质量比为71∶64,则RO 的化学式为
2
A.CO B.NO C.SO D.ClO
2 2 2 2
第 II 卷(非选择题,共 56 分)
二、填空题(本题包括5个小题,共29分)
23.(6分)合理利用与开发能源,增强安全意识是我们大家共同关注的社会问题。
(1)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲
烷的化学式为 。
(2)在实验室里不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧起来,应立刻用
灭火,请写出酒精燃烧的化学方程式 。
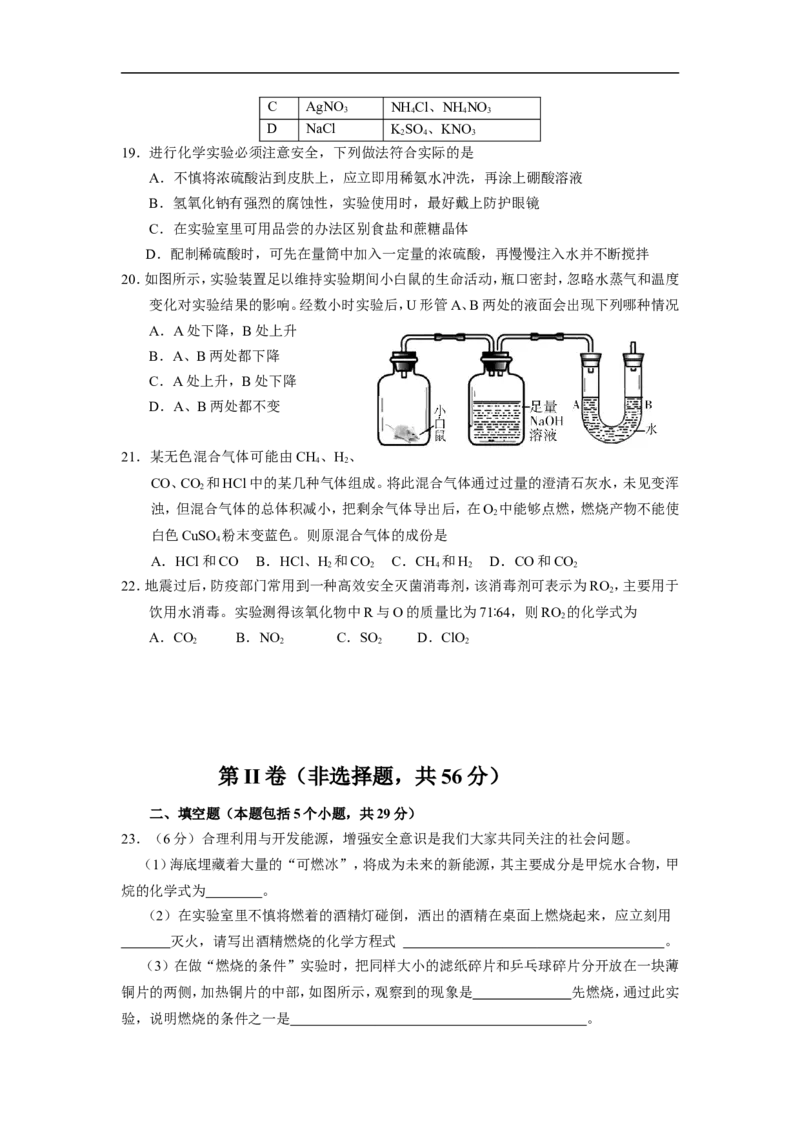
(3)在做“燃烧的条件”实验时,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄
铜片的两侧,加热铜片的中部,如图所示,观察到的现象是 先燃烧,通过此实
验,说明燃烧的条件之一是 。[来源:Z*xx*k.Com]
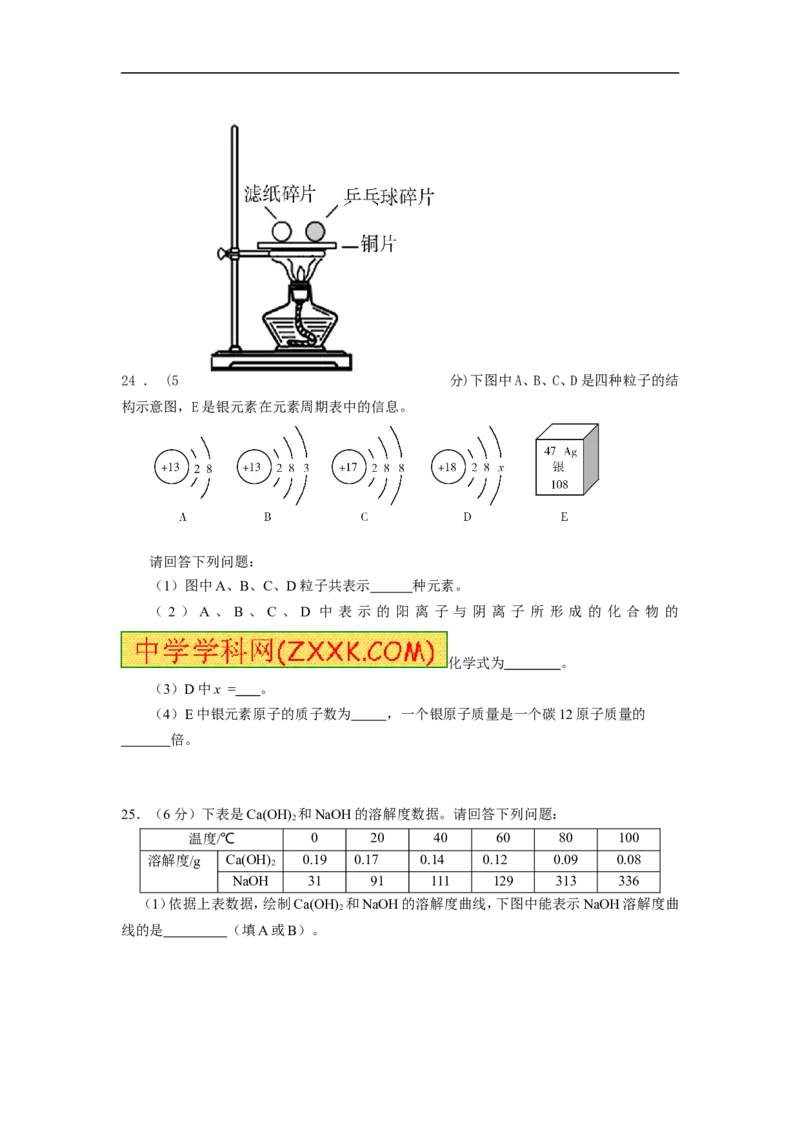
24 . (5 分)下图中A、B、C、D是四种粒子的结
构示意图,E是银元素在元素周期表中的信息。
请回答下列问题:
(1)图中A、B、C、D粒子共表示 种元素。
( 2 ) A 、 B 、 C 、 D 中 表 示 的 阳 离 子 与 阴 离 子 所 形 成 的 化 合 物 的
化学式为 。
(3)D中x = 。
(4)E中银元素原子的质子数为 ,一个银原子质量是一个碳12原子质量的
倍。
25.(6分)下表是Ca(OH) 和NaOH的溶解度数据。请回答下列问题:
2
温度/℃ 0 20 40 60 80 100
溶解度/g Ca(OH) 0.19 0.17 0.14 0.12 0.09 0.08
2 [来源:Z+xx+k.Com] [来源:学科网] [来源:学科网]
NaOH 31 91 111 129 313 336
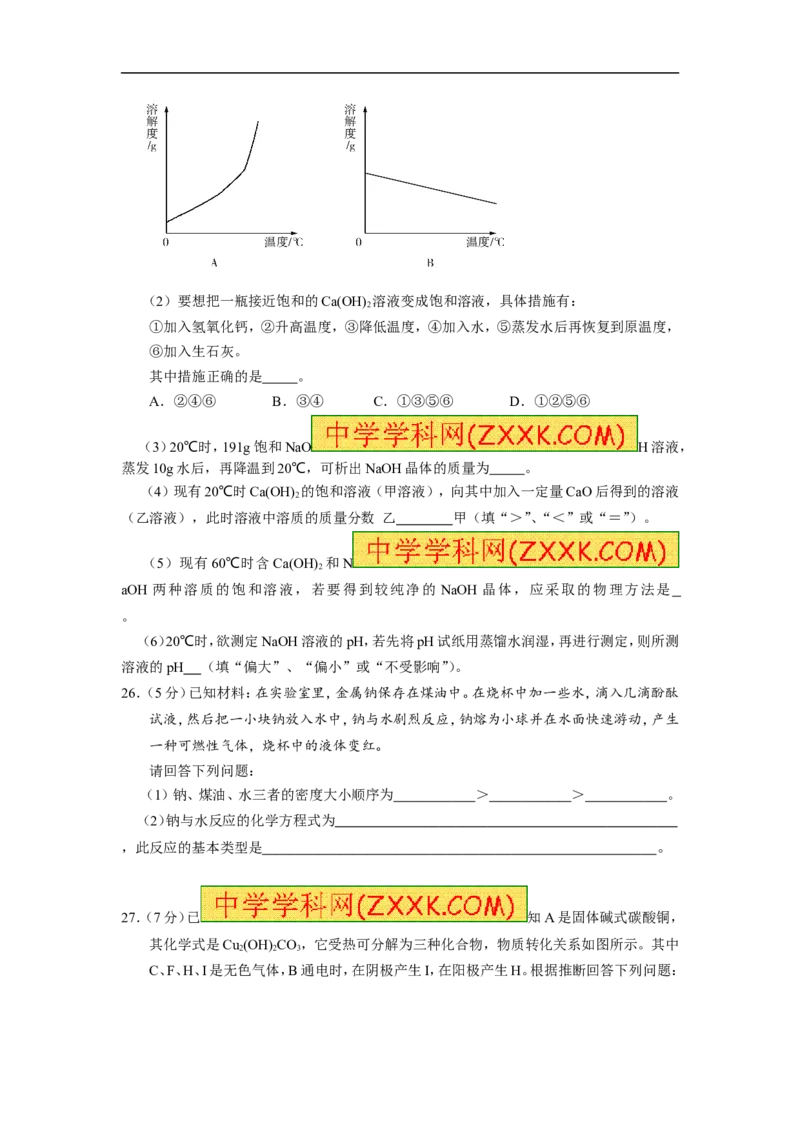
(1)依据上表数据,绘制Ca(OH) 和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲
2
线的是 (填A或B)。(2)要想把一瓶接近饱和的Ca(OH) 溶液变成饱和溶液,具体措施有:
2
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,
⑥加入生石灰。
其中措施正确的是 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaO H溶液,
蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
(4)现有20℃时Ca(OH) 的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液
2
(乙溶液),此时溶液中溶质的质量分数 乙 甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH) 和N
2
aOH 两种溶质的饱和溶液,若要得到较纯净的 NaOH 晶体,应采取的物理方法是
。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测
溶液的pH (填“偏大”、“偏小”或“不受影响”)。
26.(5分)已知材料:在实验室里,金属钠保存在煤油中。在烧杯中加一些水,滴入几滴酚酞
试液,然后把一小块钠放入水中,钠与水剧烈反应,钠熔为小球并在水面快速游动,产生
一种可燃性气体,烧杯中的液体变红。
请回答下列问题:
(1)钠、煤油、水三者的密度大小顺序为 > > 。
(2)钠与水反应的化学方程式为
,此反应的基本类型是 。
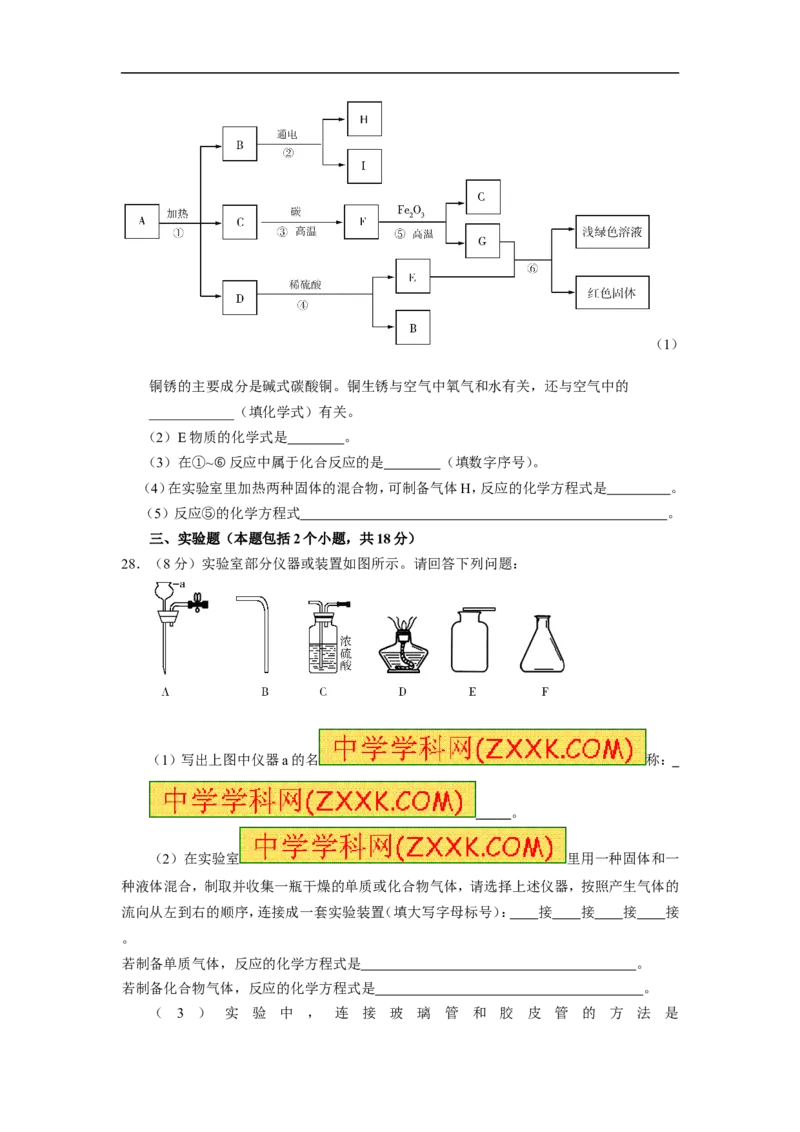
27.(7分)已 知A是固体碱式碳酸铜,
其化学式是Cu (OH) CO,它受热可分解为三种化合物,物质转化关系如图所示。其中
2 2 3
C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:(1)
铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的
____________(填化学式)有关。
(2)E物质的化学式是 。
(3)在①~⑥反应中属于化合反应的是 (填数字序号)。
(4)在实验室里加热两种固体的混合物,可制备气体H,反应的化学方程式是 。
(5)反应⑤的化学方程式 。
三、实验题(本题包括2个小题,共18分)
28.(8分)实验室部分仪器或装置如图所示。请回答下列问题:
(1)写出上图中仪器a的名 称:
。
(2)在实验室 里用一种固体和一
种液体混合,制取并收集一瓶干燥的单质或化合物气体,请选择上述仪器,按照产生气体的
流向从左到右的顺序,连接成一套实验装置(填大写字母标号): 接 接 接 接
。
若制备单质气体,反应的化学方程式是 。
若制备化合物气体,反应的化学方程式是 。
( 3 ) 实 验 中 , 连 接 玻 璃 管 和 胶 皮 管 的 方 法 是。
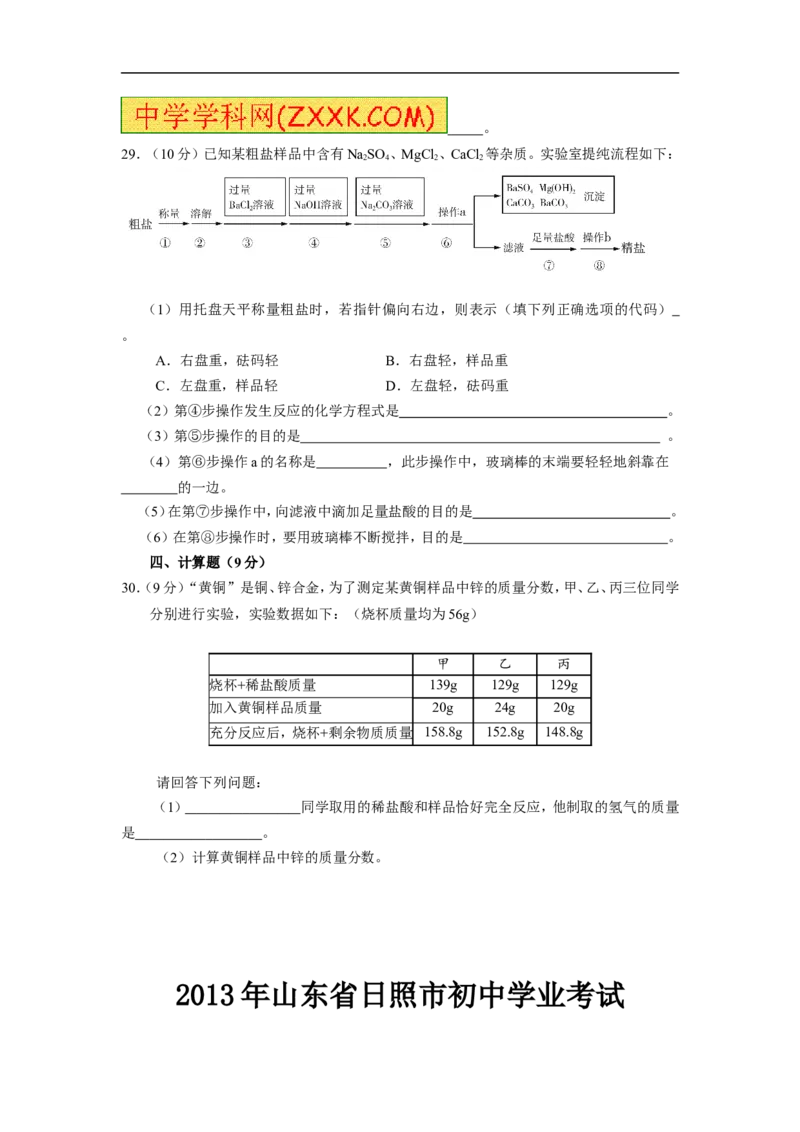
29.(10分)已知某粗盐样品中含有NaSO 、MgCl 、CaCl 等杂质。实验室提纯流程如下:
2 4 2 2
(1)用托盘天平称量粗盐时,若指针偏向右边,则表示(填下列正确选项的代码)
。
A.右盘重,砝码轻 B.右盘轻,样品重
C.左盘重,样品轻 D.左盘轻,砝码重
(2)第④步操作发生反应的化学方程式是 。
(3)第⑤步操作的目的是 。
(4)第⑥步操作a的名称是 ,此步操作中,玻璃棒的末端要轻轻地斜靠在
的一边。
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是 。
(6)在第⑧步操作时,要用玻璃棒不断搅拌,目的是 。
四、计算题(9分)
30.(9分)“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学
分别进行实验,实验数据如下:(烧杯质量均为56g)
甲 乙 丙
烧杯+稀盐酸质量 139g 129g 129g
加入黄铜样品质量 20g 24g 20g
充分反应后,烧杯+剩余物质质量 158.8g 152.8g 148.8g
请回答下列问题:
(1) 同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量
是 。
(2)计算黄铜样品中锌的质量分数。
2013 年山东省日照市初中学业考试化学试题参考答案与评分标准
评分说明:
1.本答案供阅卷评分使用,考生若写出其他正确答案,可参照评分标准给分。
2.化学方程式未配平的,不给分;化学计量数是最简比的整数倍而没化简的,不给分。
3.化学方程式的书写中,若错写反应条件不得分;若漏写反应条件扣1分。
4.化学专用名词出现错别字或元素符号有错误,都要参照评分标准扣分。
第I卷(选择题,共44分)
一、选择题(本题包括22小题,每小题2分,共44分。多选、错选均不得分。)
1.B 2.A 3.C 4.D 5.D 6.B 7.A 8.B 9.B 10.C
11.B 12.A 13.D 14.A 15.C 16.C 17.C 18.D 19.B 20.C
21.A 22.D
第II卷(非选择题,共56分)
二、填空题(本题包括5个小题,共29分)
23.( 6分)
(1)CH (1分)
4
(2)湿抹布(1分) C HOH+3O 2CO+3H O(2分)
2 5 2 2 2
( 3 ) 乒 乓 球 碎 片 ( 1 分 ) 温 度 需 达 到 可 燃 物 的 着 火
点 (1分)
24.(5分,每空1分)
(1)三 (2) AlCl (3)8 (4)47 9
3
25.(6分,每空1分)
(1)A (2)D (3)9.1 g (漏写单位不得分) (4)<
(5)降温结晶,过滤 (6)偏小
26.(5分)
(1)水 钠 煤油(2分,顺序全对得2分,错一处就不得分)
(2) 2Na+2HO=2NaOH+H ↑(2分) 置换反应(1分)
2 2
27.(7分)
(1)CO(1分) (2)CuSO (1分) (3)③(1分)
2 4
MnO
(4)2KClO 2 2KCl+3O ↑ (2分)
3 2
△
高温
(5)3CO+Fe O 2Fe+3CO (2分)
2 3 2三、实验题(本题包括2个小题,共18分)
28.(8分)
(1)长颈漏斗(1分)
(2)F A C B E(2分)
2HO 2HO+ O ↑(2分)
2 2 2 2
CaCO +2HCl=CaCl +H O+CO↑(2分)
3 2 2 2
(3)先把玻璃管口用水湿润,然后稍稍用力即可把玻璃管插入胶皮管(1分)
29.(10分)
(1)D(1分)
(2)MgCl + 2NaOH=Mg(OH) ↓+ 2NaCl (2分)
2 2
(3)除去杂质CaCl 和加入的过量试剂BaCl (2分)
2 2
(4)过滤(1分) 三层滤纸(1分)
(5)除去加入的过量试剂NaOH和NaCO(2分)
2 3
(6)防止蒸发时因局部温度过高,造成液滴飞溅(1分)
四、计算题(9分)
30.(9分)
【解】(1)丙(2分) 0.2g(1分,漏写单位不得分)
(2) 设:黄铜样品中参加反应锌的
质量为x
Zn + 2HCl = ZnCl + H↑(2分)
2 2
65 2
x 0.2g(1分)
(1分)
x= 6.5g (1分)
黄铜样品中锌的质量分数:
(1分)
答:(1)丙 0.2g
(2)黄铜样品中锌的质量分数为32.5%。