文档内容
淄博市 2014 年初中学业水平测试
化学试题
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40
[来源:学.科.网Z.X.X.K]
第一卷(选择题 共20分)
一、 选择题(本题包括15个小题,1-10小题每小题1分,11-15小题每小题2分,共20分。
每小题只有一个选项符合题意)
1、化学是在原子分子水平上研究物质及其变化规律的基础自然科学,他它指导我们更好地
认识、改造和应用物质。现代科技的发展已经实现了对原子、分子的移动和排列,以及改造和
创造分子。若用这种方法制造葡萄糖(C H O),则不需要的原子是( )
6 12 6
A.碳原子B.氧原子C.氮原子D.氢原子
2、化学实验是进行科学探究的重要方式,具备基本的化学实验技能是学习化学和进行探究
活动的基础。下列实验操作正确的是( )
3、物质世界每时每刻都在发生各种变化。下列过程主要是通过物理变化实现的是
( )A.酸雨形成B.钢铁锈蚀C.海水
“制碱”D.海水“晒盐”
4、质量守恒定律是化学反应、乃至自然界最基本的定律之一,依据质量守恒定律我们可以精
确地研究化学反应。最早传播和用文字记载并使人们普遍接受质量守恒定律的科学家是(
)
A.拉瓦锡B.波义耳C.汤姆森D.卢瑟福
5、有机物种类繁多, 在已发现的数千万种物质中,90%以上的都是有机物。下列物质都属于有机物的一组是( )
A.氨基酸 油脂B.小苏打 淀粉C.氯酸钾 蔗糖D.氧化钙 塑料
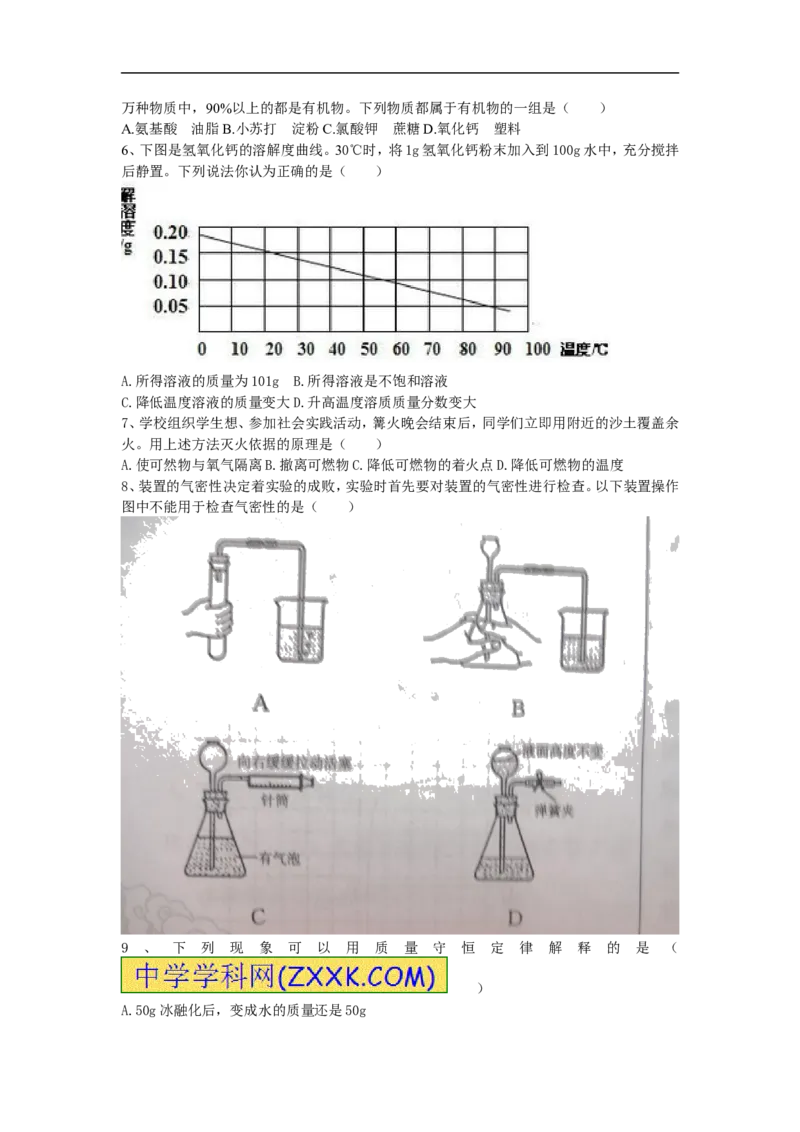
6、下图是氢氧化钙的溶解度曲线。30℃时,将1g氢氧化钙粉末加入到100g水中,充分搅拌
后静置。下列说法你认为正确的是( )
A.所得溶液的质量为101g B.所得溶液是不饱和溶液
C.降低温度溶液的质量变大D.升高温度溶质质量分数变大
7、学校组织学生想、参加社会实践活动,篝火晚会结束后,同学们立即用附近的沙土覆盖余
火。用上述方法灭火依据的原理是( )
A.使可然物与氧气隔离B.撤离可燃物C.降低可燃物的着火点D.降低可燃物的温度
8、装置的气密性决定着实验的成败,实验时首先要对装置的气密性进行检查。以下装置操作
图中不能用于检查气密性的是( )
9 、 下 列 现 象 可 以 用 质 量 守 恒 定 律 解 释 的 是 (
)
A.50g冰融化后,变成水的质量还是50gB.木条燃烧后,灰烬的质量比木条的质量少
C.5g 食 盐 晶 体 溶 于 95g 水 中 , 溶 液 的 质 量 为
100g
D.50mL水和50m L酒精混合后,溶液的
体积小于100mL
10、化学学习中经常要查阅各种数据或相关的图表。若要推测一个复分解反应能否发生,以
下图表能给你提供帮助的是( )
A. 元素周期表B.常见物质的溶解性表
C.相对原子质量表D.常见元素的化合价表
11、新颁布的《环境空气质量标准》自2016年1月1日起在全国实施,它规定环境空气污染物
的 基 本 项 目 包 括 : SO 、 NO 、 CO 、 O 、 PM10 、 PM2.5 等 , 其 中 的 “ P
2 2 3
M2.5”是指( )
A.空气的湿度 B.空气的透明度
C.空气中有害气体的浓度 D.空气中直径不超过2.5um的颗粒物
12、如图是钠元素和硫元素的原子结构示意图,以及这两种元素摘自元素周期表的图示,下
列说法错误的是( )
A.钠元素和硫元素的原子序数分别是11和16
B. 钠元素和硫元素的核外电子数分别是1和6
C. 钠元素和硫元素的原子核外都有3个电子层
D. 钠元素和硫元素形成化合物的化学式为NaS
213、在初中化学学习中接触过几种循环,下列说法你认为正确的是( )
A .水的天然循环中水分子和水分子的
能量都不变
B.二氧化碳的循环与大自然的森林绿化面积无关
C.自然界中的氧循环主要是通过化学变化实现的
D.自然界中的碳循环主要是通过物理变化实现的
14、化学方程式能简明、科学的描述化学反应。以下化学方程式正确的是( )
A.2HO 通电 2H+O
2 2 2
B.Cu+HSO = CuSO +H ↑
2 4 4 2
C.Mg+O 点燃 MgO
2 2
D.Na CO+CaCl =CaCO ↓ +2NaCl
2 3 2 3
15、微粒观是化学基本观念最基础、最重要的组成部分,从微粒观的角度认识和研究物质是
学习化学必须具备的思维方法。以下描述错误的是( )
A.原子的质量就是它的相对原子质量
B.分子、原子和离子都是构成物质的基本粒子
C.分子自身具有一定的能量,总是在不断的运动
D.在化学反应中,原子核是不变的,发生改变的只是原子核外的电子
第二卷(非选择题 共30分)
二、 理解与应用(本题包括3个小题,共12分)
16、(4分)海洋是人类巨大的资源宝库,从海水里提取MgCl 中的金属元素可广泛用于飞机
2
制造业,该金属元素的名称是______;海底蕴藏着大量的化石燃料,其中天然气的主要成分
是________(填写名称),其分子中碳元素和氢元素的原子个数比为________,写
出 其 燃 烧 的 化 学 方 程 式
________________________。
17、(4分)在宏观、微观和符号之间建立联系是化学学科的特点,对物质进行分类是化学研
究的重要方法。现有物质①纯碱; ②锌粒;③硝酸钾;④氧化铝;⑤尿素,请按要求填写:由
原子直接构成的是________(填写化学式),属于氧化物的是________(填写化学式),
属于盐的是________(填写序号),可用作化学肥料的是________(填写序号)。
18、(4分)学习了“常见的酸和碱”后某小组同学对中和反应进一步探究。同学们分别测定
了稀HSO 和NaOH溶液的pH(20℃),其中NaOH溶液的pH_____7(填“大于” “小
2 4
于”或 “等于”)。向一定量的NaOH溶液中逐滴滴入HSO ,反应的化学方程式为_____
2 4
_______________________。如图是利用pH传感器实时监测稀HSO 和NaOH溶液反应过
2 4
程中混合液的pH的变化情况,并借助计算机绘制出了混合液中pH变化的曲线。R点显示混
合溶液的pH小于7,说明此时___________过量。在探究过程中,同学们选用pH计而不用
pH试纸来测定溶液的pH,你认为这样做的原因是________________________________。三、 实验与探究(本题包括2个小题,共12分)
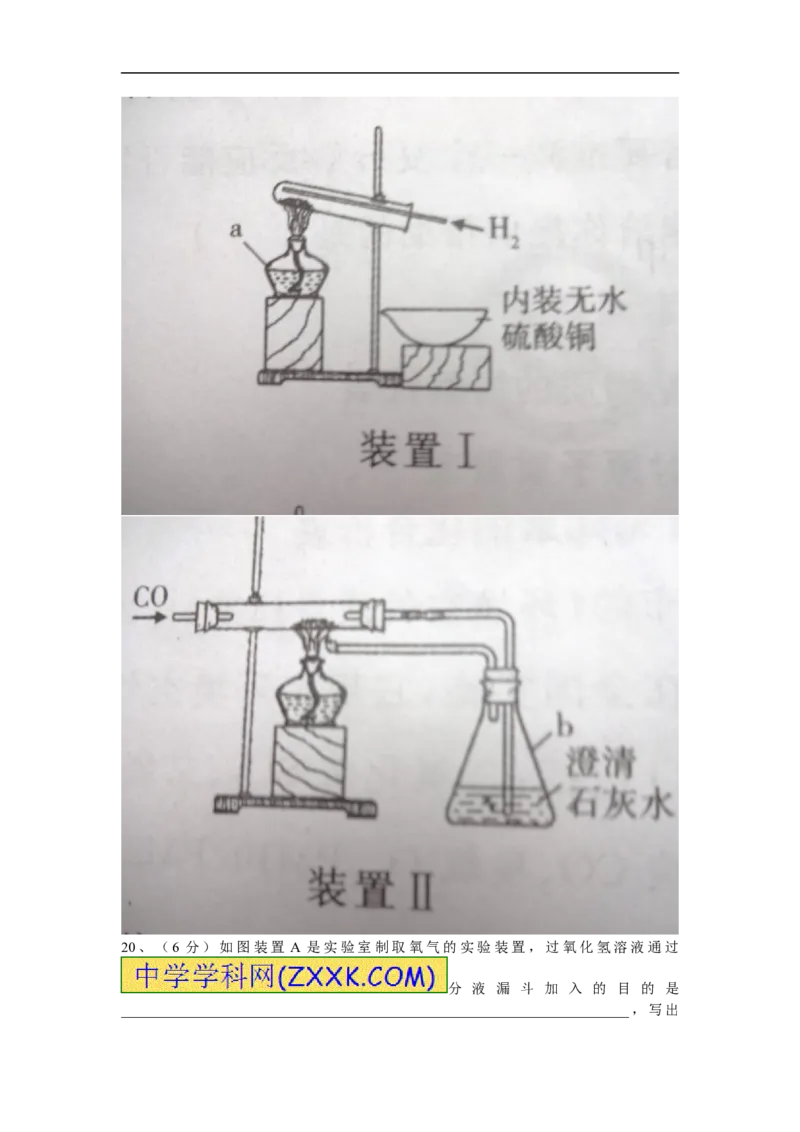
19、(6分)金属冶炼的过程中,氢气和一氧化碳气体常用作还原剂,在加热条件下,氢气和一
氧 化 碳 气 体 都 能 从 金 属 的 氧 化 物 中 把 金 属 还 原 出 来 。 下 图 分 别 是 氢气和一氧化碳还原氧化铜粉末的实验
装置,据图回答问题。
⑴写出编号仪器的名称:a_____________b_____________
⑵实验完毕后,在蒸发皿中看到的现象时______________________。
⑶请仔细观察装置II,此装置中至少有______个化学反应发生,任意写出其中一个反应的化
学方程式______________________。
⑷实验装置的设计必须要考虑反应物和生成物的性质以及反应发生的条件等因素。请认真
分析I、II两套实验装置的不同之处,并由此推断氢气和一氧化碳两种气体性质的不同点是
___
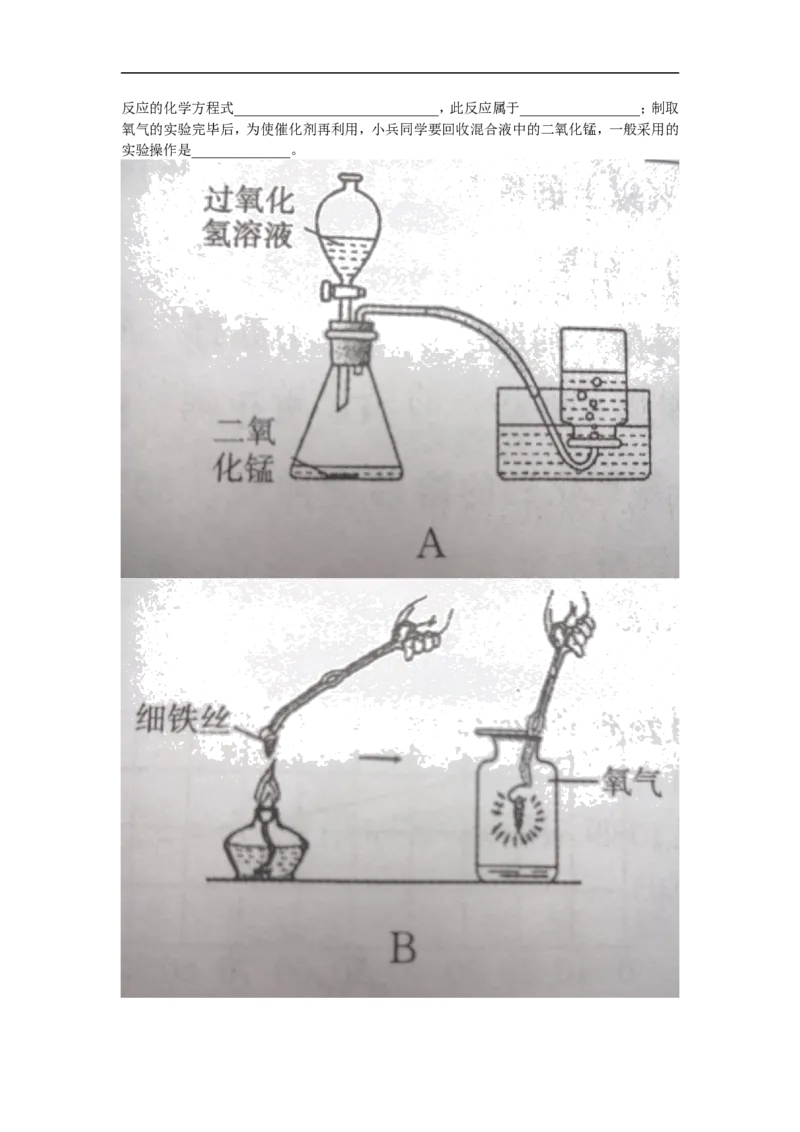
____________________________________________。20、(6 分)如图装置 A 是实验室制取氧气的实验装置,过氧化氢溶液通过
分 液 漏 斗 加 入 的 目 的 是
________________________________________________________________________,写出反应的化学方程式_____________________________,此反应属于_________________;制取
氧气的实验完毕后,为使催化剂再利用,小兵同学要回收混合液中的二氧化锰,一般采用的
实验操作是______________。同学们利用收集的氧气进行“铁丝在氧气里燃烧”的探究实验,如图B,请你参与探究并回
答下列为题。
铁丝在氧气中燃烧生成了黑色固体,小明同学猜测铁丝燃烧时溅落的黑色固体中可能含有
铁,并决定用化学方法来验证猜想。小明将冷却后的黑色固体研碎,取少量放入试管中,加入
_________________,观察到的现象是_________________,由此推测,铁丝在氧气中燃烧时
溅落的黑色固体物质中含有少量铁。
四、 分析与算(本题包括1 个小题,
共6分)
21、(6分)某学校化学兴趣小组的同学对我市南部山区的大理石矿区进行调查并取样。样品
的主要成分是碳酸钙(其中含有二氧化硅等杂质)。下面是同学们的实验探究过程,请你参与
并回答有关。
【实验目的】测定大理石样品中碳酸钙的质量分数。
【查阅资料】二氧化硅等杂质不溶于水,也不与盐酸反应。
【实验过程】准确称量5.0g大理石样品于烧杯中,向其中加入40mL质量分数为20%的盐酸,
立即将烧杯放在电子秤上称量。每分钟记录一次数据(提示:反应结束后盐酸有剩余)。
相关的实验数据如下表:
时间/min 0 1 2 3 4 5 6 7 8
质量/g 102.0 101.0 100.5 100.2 100.1 100.4 100.1 100.1 100.1
[ 来
源:Zxxk.Com]
【数据处理】
⑴表中有一个称量数据是不合理的,该数据的测定时间是_____分钟。
⑵计算样品中碳酸钙的质量分数。(写出计算过程,计算结果保留一位小数)
【反思交流】实验结束后,部分同学认为测得的碳酸钙质量分数偏大,请你分析出现此情况的
原因可能是________________________________________________________________。答案
[来源:学科网]
题号 1 2 3 4 5 6 7 8 9 10
答案 C D D A A C A B B B
题号 11 12 13 14 15
答案 D B C D A
16、镁 甲烷 1:4 CH + 2O
4 2
CO + 2H O
2 2
17、Zn Al O ①③ ③⑤
2 3
18、大于 H SO + 2NaOH == Na SO + 2H O 稀HSO pH计使用方便,可随时测出溶
2 4 2 4 2 2 4
液的pH。
19、⑴酒精灯 锥形瓶 ⑵白色固体变为蓝色
⑶3 CuO + CO Cu + CO [或CO + Ca(OH) == CaCO ↓+ H O
2 2 2 3 2
或2C O+ O == 点 = 燃 = 2CO
2 2
⑷氢气无毒,而一氧化碳有毒
20、控制过氧化氢溶液的滴加速度 2H O 2H O + O ↑ 分解反应 过滤 稀盐酸
2 2 2 2
有气泡产生
21、⑴5
⑵解:设样品中碳酸钙的质量为x
[来源:学科网ZXXK]
CaCO + 2HCl == CaCl + CO ↑+ H O
3 2 2 2
100 44
X 102.0g-100.1g
x=4.318g
则样品中CaCO 的质量分数为:
3
答:样品中碳酸钙的质量分数为86.4%。
[来源:Z#xx#k.Com]
【反思交流】
烧 杯 减 少 的 质 量 除 二 氧 化 碳 外 还 含 有 盐 酸 挥
发出的氯化氢气体。