文档内容
2017 年山东省济宁市中考化学试卷
一、选择题(每小题只有一个选项符合题意,共16分)
1.化学与人类生产、生活密切相关,下列应用不涉及化学变化的是( )
A.小苏打用作糕点膨松剂 B.生石灰用作袋装食品干燥剂
C.肥皂水用来区别硬水、软水 D.活性炭用来去除冰箱内异味
2.对下面几种物质的分类,正确的是( )
①CH ②P O ③MgO ④BaCl ⑤HNO ⑥NH HCO .
4 2 5 2 3 4 3
A.②③⑤属于氧化物 B.⑤⑥属于酸
C.④⑥属于盐 D.①⑥属于有机物
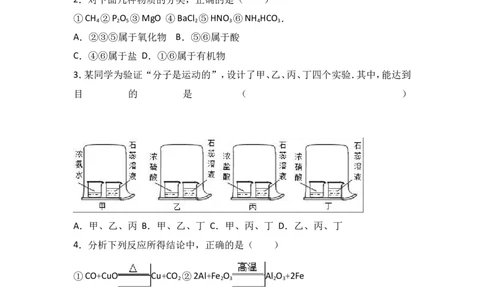
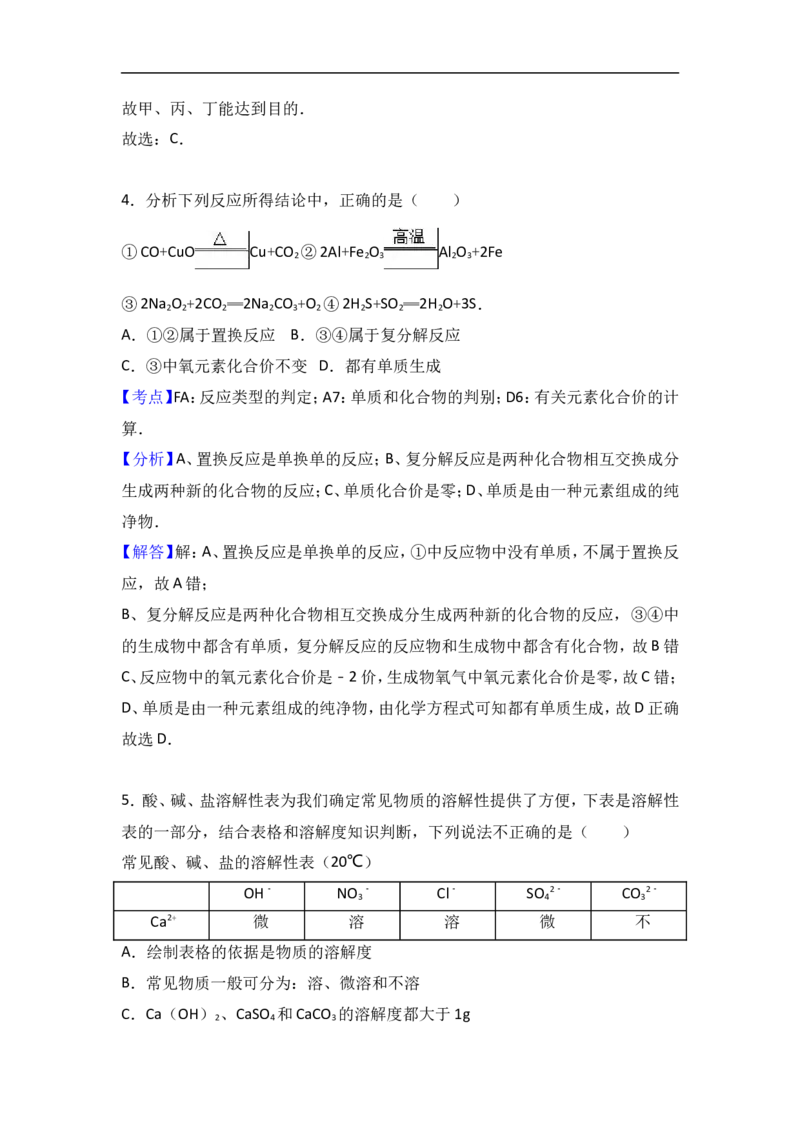
3.某同学为验证“分子是运动的”,设计了甲、乙、丙、丁四个实验.其中,能达到
目 的 是 ( )
A.甲、乙、丙 B.甲、乙、丁 C.甲、丙、丁 D.乙、丙、丁
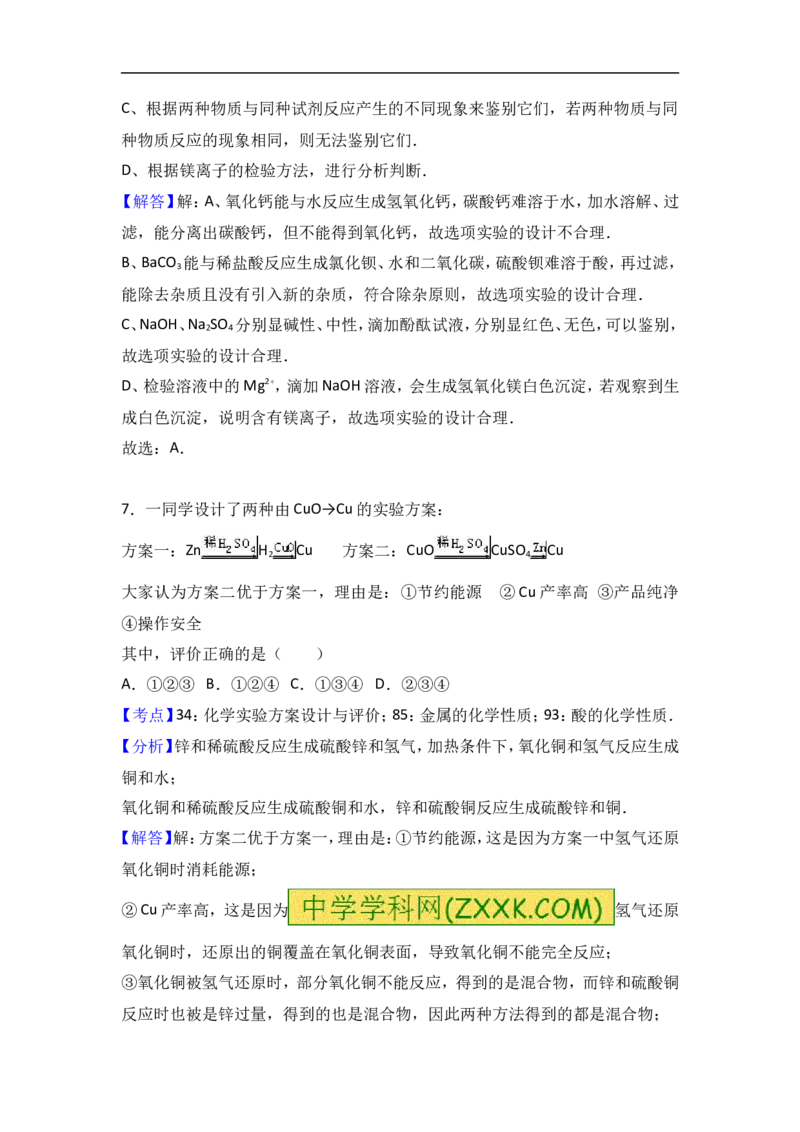
4.分析下列反应所得结论中,正确的是( )
①CO+CuO Cu+CO ②2Al+Fe O Al O +2Fe
2 2 3 2 3
③2Na O +2CO ═2Na CO +O ④2H S+SO ═2H O+3S.
2 2 2 2 3 2 2 2 2
A.①②属于置换反应 B.③④属于复分解反应
C.③中氧元素化合价不变 D.都有单质生成
5 . 酸 、 碱 、 盐 溶 解 性 表 为 我 们 确 定 常 见 物 质 的
溶解性提供了方便,下表是溶解
性表的一部分,结合表格和溶解度知识判断,下列说法不正确的是( )常见酸、碱、盐的溶解性表(20℃)
OH﹣ NO ﹣ Cl﹣ SO 2﹣ CO 2﹣
3 4 3
Ca2+ 微 溶 溶 微 不
[来源:学+科+网Z+X+X+K]
A.绘制表格的依据是物质的溶解度
B.常见物质一般可分为:溶、微溶和不溶
C.Ca(OH) 、CaSO 和CaCO 的溶解度都大于1g
2 4 3
D.Ca2+、NO ﹣、Cl﹣三种离子在溶液中能大量共存
3
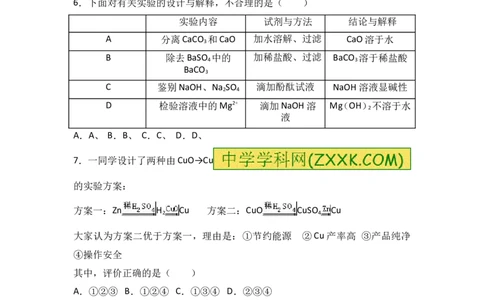
6.下面对有关实验的设计与解释,不合理的是( )
实验内容 试剂与方法 结论与解释
A 分离CaCO 和CaO 加水溶解、过滤 CaO溶于水
3
B 除去BaSO 中的 加稀盐酸、过滤 BaCO 溶于稀盐酸
4 3
BaCO
3
C 鉴别NaOH、Na SO 滴加酚酞试液 NaOH溶液显碱性
2 4
D 检验溶液中的Mg2+ 滴加NaOH溶 Mg(OH)不溶于水
2
液
A.A、 B.B、 C.C、 D.D、
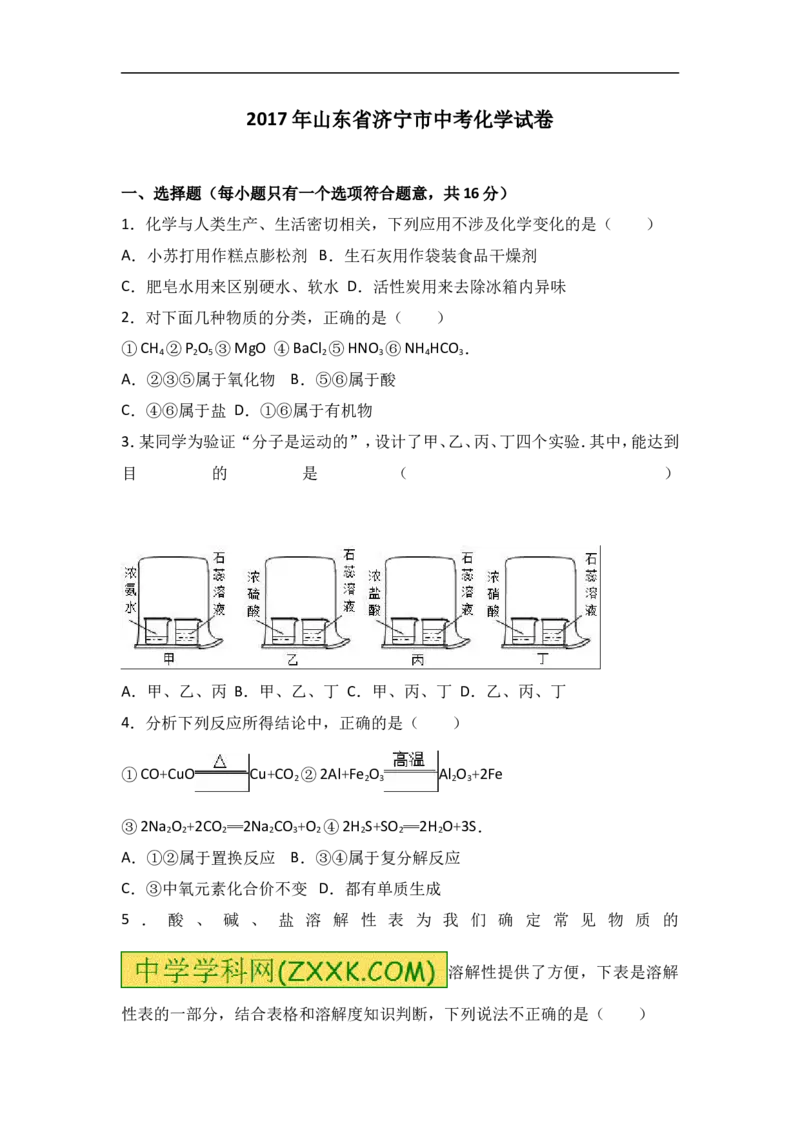
7.一同学设计了两种由CuO→Cu
的实验方案:
方案一:Zn H Cu 方案二:CuO CuSO Cu
2 4
大家认为方案二优于方案一,理由是:①节约能源 ②Cu产率高 ③产品纯净
④操作安全
其中,评价正确的是( )
A.①②③ B.①②④ C.①③④ D.②③④
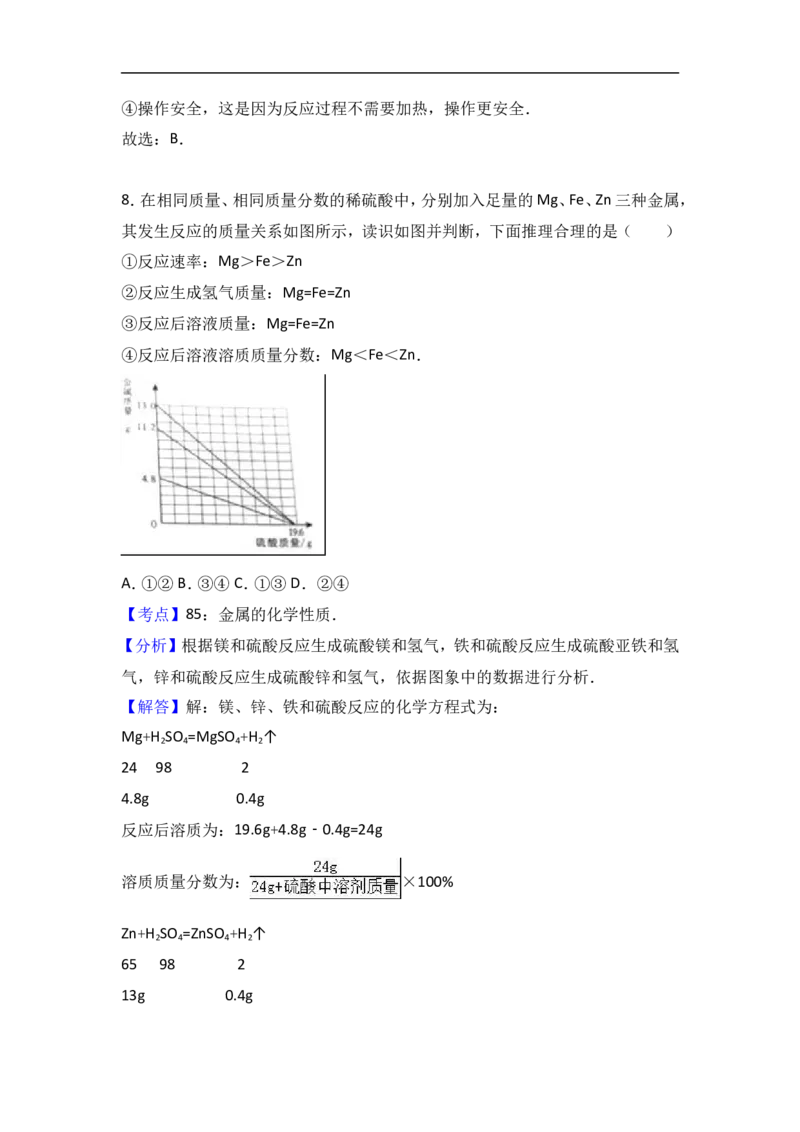
8.在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,
其发生反应的质量关系如图所示,读识如图并判断,下面推理合理的是( )
①反应速率:Mg>Fe>Zn
②反应生成氢气质量:Mg=Fe=Zn
③反应后溶液质量:Mg=Fe=Zn
④反应后溶液溶质质量分数:Mg<Fe<Zn.A.①②B.③④C.①③D.②④
9.有四瓶无色溶液,他们分别是AgNO 、BaCl 、K CO 和Mg(NO )溶液,仅利用下
3 2 2 3 3 2
面试剂就能将他们区别开的是( )
A.HCl、Na SO B.NaCl、HNO C.HNO 、Ba(NO ) D.NaCl、NaOH
2 4 3 3 3 2
10.一澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl﹣、OH﹣和SO 离子的一种
或几种.为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成.继续滴加NaOH溶液至不再产
生沉淀为止,过滤;
③ 向 实 验 ② 得 到 的 滤 液 中 滴 加 Na CO 溶 液 , 又 观
2 3
察到沉淀生成.
分析实验得出的以下结论中,正确的是( )
A.溶液中一定含有H+、Ba2+、Cl﹣,一定不含有Na+、Fe3+、OH﹣、SO
B.溶液中一定含有H+、Ba2+、Fe3+、Cl﹣,一定不含有Na+、OH﹣和SO
C.溶液中一定含有H+、Ba2+、Fe3+、Cl﹣,一定不含有OH﹣、SO ,可能含有Na+
D.溶液中一定含有H+、Ba2+、Na+、Fe3+,一定不含有OH﹣、SO ,可能含有Cl﹣
二、填空与简答(共17分)
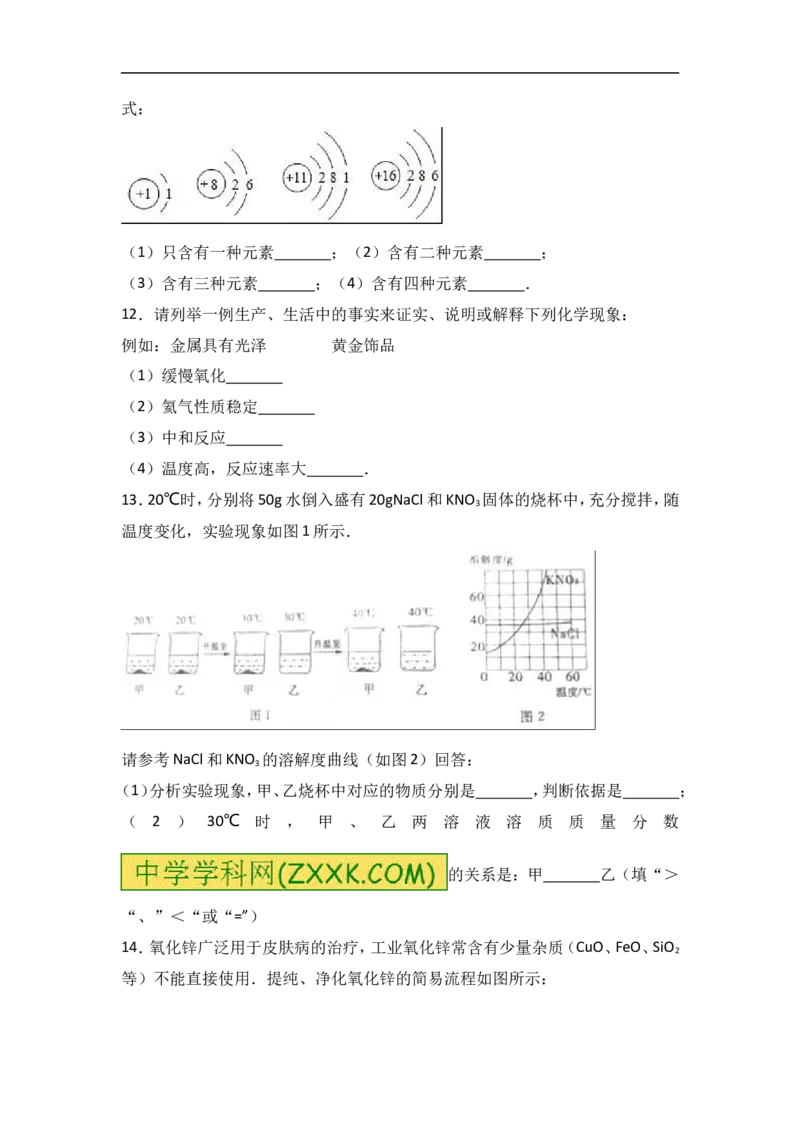
11.读识下面几种常见元素的原子结构示意图,请写出一种符合要求物质的化学式:
(1)只含有一种元素 ;(2)含有二种元素 ;
(3)含有三种元素 ;(4)含有四种元素 .
12.请列举一例生产、生活中的事实来证实、说明或解释下列化学现象:
例如:金属具有光泽 黄金饰品
(1)缓慢氧化
(2)氦气性质稳定
(3)中和反应
(4)温度高,反应速率大 .
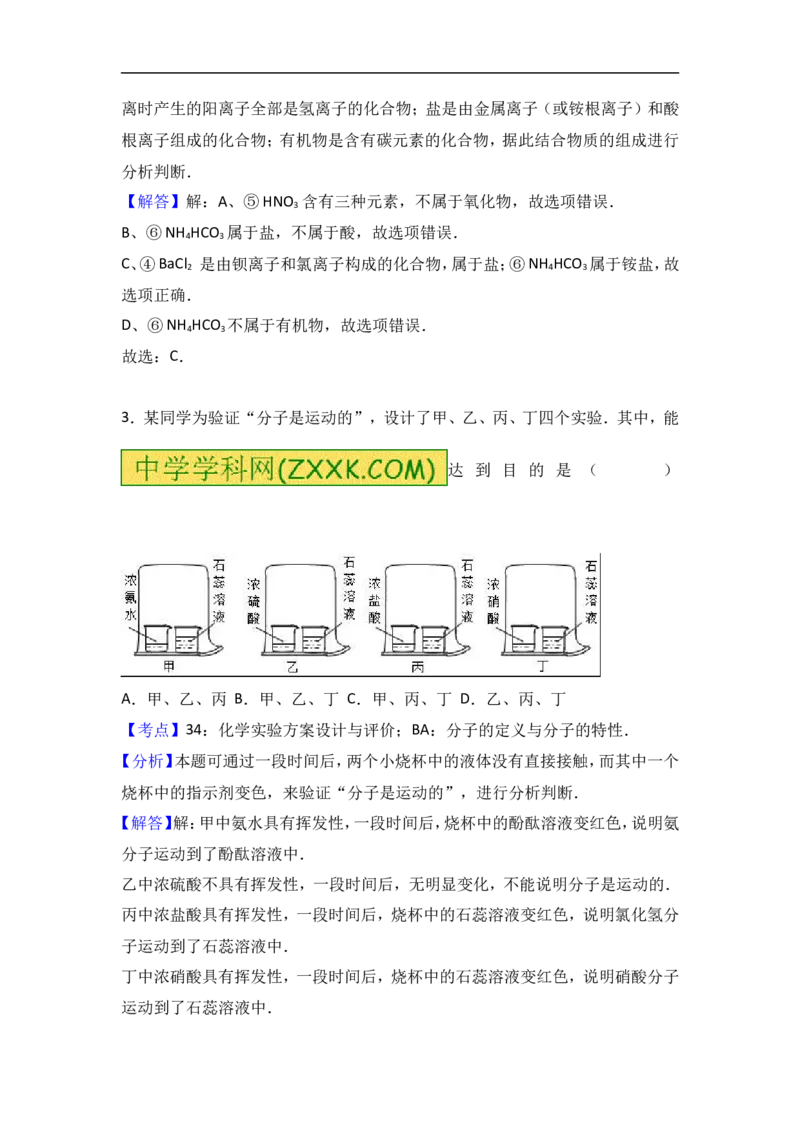
13.20℃时,分别将50g水倒入盛有20gNaCl和KNO 固体的烧杯中,充分搅拌,随
3
温度变化,实验现象如图1所示.
请参考NaCl和KNO 的溶解度曲线(如图2)回答:
3
(1)分析实验现象,甲、乙烧杯中对应的物质分别是 ,判断依据是 ;
( 2 ) 30℃ 时 , 甲 、 乙 两 溶 液 溶 质 质 量 分 数
的关系是:甲 乙(填“>
“、”<“或“=”)
14.氧化锌广泛用于皮肤病的治疗,工业氧化锌常含有少量杂质(CuO、FeO、SiO
2
等)不能直接使用.提纯、净化氧化锌的简易流程如图所示:参考资料:SiO 既不溶于水也不与酸反应
2
(1)反应器Ⅰ中加入足量稀硫酸,充分反应后,生成硫酸盐的化学式为 ;
(2)残渣中除金属锌外,还有 ;
(3)操作一、操作二和操作三采用的分离方法是 ;
(4)操作四发生反应的化学方程式为 .
15.蛋白粉是由大豆蛋白、酪蛋白、乳清蛋白或上述几种蛋白混合制成的粉剂,其
用途是为营养不良或疾病导致蛋白质缺乏的人群补充营养.请回答:
(1)蛋白粉补充的营养成分是 ;
(2)市售劣质蛋白粉往往添加食用香精、淀粉,从颜色和味道都难以分辨.用少量
样品验证这种蛋白粉中含有淀粉的方法是 .
三、实验与探究(共11分)
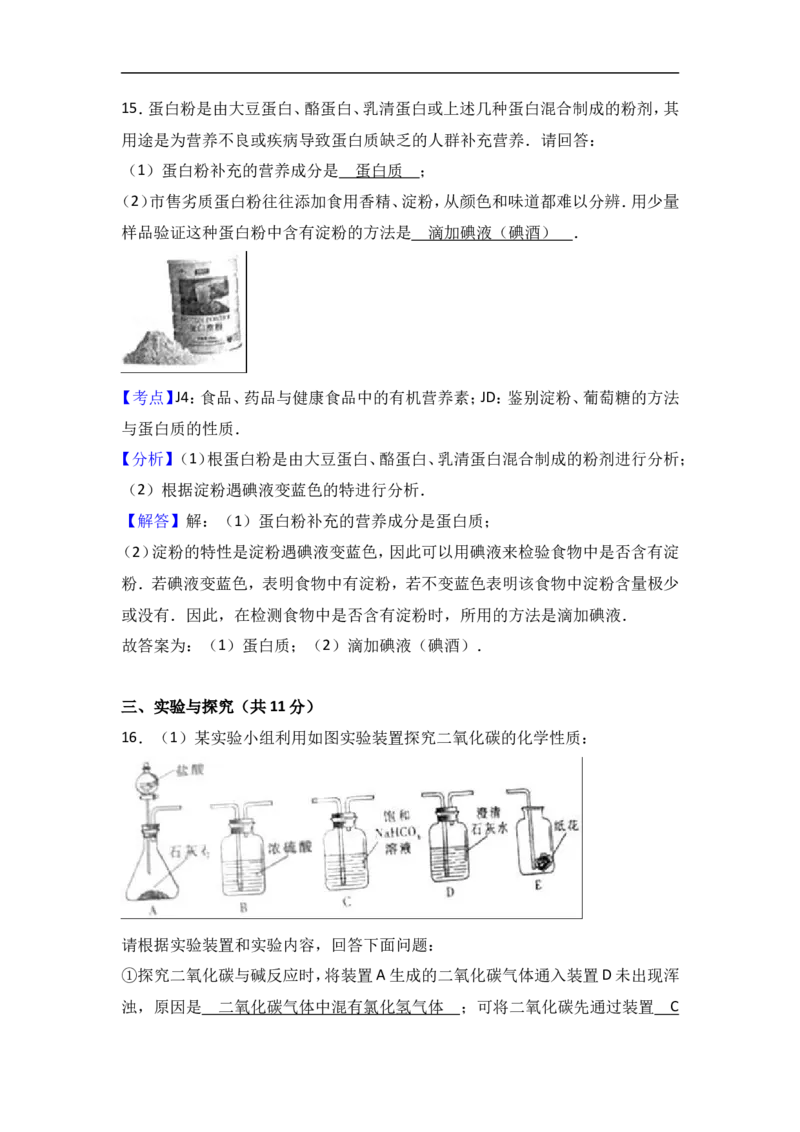
16.(1)某实验小组利用如图实验装置探究二氧化碳的化学性质:
请根据实验装置和实验内容,回答下面问题:
①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑
浊,原因是 ;可将二氧化碳先通过装置 ,再通入装置D,理由是(用化学方程式表示);
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸
泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是
;结合上面实验,装置正确的连接顺序是 (填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分
是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设
计实验验证 小莉提供的食用碱样
品是否含有氯化钠.
实验步骤 实验现象 结论与解释
1.取一定量的食用碱样品放入试管,加入 样品溶解 食用碱溶于水
蒸馏水、振荡
四、分析与计算(共6分)
17.观看足球比赛时,经常会看到绿茵场上运动员因拼抢摔倒受伤,医生向受伤
部位喷射氯乙烷(CH CH Cl),并用药棉不断揉搓,运动员疼痛很快消除,重新投入
3 2
比赛.
请阅读信息后,回答:
(1)氯乙烷中C、H、Cl三种元素的原子个数比为 ;
(2)氯乙烷中C、H、Cl三种元素的质量比为 .
18.(1)探究小组欲从含有FeCl 、CuCl 的废液中回收金属铜,取一定量的废液样
3 2
品加入少量铁粉,一段时间后铁粉完全溶解,但未发现红色固体沉积.
出现这种现象的可能原因是 ;经查阅资料,铁粉在废液中发生两个化学反应:
①2FeCl +Fe═3FeCl ②CuCl +Fe═FeCl +Cu
3 2 2 2
(2)探究小组另取废液,向废液中加入一定且足量的铁粉至充分反应,溶液变为
浅绿色,过滤、干燥,称得固体沉积物质量与加入铁粉质量相等.
①固体沉积物质量与加入铁粉质量相等的原因是 ;
[来源:学科网ZXXK]
②经测定,反应后得到铜的质量为1.6g,其中,反应①消耗铁粉的质量是 ,
反应②消耗铁粉的质量是 (计算结果精确到0.1).2017 年山东省济宁市中考化学试卷
参考答案与试题解析
一、选择题(每小题只有一个选项符合题意,共16分)
1.化学与人类生产、生活密切相关,下列应用不涉及化学变化的是( )
A.小苏打用作糕 点膨松剂B . 生
石灰用作袋装食品 干燥剂
C.肥皂水用来区别硬水、软水 D.活性炭用来去除冰箱内异味
【考点】E3:化学变化和物理变化的判别.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、小苏打用作糕点膨松剂是利用碳酸氢钠受热分解生成碳酸钠、水和
二氧化碳,利用了化学变化,故A错;
B、生石灰用作袋装食品干燥剂,是利用生石灰与水反应生成氢氧化钙,利用了化
学变化,故B错;
C、肥皂水用来区别硬水、软水是利用加入肥皂水后,泡沫多的是软水,泡沫少的
是硬水,其中 包含着化学变化,故C错;
D、活性炭用来去除冰箱内异味,是利用活性炭的吸附性,没有新物质生成,不涉
及化学变化,故D正确.
故选D.
2.对下面几种物质的分类,正确的是( )
①CH ②P O ③MgO ④BaCl ⑤HNO ⑥NH HCO .
4 2 5 2 3 4 3
A.②③⑤属于氧化物 B.⑤⑥属于酸
C.④⑥属于盐 D.①⑥属于有机物
【考点】A9:常见的氧化物、酸、碱和盐的判别;AC:有机物与无机物的区别.
【分析】根据氧化物是指有两种元素组成且一种是氧元素的化合物;酸是指在电离时产生的阳离子全部是氢离子的化合物;盐是由金属离子(或铵根离子)和酸
根离子组成的化合物;有机物是含有碳元素的化合物,据此结合物质的组成进行
分析判断.
【解答】解:A、⑤HNO 含有三种元素,不属于氧化物,故选项错误.
3
B、⑥NH HCO 属于盐,不属于酸,故选项错误.
4 3
C、④BaCl 是由钡离子和氯离子构成的化合物,属于盐;⑥NH HCO 属于铵盐,故
2 4 3
选项正确.
D、⑥NH HCO 不属于有机物,故选项错误.
4 3
故选:C.
3.某同学为验证“分子是运动的”,设计了甲、乙、丙、丁四个实验.其中,能
达 到 目 的 是 ( )
A.甲、乙、丙 B.甲、乙、丁 C.甲、丙、丁 D.乙、丙、丁
【考点】34:化学实验方案设计与评价;BA:分子的定义与分子的特性.
【分析】本题可通过一段时间后,两个小烧杯中的液体没有直接接触,而其中一个
烧杯中的指示剂变色,来验证“分子是运动的”,进行分析判断.
【解答】解:甲中氨水具有挥发性,一段时间后,烧杯中的酚酞溶液变红色,说明氨
分子运动到了酚酞溶液中.
乙中浓硫酸不具有挥发性,一段时间后,无明显变化,不能说明分子是运动的.
丙中浓盐酸具有挥发性,一段时间后,烧杯中的石蕊溶液变红色,说明氯化氢分
子运动到了石蕊溶液中.
丁中浓硝酸具有挥发性,一段时间后,烧杯中的石蕊溶液变红色,说明硝酸分子
运动到了石蕊溶液中.故甲、丙、丁能达到目的.
故选:C.
4.分析下列反应所得结论中,正确的是( )
①CO+CuO Cu+CO ②2Al+Fe O Al O +2Fe
2 2 3 2 3
③2Na O +2CO ═2Na CO +O ④2H S+SO ═2H O+3S.
2 2 2 2 3 2 2 2 2
A.①②属于置换反应 B.③④属于复分解反应
C.③中氧元素化合价不变 D.都有单质生成
【考点】FA:反应类型的判定;A7:单质和化合物的判别;D6:有关元素化合价的计
算.
【分析】A、置换反应是单换单的反应;B、复分解反应是两种化合物相互交换成分
生成两种新的化合物的反应;C、单质化合价是零;D、单质是由一种元素组成的纯
净物.
【解答】解:A、置换反应是单换单的反应,①中反应物中没有单质,不属于置换反
应,故A错;
B、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,③④中
的生成物中都含有单质,复分解反应的反应物和生成物中都含有化合物,故B错
C、反应物中的氧元素化合价是﹣2价,生成物氧气中氧元素化合价是零,故C错;
D、单质是由一种元素组成的纯净物,由化学方程式可知都有单质生成,故D正确
故选D.
5.酸、碱、盐溶解性表为我们确定常见物质的溶解性提供了方便,下表是溶解性
表的一部分,结合表格和溶解度知识判断,下列说法不正确的是( )
常见酸、碱、盐的溶解性表(20℃)
OH﹣ NO ﹣ Cl﹣ SO 2﹣ CO 2﹣
3 4 3
Ca2+ 微 溶 溶 微 不
A.绘制表格的依据是物质的溶解度
B.常见物质一般可分为:溶、微溶和不溶
C.Ca(OH) 、CaSO 和CaCO 的溶解度都大于1g
2 4 3D.Ca2+、NO ﹣、Cl﹣三种离子在溶液中能大量共存
3
【考点】9Q:酸碱盐的溶解性;9R:离子或物质的共存问题.
【分析】A、根据表格是溶解性表的一部分,结合溶解性的确定方法,进行分析判断.
B、根据常见物质的溶解性,进行分析判断.
C、物质的溶解性是根据在20℃(室温)时的溶解度来划分的,溶解度大于10g,属
于易溶物质;溶解度大于1g,属于可溶物质;溶解度在0.01g~1g之间的,属于微
溶物质;小于0.01g的,属于难溶物质(习惯上叫不溶).
D、离子间若能互相结合成沉淀、气体或水,则离子不能共存.
【解答】解:A、表格是溶解性表的一部分,依据的是20℃酸、碱、盐的溶解度,故选
项说法正确.
B、常见物质的溶解性一般可分为:溶、微溶和不溶等,故选项说法正确.
C、Ca(OH)、CaSO 的溶解性是微溶,溶解度在0.01g~1g之间;CaCO 的溶解性是
2 4 3
不溶,溶解度小于0.01g,故选项说法错误.
D、Ca2+、NO ﹣、Cl﹣三种离子不能结合成沉淀、气体或水,且能在酸性溶液大量共
3
存,故选项说法正确.
故选:C.
6.下面对有关实验的设计与解释,不合理的是( )
实验内容 试剂与方法 结论与解释
[来源:学科网]
A 分离CaCO 和CaO 加水溶解、过滤 CaO溶于水
3
B 除去BaSO 中的 加稀盐酸、过滤 BaCO 溶于稀盐酸
4 3
BaCO
3
C 鉴别NaOH、Na SO 滴加酚酞试液 NaOH溶液显碱性
2 4
D 检验溶液中的Mg2+ 滴加NaOH溶 Mg(OH)不溶于水
2
液
A.A、 B.B、 C.C、 D.D、
【考点】34:化学实验方案设计与评价;8L:生石灰的性质与用途;9H:盐的化学性
质;9U:酸、碱、盐的鉴别;9V:常见离子的检验方法及现象.
【分析】A、根据氧化钙能与水反应生成氢氧化钙,碳酸钙难溶于水,进行分析判断.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质
反应;②反应后不能引入新的杂质.C、根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同
种物质反应的现象相同,则无法鉴别它们.
D、根据镁离子的检验方法,进行分析判断.
【解答】解:A、氧化钙能与水反应生成氢氧化钙,碳酸钙难溶于水,加水溶解、过
滤,能分离出碳酸钙,但不能得到氧化钙,故选项实验的设计不合理.
B、BaCO 能与稀盐酸反应生成氯化钡、水和二氧化碳,硫酸钡难溶于酸,再过滤,
3
能除去杂质且没有引入新的杂质,符合除杂原则,故选项实验的设计合理.
C、NaOH、Na SO 分别显碱性、中性,滴加酚酞试液,分别显红色、无色,可以鉴别,
2 4
故选项实验的设计合理.
D、检验溶液中的Mg2+,滴加NaOH溶液,会生成氢氧化镁白色沉淀,若观察到生
成白色沉淀,说明含有镁离子,故选项实验的设计合理.
故选:A.
7.一同学设计了两种由CuO→Cu的实验方案:
方案一:Zn H Cu 方案二:CuO CuSO Cu
2 4
大家认为方案二优于方案一,理由是:①节约能源 ②Cu产率高 ③产品纯净
④操作安全
其中,评价正确的是( )
A.①②③ B.①②④ C.①③④ D.②③④
【考点】34:化学实验方案设计与评价;85:金属的化学性质;93:酸的化学性质.
【分析】锌和稀硫酸反应生成硫酸锌和氢气,加热条件下,氧化铜和氢气反应生成
铜和水;
氧化铜和稀硫酸反应生成硫酸铜和水,锌和硫酸铜反应生成硫酸锌和铜.
【解答】解:方案二优于方案一,理由是:①节约能源,这是因为方案一中氢气还原
氧化铜时消耗能源;
②Cu产率高,这是因为 氢气还原
氧化铜时,还原出的铜覆盖在氧化铜表面,导致氧化铜不能完全反应;
③氧化铜被氢气还原时,部分氧化铜不能反应,得到的是混合物,而锌和硫酸铜
反应时也被是锌过量,得到的也是混合物,因此两种方法得到的都是混合物;④操作安全,这是因为反应过程不需要加热,操作更安全.
故选:B.
8.在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,
其发生反应的质量关系如图所示,读识如图并判断,下面推理合理的是( )
①反应速率:Mg>Fe>Zn
②反应生成氢气质量:Mg=Fe=Zn
③反应后溶液质量:Mg=Fe=Zn
④反应后溶液溶质质量分数:Mg<Fe<Zn.
A.①②B.③④C.①③D.②④
【考点】85:金属的化学性质.
【分析】根据镁和硫酸反应生成硫酸镁和氢气,铁和硫酸反应生成硫酸亚铁和氢
气,锌和硫酸反应生成硫酸锌和氢气,依据图象中的数据进行分析.
【解答】解:镁、锌、铁和硫酸反应的化学方程式为:
Mg+H SO =MgSO +H ↑
2 4 4 2
24 98 2
4.8g 0.4g
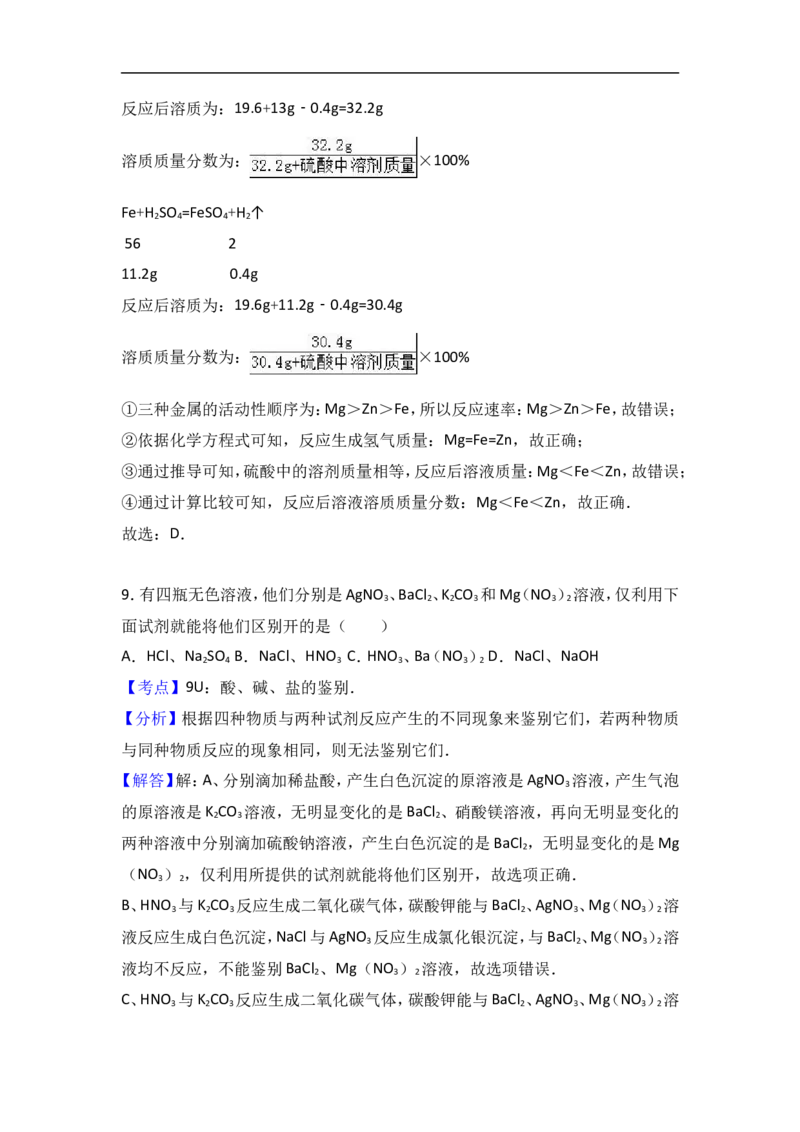
反应后溶质为:19.6g+4.8g﹣0.4g=24g
溶质质量分数为: ×100%
Zn+H SO =ZnSO +H ↑
2 4 4 2
65 98 2
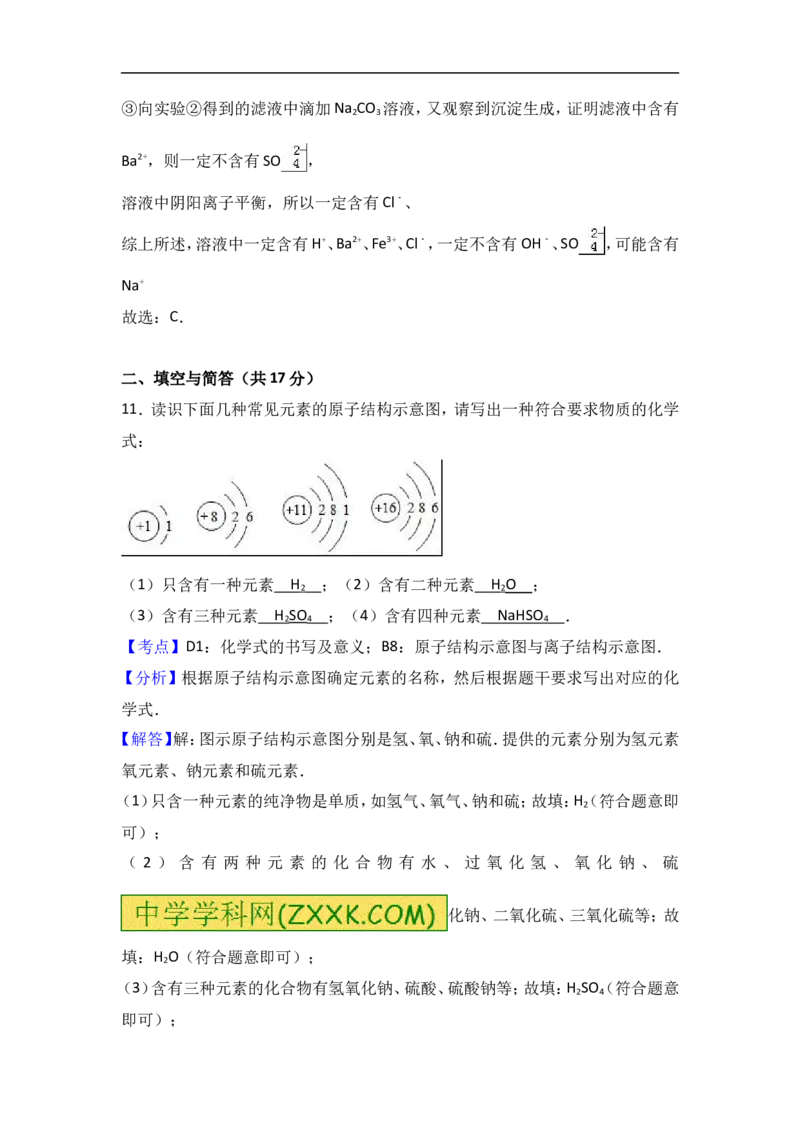
13g 0.4g反应后溶质为:19.6+13g﹣0.4g=32.2g
溶质质量分数为: ×100%
Fe+H SO =FeSO +H ↑
2 4 4 2
56 2
11.2g 0.4g
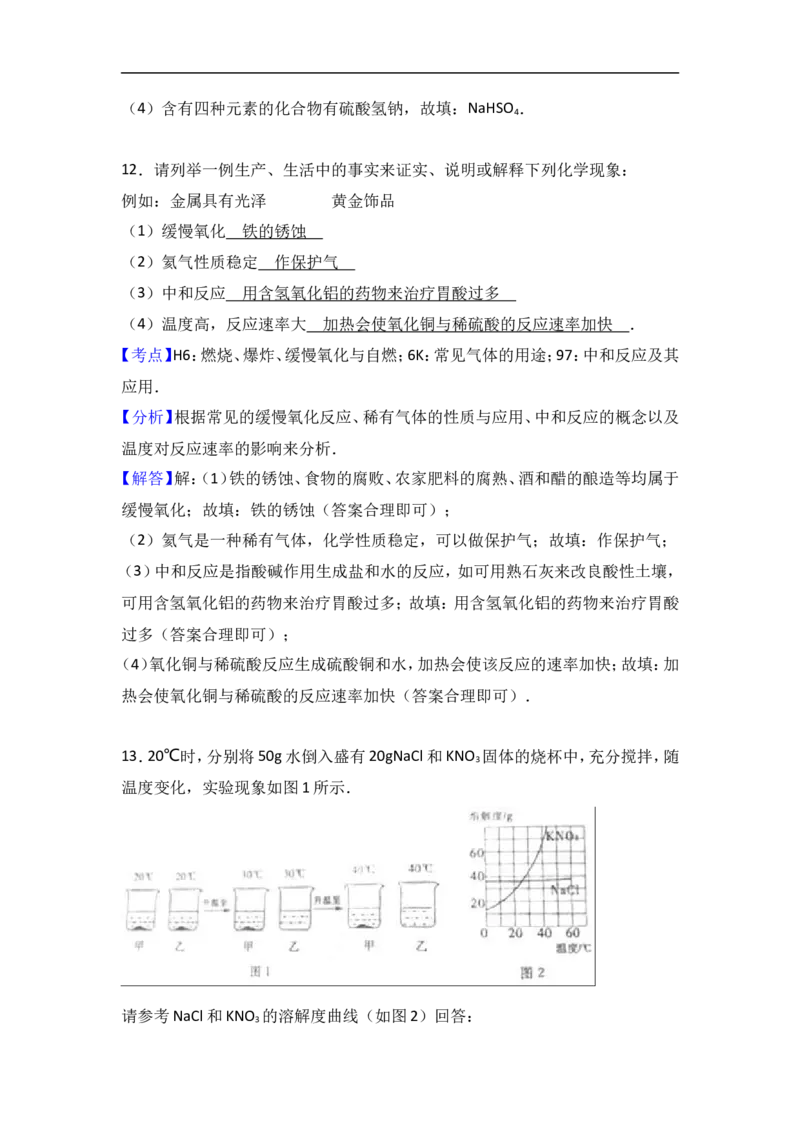
反应后溶质为:19.6g+11.2g﹣0.4g=30.4g
溶质质量分数为: ×100%
①三种金属的活动性顺序为:Mg>Zn>Fe,所以反应速率:Mg>Zn>Fe,故错误;
②依据化学方程式可知,反应生成氢气质量:Mg=Fe=Zn,故正确;
③通过推导可知,硫酸中的溶剂质量相等,反应后溶液质量:Mg<Fe<Zn,故错误;
④通过计算比较可知,反应后溶液溶质质量分数:Mg<Fe<Zn,故正确.
故选:D.
9.有四瓶无色溶液,他们分别是AgNO 、BaCl 、K CO 和Mg(NO )溶液,仅利用下
3 2 2 3 3 2
面试剂就能将他们区别开的是( )
A.HCl、Na SO B.NaCl、HNO C.HNO 、Ba(NO ) D.NaCl、NaOH
2 4 3 3 3 2
【考点】9U:酸、碱、盐的鉴别.
【分析】根据四种物质与两种试剂反应产生的不同现象来鉴别它们,若两种物质
与同种物质反应的现象相同,则无法鉴别它们.
【解答】解:A、分别滴加稀盐酸,产生白色沉淀的原溶液是AgNO 溶液,产生气泡
3
的原溶液是K CO 溶液,无明显变化的是BaCl 、硝酸镁溶液,再向无明显变化的
2 3 2
两种溶液中分别滴加硫酸钠溶液,产生白色沉淀的是BaCl ,无明显变化的是Mg
2
(NO ) ,仅利用所提供的试剂就能将他们区别开,故选项正确.
3 2
B、HNO 与K CO 反应生成二氧化碳气体,碳酸钾能与BaCl 、AgNO 、Mg(NO )溶
3 2 3 2 3 3 2
液反应生成白色沉淀,NaCl与AgNO 反应生成氯化银沉淀,与BaCl 、Mg(NO )溶
3 2 3 2
液均不反应,不能鉴别BaCl 、Mg(NO ) 溶液,故选项错误.
2 3 2
C、HNO 与K CO 反应生成二氧化碳气体,碳酸钾能与BaCl 、AgNO 、Mg(NO )溶
3 2 3 2 3 3 2液反应生成白色沉淀,Ba(NO )与BaCl 、AgNO 、Mg(NO )溶液均不反应,不能
3 2 2 3 3 2
鉴别,故选项错误.
D、分别滴加氯化钠溶液,能与氯化钠溶液产生白色沉淀的是AgNO 溶液,再将硝
3
酸银溶液分别滴加至另外三种溶液中,能产生白色沉淀是BaCl 、K CO ,无明显变
2 2 3
化的是Mg(NO ) 溶液;BaCl 、K CO 与NaOH溶液均不反应,无法鉴别BaCl 、
3 2 2 2 3 2
K CO ;故选项错误.
2 3
故选:A.
10.一澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl﹣、OH﹣和SO 离子的一种
或几种.为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成.继续滴加NaOH溶液至不再产
生沉淀为止,过滤;
③向实验②得到的滤液中滴加Na CO 溶液,又观察到沉淀生成.
2 3
分析实验得出的以下结论中,正确的是( )
A.溶液中一定含有H+、Ba2+、Cl﹣,一定不含有Na+、Fe3+、OH﹣、SO
B.溶液中一定含有H+、Ba2+、Fe3+、Cl﹣,一定不含有Na+、OH﹣和SO
C.溶液中一定含有H+、Ba2+、Fe3+、Cl﹣,一定不含有OH﹣、SO ,可能含有Na+
D.溶液中一定含有H+、Ba2+、Na+、Fe3+,一定不含有OH﹣、SO ,可能含有Cl﹣
【考点】9V:常见离子的检验方法及现象.
【分析】①溶液的pH=1,该溶液显酸性,不含有OH﹣;
②取部分样品溶液滴加NaOH溶液,有沉淀生成,一定含Fe3+;
③向实验②得到的滤液中滴加Na CO 溶液,又产生白色沉淀,证明滤液中含有
2 3
Ba2+.
【解答】解:①经测定,溶液的pH=1,该溶液显酸性,一定含有H+、一定不含有OH
﹣;
②取部分样品溶液滴加NaOH溶液,有沉淀生成.一定含Fe3+;③向实验②得到的滤液中滴加Na CO 溶液,又观察到沉淀生成,证明滤液中含有
2 3
Ba2+,则一定不含有SO ,
溶液中阴阳离子平衡,所以一定含有Cl﹣、
综上所述,溶液中一定含有H+、Ba2+、Fe3+、Cl﹣,一定不含有OH﹣、SO ,可能含有
Na+
故选:C.
二、填空与简答(共17分)
11.读识下面几种常见元素的原子结构示意图,请写出一种符合要求物质的化学
式:
(1)只含有一种元素 H ;(2)含有二种元素 H O ;
2 2
(3)含有三种元素 H SO ;(4)含有四种元素 NaHSO .
2 4 4
【考点】D1:化学式的书写及意义;B8:原子结构示意图与离子结构示意图.
【分析】根据原子结构示意图确定元素的名称,然后根据题干要求写出对应的化
学式.
【解答】解:图示原子结构示意图分别是氢、氧、钠和硫.提供的元素分别为氢元素
氧元素、钠元素和硫元素.
(1)只含一种元素的纯净物是单质,如氢气、氧气、钠和硫;故填:H(符合题意即
2
可);
( 2 ) 含 有 两 种 元 素 的 化 合 物 有 水 、 过 氧 化 氢 、 氧 化 钠 、 硫
化钠、二氧化硫、三氧化硫等;故
填:H O(符合题意即可);
2
(3)含有三种元素的化合物有氢氧化钠、硫酸、硫酸钠等;故填:H SO(符合题意
2 4
即可);(4)含有四种元素的化合物有硫酸氢钠,故填:NaHSO .
4
12.请列举一例生产、生活中的事实来证实、说明或解释下列化学现象:
例如:金属具有光泽 黄金饰品
(1)缓慢氧化 铁的锈蚀
(2)氦气性质稳定 作保护气
(3)中和反应 用含氢氧化铝的药物来治疗胃酸过多
[来源:Z*xx*k.Com]
(4)温度高,反应速率大 加热会使氧化铜与稀硫酸的反应速率加快 .
【考点】H6:燃烧、爆炸、缓慢氧化与自燃;6K:常见气体的用途;97:中和反应及其
应用.
【分析】根据常见的缓慢氧化反应、稀有气体的性质与应用、中和反应的概念以及
温度对反应速率的影响来分析.
[来源:Zxxk.Com]
【解答】解:(1)铁的锈蚀、食物的腐败、农家肥料的腐熟、酒和醋的酿造等均属于
缓慢氧化;故填:铁的锈蚀(答案合理即可);
(2)氦气是一种稀有气体,化学性质稳定,可以做保护气;故填:作保护气;
(3)中和反应是指酸碱作用生成盐和水的反应,如可用熟石灰来改良酸性土壤,
可用含氢氧化铝的药物来治疗胃酸过多;故填:用含氢氧化铝的药物来治疗胃酸
过多(答案合理即可);
(4)氧化铜与稀硫酸反应生成硫酸铜和水,加热会使该反应的速率加快;故填:加
热会使氧化铜与稀硫酸的反应速率加快(答案合理即可).
13.20℃时,分别将50g水倒入盛有20gNaCl和KNO 固体的烧杯中,充分搅拌,随
3
温度变化,实验现象如图1所示.
请参考NaCl和KNO 的溶解度曲线(如图2)回答:
3(1)分析实验现象,甲、乙烧杯中对应的物质分别是 氯化钠、硝酸钾 ,判断依
据是 甲物质的溶解度受温度变化影响较小 ;
(2)30℃时,甲、乙两溶液溶质质量分数的关系是:甲 < 乙(填“>“、”<
“或“=”)
【 考点】7N:固体溶解度曲线及其
作用;7R:溶质的质量分数.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和
溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从
而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:(1)20℃时,分别将50g水倒入盛有20gNaCl和KNO 固体的烧杯中,
3
充分搅拌,随温度升高,乙烧杯中的固体明显减少,甲烧杯中的固体变化不明显,
所以甲、乙烧杯中对应的物质分别是:氯化钠、硝酸钾;
(2)20℃时,分别将50g水倒入盛有20gNaCl和KNO 固体的烧杯中,充分搅拌,温
3
度升高到30℃,乙烧杯中的 固体
完全溶解,所以甲、乙两溶液溶质质量分数的关系是:甲<乙.
故答案为:(1)氯化钠、硝酸钾,甲物质的溶解度受温度变化影响较小;
(2)<.
14.氧化锌广泛用于皮肤病的治疗,工业氧化锌常含有少量杂质(CuO、FeO、SiO
2
等)不能直接使用.提纯、净化氧化锌的简易流程如图所示:
参考资料:SiO 既不溶于水也不与酸反应
2
(1)反应器Ⅰ中加入足量稀硫酸,充分反应后,生成硫酸盐的化学式为 ZnSO 、
4
CuSO 、 FeSO ;
4 4(2)残渣中除金属锌外,还有 S i
O 等 ;
2
(3)操作一、操作二和操作三采用的分离方法是 过滤 ;
(4)操作四发生反应的化学方程式为 ZnCO ZnO + CO ↑ .
3 2
【考点】AF:物质的相互转化和制备;85:金属的化学性质;93:酸的化学性质;G5:
书写化学方程式、.
【分析】(1)反应器Ⅰ中加入足量稀硫酸,稀硫酸和氧化锌反应生成硫酸锌和水,
和氧化铜反应生成硫酸铜和水,和氧化亚铁反应生成硫酸亚铁和水;
(2)残渣中除金属锌外,还有SiO 等;
2
(3)操作一、操作二和操作三采用的分离方法是过滤,通过过滤能够把固体和液
体分离;
(4)操作四中,高温条件下,碳酸锌分解生成氧化锌和二氧化碳.
【解答】解:(1)反应器Ⅰ 中加入
足量稀硫酸,充分反应后,生成的硫酸盐有ZnSO 、CuSO 、FeSO .
4 4 4
故填:ZnSO 、CuSO 、FeSO .
4 4 4
(2)残渣中除金属锌外,还有SiO 等.
2
故填:SiO 等.
2
(3)操作一、操作二和操作三采用的分离方法是过滤,通过过滤能够把固体和液
体分离.
故填:过滤.
(4)操作四中,高温条件下,碳酸锌分解生成氧化锌和二氧化碳,反应的化学方程
式为:ZnCO ZnO+CO ↑.
3 2
故填:ZnCO ZnO+CO ↑.
3 215.蛋白粉是由大豆蛋白、酪蛋白、乳清蛋白或上述几种蛋白混合制成的粉剂,其
用途是为营养不良或疾病导致蛋白质缺乏的人群补充营养.请回答:
(1)蛋白粉补充的营养成分是 蛋白质 ;
(2)市售劣质蛋白粉往往添加食用香精、淀粉,从颜色和味道都难以分辨.用少量
样品验证这种蛋白粉中含有淀粉的方法是 滴加碘液(碘酒) .
【考点】J4:食品、药品与健康食品中的有机营养素;JD:鉴别淀粉、葡萄糖的方法
与蛋白质的性质.
【分析】(1)根蛋白粉是由大豆蛋白、酪蛋白、乳清蛋白混合制成的粉剂进行分析;
(2)根据淀粉遇碘液变蓝色的特进行分析.
【解答】解:(1)蛋白粉补充的营养成分是蛋白质;
(2)淀粉的特性是淀粉遇碘液变蓝色,因此可以用碘液来检验食物中是否含有淀
粉.若碘液变蓝色,表明食物中有淀粉,若不变蓝色表明该食物中淀粉含量极少
或没有.因此,在检测食物中是否含有淀粉时,所用的方法是滴加碘液.
故答案为:(1)蛋白质;(2)滴加碘液(碘酒).
三、实验与探究(共11分)
16.(1)某实验小组利用如图实验装置探究二氧化碳的化学性质:
请根据实验装置和实验内容,回答下面问题:
①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑
浊,原因是 二氧化碳气体中混有氯化氢气体 ;可将二氧化碳先通过装置 C,再通入装置D,理由是 HC l + NaHCO =NaC l + H O + CO ↑ ( 用化学方程式表示);
3 2 2
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸
泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是
通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸能使紫色变红
色 ;结合上面实验,装置正确的
连接顺序是 ACB E (填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分
是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设
计实验验证小莉提供的食用碱样品是否含有氯化钠.
实验步骤 实验现象 结论与解释
1.取一定量的食用碱样品放入试管, 样品溶解 食用碱溶于水
加入蒸馏水、振荡
2 .向食用碱溶液的试管中,滴加几 有白色沉淀 还需要证明白色沉淀
滴硝酸银溶液,振荡 生成 不溶于稀硝酸
3 .向白色沉淀中滴加稀硝酸 沉淀不溶解 证明食用碱样品中含
有氯化钠
【考点】6X:探究二氧化碳的性质;G5:书写化学方程式、.
【分析】二氧化碳的化学性质有:既不能燃烧也不能支持燃烧,也不供给呼吸;能
与水反应生成碳酸;能与碱反应.将装置A生成的二氧化碳气体通入装置D未出
现浑浊,原因是:二氧化碳气体中混有氯化氢气体,可将二氧化碳先通过饱和碳
酸氢钠溶液,因为氯化氢气体和碳酸氢钠反应生成氯化钠和水和二氧化碳;首先
将二氧化碳通过石蕊溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿
润纸花,这样做的目的是:通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸
能使紫色变红色;结合上面实验,装置正确的连接顺序是:ACBE.食用碱的主要成
分是碳酸钠,可能含有少量氯化钠的实验步骤是:2.向食用碱溶液的试管中,滴
加几滴硝酸银溶液,振荡,有白色沉淀生成,还需要证明白色沉淀不溶于稀硝酸;
3.向白色沉淀中滴加稀硝酸,沉淀不溶解,证明食用碱样品中含有氯化钠.
【解答】解:(1)将装置A生成的二氧化碳气体通入装置D未出现浑浊,原因是:二氧化碳气体中混有氯化氢气体,可将二氧化碳先通过饱和碳酸氢钠溶液,因为氯
化氢气体和碳酸氢钠反应生成氯化钠和水和二氧化碳;首先将二氧化碳通过石蕊
溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目
的是:通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸能使紫色变红色;结
合上面实验,装置正确的连接顺序是:ACBE;故答案为:①二氧化碳气体中混有氯
化氢气体;C;HCl+NaHCO =NaCl+H O+CO ↑;②通过对比实验,证明二氧化碳和水
3 2 2
反应生成碳酸,碳酸能使紫色变红色;ACBE;
(2)食用碱的主要成分是碳酸钠,可能含有少量氯化钠的实验步骤是:2.向食用
碱溶液的试管中,滴加几滴硝酸银溶液,振荡,有白色沉淀生成,还需要证明白色
沉淀不溶于稀硝酸;3.向白色沉淀中滴加稀硝酸,沉淀不溶解,证明食用碱样品
中含有氯化钠;故答案为:2.向食用碱溶液的试管中,滴加几滴硝酸银溶液,振荡;
有白色沉淀生成;还需要证明白色沉淀不溶于稀硝酸;3.向白色沉淀中滴加稀硝
酸;沉淀不溶解;证明食用碱样品中含有氯化钠;
四、分析与计算(共6分)
17.观看足球比赛时,经常会看到绿茵场上运动员因拼抢摔倒受伤,医生向受伤
部位喷射氯乙烷(CH CH Cl),并用药棉不断揉搓,运动员疼痛很快消除,重新投入
3 2
比赛.
请阅读信息后,回答:
(1)氯乙烷中C、H、Cl三种元素的原子个数比为 2 : 5 : 1 ;
(2)氯乙烷中C、H、Cl三种元素的质量比为 4 8 : 1 0 : 7 1 .
【考点】D9:元素质量比的计算.
【分析】(1)根据氯乙烷的化学式来分析;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行
分析判断.
【解答】解:(1)由化学式可知,1个氯乙烷分子是由2个碳原子、5个氢原子和1个氯原子构成的,则氯乙烷中C、H、Cl三种元素的原子个数比为2:5:1;故填:2:
5:1;
(2)氯乙烷中碳、氢、氯三种元素的质量比为(12×2):(1×5):(35.5×1)=48:
10:71,故填:48:10:71.
18.(1)探究小组欲从含有FeCl 、CuCl 的废液中回收金属铜,取一定量的废液样
3 2
品加入少量铁粉,一段时间后铁粉完全溶解,但未发现红色固体沉积.
出现这种现象的可能原因是 加入的铁先和氯化铁反应,由于铁的量不足,没有
来得及和氯化铜反应 ;
经查阅资料,铁粉在废液中发生两个化学反应:
①2FeCl +Fe═3FeCl ②CuCl +Fe═FeCl +Cu
3 2 2 2
(2)探究小组另取废液,向废液中加入一定且足量的铁粉至充分反应,溶液变为
浅绿色,过滤、干燥,称得固体沉积物质量与加入铁粉质量相等.
①固体沉积物质量与加入铁粉质量相等的原因是 铁和氯化铁反应固体质量是
减少的,而铁和氯化铜反应固体质量是增大的,当两者变化量相同时则固体沉积
物质量和加入的铁质量相等 ;
②经测定,反应后得到铜的质量为1.6g,其中,反应①消耗铁粉的质量是 0.2 g
,反应②消耗铁粉的质量是 1.4 g (计算结果精确到0.1).
【考点】G6:根据化学反应方程式的计算.
【分析】(1)根据提示的反应以及对应的现象结合加入的少量铁粉等要素分析;
(2)①根据固体变化情况分析;
②根据给出的数据结合对应的化学方程式计算.
【解答】解:
(1)根据①2FeCl +Fe═3FeCl ②CuCl +Fe═FeCl +Cu以及对应的现象可知,铁参加
3 2 2 2
了反应,但是却没有得到铜,说明先发生的是第一个反应,结果铁的质量很少,导
致没机会和氯化铜反应,从而没有得到铜;
( 2 ) ① 2FeCl +Fe═ 3FeCl 这 个 方 程 式 时 固 体 减 少 的 反 应 ;
3 2
②CuCl +Fe═FeCl +Cu这个反应加入56g铁就生成64g的铜,是固体增加的反应.
2 2
当第一个的减少量和第二个的增加量相等时,固体沉积物质量与加入铁粉质量相
等.②设反应②消耗的铁的质量为y.反应②导致的固体增加量为a
CuCl +Fe═FeCl +Cu 固体增加量
2 2
56 64 64﹣56=8
y 1.6g a
= =
y=1.4g
a=0.2g
由于固体沉积物质量与加入铁粉质量相等,也就是铜的质量等于加入的全部的铁
的质量,所以1.6g﹣1.4g=0.2g.
或者根据第一个反应固体减少量为加入的铁的质量,等于第二个反应的固体增减
量0.2g,所以第一个反应消耗的铁的质量为0.2g.
故答案为:
(1)加入的铁先和氯化铁反应,由于铁的量不足,没有来得及和氯化铜反应;
(2)①铁和氯化铁反应固体质量是减少的,而铁和氯化铜反应固体质量是增大
的,当两者变化量相同时则固体沉积物质量和加入的铁质量相等;
②0.2g; 1.4g.2017年7月6日