文档内容
九年级化学下册结业测试(一)
〔满分:100分 限时:60分钟〕
一、选择题(每小题3分,共36分)
1.下列相关材料中不属于合成材料的是 ( )
A.钛合金眼镜框 B.橡胶弹力耳绳 C.聚丙烯纤维布
D.塑料防护眼镜
2.(2021湖南长沙中考)由袁隆平院士领衔的科研团队研发的杂交水稻双季亩产已经突
破1500公斤大关,意味着离袁老的“禾下乘凉梦”更近了一步。大米为我们提
供的营养素主要是 ( )
A.油脂 B.糖类 C.蛋白质
D.维生素
3.(2021四川成都中考)下列说法正确的是 ( )
A.血红蛋白在呼吸过程中起载体作用 B.油脂是供能物质,应大量
摄入
C.缺乏维生素C会引起夜盲症 D.缺锌会引起贫血
4.(2021独家原创试题)2021年7月13日,全球首台抗台风型漂浮式海上风电机组在
广东阳江海域成功安装,这是三峡集团牵头打造的又一海上风电“大国重器”。
建造风电机组的塔架用到了大量的钢铁,下列说法不正确的是 ( )
A.利用钢铁作塔架,是因为钢的硬度比铁大
B.铁制品在潮湿的空气中比在干燥的空气中更容易生锈
C.在铁制品表面涂漆可以防止金属的锈蚀
D.生锈的铁制品没有回收价值
5.(2021河南郑州二模)溶液在生产、生活及实验室中,都有着广泛的应用,下列有关
溶液的说法正确的是 ( )
A.具有均一、稳定性的液体一定是溶液 B.饱和溶液的浓度一定比不
饱和溶液的浓度大
C .配制溶液时,搅拌可以增大固体物质的溶解度 D.同种溶质的饱和溶液与不
饱和溶液可以相互转化
6.(2021北京昌平二模)如图1所示,在白色点滴板1~6的孔穴中,分别滴加2滴无
色酚酞溶液。下列说法不正确的是 ( )A.孔穴3起空白对照作用
B.因为孔穴2和5中是酸溶液,所以都为无色
C.孔穴6中溶液变为红色,说明碳酸钾溶液显碱性
D.再向孔穴1中滴加足量盐酸,溶液的颜色变为蓝色
7.(2021河南焦作二模)实验室用质量分数为6%的氯化钠溶液(密度为1.04g/cm3)配制
50g质量分数为3%的氯化钠溶液。下列说法正确的是 ( )
A.实验步骤:计算、称量、量取、溶解、装瓶 B.量取6%的氯化钠溶液时选
用100mL的量筒
C.需要加水的质量是50g D.量取水时,仰视读数,会
使配制的氯化钠溶液浓度偏小
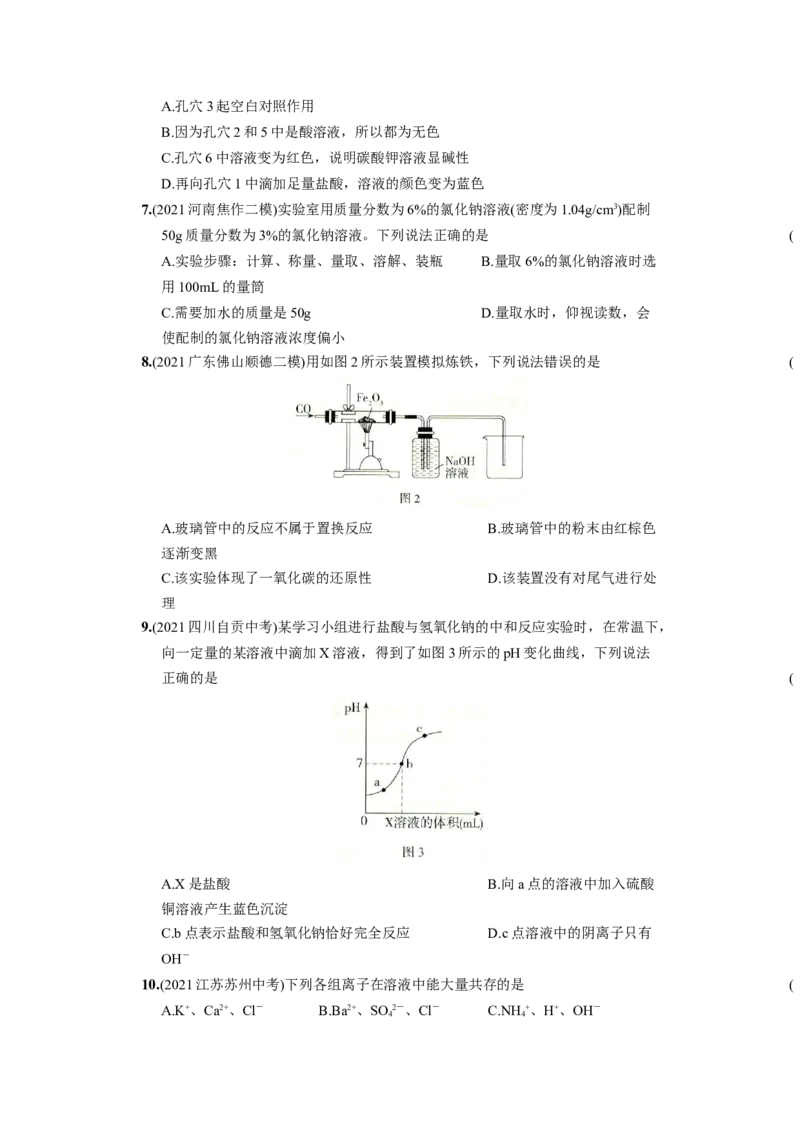
8.(2021广东佛山顺德二模)用如图2所示装置模拟炼铁,下列说法错误的是 ( )
A.玻璃管中的反应不属于置换反应 B.玻璃管中的粉末由红棕色
逐渐变黑
C.该实验体现了一氧化碳的还原性 D.该装置没有对尾气进行处
理
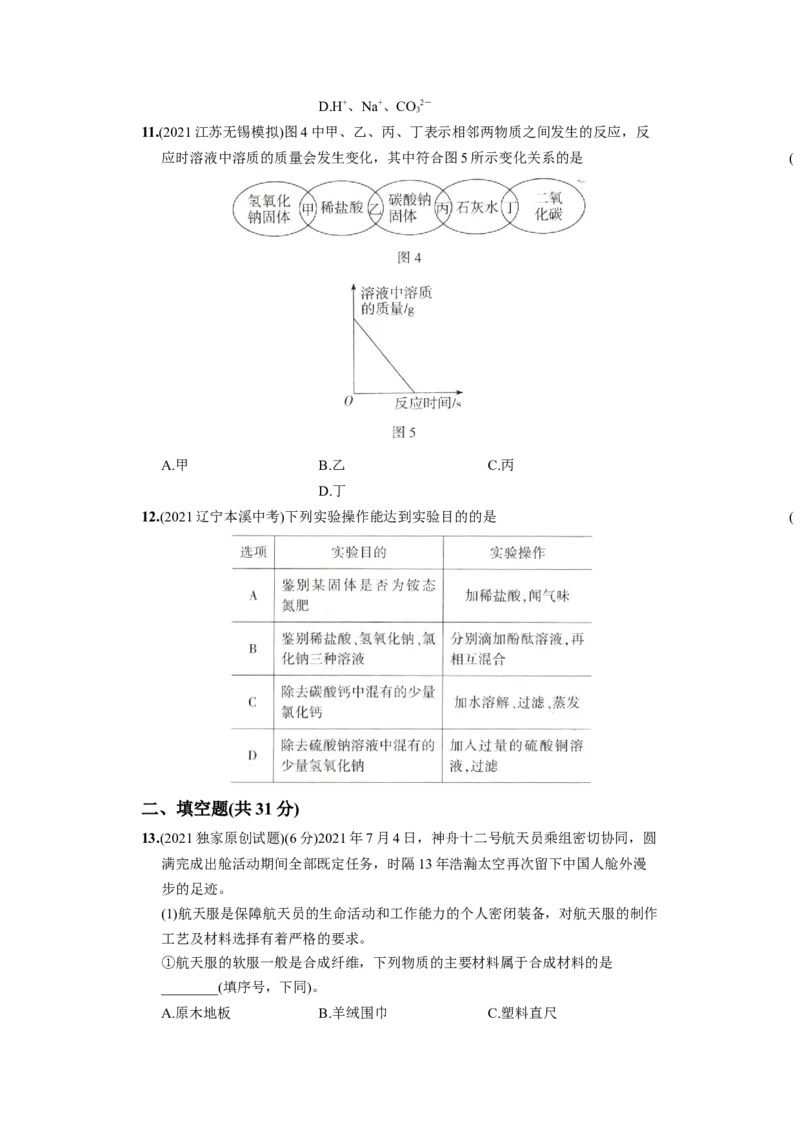
9.(2021四川自贡中考)某学习小组进行盐酸与氢氧化钠的中和反应实验时,在常温下,
向一定量的某溶液中滴加X溶液,得到了如图3所示的pH变化曲线,下列说法
正确的是 ( )
A.X是盐酸 B.向a点的溶液中加入硫酸
铜溶液产生蓝色沉淀
C.b点表示盐酸和氢氧化钠恰好完全反应 D.c点溶液中的阴离子只有
OH-
10.(2021江苏苏州中考)下列各组离子在溶液中能大量共存的是 ( )
A.K+、Ca2+、Cl- B.Ba2+、SO 2-、Cl- C.NH+、H+、OH-
4 4D.H+、Na+、CO2-
3
11.(2021江苏无锡模拟)图4中甲、乙、丙、丁表示相邻两物质之间发生的反应,反
应时溶液中溶质的质量会发生变化,其中符合图5所示变化关系的是 ( )
A.甲 B.乙 C.丙
D.丁
12.(2021辽宁本溪中考)下列实验操作能达到实验目的的是 ( )
二、填空题(共31分)
13.(2021独家原创试题)(6分)2021年7月4日,神舟十二号航天员乘组密切协同,圆
满完成出舱活动期间全部既定任务,时隔13年浩瀚太空再次留下中国人舱外漫
步的足迹。
(1)航天服是保障航天员的生命活动和工作能力的个人密闭装备,对航天服的制作
工艺及材料选择有着严格的要求。
①航天服的软服一般是合成纤维,下列物质的主要材料属于合成材料的是
________(填序号,下同)。
A.原木地板 B.羊绒围巾 C.塑料直尺D.玻璃水杯
②航天服的壳架一般是铝钛合金,壳架上还涂上了抗热涂层。下列不属于铝钛合
金材料性质的是________。
A.密度小 B.硬度大 C.耐腐蚀
D.熔点低
(2)航天飞行会导致航天员骨钙丢失、肌肉萎缩、红细胞数量减少,要针对航天员
的生理指数改变对膳食中的营养素进行适当调整。
①钙是人体必需的________(填“常量”或“微量”)元素,幼儿及青少年缺钙会
患________和发育不良。
②下列航天食品中富含蛋白质的是________,人体通过食物获得的蛋白质,在胃肠
道内与水发生反应,生成________。
A.新鲜水果 B.米饭 C.牛肉
D.蘑菇
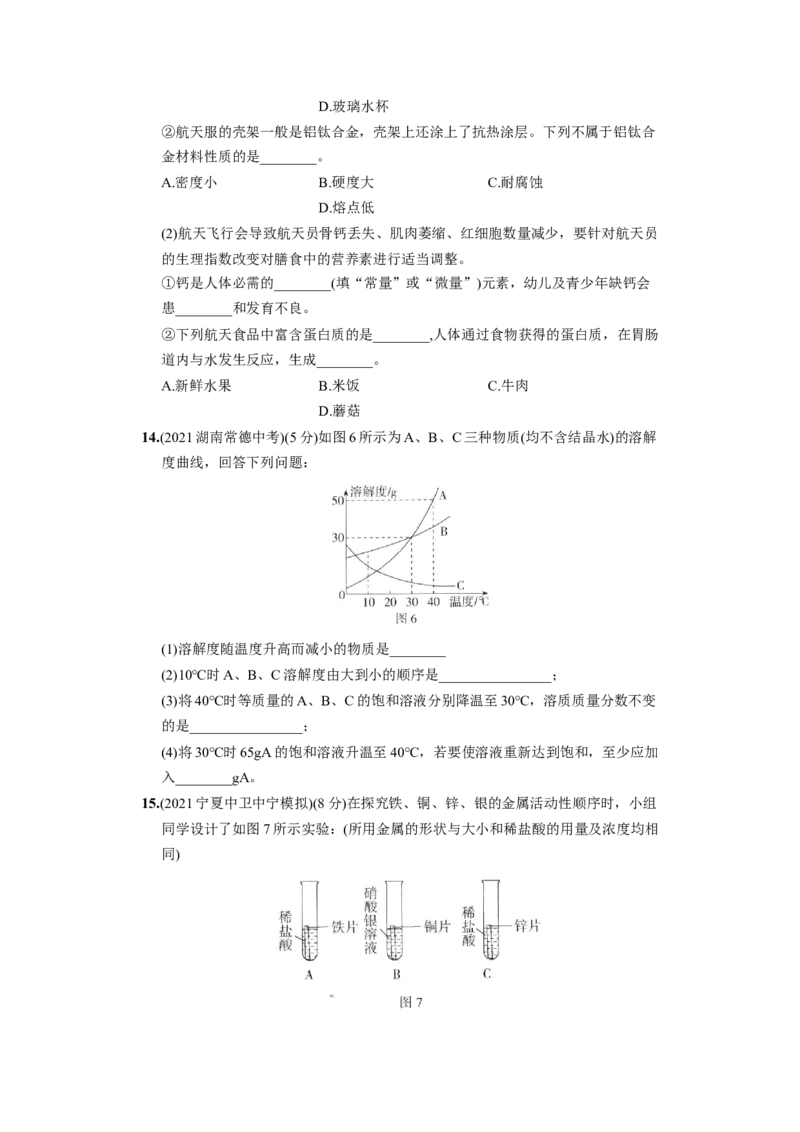
14.(2021湖南常德中考)(5分)如图6所示为A、B、C三种物质(均不含结晶水)的溶解
度曲线,回答下列问题:
(1)溶解度随温度升高而减小的物质是________
(2)10℃时A、B、C溶解度由大到小的顺序是________________;
(3)将40℃时等质量的A、B、C的饱和溶液分别降温至30℃,溶质质量分数不变
的是________________;
(4)将30℃时65gA的饱和溶液升温至40℃,若要使溶液重新达到饱和,至少应加
入________gA。
15.(2021宁夏中卫中宁模拟)(8分)在探究铁、铜、锌、银的金属活动性顺序时,小组
同学设计了如图7所示实验:(所用金属的形状与大小和稀盐酸的用量及浓度均相
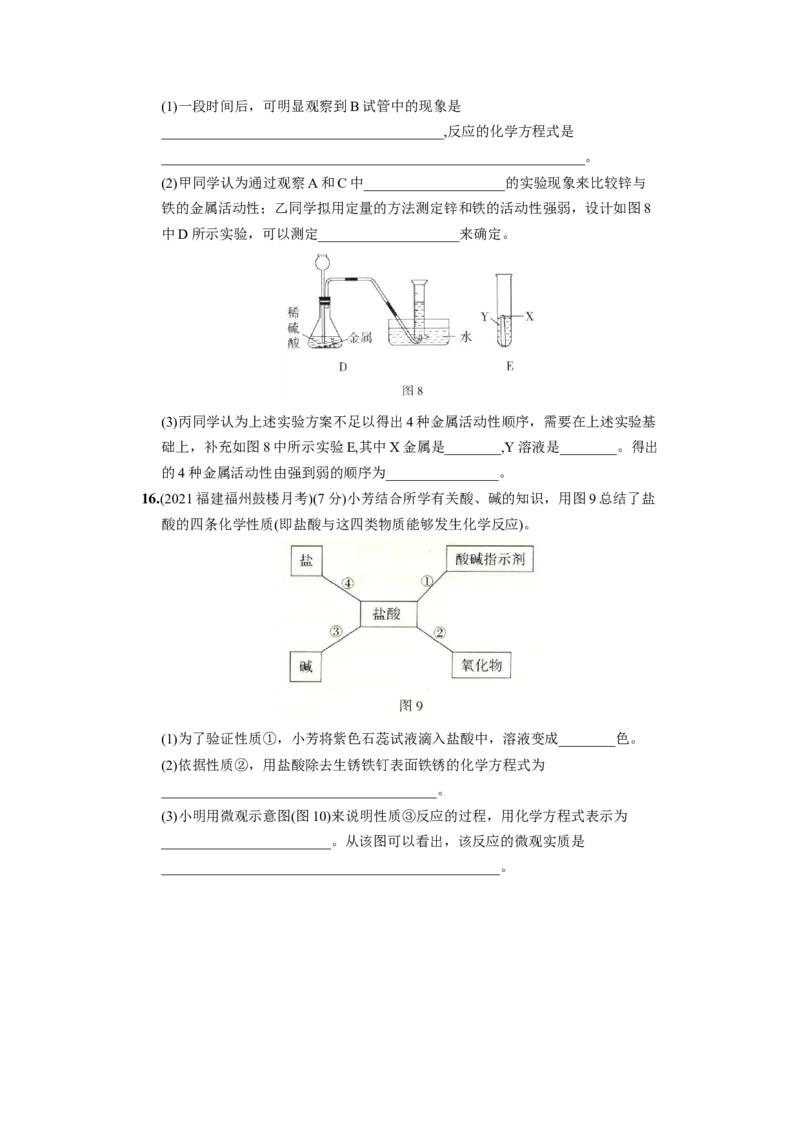
同)(1)一段时间后,可明显观察到B试管中的现象是
________________________________________,反应的化学方程式是
____________________________________________________________。
(2)甲同学认为通过观察A和C中____________________的实验现象来比较锌与
铁的金属活动性;乙同学拟用定量的方法测定锌和铁的活动性强弱,设计如图8
中D所示实验,可以测定____________________来确定。
(3)丙同学认为上述实验方案不足以得出4种金属活动性顺序,需要在上述实验基
础上,补充如图8中所示实验E,其中X金属是________,Y溶液是________。得出
的4种金属活动性由强到弱的顺序为________________。
16.(2021福建福州鼓楼月考)(7分)小芳结合所学有关酸、碱的知识,用图9总结了盐
酸的四条化学性质(即盐酸与这四类物质能够发生化学反应)。
(1)为了验证性质①,小芳将紫色石蕊试液滴入盐酸中,溶液变成________色。
(2)依据性质②,用盐酸除去生锈铁钉表面铁锈的化学方程式为
_______________________________________。
(3)小明用微观示意图(图10)来说明性质③反应的过程,用化学方程式表示为
________________________。从该图可以看出,该反应的微观实质是
________________________________________________。(4)为了验证性质④反应能够发生,你选择的物质是________。
A.Na CO B.CuSO C.NaCl
2 3 4
17.(2021四川德阳中考)(5分)为探究某化工厂固体废物的成分,以便回收有用物质,
除掉有害物质。已知固体废物的主要成分是NaCl 还可能含有NaCO、KSO 、
2 2 3 2 4
NH NO 、MgSO 、FeCl ,通过以下探究回答下列问题。
4 3 4 3
(1)气体乙的化学式为________________。
(2)无色溶液A中存在的阴离子有________________。
(3)反应生成气体甲的化学方程式为________________________________________。
(4)原固体废物中一定存在的物质有____________________。
三、实验探究题(共20分)
18.(2021四川自贡中考改编)(12分)在我市贡井区、大安区交界处有个地名叫“石灰
窑”,生产生石灰有悠久的历史。某校化学实验室一瓶装满生石灰的塑料试剂瓶
已经膨胀破裂,该校化学兴趣小组的同学在化学老师的指导下,对该生石灰取样
开展了以下探究活动:
【提出问题】生石灰样品的成分是什么?
【猜想与假设】生石灰样品的成分可能是CaO、Ca(OH) 和CaCO 中的一种或几
2 3
种。
【设计实验】兴趣小组设计如下实验进行探究。【反思评价】(4)经过讨论,发现通过(2)不能得出样品中一定含有Ca(OH) ,理由
2
是________________________
______________________________________________________________________
__________。
(5)通过小组合作,最后得出样品中肯定含有CaO和CaCO ,可能含有Ca(OH) 。
3 2
请写出生成CaCO 的化学方程式:
3
____________________________________________________________。
【应用交流】(6)生石灰要________保存。
【拓展延伸】(7)兴趣小组在实验室制取二氧化碳气体的发生装置中连接上压强传
感器如图12,测得实验过程中试管内气体压强变化情况如图13。下列说法正确
的是________(填字母)。
A.ab段试管中液面逐渐上升 B.bc段石灰石与盐酸脱离接
触
C.c点的对应操作是打开弹簧夹
19.(2021四川广安中考)(8分)中国医学著作博大精深,许多化学物质很早就出现在了我国医书中。如李时珍的《本草纲目》中就有绿矾(FeSO ·7H O)的相关记载。绿
4 2
矾又名皂矾、青矾,性酸、凉、无毒,主要药用功能是除湿、解毒、收敛、止血。
(1)请写出铁与稀硫酸反应的化学方程式:
________________________________________。
(2)某实验小组欲用久置的硫酸亚铁溶液制备绿矾(FeSO ·7H O)晶体,小明同学提
4 2
出该硫酸亚铁溶液可能变质了,于是进行了以下探究活动:
【查阅资料】①FeSO 易被空气中的氧气氧化成Fe (SO ) 而变质。
4 2 4 3
②Fe2+在溶液中呈浅绿色,Fe3+在溶液中呈黄色。
③Fe3+的检验:向含Fe3+的溶液中滴加无色的KSCN(硫氰化钾)溶液,溶液会变为
血红色。
【猜想与假设】猜想Ⅰ.该硫酸亚铁溶液没有变质。
猜想Ⅱ.该硫酸亚铁溶液已经变质。
【设计实验并验证】
【实验拓展1】下列各组物质在溶液中能大量共存,且形成无色溶液的是
________。
A.CuSO 、NH Cl、Ba(OH) B.FeSO 、NaSO 、KCl
4 4 2 4 2 4
C.FeCl 、NaOH、HCl D.NaCl、MgSO 、KNO
3 4 3
【实验拓展2】该实验小组继续查阅资料得知,单质铁能与硫酸铁溶液反应生成
硫酸亚铁。于是向上述久置的硫酸亚铁溶液中加入过量铁粉,写出其中的化学方
程式:________________________________________。
四、计算题(共13分)
20.(2021山东菏泽中考)(8分)孔雀石主要成分是碱式碳酸铜[Cu (OH) CO],另外还含
2 2 3
有少量的SiO 等杂质(杂质不与硫酸发生反应)。某化学兴趣小组为测定孔雀石中
2
Cu (OH) CO 的含量,进行如下实验。取30g孔雀石样品,粉碎后放入烧杯中,
2 2 3
将200g稀硫酸分成四等份,分四次加入烧杯中,测出每次完全反应后烧杯内物
质的总质量。实验数据记录如下:
请完成:(1)Cu (OH) CO+2H SO =2CuSO +CO ↑+________。
2 2 3 2 4 4 2
(2)该反应中生成气体的总质量是________g。
(3)所用稀硫酸的溶质质量分数。(写出计算过程)
21.(2021湖北黄石中考)(5分)取一氧化碳还原氧化铜实验的固体残留物20g,向其中加
入稀硫酸,剩余固体质量与加入稀硫酸质量关系如图14所示,请回答下列问题。
(1)所取固体残留物中铜的质量为________g。
(2)求a点处溶液中溶质的质量分数(写出计算过程)。《参考答案及解析》
结业测试(一)
一、选择题
1.A 钛合金属于金属材料;合成橡胶、聚丙烯纤维及塑料都属于合成材料。
2.B 大米中富含淀粉,淀粉属于糖类。
3.A 血红蛋白在呼吸过程中能携带氧气,起载体作用;油脂是人体重要的供能物质,
但大量摄入易引起肥胖和心脑血管疾病等,应控制摄入量;缺乏维生素A会引起
夜盲症,缺乏维生素C会引起坏血病;缺铁会引起贫血。
4.D 钢是铁的合金,硬度比铁大,利用钢铁作塔架,利用了钢的硬度比铁大;铁制
品在潮湿的空气中比在干燥的空气中更容易生锈;在铁制品表面涂漆,可以阻止
铁与氧气、水等接触,防止金属的锈蚀;回收生锈的铁制品,可以节约资源,保
护环境。
5.D 具有均一、稳定性的液体不一定是溶液,如水是纯净物,不是溶液;饱和溶
液的浓度不一定比不饱和溶液的浓度大;搅拌只能加快溶解速率,不能增大固体
物质的溶解度;同种溶质的饱和溶液与不饱和溶液,可以通过改变溶质、溶剂的
质量及温度等,实现相互转化。
6.D 孔穴3起空白对照作用,A说法正确;孔穴2和5中是酸溶液,无色酚酞溶液
遇酸不变色,仍为无色,说法正确;无色酚酞溶液遇碱性溶液变红,孔穴6中溶
液变为红色,说明碳酸钾溶液显碱性,C说法正确;再向孔穴1中滴加足量盐酸,
盐酸能与石灰水反应生成氯化钙和水,溶液的颜色变为无色,D说法错误。
7.D 用质量分数为6%的氯化钠溶液配制50g质量分数为3%的氯化钠溶液,其操作
步骤是计算、量取、混匀、装瓶,A说法错误。设需要6%的氯化钠溶液的体积
为x,根据稀释前后溶质的质量不变,则1.04g/cm3×x×6%=50g×3%,解得
x≈24.0cm3=24.0mL,则量取6%的氯化钠溶液时选用25mL的量筒,B说法错误。
需要加水的质量为50g-=25g,C说法错误。用量筒量取水时,仰视读数,会造成实
际量取的水的体积偏大,则使溶质质量分数偏小,D说法正确。
8.D 玻璃管中的反应是一氧化碳与氧化铁反应生成铁和二氧化碳,该反应的反应物
均为化合物,不属于置换反应;玻璃管中的粉末由红棕色逐渐变黑;一氧化碳夺
取了氧化铁中的氧,体现了一氧化碳的还原性;该装置中盛氢氧化钠溶液的洗气
瓶能收集一氧化碳。
9.C 由题图可知,开始溶液的pH小于7,随着反应的进行,pH逐渐增大,说明该
实验是将氢氧化钠溶液滴到盐酸中,故X溶液是氢氧化钠溶液;a点时,pH小于
7,盐酸还未完全反应,溶液中的溶质为氯化钠和氯化氢,加入硫酸铜溶液,不会产生沉淀;b点时,pH=7,氢氧化钠和盐酸恰好完全反应;c点时,pH>7,此时
氢氧化钠过量,溶液中的溶质为氯化钠和氢氧化钠,阴离子有氢氧根离子和氯离
子。
10.A B项,Ba2+和SO 2-结合生成BaSO 沉淀,不能大量共存;C项,NH +和OH-
4 4 4
结合生成氨气和水,H+和
OH-结合生成水,不能大量共存;D项,H+和CO2-结合生成二氧化碳和水,不
3
能大量共存。
11.D 氢氧化钠固体与稀盐酸反应生成氯化钠和水,随着反应的进行,溶液中溶质
的质量逐渐增加。稀盐酸与碳酸钠固体反应生成氯化钠、水和二氧化碳,随着反
应的进行,溶液中溶质的质量逐渐增加。碳酸钠固体与石灰水反应生成碳酸钙沉
淀和氢氧化钠,随着反应的进行,溶液中溶质的质量增加。二氧化碳与石灰水反
应生成碳酸钙沉淀和水,随着反应的进行,溶液中溶质的质量逐渐减小,石灰水
完全反应时减小至.故选D。
12.B A项,铵态氮肥能与碱反应生成氨气,氨气具有刺激性气味,故应加熟石灰
混合研磨,闻气味;B项,分别滴加酚酞溶液,使酚酞溶液变红的是氢氧化钠溶
液,不变色的是稀盐酸和氯化钠溶液,将另外两种溶液分别滴加到变红的氢氧化
钠溶液中,能使溶液由红色变为无色的是稀盐酸,则剩下的一种溶液是氯化钠溶
液;C项,碳酸钙难溶于水,氯化钙溶于水,加水溶解、过滤、洗涤、干燥才能
得到碳酸钙;D项,加入过量的硫酸铜溶液,硫酸铜和氢氧化钠反应生成氢氧化
铜沉淀和硫酸钠,过滤后虽然除去了杂质,但是引入了新的杂质硫酸铜。
二、填空题
13.[答案]
(1)①C ②D
(2)①常量 佝偻病 ②C 氨基酸
[解析]
(1)①原木地板是用木材制成的,木材属于天然材料;羊绒围巾是用羊绒制成的,
羊绒属于天然有机高分子材料;塑料直尺是用塑料制成的,塑料属于三大合成材
料之一;玻璃水杯是用玻璃制成的,玻璃属于无机非金属材料。②铝钛合金具有
密度小、硬度大、耐腐蚀、耐高温等性质。
(2)①钙是人体必需的常量元素,幼儿及青少年缺钙会患佝偻病和发育不良。②新
鲜水果中富含维生素;米饭中富含淀粉,淀粉属于糖类;牛肉中富含蛋白质;蘑
菇中富含维生素。人体通过食物获得的蛋白质,在胃肠道内与水发生反应,生成
氨基酸。
14.[答案]
(1)C (2)B>C>A (3)C (4)10
[解析]
(1)由溶解度曲线可知,C物质的溶解度随温度升高而减小。(2)10℃时,三种物质的溶解度由大到小的顺序是B>C>A。
(3)将40℃时等质量的A、B、C的饱和溶液分别降温至30℃,C的溶解度变大,
C的溶液变为不饱和溶液,但溶质质量与溶剂质量都不变,故溶质质量分数也不
变;A、B的溶解度减小,有晶体析出,溶质质量分数均变小。
(4)30℃时,A的溶解度为30g,65g A的饱和溶液中溶质的质量为65g×=15g,水的质
量为65g-15g=50g,升温至40℃时,溶解度变为50g,50g水最多能溶解溶质的质量
为50g×=25g,所以若要使溶液重新达到饱和,应加入A的质量为25g-15g=10g。
15.[答案]
(1)铜片的表面覆盖了一层银白色物质,溶液由无色变为蓝色
Cu+2AgNO =Cu(NO )+2Ag
3 3 2
(2)产生气泡的速率 相同时间内收集气体的体积(或收集相同体积的气体所用的
时间)
(3)铁(合理即可) CuSO 溶液(合理即可) 锌、铁、铜、银
4
[解析]
(1)铜与硝酸银溶液反应生成硝酸铜和银,一段时间后,可观察到铜片的表面覆盖
了一层银白色物质,溶液由无色变为蓝色。
(2)通过观察A和C中产生气泡的速率,可以比较锌与铁的金属活动性。
(3)由A、C实验证明锌的活动性大于铁,由B实验证明铜的活动性大于银,需设
计实验证明铁和铜的活动性,药品可以用金属铁与硫酸铜溶液,也可以用金属铜
与硫酸亚铁溶液等。金属活动性由强到弱的顺序为锌、铁、铜、银。
16.[答案]
(1)红
(2)6HCl+Fe O=2FeCl +3H O
2 3 3 2
(3)HCl+NaOH=NaCl+H O 氢离子和氢氧根离子结合生成水分子
2
(4)A
[解析]
(1)盐酸显酸性,能使紫色石蕊试液变红。
(2)铁锈的主要成分为氧化铁,与盐酸反应生成氯化铁和水。
(3)由题图可以看出,氢氧化钠和盐酸反应生成氯化钠和水,该反应的微观实质是
氢离子和氢氧根离子结合生成水分子。
(4)反应④是盐与盐酸的反应,氯化钠、硫酸铜都不与盐酸反应;碳酸钠和盐酸反
应生成氯化钠、水和二氧化碳。
17.[答案]
(1)CO
2
(2)Cl-、CO2-、NO -、OH-
3 3
(3)NH NO +NaOH=NaNO +NH↑+H O
4 3 3 3 2
(4)氯化钠、碳酸钠、硝酸铵(或NaCl、NaCO、NH NO )
2 3 4 3[解析]固体废物中加水溶解,加适量氯化钡溶液,生成白色沉淀和无色溶液,则
固体废物一定不含氯化铁;白色沉淀中加入足量稀硝酸,得到气体乙和无色溶液
C,Na CO、KSO 、MgSO 与氯化钡反应均能产生白色沉淀,但只有碳酸钠与氯
2 3 2 4 4
化钡反应生成的碳酸钡沉淀能溶于硝酸,则固体废物中一定不含KSO 、MgSO ,
2 4 4
一定含NaCO;碳酸钡与稀硝酸反应生成硝酸钡、水和二氧化碳,故气体乙为
2 3
二氧化碳;固体废物中加入过量的氢氧化钠溶液,生成有刺激性气味的气体甲和
无色溶液A,气体甲为氨气,则固体废物中一定含NH NO ;又知固体废物的主要
4 3
成分为氯化钠,所以原固体废物中一定存在的物质有氯化钠、碳酸钠、硝酸铵。
(2)固体废物中含氯化钠、碳酸钠、硝酸铵,加入过量的氢氧化钠溶液,硝酸铵与
氢氧化钠反应生成硝酸钠、氨气和水,则无色溶液A中含有氯化钠、碳酸钠、硝
酸钠、氢氧化钠,故存在的阴离子有Cl-、CO2-、NO -、OH-。
3 3
三、实验探究题
18.[答案]
(1)有CaO
(2)酚酞试液
(3)有气泡产生
(4)CaO与水反应生成Ca(OH) ,使溶液显碱性
2
(5)Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
(6)密闭
(7)BC
[解析]
(1)氧化钙和水反应放热,烧杯壁发热,说明样品中含有氧化钙。
(2)碱性溶液能使酚酞试液变红,根据实验现象和实验结论,可知滴入的是酚酞试
液。
(3)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故观察到的现象是有气泡产
生。
(4)由于CaO与水反应生成Ca(OH) ,也能使溶液显碱性,所以通过
2
(2)不能得出样品中一定含有Ca(OH) 的结论。
2
(5)氢氧化钙与二氧化碳反应生成碳酸钙和水。
(6)生石灰易与水反应,要密闭保存。
(7)ab段压强增大,说明气体发生装置内气体增多,此时弹簧夹处于夹紧状态,
试管中液面下降,A错误;bc段压强达到稳定,此时反应停止,固液分离,B正
确;c点之后压强减小,说明气体从发生装置中排出,因此c点对应操作是打开
弹簧夹,C正确。
19.[答案]
(1)Fe+HSO =FeSO +H ↑
2 4 4 2
(2)【设计实验并验证】【实验拓展1】D
【实验拓展2】Fe+Fe (SO )=3FeSO
2 4 3 4
[解析]
(1)铁与稀硫酸反应生成硫酸亚铁和氢气。
(2)【设计实验并验证】由于试管中溶液变成血红色,根据查阅到的资料可知,加
入的是KSCN溶液;溶液中检测到铁离子的存在,所以该硫酸亚铁溶液已经变质。
【实验拓展1】A项中,硫酸铜溶液呈蓝色,且硫酸铜能和氢氧化钡反应生成沉
淀,氯化铵能和氢氧化钡反应生成氨气,不能大量共存;B项中,硫酸亚铁溶液
呈浅绿色;C项中,氯化铁能和氢氧化钠反应生成红褐色沉淀,NaOH能和HCl
反应生成NaCl和HO,不能大量共存;D项中,三种物质间彼此不反应,能大量
2
共存,且不存在有色离子。
【实验拓展2】硫酸铁和铁反应生成硫酸亚铁。
四、计算题
20.[答案]
(1)3H O
2
(2)5.5
(3)解:设前两次使用的100g稀硫酸中溶质质量为x。
Cu (OH) CO+2H SO =2CuSO +CO ↑+3H O
2 2 3 2 4 4 2 2
2×98 44
x 4.4g
= x=19.6g
稀硫酸的溶质质量分数×100%=19.6%
答:所用稀硫酸的溶质质量分数为19.6%。
[解析]
(1)根据质量守恒定律,化学反应前后原子的数目、种类不变,可知化学方程式为
Cu (OH) CO+2H SOO =2CuSO +CO ↑+3H O。
2 2 3 2 4 4 2 2
(2)第一次、第二次加入稀硫酸后生成气体的质量各为2.2g,第三次为1.1g,生成气
体的总质量为
2.2g+2.2g+1.1g=5.5g。
(3)结合表格数据可知,前两次加入的稀硫酸完全反应,可计算前两次消耗硫酸的
质量,从而可以计算稀硫酸中溶质的质量分数。
21.[答案]
(1)17.5
(2)解:a点处表示氧化铜和稀硫酸恰好反应,设生成硫酸铜的质量为x。CuO+HSO =CuSO +H O
2 4 4 2
80 160
2.5g x
= x=5g
a点处溶液中溶质的质量分数为×100%=12.5%
答:a点处溶液中溶质的质量分数为12.5%。
[解析]
(1)由图示知,一氧化碳还原氧化铜实验的固体残留物中有铜和氧化铜,氧化铜和
稀硫酸反应,铜和稀硫酸不反应,剩余的固体质量为铜的质量。
(2)a点处表示氧化铜和稀硫酸恰好反应,溶液中的溶质为硫酸铜,根据氧化铜与
硫酸反应的化学方程式,由氧化铜的质量可以计算硫酸铜的质量,从而可以计算
a点处溶液中溶质的质量分数。