文档内容
2024 年中考第一次模拟考试(山西卷)
化 学
(考试时间:70分钟 试卷满分:70分)
第I卷 选择题(共20分)
一、选择题(本大题共10个小题,每个小题2分,共20分。在每小题给出的4个选项中,只有1个选项
符合题目要求,请选出并在答题卡上将该选项涂黑)
1.山西广胜寺飞虹塔由于塔身五彩斑斓如雨后彩虹,故名“飞虹塔”,是五座佛主舍利塔和中国现存四
座古塔之一。飞虹塔的塔刹为宝瓶式铜制,项轮为铁铸,流苏为绿色琉璃。用铜制作比用铁制作的优点是
A.密度大 B.不易生锈 C.储量丰富 D.耐高温
【答案】B
【解析】铜的金属性比铁的弱,故而常温条件下,铜制品不易腐蚀。
2.2023年10月,我国科学家成功构建255个光子的量子计算原型机“九章三号”,再度刷新光量子信息
技术世界纪录,加快了我国硅芯片的换道超车。下列物质中硅的化合价为+2的是
A.Si B.SiO C.SiO D.NaSiO
2 2 3
【答案】C
【解析】已知氧元素的化合价为-2价,根据化合物中的各种元素的化合价代数为 0,可知SiO中硅元素的
化合价为+2。
3.2023年6月7日是第5个世界食品安全日,我国粮食安全宣传周的活动主题为“践行大食物观,保障粮
食安全”。 “红烧鱼”在这道美味佳肴中,鱼肉富含的营养元素主要是
A.水 B.蛋白质 C.油脂 D.糖类
【答案】B
【解析】肉类富含的营养素是蛋白质。
4.宋代诗人陆游在《村居书喜》中写道:“花气袭人知昼暖”闻到花香说明
A.分子的数目增多 B.分子的质量很小
C.分子之间有间隔 D.分子在不断运动
【答案】D
【解析】由于分子在不停息的、不断运动,故而能“闻到宅香”
5.2023冬季甲流高发。帕拉米韦(化学式CHN O)是一种抗病毒药,适用于流感病毒引起的流行性感冒。
4 4
下列关于它的表述正确的一项是
A.属于氧化物 B.属于混合物
C.由四种元素组成 D.含有2个氮分子【答案】C
【解析】A.氧化物的概念可知,由俩种元素组成,其中一种元素是氧元素。故A错。
A. C H NOP为纯净物,混合物没有化学式。
9 14 5 4
B. C H NOP化学式可知,其由由五种元素组成
9 14 5 4
C. 一个C H NOP分子由9个C、14个H、5个N、4个O、1个P原子构成。
9 14 5 4
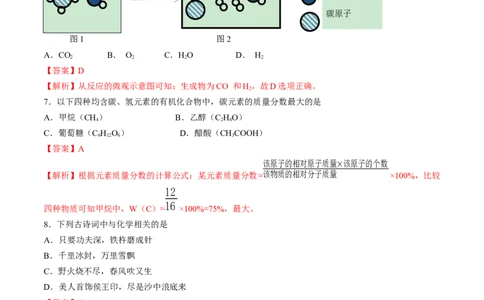
6.在一定条件下,图1的微粒之间可发生如下化学反应,反应后生成图2中的新微粒用符号表示正确的一
个选项是
一定条件
氢原子
甲 氧原子
乙 碳原子
图1 图2
A.CO B. O C.HO D. H
2 2 2 2
【答案】D
【解析】从反应的微观示意图可知:生成物为CO 和H,故D选项正确。
2
7.以下四种均含碳、氢元素的有机化合物中,碳元素的质量分数最大的是
A.甲烷(CH) B.乙醇(C HO)
4 2 6
C.葡萄糖(C H O) D.醋酸(CHCOOH)
6 12 6 3
【答案】A
该原子的相对原子质量×该原子的个数
【解析】根据元素质量分数的计算公式:某元素质量分数= 该物质的相对分子质量 ×100%,比较
12
16
四种物质可知甲烷中,W(C)= ×100%=75%,最大。
8.下列古诗词中与化学相关的是
A.只要功夫深,铁杵磨成针
B.千里冰封,万里雪飘
C.野火烧不尽,春风吹又生
D.美人首饰侯王印,尽是沙中浪底来
【答案】C
【解析】A、B、D选项中没有新物质生成,属于物理变化,故错误。C. 野火烧不尽,春风吹又生,燃
烧有新物质生成,属于化学变化,故C正确。
9.空气是地球上的重要组成部分,也是人类赖以生存的必要元素之一。人类对空气的认识经历了漫长的
历程,测定空气中氧气的含量实验操作如下,正确的一项是
A.可以用木炭代替红磷
B.实验前夹紧止水夹,冷却至室温后打开止水夹
C.实验之前需要预先在集气瓶底放少量水,目的是防止集气瓶炸裂
D.点燃红磷后将燃烧匙缓慢伸入集气瓶内【答案】B
【解析】A.木炭燃烧后生成了二氧化碳,不能用木炭代替红磷,故A项错误。B.实验前夹紧止水夹,防
止漏气。冷却至室温后打开止水夹,测定能准确,故B项正确。C.五氧化二磷会污染空气,且能溶于水,
实验之前需要预先在集气瓶底放少量水,目的是减少对空气的污染,故C项错误。D.点燃红磷后将燃烧
匙立即伸入集气瓶内,缓慢会造成测量结果不准确,故D项错误。
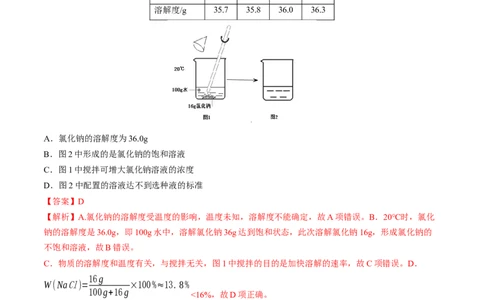
10.农业上常用浓度为16%的氯化钠溶液来选种。如图为配置氯化钠选种液的过程,结合图表信息,有关
分析正确的一项是
氯化钠在不同温度时的溶解度
温度/℃ 0 10 20 30
溶解度/g 35.7 35.8 36.0 36.3
A.氯化钠的溶解度为36.0g
B.图2中形成的是氯化钠的饱和溶液
C.图1中搅拌可增大氯化钠溶液的浓度
D.图2中配置的溶液达不到选种液的标准
【答案】D
【解析】A.氯化钠的溶解度受温度的影响,温度未知,溶解度不能确定,故A项错误。B.20℃时,氯化
钠的溶解度是36.0g,即100g水中,溶解氯化钠36g达到饱和状态,此次溶解氯化钠16g,形成氯化钠的
不饱和溶液,故B错误。
C.物质的溶解度和温度有关,与搅拌无关,图1中搅拌的目的是加快溶解的速率,故C项错误。D.
16g
W(NaCl)= ×100%≈13.8%
100g+16g
<16%,故D项正确。
第Ⅱ卷 非选择题(共50分)
二、工程、技术应用题(本大题共2个小题。化学方程式每空2分,其余每空1分,共16分。)
(10分)【化学与工程】
“科技是国之利器,国家赖之以强,企业赖之以赢,人民生活赖之以好。”我国持续推动科技创新,在航
海、工业、农业、生活方面硕果累累。运用所学化学知识,分析图文信息,解答下题的相关问题。火箭发射 绿色能源 特色种植业 杏花村酒
11.2023年10月26日,搭载着神州十七号载人飞船的长征二号运载火箭在酒泉卫星发射中心点火发射。
长征二号的壳体主要是钛合金而不用不锈钢,其原因是________________(写一条即可)。钛合金属于什
么材料__________。
12.中国石化“万吨级天然气制乙炔成套技术”即将出口乌兹别克斯坦,为当地提供绿色能源技术“中国
方案”。天然气的主要成分为_____(写化学式);天然气燃烧的化学方程式为_________________________。
13.振兴乡村,发展农业,化肥起着重要的作用。葵花种植时施有机肥为主,写出你知道的两种复合肥
_______、_______(写化学式)。
14.山西汾酒的酿造具有悠久的历史,它以高粱为原料,经过发酵、蒸馏等数十道工序制作而成。发酵、
蒸馏的过程中发生的变化______(填“相同”或“不相同”),蒸馏可以提高酒精的浓度,蒸馏过程中所
发生变化的微观实质是________;在日常生活中使用酒精时,对其安全,需要提出的要求是_______(合
理即可)。
【答案】11.熔点高(或密度小) 金属
12.CH
4
13.KNO KHPO (合理即可)
3 2 4
14.不同 酒精分子间隔先变大后变小 不要靠近热源、远离明火(合理即可)
(6分)【化学与技术】
15.乙醇(C HO)能替代传统的化石燃料,减少对环境的污染,具有高能效和应用广泛的特点。农业有
2 6
机废料中含有大量的纤维素等化合物,被认为是制乙醇的潜在原料之一。用农业有机废料生产乙醇的主要
流程如图所示。请分析流程,回答有关问题。
(1)常见的农业有机废料是__________(写一种)。
(2)经检测自来水为硬水,即自来水中含有大量的 Ca2+(或Mg2+)。鉴别软硬水可以向水样中滴加
__________,生活中硬水软化的办法为_________。
(3)水解反应的最适PH值为4.5,水解罐材质应具备_____________性质(写一种)。
(4)写出燃料乙醇燃烧的化学方程式_____________________________________________。
【答案】(1)玉米秸秆(合理即可)
(2)肥皂水 煮沸
(3)耐酸性(4)
【解析】(1)常见的农业有机废料是玉米秸秆(合理即可)
(2)鉴别软硬水可以向水样中滴加肥皂水,若产生的泡沫少,浮渣较多,则为硬水。若产生大量的泡沫,
浮渣较少,则为软水。生活中硬水软化的办法为煮沸。
(3)水解反应的最适PH值为4.5,水解池中溶液呈现酸性,故水解罐材质应具备耐酸性的特质。
(4)乙醇燃烧的化学方程式为 。
三、科普阅读题(本大题共1个小题。化学方程式每空2分,其余每空1分,共7分。)
16.(7分)
碳酸氢钠
碳酸氢钠,俗称小苏打,是一种白色结晶性粉末,无臭,味咸,易溶于水。它是一种重要的无机化工原料,
在许多领域都有广泛的应用。
在常温下性质稳定,但在高温下易分解为碳酸钠、水和二氧化碳。碳酸氢钠呈碱性,可以中和酸性物质,
故而在医疗领域,碳酸氢钠可以用于治疗胃酸过多;环境保护领域,它可以中和酸性废水,减少对环境的
污染。在食品加工中,碳酸氢钠被用作膨松剂、发酵剂和酸度调节剂,它可以使食品变得蓬松、柔软,并
调节食品的酸碱度。除此之外,公共场所常用的泡沫灭火器是用硫酸铝和碳酸氢钠两种溶液反应的化学方
程式为:Al (SO )+6NaHCO=2Al(OH) +3Na SO +6X。
2 4 3 3 3 2 4
需要注意的是,碳酸氢钠在使用时应遵循相关的安全规定和使用说明,避免过度使用或误用。
(1)碳酸氢钠具有的物理性质是______________。(写一条)
(2)在医疗领域,碳酸氢钠可以用于治疗胃酸过多的化学方程式为____________________。反应的微观
实质为_________________________________。
(3)使用泡沫灭火器时,硫酸铝和碳酸氢钠发生反应的化学方程式中X的化学式为______
(4)碳酸氢钠溶液的pH_______(填“大于7”“等于7”或“小于7”)。
(5)为确保其安全性和有效性,在存储和运输过程中,应注意采取_______________和防火等措施。
【答案】(1)白色结晶性粉末,无臭,味咸,易溶于水
(2)NaHCO +HCl=NaCl+H O+CO↑ 氢离子和碳酸根离子反应生成水分子和二氧化碳分子
3 2 2
(3)CO
2
(4)大于7
(5)防潮或防晒(合理即可)
【解析】
(1)颜色、状态、溶解性、气温为物理性质。碳酸氢钠具有的物理性质是白色结晶性粉末,无臭,味咸,
易溶于水
(2)胃酸为盐酸,故而在医疗领域,碳酸氢钠可以用于治疗胃酸过多的化学方程式为
NaHCO +HCl=NaCl+H O+CO↑
3 2 2
(3)化学反应遵循质量守恒定律,即化学反应前后原子的种类、数目、质量不变,结合题意X的化学计量为6,推出X的化学式为CO
2
(4)碳酸氢钠溶液呈碱性,故其溶液的pH大于7
(5)题意可知,碳酸氢钠易溶于水,应防潮,在高温下易分解为碳酸钠、水和二氧化碳应防晒
四、物质性质及应用题(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分。)
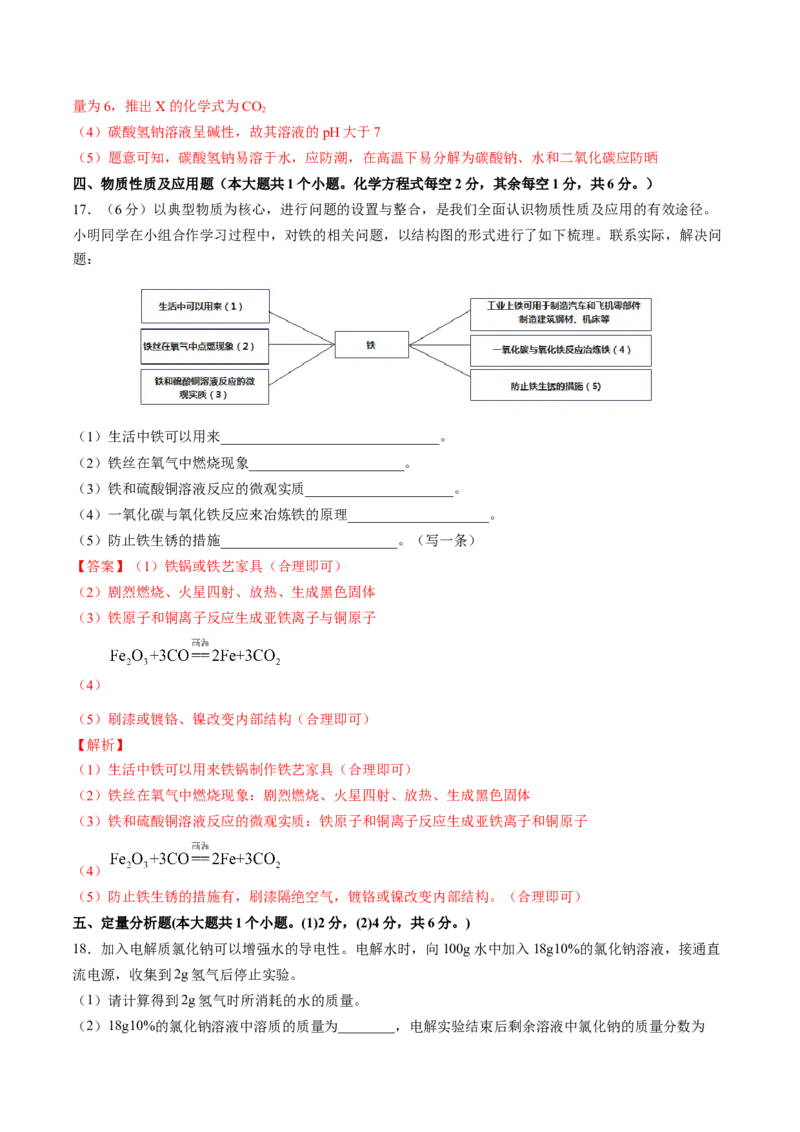
17.(6分)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。
小明同学在小组合作学习过程中,对铁的相关问题,以结构图的形式进行了如下梳理。联系实际,解决问
题:
(1)生活中铁可以用来_______________________________。
(2)铁丝在氧气中燃烧现象______________________。
(3)铁和硫酸铜溶液反应的微观实质_____________________。
(4)一氧化碳与氧化铁反应来冶炼铁的原理____________________。
(5)防止铁生锈的措施_________________________。(写一条)
【答案】(1)铁锅或铁艺家具(合理即可)
(2)剧烈燃烧、火星四射、放热、生成黑色固体
(3)铁原子和铜离子反应生成亚铁离子与铜原子
(4)
(5)刷漆或镀铬、镍改变内部结构(合理即可)
【解析】
(1)生活中铁可以用来铁锅制作铁艺家具(合理即可)
(2)铁丝在氧气中燃烧现象:剧烈燃烧、火星四射、放热、生成黑色固体
(3)铁和硫酸铜溶液反应的微观实质:铁原子和铜离子反应生成亚铁离子和铜原子
(4)
(5)防止铁生锈的措施有,刷漆隔绝空气,镀铬或镍改变内部结构。(合理即可)
五、定量分析题(本大题共1个小题。(1)2分,(2)4分,共6分。)
18.加入电解质氯化钠可以增强水的导电性。电解水时,向100g水中加入18g10%的氯化钠溶液,接通直
流电源,收集到2g氢气后停止实验。
(1)请计算得到2g氢气时所消耗的水的质量。
(2)18g10%的氯化钠溶液中溶质的质量为________,电解实验结束后剩余溶液中氯化钠的质量分数为_____。
【答案】(1)解:设得到2g氢气时所消耗的水的质量为x。
36 4
x 2g
36 4
=
x 2g
x=18g
答:得到2g氢气时所消耗的水的质量为18g。
(2)1.8g 1.8%
【解析】18g10%的氯化钠溶液中溶质的质量为:m(NaCl)=m(氯化钠溶液)×10%=1.8g。
电解实验结束后剩余溶液中氯化钠的质量分数为:w(NaCl)= 1.8%。
六、实验探究题(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分。)
【实验设计】
19.(6分)同学们完成了如图所示的实验后,对相关问题进行思考和讨论。请结合图文信息完成下列任
务。
实验1 实验2
(1)实验方法:
①利用装置A、F制备并收集氧气,收集并进行验满。验满的方法为______________________
②取2支试管A、B,分别加入3g氯化钾,然后向A试管加入20℃的水10mL,向B试管加入60℃的水
10mL,充分振荡,观察现象。
(2)实验原理:实验1中反应的化学方程式为_______________________________________
(3)实验现象:
①带火星的木条复燃。
②A试管中氯化钾部分溶解,B试管中氯化钾全部溶解。
(4)实验结论:
①带火星的木条复燃,说明氧气具有_____________。
②对比A、B试管中氯化钾的溶解现象,说明影响物质溶解性的一个因素为_______________。
(5)实验后,接下来必须要做的事情是整理实验台,完善实验报告,离开实验室。问题与交流:为保证实验1的成功,你认为需要注意的是____________________。(写一条)
【答案】(1)将带火星的木条放在b口处,若带火星的木条复燃,则说明已经收集满。
(2)
(4)①助燃性 ②温度
(5)检查装置的气密性(合理即可)
【解析】(1)氧气的密度比空气大,故用长进短出来收集气体,将带火星的木条放在b口处,若带火星的
木条复燃,则说明已经收集满。
(2)装置类型为固固加热型,且试管口没有放棉花,因此推断发生的反应为:
(4)①带火星的木条复燃,说明氧气具有助燃性 ②由实验2可看出氯化钾的溶解性与温度有关,温度越
高,其在水中的溶解能力越强。
(5)有气体生成或有气体参与的反应,都应该检查装置的气密性(合理即可)
【科学探究】
20.(9分)燃烧是人类,最早利用的化学反应之一,燃烧与人类的生活以及社会的发展有着密切的联系。
某校实践小组同学们在老师的组织下,带着极大的兴趣以“探究燃烧的奥妙”展开了如下项目化的学习。
任务一:调查燃烧的价值
【咨询交流】同学们通过上网搜索、图书馆翻阅资料、社区调查、学习小组讨论等方式,列举出了许多生
活中对燃烧的利用_________________________(写一条)。煤油的主要成分为十二烷(化学式:C H ),
12 26
写出十二烷在氧气中充分燃烧生成两种氧化物的化学方程式 。
任务二:学习科学探究的一般过程
任务三:探究燃烧的条件
【提出问题】燃烧是否需要①可燃物、②与氧气接触、③可燃物达到燃烧所需要的最低温度?
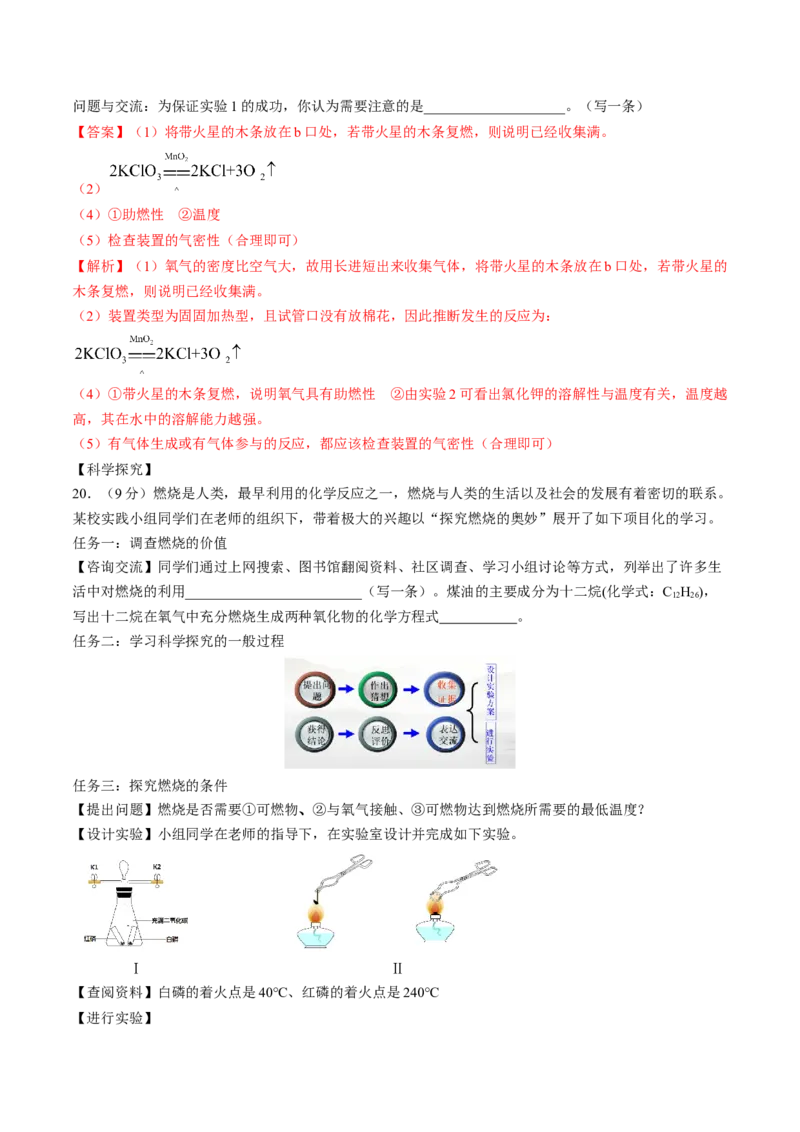
【设计实验】小组同学在老师的指导下,在实验室设计并完成如下实验。
Ⅰ Ⅱ
【查阅资料】白磷的着火点是40℃、红磷的着火点是240℃
【进行实验】实验步骤 实验现象 实验结论
步骤1:按如图Ⅱ用坩埚钳夹持石头、木 石头不能燃烧,木条可以燃烧 物质燃烧需要满足的条
条分别置于酒精灯上的点燃 件:
______________________
步骤2:室温下,按如图Ⅰ组装装置,装 白磷和红磷均不能燃烧 物质燃烧需要满足的条
入药品。将锥形瓶浸入80℃的热水中 件:
______________________
步骤3:取出锥形瓶,恢复至室温并擦 白磷和红磷均不能燃烧 物质燃烧需要满足的条
干;打开止水夹K 和 K₂,从K 处缓慢 件:
1 1
通入约200mL氧气,再关闭K 和K 可燃物达到燃烧所需要的
1 2
最低温度
步骤4:将锥形瓶再次浸入80℃的热水 ________________________
中,观察现象
【反思评价】
(1)物质燃烧一般需要同时满足以上三个条件。
(2)从环保角度分析,装置Ⅰ的优点:__________________________。
(3)小明同学提出可以通过提高和降低可燃物的着火点达到灭火的目的。你是否认同小明的观点,请说
明理由__________________________________________________。
任务四:设计调控燃烧的宣传活动
活动主题 远离火灾,珍爱生命 活动对象 小区居民
时间地点 11.9日上午、安全小区 活动形式 演讲、小品表演、张贴广告或海
报
活动目的 ①通过张贴海报引导人们懂得火灾的危险性,敲响安全防范的警钟。
②通过主题演讲、小品表演等方式普及灭火知识。
③活动总结、撰写实践报告。
【成果分享】同学们通过各种方式,学到了灭火的原理和调控燃烧的重要性。在项目化学习的
成果报告中,同学们提到国内外一些煤田因发生煤层自燃造成资源浪费和环境污染的现象。若煤层一旦发
生自燃现象,请你给出一条合理的灭火建议:____________________________。
【答案】【咨询交流】供暖(合理即可);
【进行实验】物质具有可燃性(可燃物);可燃物与氧气接触;白磷燃烧,产生大量的白烟,放热,且红
磷不燃烧;
【反思评价】(2)白磷燃烧会产生有毒的五氧化二磷,装置密封可以防止五氧化二磷逸出污染大气。
(3)不认同,着火点是物质的一种属性,一般不随外界条件的改变而改变。
【成果分享】取土填埋(合理即可)
【解析】【咨询交流】生活中对燃烧的利用如供暖、做饭、照明等(合理即可);
【进行实验】石头不能燃烧,木条可以燃烧说明物质燃烧需要满足的条件:物质具有可燃性(可燃物);
因为锥形瓶内充满二氧化碳,白磷和红磷均不能燃烧,说明物质燃烧需要满足的条件:可燃物与氧气接触;冲入100ml氧气,浸入80℃的热水,温度达到了白磷燃烧的着火点,所以白磷会燃烧产生大量的白烟,放
热,温度没有达到红磷的着火点240℃,所以不能燃烧;
【反思评价】(2)白磷燃烧会产生有毒的五氧化二磷,装置密封可以防止五氧化二磷逸出污染大气。
(3)不认同,着火点是物质的一种属性,一般不随外界条件的改变而改变。
【成果分享】灭火只需要破坏燃烧条件中的一个即可,可以通过取土填埋等隔绝空气的方法灭火(合理即
可)