文档内容
2024 年中考第二次模拟考试(山西卷)
化 学
(满分70分,化学与物理考试时间共150分钟)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 K 39
第Ⅰ卷 选择题(共20分)
一、选择题(本大题共10个小题。每小题2分,共20分。在每小题给出的4个选项中,只有
1个选项符合题目要求。)
1.【新情境·社会热点】2023年6月28日,十四届全国人大常委会第三次会议决定,将8月15日设立为全
国生态日,以推动生态文明建设。下列做法有利于生态保护的是 ( )
A.燃放烟花爆竹 B.直接排放废水 C.深埋有害垃圾 D.开展植树造林
【答案】D
【解析】燃放烟花爆竹、直接排放废水、深埋有害垃圾都会造成环境污染。植树造林有助于气候调节、水
土保持、生物多样性维护,提升生活环境和经济效益。
2.体现山西地域特色“上党堆锦”是国家级非物质文化遗产之一,它“纸做底、棉为胎、绸为面、施以
色、堆成画”,其中棉属于下列选项中的 ( )
A.金属材料 B.天然纤维 C.合成材料 D.复合材料
【答案】B
【解析】A. 金属材料:通常具有良好的导电性和导热性,强度高,耐腐蚀性好,但可能较重和易受磁场
影响。
B. 天然纤维:来源于植物(如棉、麻等)或动物,具有良好的生物降解性和吸湿性,但通常强度较低,
易受潮和生物侵蚀。
C. 合成材料:由人工合成,具有较高的机械性能和耐腐蚀性,可根据需要设计制造,但可能存在环境污
染和可持续性问题。
D. 复合材料:由两种或更多种材料组合而成,具有各种特性的优点,如高强度、轻质、耐腐蚀性等,但
制造成本较高,维修较困难。
故棉属于天然纤维。
3.“秋风萧瑟天气凉,草木摇落露为霜。”诗中所写白露凝为霜的过程中发生的变化是 ( )
A.分子数目的变化 B.分子质量的变化 C.分子间隔的变化 D.分子种类的变化
【答案】C【解析】白露凝为霜是水由液态变为固态(物理变化),是分子间隔发生变化,由于温度下降,水蒸气凝结
成液态水,然后再冷却形成霜,这过程中水分子之间的间隔会逐渐减小。
4.化合价表示原子之间形成化合物时表现出的一种性质。下列纯净物中化合价标注正确的一项是 ( )
A.\s\up11(+1) B.\s\up11( -2) C.\s\up11( +4 ) D.\s\up11( +7 )
【答案】C
【解析】A(×)单质中元素的化合价为0,H中氢元素的化合价为0。
B、D(×)化合物中各元素的正、负化合价代数和为零。
CaCl 中氯元素的化合价为-1,CaSO 中硫元素的化合价为+6。
2 4
C(√)氢为+1价,C为+4价,O为-2价,2×1+4+3×(-2)=0.
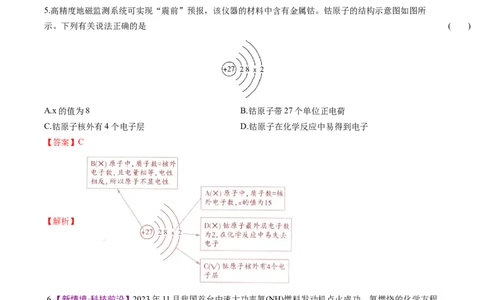
5.高精度地磁监测系统可实现“震前”预报,该仪器的材料中含有金属钴。钴原子的结构示意图如图所
示。下列有关说法正确的是 ( )
A.x的值为8 B.钴原子带27个单位正电荷
C.钴原子核外有4个电子层 D.钴原子在化学反应中易得到电子
【答案】C
【解析】
6.【新情境·科技前沿】2023年11月我国首台中速大功率氨(NH)燃料发动机点火成功,氨燃烧的化学方程
点燃式为4NH +3O 2N+6X,X的化学式是 ( )
3 2 2
A.NO B.H O C.H O D.HNO
2 2 2 3
【答案】B
【解析】依据质量守恒定律,化学反应前后原子种类和数目不变,反应前有4个N原子、12个H原子、6
个0原子,反应后有4个N原子,6个X分子中有12个H原子、6个0原子,所以1个X分子中有2个H
原子、1个0原子,故X的化学式为HO。
2
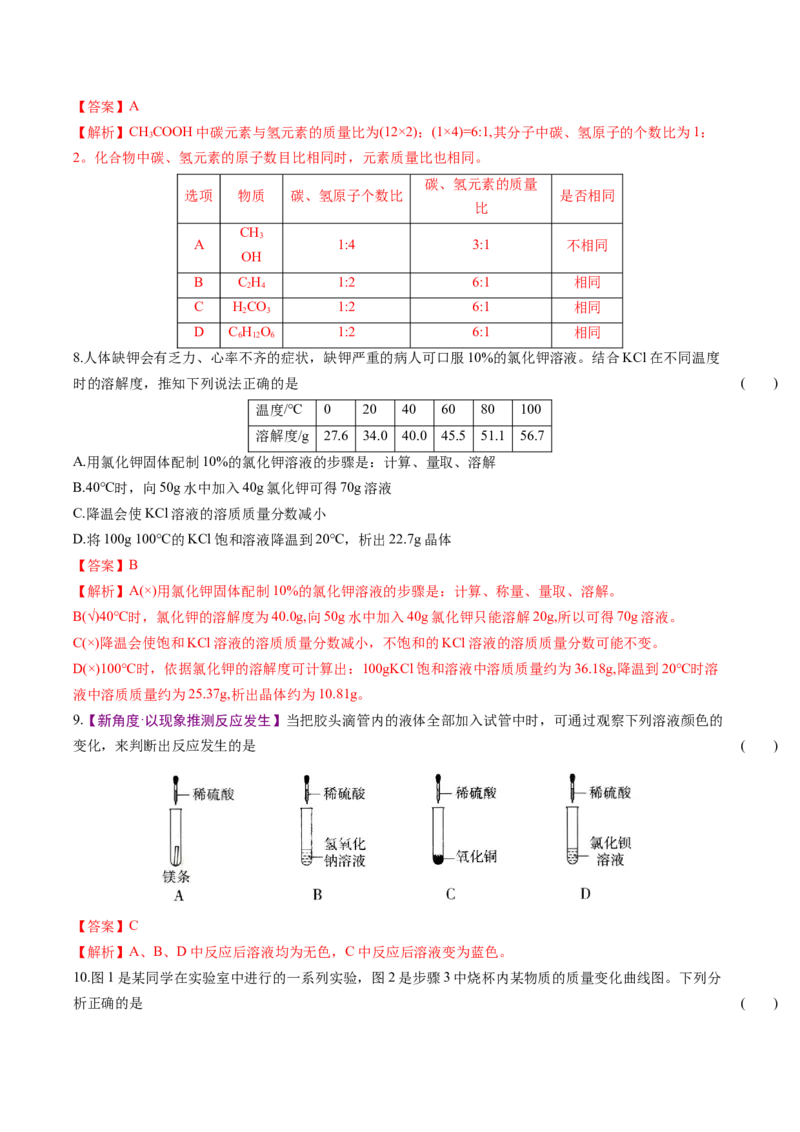
7.山西特产老陈醋的主要成分是醋酸(CHCOOH),下列物质与醋酸中碳元素和氢元素的质量比不相同的是 ( )
3
A.CHOH B.C H C.H CO D.C H O
3 2 4 2 3 6 12 6【答案】A
【解析】CHCOOH中碳元素与氢元素的质量比为(12×2):(1×4)=6:1,其分子中碳、氢原子的个数比为1:
3
2。化合物中碳、氢元素的原子数目比相同时,元素质量比也相同。
碳、氢元素的质量
选项 物质 碳、氢原子个数比 是否相同
比
CH
3
A 1:4 3:1 不相同
OH
B C H 1:2 6:1 相同
2 4
C HCO 1:2 6:1 相同
2 3
D C H O 1:2 6:1 相同
6 12 6
8.人体缺钾会有乏力、心率不齐的症状,缺钾严重的病人可口服10%的氯化钾溶液。结合KCl在不同温度
时的溶解度,推知下列说法正确的是 ( )
温度/℃ 0 20 40 60 80 100
溶解度/g 27.6 34.0 40.0 45.5 51.1 56.7
A.用氯化钾固体配制10%的氯化钾溶液的步骤是:计算、量取、溶解
B.40℃时,向50g水中加入40g氯化钾可得70g溶液
C.降温会使KCl溶液的溶质质量分数减小
D.将100g 100℃的KCl饱和溶液降温到20℃,析出22.7g晶体
【答案】B
【解析】A(×)用氯化钾固体配制10%的氯化钾溶液的步骤是:计算、称量、量取、溶解。
B(√)40℃时,氯化钾的溶解度为40.0g,向50g水中加入40g氯化钾只能溶解20g,所以可得70g溶液。
C(×)降温会使饱和KCl溶液的溶质质量分数减小,不饱和的KCl溶液的溶质质量分数可能不变。
D(×)100℃时,依据氯化钾的溶解度可计算出:100gKCl饱和溶液中溶质质量约为36.18g,降温到20℃时溶
液中溶质质量约为25.37g,析出晶体约为10.81g。
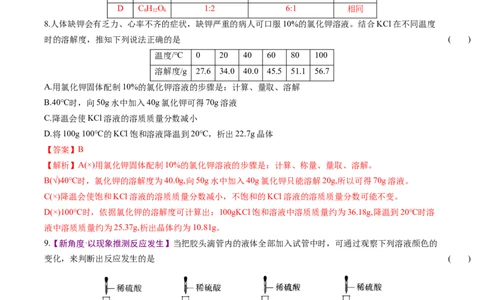
9.【新角度·以现象推测反应发生】当把胶头滴管内的液体全部加入试管中时,可通过观察下列溶液颜色的
变化,来判断出反应发生的是 ( )
【答案】C
【解析】A、B、D中反应后溶液均为无色,C中反应后溶液变为蓝色。
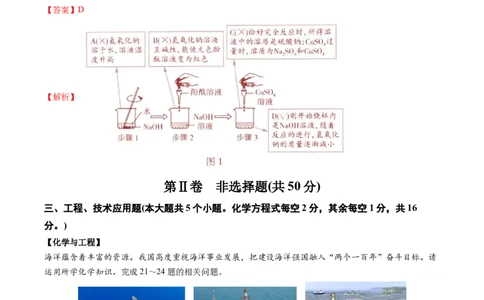
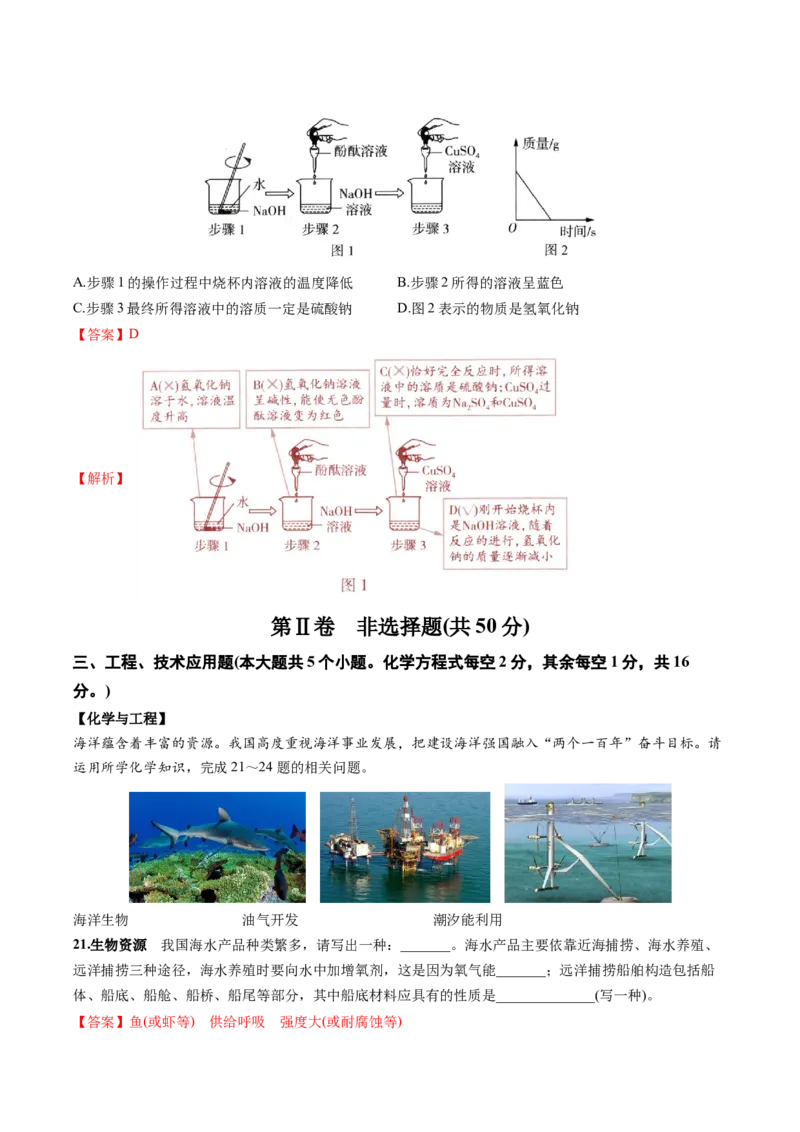
10.图1是某同学在实验室中进行的一系列实验,图2是步骤3中烧杯内某物质的质量变化曲线图。下列分
析正确的是 ( )A.步骤1的操作过程中烧杯内溶液的温度降低 B.步骤2所得的溶液呈蓝色
C.步骤3最终所得溶液中的溶质一定是硫酸钠 D.图2表示的物质是氢氧化钠
【答案】D
【解析】
第Ⅱ卷 非选择题(共 50 分)
三、工程、技术应用题(本大题共5个小题。化学方程式每空2分,其余每空1分,共16
分。)
【化学与工程】
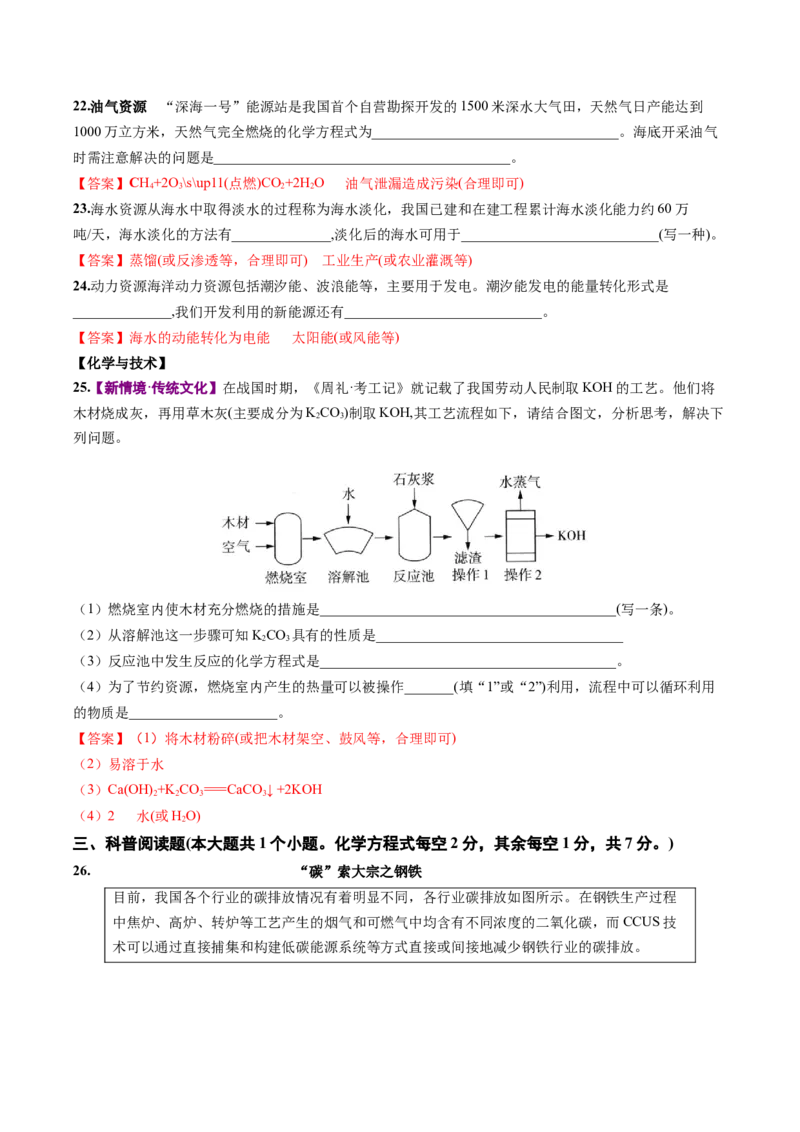
海洋蕴含着丰富的资源。我国高度重视海洋事业发展,把建设海洋强国融入“两个一百年”奋斗目标。请
运用所学化学知识,完成21~24题的相关问题。
海洋生物 油气开发 潮汐能利用
21.生物资源 我国海水产品种类繁多,请写出一种:_______。海水产品主要依靠近海捕捞、海水养殖、
远洋捕捞三种途径,海水养殖时要向水中加增氧剂,这是因为氧气能_______;远洋捕捞船舶构造包括船
体、船底、船舱、船桥、船尾等部分,其中船底材料应具有的性质是______________(写一种)。
【答案】鱼(或虾等) 供给呼吸 强度大(或耐腐蚀等)22.油气资源 “深海一号”能源站是我国首个自营勘探开发的1500米深水大气田,天然气日产能达到
1000万立方米,天然气完全燃烧的化学方程式为___________________________________。海底开采油气
时需注意解决的问题是__________________________________________。
【答案】CH+2O \s\up11(点燃)CO+2H O 油气泄漏造成污染(合理即可)
4 3 2 2
23.海水资源从海水中取得淡水的过程称为海水淡化,我国已建和在建工程累计海水淡化能力约60万
吨/天,海水淡化的方法有______________,淡化后的海水可用于____________________________(写一种)。
【答案】蒸馏(或反渗透等,合理即可) 工业生产(或农业灌溉等)
24.动力资源海洋动力资源包括潮汐能、波浪能等,主要用于发电。潮汐能发电的能量转化形式是
______________,我们开发利用的新能源还有____________________________。
【答案】海水的动能转化为电能 太阳能(或风能等)
【化学与技术】
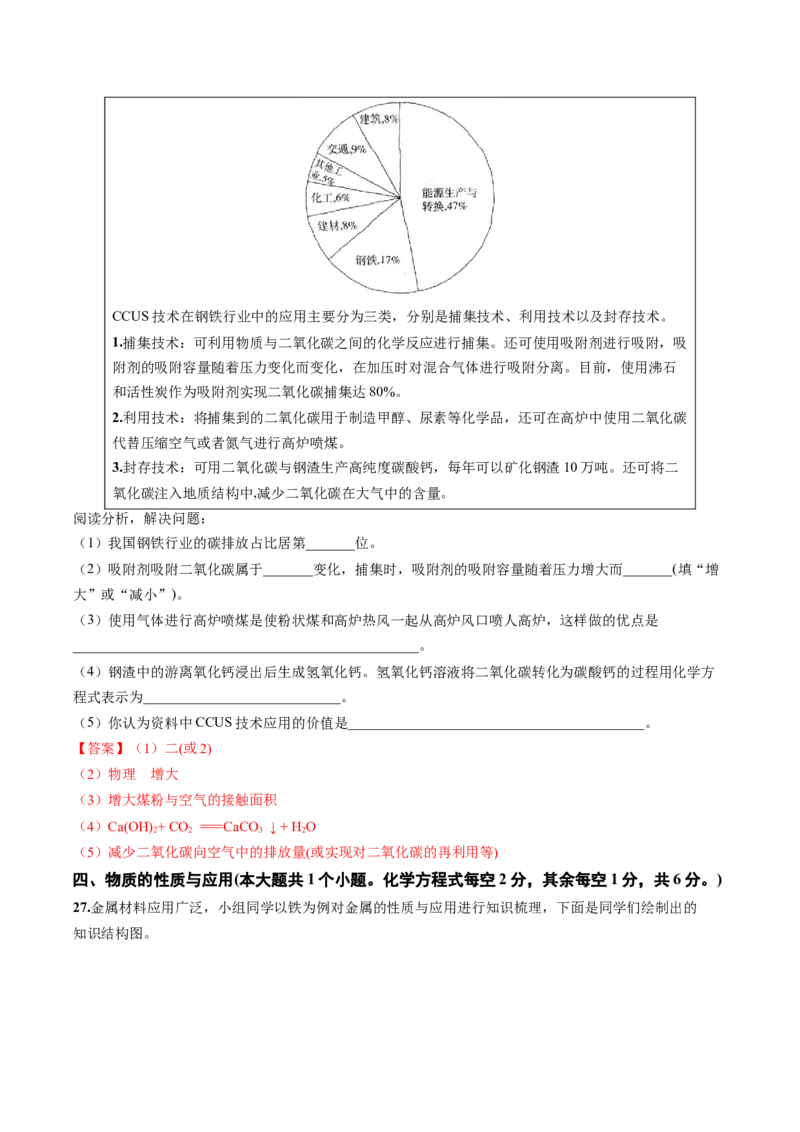
25.【新情境·传统文化】在战国时期,《周礼·考工记》就记载了我国劳动人民制取KOH的工艺。他们将
木材烧成灰,再用草木灰(主要成分为KCO)制取KOH,其工艺流程如下,请结合图文,分析思考,解决下
2 3
列问题。
(1)燃烧室内使木材充分燃烧的措施是__________________________________________(写一条)。
(2)从溶解池这一步骤可知KCO 具有的性质是___________________________________
2 3
(3)反应池中发生反应的化学方程式是__________________________________________。
(4)为了节约资源,燃烧室内产生的热量可以被操作_______(填“1”或“2”)利用,流程中可以循环利用
的物质是_____________________。
【答案】(1)将木材粉碎(或把木材架空、鼓风等,合理即可)
(2)易溶于水
(3)Ca(OH) +K CO=CaCO ↓ +2KOH
2 2 3 3
(4)2 水(或HO)
2
三、科普阅读题(本大题共1个小题。化学方程式每空2分,其余每空1分,共7分。)
26. “碳”索大宗之钢铁
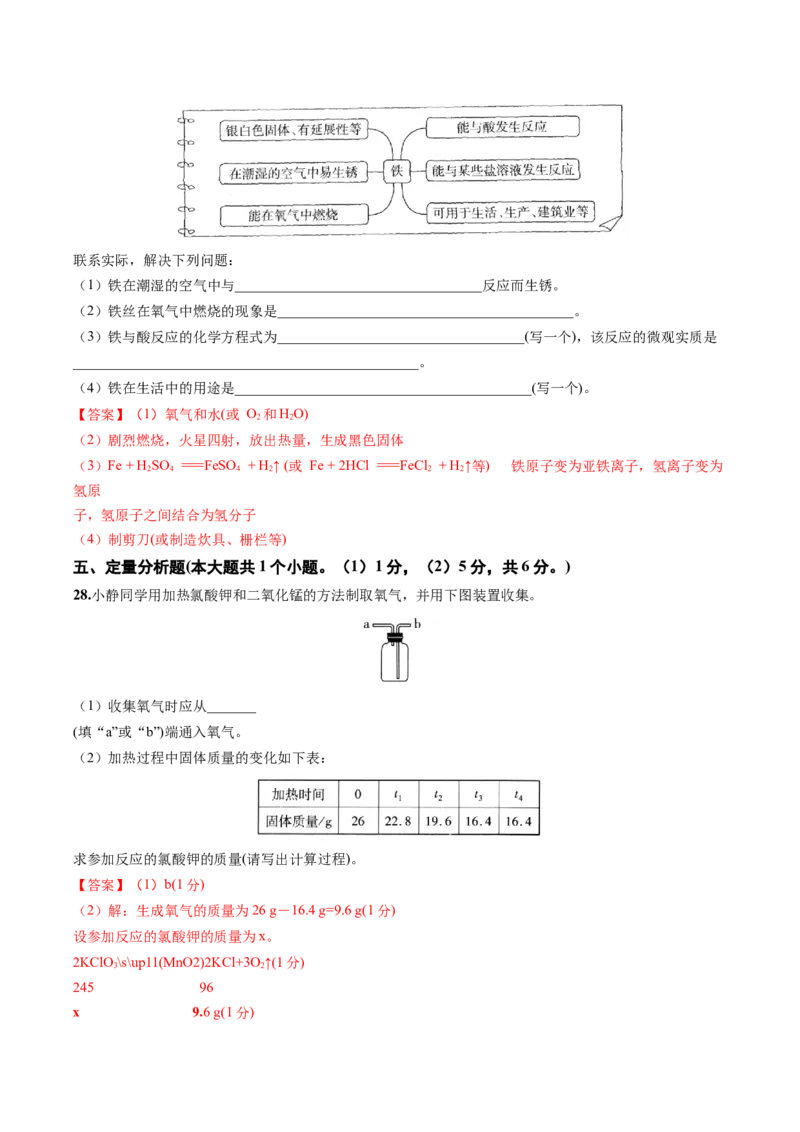
目前,我国各个行业的碳排放情况有着明显不同,各行业碳排放如图所示。在钢铁生产过程
中焦炉、高炉、转炉等工艺产生的烟气和可燃气中均含有不同浓度的二氧化碳,而CCUS技
术可以通过直接捕集和构建低碳能源系统等方式直接或间接地减少钢铁行业的碳排放。CCUS技术在钢铁行业中的应用主要分为三类,分别是捕集技术、利用技术以及封存技术。
1.捕集技术:可利用物质与二氧化碳之间的化学反应进行捕集。还可使用吸附剂进行吸附,吸
附剂的吸附容量随着压力变化而变化,在加压时对混合气体进行吸附分离。目前,使用沸石
和活性炭作为吸附剂实现二氧化碳捕集达80%。
2.利用技术:将捕集到的二氧化碳用于制造甲醇、尿素等化学品,还可在高炉中使用二氧化碳
代替压缩空气或者氮气进行高炉喷煤。
3.封存技术:可用二氧化碳与钢渣生产高纯度碳酸钙,每年可以矿化钢渣10万吨。还可将二
氧化碳注入地质结构中,减少二氧化碳在大气中的含量。
阅读分析,解决问题:
(1)我国钢铁行业的碳排放占比居第_______位。
(2)吸附剂吸附二氧化碳属于_______变化,捕集时,吸附剂的吸附容量随着压力增大而_______(填“增
大”或“减小”)。
(3)使用气体进行高炉喷煤是使粉状煤和高炉热风一起从高炉风口喷人高炉,这样做的优点是
_________________________________________________。
(4)钢渣中的游离氧化钙浸出后生成氢氧化钙。氢氧化钙溶液将二氧化碳转化为碳酸钙的过程用化学方
程式表示为____________________________。
(5)你认为资料中CCUS技术应用的价值是__________________________________________。
【答案】(1)二(或2)
(2)物理 增大
(3)增大煤粉与空气的接触面积
(4)Ca(OH) + CO =CaCO ↓ + H O
2 2 3 2
(5)减少二氧化碳向空气中的排放量(或实现对二氧化碳的再利用等)
四、物质的性质与应用(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分。)
27.金属材料应用广泛,小组同学以铁为例对金属的性质与应用进行知识梳理,下面是同学们绘制出的
知识结构图。联系实际,解决下列问题:
(1)铁在潮湿的空气中与___________________________________反应而生锈。
(2)铁丝在氧气中燃烧的现象是__________________________________________。
(3)铁与酸反应的化学方程式为___________________________________(写一个),该反应的微观实质是
_________________________________________________。
(4)铁在生活中的用途是__________________________________________(写一个)。
【答案】(1)氧气和水(或 O 和HO)
2 2
(2)剧烈燃烧,火星四射,放出热量,生成黑色固体
(3)Fe + H SO =FeSO + H ↑ (或 Fe + 2HCl =FeCl + H ↑等) 铁原子变为亚铁离子,氢离子变为
2 4 4 2 2 2
氢原
子,氢原子之间结合为氢分子
(4)制剪刀(或制造炊具、栅栏等)
五、定量分析题(本大题共1个小题。(1)1分,(2)5分,共6分。)
28.小静同学用加热氯酸钾和二氧化锰的方法制取氧气,并用下图装置收集。
(1)收集氧气时应从_______
(填“a”或“b”)端通入氧气。
(2)加热过程中固体质量的变化如下表:
求参加反应的氯酸钾的质量(请写出计算过程)。
【答案】(1)b(1分)
(2)解:生成氧气的质量为26 g-16.4 g=9.6 g(1分)
设参加反应的氯酸钾的质量为x。
2KClO\s\up11(MnO2)2KCl+3O ↑(1分)
3 2
245 96
x 9.6 g(1分)(1分)
x =24.5 g(1分)
答:参加反应的氯酸钾的质量是24.5g。
六、实验探究题(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分。)
【实验设计】
29.某化学兴趣小组同学以燃烧条件为主题进行实验探究。
(1)实验装置:如图1所示。
(2)实验原理:图1中发生反应的化学方程式为__________________________________________。
(3)实验现象:图1中发生燃烧的物质是____________________________。
(4)实验结论:________________________________________________________。
问题与交流:①图1所示实验成功的关键是___________________________________(写一点)。
②实验中同学们闻到刺激性气味,刺激呼吸道,于是设计了如图2所示的改进装置,改进后的优点是
__________________________________________(写一条)。
【科学探究】
【答案】(2)4P+5O\s\up11(点燃)2PO
2 2 5
(3)铜片上的白磷
(4)燃烧需要可燃物与氧气接触,且温度达到着火点
问题与交流:①热水量要足(或铜片不能太厚,合理即可)
②更环保(合理叙述均可)
【解析】磷燃烧生成的五氧化二磷会刺激人体呼吸道,改进装置后反应在密闭容器中进行,更安全、更环
保。
30.硬水是含有较多可溶性钙、镁化合物的水。某校社会实践小组的同学们对当地水质硬度、属于何种硬
度、如何降低水的硬度及用软水自制汽水等问题产生了浓厚的兴趣,为此展开了项目学习之旅。
任务一:测量水的硬度
【查阅资料】同学们查阅了相关资料,了解到国家有关水的硬度的标准如下表(钙离子质
量浓度指的是单位体积溶液中钙离子的质量):
中等硬度的
类别 软水 硬水 非常硬的水
水钙离子质量浓度(mg/L) 0~17.1 17.1~60 60~120 ≥120
【进行测量】同学们取水样,检测其钙离子质量浓度为36.2mg/L,说明该水属于______________。
任务二:探究水质属于何种硬度
【信息检索】水的硬度包括暂时性硬度和永久性硬度。暂时性硬度主要是由钙、镁的碳酸氢盐
[Ca(HCO )、Mg(HCO )]所形成的硬度,煮沸后可将可溶性钙、镁化合物转化为沉淀;永久性硬度主要是
3 2 3 2
由钙、镁的硫酸盐、氯化物等盐类所形成的硬度。
【进行实验】
实验步骤 实验现象 实验结论
①取少量水样于试管中,加热,将生成的气体通入澄清石灰
______________ 说明水样中有HCO -
3
水
②向上述溶液中继续滴加_______和稀硝酸 有白色沉淀产生 说明水样中有Cl-
【交流反思】
(1)同学们通过实验得出当地水质是由两种硬度造成的,步骤②中发生反应的化学方程式是
___________________________________(写一个)。
(2)有同学对“水样中有Cl~”的结论产生质疑,理由是
__________________________________________。
任务三:探究如何降低水的硬度
【小组研讨】硬水的使用会给生活和生产带来许多危害。永久性硬度的水可以采用特定的阳离子交换树
脂,用钠离子将水中的_______离子置换出来;暂时性硬度的水可以用_______的方法降低水的硬度。
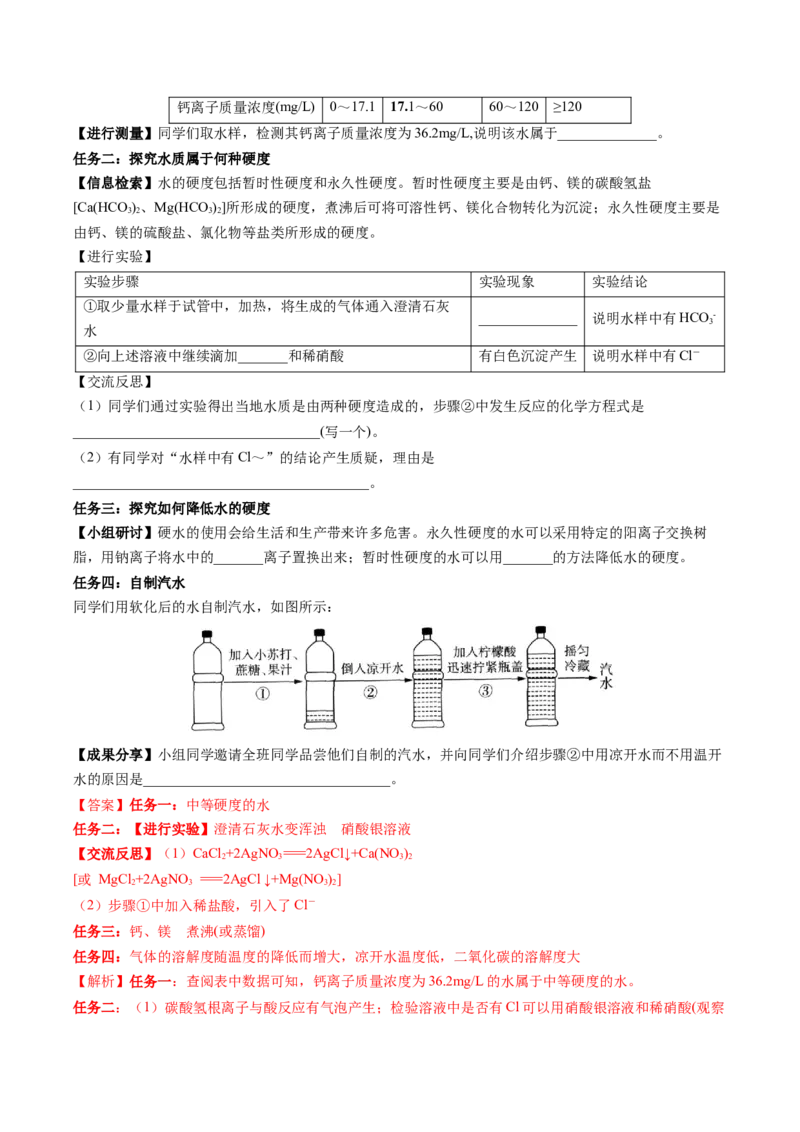
任务四:自制汽水
同学们用软化后的水自制汽水,如图所示:
【成果分享】小组同学邀请全班同学品尝他们自制的汽水,并向同学们介绍步骤②中用凉开水而不用温开
水的原因是___________________________________。
【答案】任务一:中等硬度的水
任务二:【进行实验】澄清石灰水变浑浊 硝酸银溶液
【交流反思】(1)CaCl +2AgNO =2AgCl↓+Ca(NO )
2 3 3 2
[或 MgCl +2AgNO =2AgCl ↓+Mg(NO)]
2 3 3 2
(2)步骤①中加入稀盐酸,引入了Cl-
任务三:钙、镁 煮沸(或蒸馏)
任务四:气体的溶解度随温度的降低而增大,凉开水温度低,二氧化碳的溶解度大
【解析】任务一:查阅表中数据可知,钙离子质量浓度为36.2mg/L的水属于中等硬度的水。
任务二:(1)碳酸氢根离子与酸反应有气泡产生;检验溶液中是否有Cl可以用硝酸银溶液和稀硝酸(观察是否有白色沉淀产生)。
(2)由于步骤①引入了Cl-,所以不能证明水样中有Cl-。
任务三:永久性硬度的水中的Ca2+、Mg2+不能通过煮沸使其沉淀,所以为了降低硬度,可用钠离子交换水
中的钙离子和镁离子。暂时性硬度主要是由钙、镁的碳酸氢盐[Ca(HCO )、Mg(HCO )]所形成的硬度,煮
3 2 3 2
沸后可将可溶性钙、镁化合物转化为沉淀,所以暂时性硬度的水可以用煮沸的方法降低其硬度。
任务四:气体的溶解度随温度的降低而增大,凉开水温度低,二氧化碳的溶解度大。