文档内容
绝密★启用前
2024 年中考押题预测卷【广东卷】
化 学
(考试时间:60分钟 试卷满分:90分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 Mn-55
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.《茶经》记载茶叶制作过程:“晴采之,蒸之,捣之,拍之,焙之,穿之,封之,茶之干矣”。以下
涉及化学变化的是( )
A.采 B.拍 C.焙 D.封
2.化学与我们的生活相关。下列说法正确的是( )
①用闻气味儿的方法区分羊毛纤维和棉纤维
②回收废旧金属有利于节约资源
③天然气泄漏应立即打开排气扇换气
④用聚氯乙烯塑料包装食品
⑤减少燃煤发电,增加太阳能发电,有利于治理雾霾
A.①②⑤ B.②⑤
B.①④⑤ D.①③④
3.科学思维是化学核心素养的重要组成部分,下列示例说法正确的是( )
A.比较:金刚石和石墨的组成元素相同,故两者的物理性质相同
B.分类:CO 引起温室效应,属于空气污染物
2
C.分析:稀有气体用于霓虹灯,因为通电时稀有气体能发出不同颜色的光
D.推理:分子是由原子构成的,所以氯化钠分子是由氯原子和钠原子构成的
4.2024年3月22日是第三十二届“世界水日”,其主题为“Water for Peace”(以水促和平)。下列有关水
的说法正确的是( )
A.可用肥皂水区别硬水和软水
B.用水灭火的原理是降低可燃物的着火点C.水是良好的溶剂,能将有机合成材料溶解掉
D.河水经过沉降、过滤杀菌消毒等净化过程后就变成纯水
5.合理膳食能为人体提供必要的营养物质。下列有关说法正确的是( )
A.Hg是人体必需的微量元素
B.不同的蛋白质都含有氮元素
C.植物油脂里富含淀粉,能为人体提供能量
D.不同的维生素性质不同但组成结构相同
6.我国进入了创新型国家行列,科技发展日新月异。下列说法正确的是( )
A.研发出可造“太空电梯”的碳纳米管,碳纳米管是新型化合物
B.玻璃钢材料使“天问一号”隔热性好,玻璃钢属于复合材料
C.柔性氮化镓太阳能电池为空间站供能,太阳能是不可再生能源
D.在我国空间站成功点燃甲烷并持续30秒,甲烷在纯氧中才能燃烧
7.2024年5月1日我国第一艘电磁弹射型航空母舰——“福建”舰已成功试航。福建舰航母飞行甲板的
钢板表面镀镍,可以防腐和增加硬度,图为镍元素在元素周期表的信息及原子结构示意图,下列说法
错误的是( )
A.镍属于金属元素
B.图中n的值为16
C.镍原子在化学变化中易失电子
D.镍原子的相对原子质量为58.6g
8.“天水麻辣烫”火遍全网,各地游客纷至沓来品尝美味,而其中最诱人的就是油泼辣椒了。辣椒富含
多种维生素外,辣椒素是辣椒中的主要化学物质,其化学式为C H NO 下列有关辣椒素的说法正确
18 27 3.
的是
A.辣椒素中含有臭氧分子
B.辣椒素中氮、氧元素质量比为1:3
C.辣椒素属于氧化物
D.辣椒素由碳、氢、氮、氧四种元素组成
9.学好化学,掌握物质的性质和用途,为人类开启智慧之旅。下列说法不正确的是( )
A.用聚乙烯塑料制作蔬菜大棚
B.用灼烧闻气味的方法可以鉴别羊毛和合成纤维
C.研制、生产可降解塑料可以解决“白色污染”问题
D.电木插座具有热固性,破裂后可以进行热修补10.氢氧化钠俗名苛性钠、火碱或烧碱。下列关于氢氧化钠的认识,正确的是( )
A.其水溶液中有 Na+、O2-、H+这三种离子
B.能与 MgO、CuO 等金属氧化物发生反应
C.其水溶液常用来检验 CO 气体
2
D.工业上可以氯化钠为原料来制得
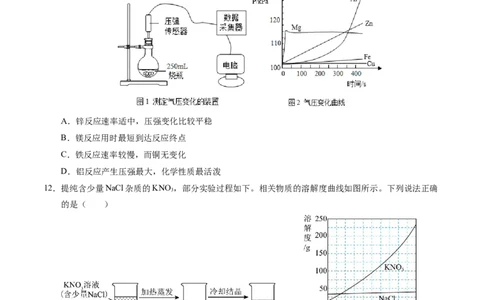
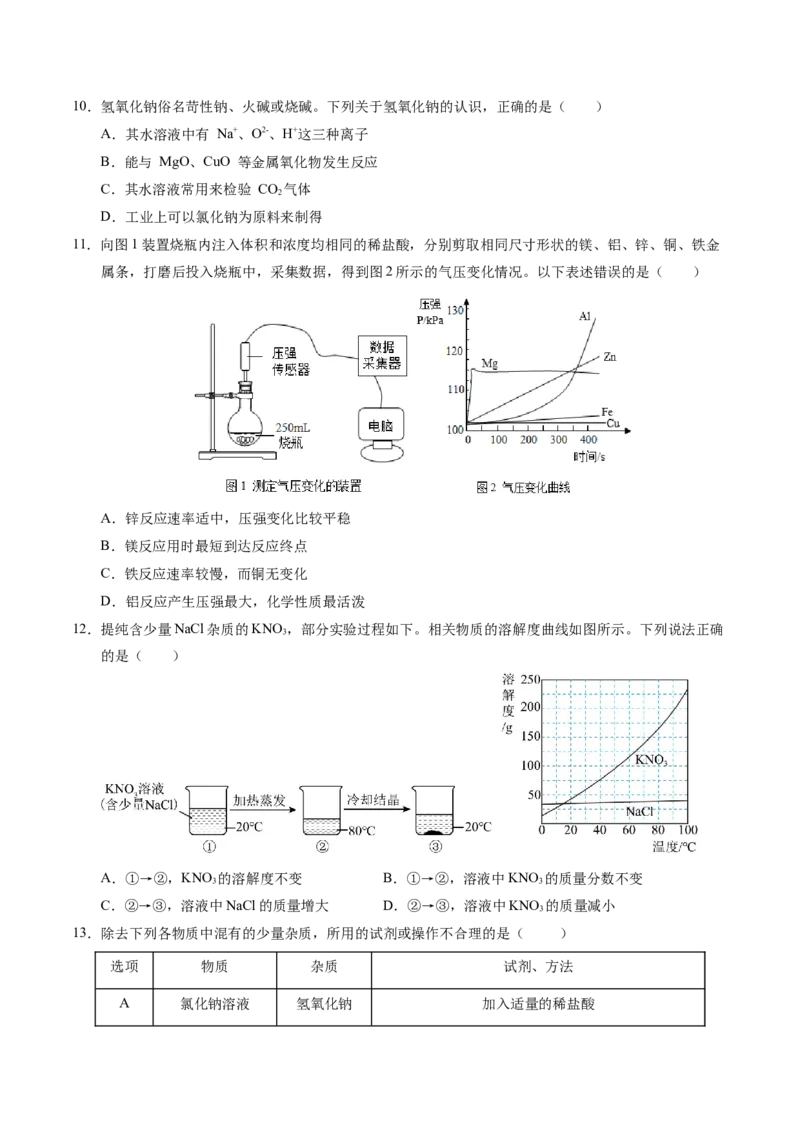
11.向图1装置烧瓶内注入体积和浓度均相同的稀盐酸,分别剪取相同尺寸形状的镁、铝、锌、铜、铁金
属条,打磨后投入烧瓶中,采集数据,得到图2所示的气压变化情况。以下表述错误的是( )
A.锌反应速率适中,压强变化比较平稳
B.镁反应用时最短到达反应终点
C.铁反应速率较慢,而铜无变化
D.铝反应产生压强最大,化学性质最活泼
12.提纯含少量NaCl杂质的KNO,部分实验过程如下。相关物质的溶解度曲线如图所示。下列说法正确
3
的是( )
A.①→②,KNO 的溶解度不变 B.①→②,溶液中KNO 的质量分数不变
3 3
C.②→③,溶液中NaCl的质量增大 D.②→③,溶液中KNO 的质量减小
3
13.除去下列各物质中混有的少量杂质,所用的试剂或操作不合理的是( )
选项 物质 杂质 试剂、方法
A 氯化钠溶液 氢氧化钠 加入适量的稀盐酸B CuO Cu 加入过量稀硫酸反应后,过滤
C 二氧化碳 一氧化碳 通过灼热的CuO
D Cu(NO ) 溶液 AgNO 加入过量的Cu反应后,过滤
3 2 3
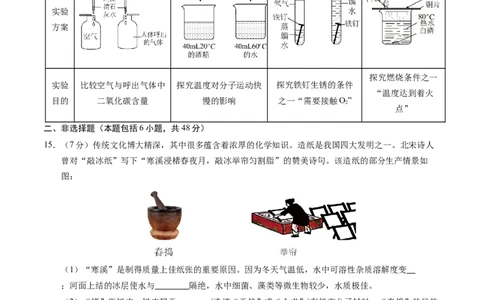
14.下列实验不能达到目的的是( )
编号 A B C D
实验
方案
探究燃烧条件之一
实验 比较空气与呼出气体中 探究温度对分子运动快 探究铁钉生锈的条件
“温度达到着火
目的 二氧化碳含量 慢的影响 之一“需要接触O”
2
点”
二、非选择题(本题包括6小题,共48分)
15.(7分)传统文化博大精深,其中很多蕴含着浓厚的化学知识。造纸是我国四大发明之一。北宋诗人
曾对“敲冰纸”写下“寒溪浸楮春夜月,敲冰举帘匀割脂”的赞美诗句。该造纸的部分生产情景如
图:
(1)“寒溪”是制得质量上佳纸张的重要原因。因为冬天气温低,水中可溶性杂质溶解度变
;河面上结的冰层使水与 隔绝,水中细菌、藻类等微生物较少,水质极佳。
(2)“楮”指树皮,树皮属于 (选填“天然”或“合成”)有机高分子材料,“舂捣”的目的
是增大反应物接触面积, 。
(3)“帘”是带筛网的捞纸工具,“举帘”工作原理与实验室中 (填一操作名称)相似。
(4)人们常采用喷洒二乙基锌Zn(C H) 溶液的方法来保护纸质文物:Zn(C H) 可以与水反应生成一
2 5 2 2 5 2
种金属氧化物和乙烷(C H)气体,请写出该反应的化学方程式: 。
2 6
(5)结合二氧化碳的性质、灭火的原理,分析二氧化碳灭火器可用来扑灭纸质图书或档案失火的主
要原因: 。
16.(5分)某固体混合物可能含有KCO、KSO 、CuSO 、CaCl 、KC1中的一种或几种,为了确定该混
2 3 2 4 4 2合物的成分,进行如下实验:
步骤I:将固体混合物溶于水,搅拌后得无色透明溶液。
步骤Ⅱ:往步骤Ⅰ溶液中滴加足量硝酸钡溶液,有白色沉淀生成。
步骤Ⅲ:过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解,并放出气体。
试判断:
(1)固体混合物中肯定有 ,肯定没有 ,可能有 。
(2)对可能有的物质,可采用向步骤Ⅲ中的滤液滴加 溶液来检验。
(3)写出步骤Ⅲ中发生的化学方程式 。
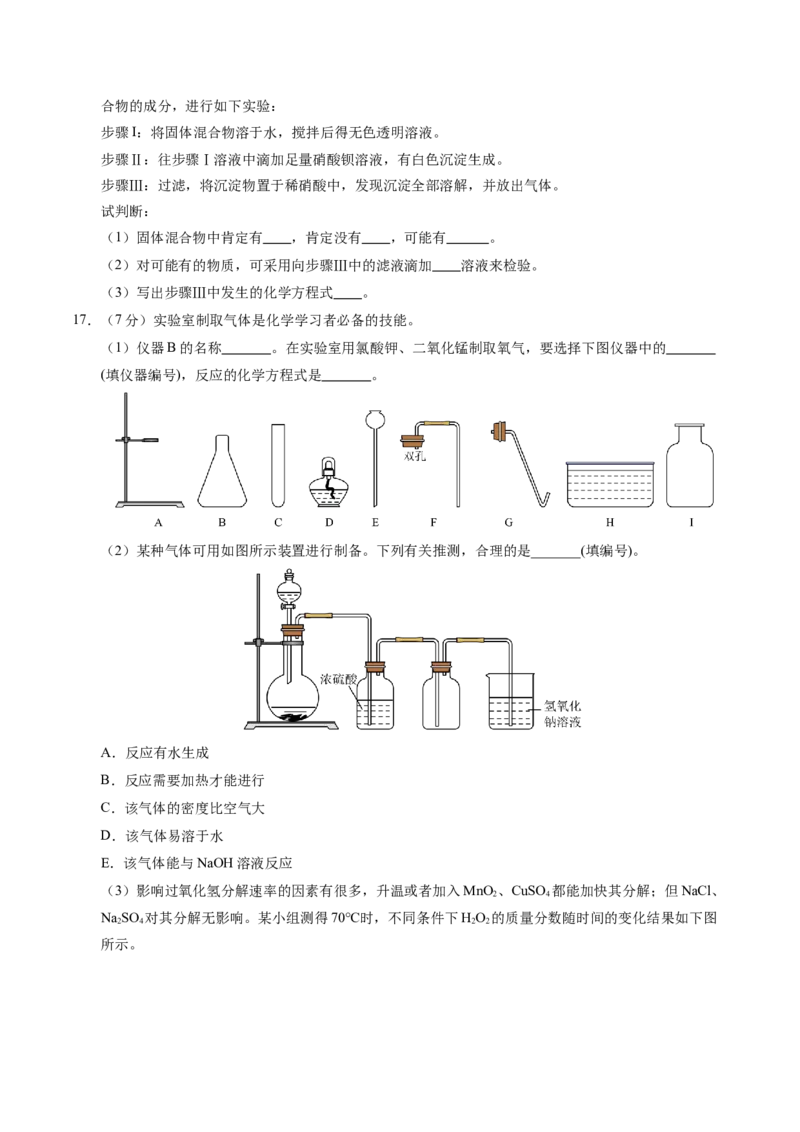
17.(7分)实验室制取气体是化学学习者必备的技能。
(1)仪器B的名称 。在实验室用氯酸钾、二氧化锰制取氧气,要选择下图仪器中的
(填仪器编号),反应的化学方程式是 。
(2)某种气体可用如图所示装置进行制备。下列有关推测,合理的是_______(填编号)。
A.反应有水生成
B.反应需要加热才能进行
C.该气体的密度比空气大
D.该气体易溶于水
E.该气体能与NaOH溶液反应
(3)影响过氧化氢分解速率的因素有很多,升温或者加入MnO 、CuSO 都能加快其分解;但NaCl、
2 4
NaSO 对其分解无影响。某小组测得70℃时,不同条件下HO 的质量分数随时间的变化结果如下图
2 4 2 2
所示。请回答以下问题:
①图甲表明,其他条件不变时,溶液的pH越 ,HO 分解越快。
2 2
②图乙表明,碱性条件下, (填离子符号)对HO 分解速率的影响大。
2 2
③综合以上信息推测,下列物质可加快HO 分解的是 (填编号)。
2 2
A KOH B.KCl
C.HCl D.MnSO
4
18.(8分)在“天宫课堂”中,王亚平老师用醋酸钠(CHCOONa)过饱和溶液做了一个“点水成冰”
3
的趣味实验。过饱和溶液是指在一定温度下,溶液里的某种溶质越过这种溶质的饱和限度,而溶质仍
未析出的溶液。醋酸钠的溶解度表如下:(水的密度为:1g/cm3)
温度/℃ 0 10 20 30 40 50 60 80 100
溶解度/g 33 40.8 46.5 54.5 65.5 83 139 153 170
(1)由上表,你可获得什么信息: (填一条即可)
(2)40℃时,在盛有50mL,水的烧杯中加入40g醋酸钠,并用玻璃棒不断搅拌,此时得到醋酸钠溶
液的质量为 。
(3)将(2)中所得溶液趁热过滤,将滤液缓慢降温至80℃,无晶体析出,得到醋酸钠的过饱和溶
液,用玻璃棒轻轻搅动;溶液会马上会析出针状结晶,就像结成了“冰块”,从而实现点水成
“冰”。
①醋酸钠的过饱和溶液是 (选填“稳定”或“不稳定”)的。“冰块”摸上去是温热的,说明
该过程 。(填“放热”或“吸热”)
②“点水成冰”实际上是溶液中析出晶体。溶液结晶过程中,下列判断正确的是 。
A.溶质的质量一定减小 B.溶质的质量分数一定减小 C.溶剂的质量一定减少
(4)在日常生活中,也能观察到水成冰的现象,从微观的角度分析,在日常生活中,水结成冰时,
发生了改变。
(5)醋酸钠溶液在生产和生活中也有广泛的应用,工厂常用10%—25%醋酸钠溶液作为污水处理
剂、能有效去除污水中所含的杂质,使水质达到排放要求,减少对水环境的污染。现要用溶质质量分
数为50%的醋酸钠溶液配制溶质质量分数为10%的醋酸钠溶液1000g,需加入水的质量为 g。
19.(11分)氢氧化钠变质的实验探究:
I:向钠离子质量分数均为2%的氯化钠溶液、氢氧化钠溶液、碳酸钠溶液中滴加酚酞,氯化钠溶液不变红,氢氧化钠溶液、碳酸钠溶液变红。
Ⅱ:一位实验员在实验室刚配制一定质量分数的氢氧化钠溶液后,突然接到紧急任务离开,几天后回
到实验室才发现没有盖上瓶塞。
(1)你认为能使酚酞变红的微粒为______。
A.Na+ B.OH- C. 或由 引发生成的OH-。
(2)氢氧化钠变质为碳酸钠,反应的化学方程式为 。溶液中的离子数量如何变化? 。
(填:不变、减少、增大)
(3)欲证明有氢氧化钠变质为碳酸钠,同学甲认为可选择试剂a:稀盐酸,同学乙认为可选择试剂
b;氯化钡溶液,你的观点是______。
A.过量稀盐酸
B.过量氯化钡溶液
C.过量稀盐酸和氯化钡溶液均可以
D.过量稀盐酸和氯化钡溶液均不可以
(4)同学丙认为氢氧化钠只有一部分变质为碳酸钠,溶液中仍然含有氢氧化钠,他通过设计以下实
验证明其结论是正确的。
第一步:取少量待测液,向其中加入过量的 溶液,过滤;
第二步:向以上滤液中加入 ,出现 的现象,则丙同学观点正确。
(5)100g质量分数为A%的氢氧化钠溶液有部分变质后,同学丁认为仍然可以通过设计实验方案计
算出A的数值,其具体的实验方案如下:向变质后的溶液中加入过量的稀盐酸,蒸发结晶,洗涤,干
燥,得到5.85g固体,从而可以计算出A的数值。你认为是否可以? (填“可以”或“不可
以”)。若不可以,请简述理由,若可以,则写出A的数值 。
20.(10分)金属材料及金属化合物在生产、生活中应用广泛。
(1)铝具有很好的抗腐蚀性能,是因为 (用化学方程式表示);
(2)镓 及其化合物应用广泛,常用于半导体、合金、磁性材料等领域.已知镓在化合物中常为
价,金属活动性顺序:
①写出镓与稀盐酸反应的化学方程式 ;
②根据上述信息,下列预测不合理的是 (填字母)
A.镓具有导电性 B.氧化镓的化学式为
C.镓能与氯化镁溶液发生置换反应 D. 或 在高温条件下能将镓的氧化物转化为金属镓
(3)二氧化锰应用广泛,可作为除锈剂、氧化剂等.通过焙烧 可制取 ,发生反应的化学
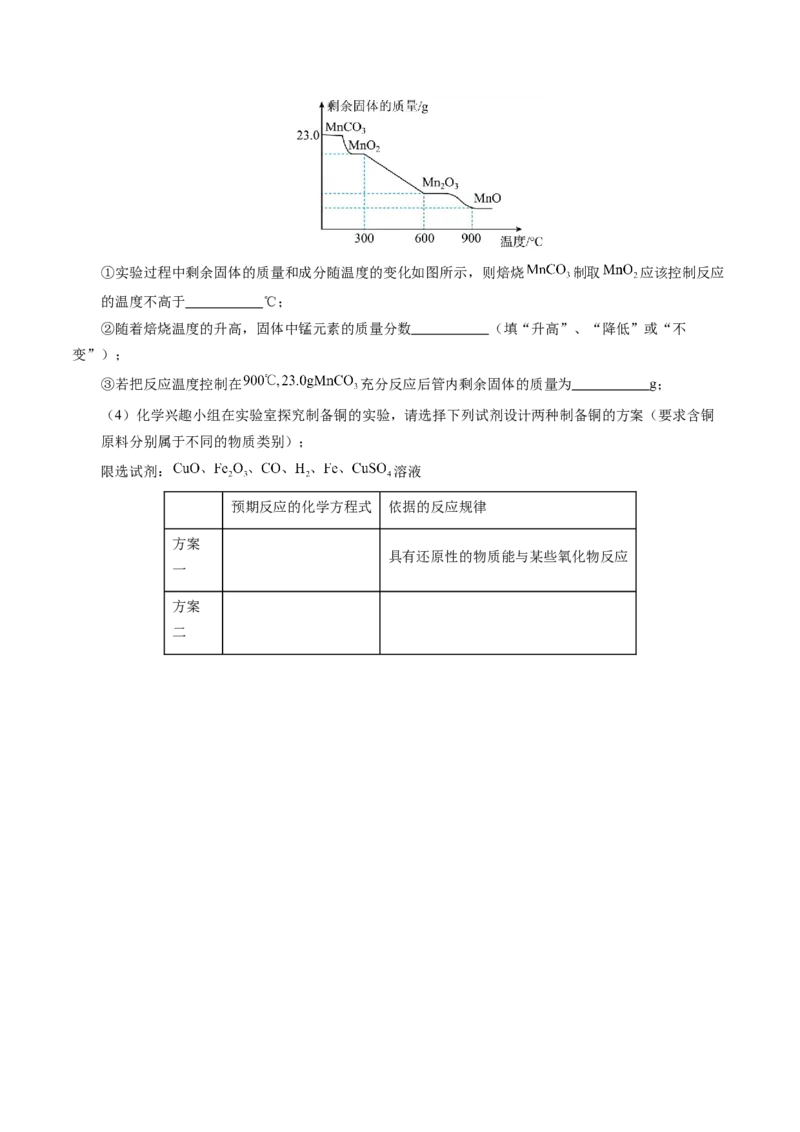
方程式为: )①实验过程中剩余固体的质量和成分随温度的变化如图所示,则焙烧 制取 应该控制反应
的温度不高于 ℃;
②随着焙烧温度的升高,固体中锰元素的质量分数 (填“升高”、“降低”或“不
变”);
③若把反应温度控制在 充分反应后管内剩余固体的质量为 g;
(4)化学兴趣小组在实验室探究制备铜的实验,请选择下列试剂设计两种制备铜的方案(要求含铜
原料分别属于不同的物质类别);
限选试剂: 溶液
预期反应的化学方程式 依据的反应规律
方案
具有还原性的物质能与某些氧化物反应
一
方案
二